Бром – тяжелая, летучая жидкость (плотность 3.1 г/см3, Ткип. 59 °С) с резким запахом, подобным запаху хлора и иода. Образует бурые пары. В отраженном свете бром почти черный, на просвет – темно-красный. При охлаждении до минус 7.3 °С бром затвердевает в желто-зеленую массу, которая напоминает по внешнему виду кристаллический иод1.
Бром хорошо растворяется в спирте, эфире, углеводородах, хлороформе и других органических растворителях. Значительно хуже бром растворим в воде (3.5% при 20 °С). Несколько лучше бром растворим в соляной и бромистоводородной кислотах, в растворах KBr.
Водный раствор брома имеет желтый цвет и называется «бромная вода». Бромная вода обладает довольно сильными окислительными свойствами. Интересно, что насыщенный раствор брома в воде не затвердевает даже при температуре минус 20 °С.
Наиболее доступными соединениями брома являются бромиды калия и натрия. Для получения из них брома эти вещества необходимо окислить в кислой среде. В качестве окислителя можно использовать перекись водорода, бромат, бихромат калия, диоксид марганца, гипохлориты, хлор2 и другие вещества.
В практикумах рекомендуют отделять полученный бром отгонкой, однако, если выход и чистота брома не имеет большого значения (например, для химических опытов) стадию отгонки можно опустить. Это значительно упростит процесс получения. Ниже приведено две методики, суть которых проста: бромид калия окисляется в присутствии серной кислоты, полученный бром собирается на дне сосуда.
Артем Чуйко получил бром следующим образом.
«Растворяем в 300 мл воды 66 г бромида калия и приливаем 18 мл концентрированной серной кислоты. Далее постепенно небольшими порциями 1 В разных источниках даются несколько отличные величины физико‐химических констант брома, что, видимо, связано с разной чистотой вещества.
2 Использование хлора и его соединений нежелательно, поскольку хлор будет загрязнять полученный продукт. добавляем 17.5 г бромата калия. Раствор желтеет, затем краснеет. Через 10 минут в растворе появляются взвешенные капли брома, которые оседают на дно. В конце реакции слой брома можно отделить пипеткой. Выход примерно 16 мл.
KBrO3 + 5KBr + 3H2SO4 = 3Br2 + 3H2O + 3K2SO4 »
Очевидным недостатком приведенного метода является использование бромата калия, который к легкодоступным веществам не принадлежит.
На форуме chemport.ru приведен другой метод получения брома, который по замыслу авторов должен быть максимально упрощенным.
« 25 г бромида натрия NaBr (около 12 мл по объему) залили 45 мл 80% серной кислоты3 (бромид не растворяли). Жидкость побурела.
(Первоначально мы собирались в 40-45% раствор бромида натрия добавить концентрированную серную кислоту, но решили максимально упростить процедуру). Затем было прилито 15 мл старого пергидроля (<30% Н2О2). Смесь стали осторожно размешивать. При заметном разогреве перемешивание прекратили, чтобы бром не закипел; смесь охладили, опустив в холодную воду. Бром скапливался на дне, кристаллики солей плавали над ним. Когда вся соль растворилась, смесь оставили еще на 5 минут. Далее можно охладить до 0-5°С для уменьшения растворимости брома в воде.
Получилось 6 мл брома (около 18 г, выход порядка 90%).
Бром можно отделить в делительной воронке или с помощью пипетки. Полученное вещество можно дополнительно подсушить концентрированной серной кислотой и перегнать.
Для проведения реакции достаточно стеклянной банки, удобно закрепить на ней резинкой полиэтиленовую пленку и, проделав дырку, приливать пергидроль и перемешивать палочкой через нее.
Даже при переливании бромной воды иногда образуется едкое бурое облако.
Старайтесь выливать прямо под слой воды.
Бром практически не растворяет в себе воду и сразу после получения уже достаточно сухой. »
3 Можно использовать аккумуляторный электролит, упаренный до образования белых паров. Пары брома имеют резкий запах, ядовиты и сильно раздражают дыхательные пути. При попадании брома на кожу образуются язвы. Работать с бромом следует под тягой, используя защитные очки и перчатки.
Хранить бром желательно в запаянных пробирках или колбах, в противном случае возможны проблемы с парами брома. В домашних условиях хранить бром крайне не рекомендуется.
Список литературы
Для подготовки данной работы были использованы материалы с сайта http://chemistry-chemists.com/
Похожие работы
... . Валентность брома в соединениях переменна, степень окисления равна -1 (в бромидах, напр. КВr), +1 (в гипобромитах, NaBrO), +3 (в бромитах, NaBrO2), +5 (в броматах, КВrО3) и + 7 (в пербромагах, NaBrO4). Химически бром весьма активен, занимая по реакционной способности место между хлором и иодом. Взаимодействие брома с серой, селеном, теллуром, фосфором, мышьяком и сурьмой сопровождается сильным ...
... . В пробирку с тетрагидроксоалюминатом натрия пропустить углекислый газ, выпадает осадок Al(OH)3: Na[Al(OH)4] + CO2 = Al(OH)3↓+ NaHCO3. Осадок промыть и высушить. Аналогично утилизируют раствор Na2[Zn(OH)4] при получении комплексного соединения из гидроксида цинка: Na2[Zn(OH)4]+ 2CO2 = Zn(OH)2↓ + 2NaHCO3. Комплексное соединение серебра – аммиачный раствор оксида серебра в дальнейшем ...
... хлор вытесняет из солей бром, йод: 2KBr + Cl2 = 2KCl + Br2 бром вытесняет из солей йод: 2KI + Br2 = 2KBr + I2↓. II. Взаимодействие органическими веществами (галогенирование - присоединение галогена). Галогены взаимодействуют со всеми классами органических соединений. Рассмотрим некоторые реакции: 1. С алканами: CH3–CH3 + Cl2 → CH2Cl–CH3 + HCl хлорэтан 2. С алкенами: CH2=CH2 ...
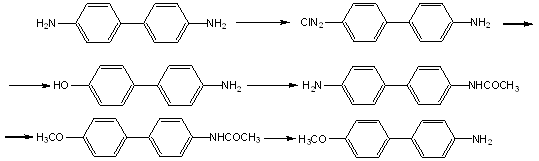
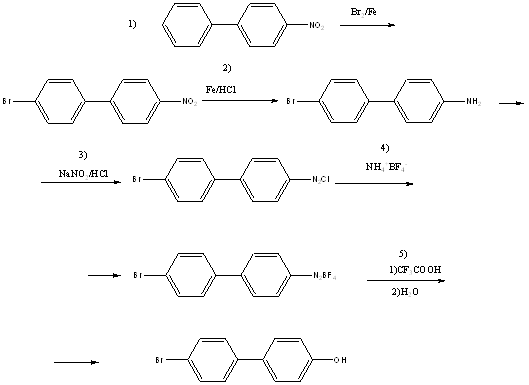
... из спирта. Получили 5,57г (выход 57%) 4-бром-4’-гидроксибифенила. т. пл. 163-1650. Лит.данные [3]: т.пл. 164-166о. 3. Обсуждение результатов Целью данной работы был синтез 4-бром-4’-гидроксибифенила. Мы рассмотрели три возможные способы его получения: 1) реакция кросс-сочетания; 2) ацилирование 4-бромбифенила с последующей реакцией Байера-Вилигера; 3) из соли 4-бромфенилдиазония. Поскольку ...








0 комментариев