На правах рукописи
ИНЖЕКЦИОННЫЕ ПРОЦЕССЫ В ЭЛЕКТРОХИМИЧЕСКИХ СИСТЕМАХ С ТВЕРДЫМ КАТИОНПРОВОДЯЩИМ ЭЛЕКТРОЛИТОМ
АВТОРЕФЕРАТ
диссертации на соискание ученой степени кандидата химических наук
2000
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы.
Ионика твердого тела, возникшая на стыке физики и химии твердого тела и электрохимии в конце 60-х годов, изучает процессы ионного транспорта в твердом теле. До последнего времени эта наука занималась в основном процессами переноса зарядов в монофазных системах. Однако в последнее время все больший интерес исследователей направлен на изучение граничных процессов.
Исследование процессов обмена основными носителями заряда между электронным и ионным проводниками, механизма переноса ионов в объеме и по поверхности полупроводниковых фаз имеют важное фундаментальное и практическое значение. Это связано как с необходимостью понимания закономерностей процессов ионного переноса в твердых телах, так и с практическим использованием процессов ионной инжекции для получения новых функциональных материалов и электрохимических систем с заданными свойствами (каталитических, сенсорных и т.п.).
Цель работы.
Изучение закономерностей протекания процессов ионной эмиссии из твердого электролита, инжекции ионов в электронный проводник, ионного обмена между твердым электролитом и электронным проводником, переноса ионов в электронном проводнике.
Научная новизна.
Впервые измерены токи эмиссии из твердых электролитов (ТЭЛ) 1,Ша20.11А12Оз и Na5Gdo.9Zro,iSi4Oi2 и контактная разность потенциалов между натрием и твердыми натрийпроводящими электролитами. Показано, что работа выхода иона Na+ из твердого электролита меньше, чем из чистого металла. Впервые исследованы процессы ионной инжекции ионов серебра и меди в твердофазных системах с использованием твердых электролитов. Показано, что токи обмена границы с интеркалатным электродом более, чем на порядок превышают токи обмена с металлическим электродом. Впервые проведено квантово-химическое моделирование миграции однозарядных катионов по поверхности рутилоподобных оксидов. Показано, что барьеры на пути миграции минимальны для катионов Na . Установлена возможность перехода поверхностной миграции протона в объемную. Экспериментально обнаружено возникновение протонной проводимости на поверхности диоксида олова и найдены условия, при которых ионная составляющая проводимости БпОг превышает 95% от общей проводимости. В распределенных структурах CsHS04 - Sn02 обнаружен максимум протонной и электронной составляющих проводимости. При изучении процессов обмена носителями заряда между натриевыми твердыми электролитами и полупроводниковыми оксидами обнаружено, что электрохимическая активность границы Sn02/Na+-T3JI по отношению к СОг и СО определяется склонностью „поверхности. ТЭЛ к гидратации.
Практическая значимость.
На основании изучения закономерностей ионного переноса между ионпроводящей и полупроводниковой фазами получены электрохимические системы, способные селективно изменять свою ЭДС при изменении концентраций Нг, СО и СОг в газовой фазе.
Разработаны методы электрохимического синтеза инжекционных электродов на основе дисульфида титана. Показана возможность их использования в качестве обратимых электродов в электрохимических устройствах различного типа. На основании полученных интеркалатных соединений созданы твердотельный переключатель и датчик влажности.
Апробация работы.
Результаты работы докладывались на 6-й Всесоюзной конференции по электрохимии (Москва), 8-й Всесоюзной конференции по физической химии и электрохимии ионных расплавов и твердых электролитов (Ленинград, 1983), 5-й Украинской конференции по электрохимии (Ужгород, 1990), Всесоюзной конференции «Микроэлектронные датчики в машиностроении», (Ульяновск, 1990), 4-й Конференции «Сенсор-91» (Ленинград, 1991), 3-м и 5-м Международным симпозиумах «Системы с быстрым ионным переносом» (Хольцау-Германия, 1991, Варшава, 1998), 1-й Европейской конференции «Ионика твердого тела» (Греция, 1994).
Публикации.
Результаты, положенные в основу диссертации, опубликованы в 11 статьях, 8 тезисах докладов на Российских и Международных конференциях и в двух авторских свидетельствах. Список основных публикаций приведен в конце автореферата.
Объем и структура работы.
Диссертация состоит из введения, восьми глав, раскрывающих основное содержание работы, выводов и списка цитируемой литературы из 93 наименований. Изложена диссертация на 108 страницах машинописного текста и содержит 38 рисунков и 17 таблиц.
На защиту выносятся:
закономерности ионной эмиссии из катионпроводящих твердых электролитов;
получение и свойства интеркалатных соединений на основе дисульфида титана;
закономерности транспорта однозарядных катионов в рутилоподобных оксидах и переноса катионов через границу твердый электролит оксид.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
В ведении осуществляется постановка задачи, сформулированы ее цели, описывается научная и практическая значимость работы.
В первой главе приводится анализ литературных данных по проблеме ионной и электронной эмиссии из твердых катионпроводящих электролитов и инжекции ионов в электродные материалы.
Рассматриваются проблемы ионного транспорта в твердых электролитах и смешанных ионно-электронных проводниках.
Во второй главе рассматриваются особенности синтеза твердых электролитов и электродных материалов, обладающих высокой ионной проводимостью, их кристаллическая структура и физические свойства. Основное внимание уделено проблемам экспериментального и теоретического исследования электрохимических систем на основе твердых электролитов. Для исследования эмиссии однозарядных катионов создана установка, позволяющая изучать термоионную эмиссию твердофазных образцов в вакууме 10»4 - 10»5 мм рт. ст. при температурах до 1000°С и ускоряющем напряжении 100-900 В.
Исследование, процессов инжекции проводили на ячейках М/М+-T3II/TiS2 (М = Си, Ag). Инжекцию ионов Ag+ в TiS2 осуществляли при постоянном напряжении дробными импульсами тока. Потенциал сульфидного электрода измеряли относительно распределенного серебряного электрода после размыкания внешней цепи и выдержки ячейки без тока в течение суток.
Для увеличения поверхности контакта М/ТЭЛ использовали электроды в виде распределенных структур: один из электродов Представлял собой смесь порошков дисульфида титана и ТЭЛ в объемном соотношении 2:3, второй - смесь порошков металла и ТЭЛ в объемном соотношении 1:1.
Зависимость Е-х (Е - потенциал, х - концентрация инжектируемого иона) для меди изучали в динамическом и квазистатическом (ступенчатом) режимах. В первом случае использовали двухкоординатный графопостроитель Н-306. Временная развертка по оси X задавалась от аналогового твердотельного интегратора с линейной E-Q характеристикой (Q - количество электричества), а на вход оси Y подавали разность потенциалов между металлическим (электрод сравнения) и сульфидным электродами. При ступенчатом режиме каждый гальваностатический импульс соответствовал примерно 0,1 атомов Си на молекулу TiS2-Контролировали изменение потенциала сульфидного электрода во времени после прерывания тока инжекции до установления стационарного состояния (экспозиция около 3 ч). Инжекцию проводили до тех пор, пока равновесный потенциал сульфидного электрода не достигал нуля. В качестве М+-ТЭЛ использовали высокопроводящие твердые электролиты СиДЬСЬЬ и RbAg4I5.
Токи обмена по иону М+ определяли методом импедансометрии. Измерения импеданса электрохимической ячейки Рг осуществляли в диапазоне частот переменного тока 0,005-500 кГц с помощью импедансметра ВМ-507. Для определения объемного сопротивления твердого электролита и расчета адсорбционных. Для изучения процессов ионной инжекцйи на поверхность и в объем полупроводниковых фаз в рамках кластерного приближения проводили квантово-химическое моделирование методом MNDO-PM3 и с использованием теории функционала плотности B3LYP. В расчетах применяли приближение Хартри-Фока-Рутана с базисом LanL2DZ(d, р) и псевдопотенциалом.
В третьей главе рассмотрены результаты экспериментального изучения процессов ионной эмиссии из твердых электролитов. Измерены токи эмиссии и проведена оценка работы выхода ионов щелочных металлов из твердых электролитов типа полиалюмината и комплексных силикатов натрия при нагревании.
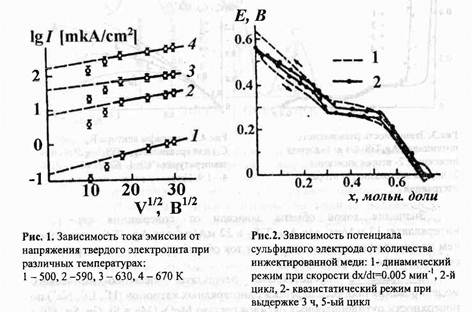
Впервые измерены токи эмиссии из твердых электролитов Ш и Nu и контактная разность потенциалов между натрием и твердыми электролитами типа Na5Si, где M=Y, Ей, Gd, Yb в интервале температур от 230 до 400°С. Показано, что работа выхода иона Na+ из твердого электролита меньше, чем из чистого металла. Плотности удельных токов насыщения Is составили для Na4 0,63 мкА/см2 (400°С, потенциал ускоряющего напряжения 1000 В) и для Na2O.10Al2O3 - 0,04 мкА/см2 (355°С, ускоряющее напряжение 900 В). С ростом температуры токи насыщения возрастают (рис. 1).
В четвертой главе представлены условия твердофазного и электрохимического синтеза интеркалатов на основе дисульфида титана.
Интеркалатные соединения дисульфида титана с серебром получали методом твердофазного синтеза по реакции: xAg + TiS2 = AgxTiS2 при 820°С. Рентгенографически выделено три фазы, различающиеся величиной стехиометрического коэффициента х.
Электрохимический синтез осуществляли путем инжекцйи меди и серебра в кристаллическую решетку сульфида титана в ячейках типа Ti/M, М+-ТЭЛ/М+-ТЭЛ/МХГП82, M+-T3JI/Ti (M=Cu, Ag). (I)
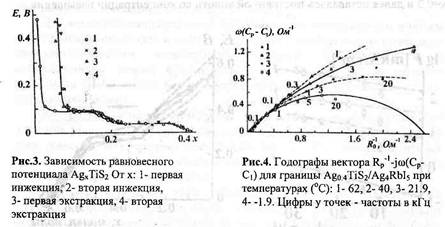
При циклировании ячейки для инжекцйи серебра наблюдается гистерезис между первым инжекционным процессом и последующими (рис.2). Количество электричества, потребляемое в первом полуцикле, существенно больше и отвечает 0,41 атомов Ag на 1 моль TiS2 , тогда как во всех последующих циклах процесс идет в интервале 0,08 < х < 0,41.
Для получения интеркалатов меди использовали два режима электрохимической инжекцйи: динамический и квазистатический (ступенчатый). Как видно из рис.3, разница между квазистатическими и динамическими кривыми Е-х относительно невелика, что свидетельствует о достаточно высокой скорости образования соединений CuxTiS2 во всем интервале составов. Характерно наличие «плато» на Е-х кривой в интервале 0,30 < х < 0,55, которое указывает на сосуществование в этом интервале составов двух» фаз: фазы I состава Cu0,3TiS2 и фазы II состава Cuo,55TiS2. Фаза II может существовать в интервале составов 0,55 < х < 0,7. При х=0,7 достигается предельное содержание меди в интеркалате. При этом составе равновесный потенциал ячейки (I) становится равным нулю.
Ионный обмен между интеркалатным соединением AgxTiS2 и ТЭЛ исследовали методом импеданса с использованием симметричной ячейки AgxTiS2/ RbAgJs/ AgxTiS2 при х=0,2 и 0,4. Поведение электродной границы описывается моделью адсорбционной релаксации двойного слоя и соответствует эквивалентной схеме обратимого по ионам Ag электрода.
В главе 5 представлены результаты квантово-химического моделирования процесса переноса однозарядных катионов (НГ, Li+, Na+) по поверхности рутилоподобных оксидов состава Ме02 (Me = Si, Ge, Sn, Pb) с полупроводниковыми свойствами. Произведен выбор кластера, адекватно описывающего поверхностные и объемные свойства оксида. Показано, что для корректного описания поведения оксида необходим кластер, состав которого превышает (Ме02)9. Поскольку основная часть расчетов производилась полуэмпирическими методами, произведено сравнение результатов на неэмпирическом и полуэмпирическом уровнях. Рассчитана ширина запрещенной зоны рассматриваемых кластеров, обнаружено хорошее совпадение между расчетными и экспериментальными данными.
Рассмотрены процессы переноса однозарядных катионов по поверхности оксидов. Показано, что на поверхности оксидов существуют поверхностные каналы миграции. Рассчитаны геометрические и энергетические параметры путей миграции катионов (рис.5). Показано, что барьеры на пути миграции катионов определяются размерами катионов, монотонно убывая по мере возрастания их радиуса, Влияние химической природы оксида, по поверхности которого протекает миграция, на процессы ионного переноса двояко. Во-первых, оно определяется размером элементарной ячейки оксида. При этом в малоразмерных оксидах затруднен транспорт катионов большого размера, а при больших расстояниях между атомами поверхности затруднен перенос катионов малого размера. Во-вторых, сильное влияние на ионную подвижность оказывает эффективный заряд иона кислорода. Чем выше этот заряд, тем больше барьеры на пути миграции катионов.
Установлено, что в отсутствие контакта полупроводникового оксида с твердым электролитом основным источником протонов на поверхности становится диссоциативная хемосорбция воды. При этом гидроксогруппы фиксируются на катионах металла кристаллической решетки, а освободившиеся протоны приобретают возможность свободного перемещения по каналам поверхности, аналогичным рассмотренным выше. Увеличение концентрации протонов на поверхности затрудняет поверхностную миграцию и создает предпосылки для перехода поверхностного протонного переноса в объемный. Барьеры на пути объемной миграции протонов ниже, чем при миграции по поверхности, однако, на пути перехода протонов с поверхности в объем находятся энергетические барьеры значительной величины.
Изучено влияние допирования оксида олова иновалентными добавками на процессы транспорта. Показано, что в присутствии сурьмы в позициях олова протонный транспорт как по поверхности, так и в объеме диоксида олова облегчается.
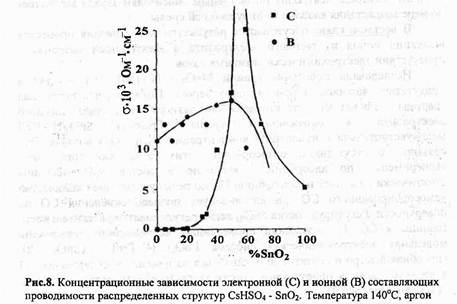
В главе 6 представлены результаты экспериментального изучения переноса протонов по поверхности и в объеме полупроводниковых оксидов в контакте с источниками протонов. Экспериментально обнаружено, что в присутствии адсорбированной воды на поверхности диоксида олова (степень заполнения поверхности не превышает 1%), проводимость диоксида олова резко повышается. Анализ годографов импеданса позволил выделить два типа процессов протонного переноса в полиметаллическом диоксиде олова - поверхностный и объемный (рис.6). По мере возрастания количества адсорбированной влаги, как и предсказывали результаты моделирования, возрастает доля объемного переноса протонов по сравнению с поверхностным. Показано, что при возникновении ионного переноса резко возрастает и электронная проводимость диоксида олова. Соотношение ионной и электронной составляющих проводимости определяется степенью заполнения поверхности водой, удельной поверхностью оксидной фазы и температурой изучаемой системы (рис.7). При оптимальных условиях ионная проводимость достигает 97-98% от общей проводимости системы, т.е. полупроводник превращается в практически чисто ионный проводник. Высокая протонная проводимость диоксида олова реализуется и в распределенных структурах CsHS04-Sn02 выше температуры перехода гидросульфата цезия в суперионное состояние (140°С). В отличие от ранее изученных распределенных систем гидросульфата цезия с оксидами кремния, алюминия и титана, нами не наблюдалось как зависимости температуры перехода системы в ионпроводящее состояние от состава распределенной системы, так и сколь либо значительного изменения общего сопротивления системы при температурах ниже температуры фазового перехода.
В интервале 140-200°С обнаружено, что суммарная проводимость распределенных структур выше проводимости отдельных фаз. Зависимость ионной и электронной составляющей проводимости от состава распределенной структуры имеет немонотонный характер. Максимумы на концентрационных зависимостях общей проводимости и ее протонной и электронной составляющих (рис. 8) наблюдаются в случае образования связной матрицы по CsHSC>4 (50% об. SnCb). Они соответствуют наибольшей величине поверхности раздела отдельных фаз, При исследовании обратимости границ РЬ02/Н+-ТЭЛ (ТЭЛ -фосфорновольфрамовая кислота и ее соли) было обнаружено, что токи обмена достигают значения 1*10»4 А/см2. Потенциал границы РЬОг/ТНГ-ТЭЛ относительно водородного электрода составляет 1,47 В, что соответствует процессу РЬ02+4Н++2е»-М>Ь2++2Н20. На основании данных о высоких токах обмена сделаны выводы о наличии процессов интеркаляции полупроводниковых рутилоподобных оксидов протонами. При этом источником протонов могут служить как протоны из твердого электролита, так и протоны, образовавшиеся при Диссоциативной хемосорбции воды. Полученные экспериментальные данные хорошо согласуются с результатами теоретического моделирования.
В главе 7 описаны результаты экспериментального исследования обмена ионами Na+ между твердыми электролитами и оксидными электродами. Методом импеданса показано, что в эквивалентной схеме ячейки имеются две параллельные цепочки, одна из которых соответствует переносу ионов натрия в объеме зерна и через контакт соседних зерен, а вторая - переносу Na+ по гидратированным границам зерен. Обратимость электродной реакции определяется переносом заряда по гидратированным границам.
Обнаружено, что в случае ТЭЛ, межзеренные границы которых не способны к гидратации, граница ТЭЛ/8п02 является, блокированной. В случае ТЭЛ, границы которых способны к гидратации, обратимость границы электрод/электролит по основным носителям заряда возрастает по мере возрастания влажности окружающей среды.
В восьмой главе обсуждаются результаты исследования процессов инжекции ионов из твердого электролита в электродный материал в присутствии электрохимически активных газов.
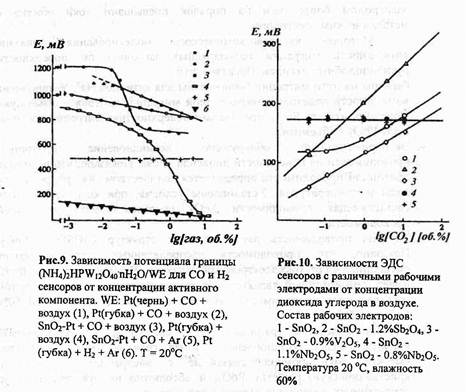
Исследовано поведение границ Ме02 / Н+-ТЭЛ на воздухе в присутствии водорода и монооксида углерода. Показано, что потенциал границы РЬО/ГЭЛ практически не зависит от состава твердого электролита и окружающей среды. Граница БпОг/КГ-ТЭЛ малочувствительна к изменению концентрации Н2 и СО в воздухе. Это связано с отсутствием хемосорбции этих газов. Как показывают эксперименты по адсорбции, введение в состав Sn02 платины практически не влияет на адсорбцию Н2, но резко увеличивает количество хемосорбированного СО и катализирует процесс окисления СО на поверхности. Регулируя состав Sn02, легко регулировать чувствительность границы к СО. На основании проведенных исследований предложена модельная электрохимическая система РЬ02/ Н+-ТЭЛ / (Sn02, Pt), способная быстро и селективно откликаться на изменение содержания СО в воздухе даже в присутствии таких газов-восстановителей, как Н2 и углеводороды (рис.9).
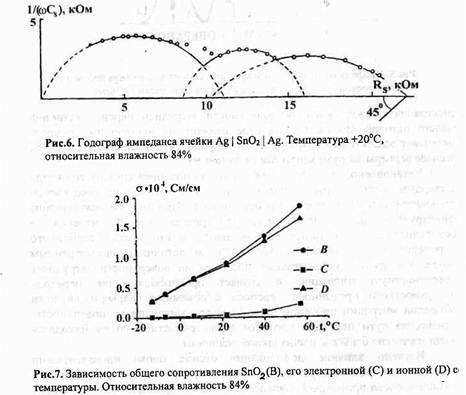
Исследовано поведение границ Ме02/ №+-ТЭЛ на воздухе в присутствии углекислого и сернистого газов. Показано, что системы, блокированные к переносу ионов Na+, не чувствительны к изменению состава газовой фазы. Сам потенциал неустойчив и чувствителен к методу изготовления границы. Системы с ТЭЛ, способными к гидратации, способны откликаться на содержание кислых газов в воздухе. Добиться селективности этих систем к отдельному газу оказалось возможным, изменяя кислотность поверхности электродов. Введение в состав Sn02 ионов, повышающих кислотность поверхности (V, Nb, Та), приводит к понижению чувствительности системы к С02 (рис. 10).
ОСНОВНЫЕ РЕЗУЛЬТАТЫ РАБОТЫ
Впервые измерены токи эмиссии из твердых электролитов Na20.11Al203 и Na5Gd0,9Zr0,iSi4O2 и контактная разность потенциалов между натрием и твердыми электролитами типа Na5MSi402, где M=Y, Eu, Gd, Yb в интервале температур от 230 до 400°С. Работа выхода иона Na+ из твердого электролита меньше, чем из чистого металла.
Впервые исследованы процессы ионной инжекции ионов серебра и меди в твердофазных системах с использованием твердых электролитов. Показано, что токи обмена границы с интеркалатным электродом более чем на порядок превышают токи обмена с металлическим электродом.
Методом квантово-химического моделирования показана возможность миграции однозарядных катионов по поверхности рутилоподобных оксидов. Показано, что барьеры на пути миграции минимальны для катионов Na+. Установлена возможность перехода поверхностной миграции протона в объемную. Показано, что для Sn02 преобладает поверхностная миграция протона, а для Pb02 - объемная.
Экспериментально обнаружено возникновение протонной проводимости на поверхности диоксида олова. Показано, что величина протонной проводимости определяется количеством адсорбированной воды и температурой, Установлены условия, при которых ионная составляющая проводимости Sn02 превышает 95% от общей проводимости.
Изучена проводимость распределенных структур CsHS04 - Sn02. Показано, что проводимость распределенных структур имеет смешанный протонно-электронный характер. Величина проводимости имеет немонотонный характер. Максимум протонной и электронной составляющих проводимости наблюдается в смеси, содержащей 50% SnC по объему.
Изучено поведение границы РЬ02 с солями фосфорвольфрамовой кислоты (ФВК). Установлено, что эта граница имеет достаточно высокие токи обмена, связанные с внедрением протонов в кристаллическую решетку РЬ02, и абсолютно не чувствительна по отношению к изменению состава газовой среды.
Показано, что эквивалентная схема импеданса электрохимической ячейки Sn02/Na+-T3/ Sn02 содержит две цепочки, одна из которых соответствует переносу Na+ в объеме зерна и через контакт соседних зерен, а вторая - переносу Na+ по гидратированным границам зерен. Электрохимическая активность границы Sn02/Na+-T3JI по отношению к С02 определяется гидратируемостью поверхности ТЭЛ и электродного материала.
На основании изучения закономерностей ионного переноса между ионпроводящей и полупроводниковой фазами получены электрохимические системы, способные селективно изменять свою ЭДС при изменении концентраций Н2, СО и С02 в газовой фазе.
Основные результаты диссертации опубликованы в следующих работах:
1. Малов Ю.И., Укше Е.А., Леонова Л.С., Букун Н.Г., Надхина СЕ. Термоионная эмиссия из твердых электролитов //Журнал физической химии. Т.56. 1982. С.1879-Ш2.
2. Вершинин Н.Н., Малов Ю.И., Надхина С.Е., Укше Е.А. Электрохимическая инжекция меди в дисульфид титанаЮлектрохимия. Т. 19. 1983.?:567-569.
3. Вершинин Н.Н., Малов Ю.И., Надхина СЕ. Электрохимическое исследованиё'сульфидов меди //Электрохимия. Т.2]. 1985. С.111-113.
4. Леонова Л.С., Коростелева А.И., Надхина СЕ. Электропроводность твердых гидратов вольфрамофосфата аммония //Электрохимия. Т.26. 1990. С. 1511 -1513 .
5. Добровольский Ю.А., Леонова Л.С, Укше Е.А., Ермолаева СИ., Надхина С. Ev Определение углекислого газа в газовых средах //Метрология. Т.6. 1991. С.38-45.
6. Dobrovolsky Уи.Д., Leonova L.S., Nadhina S. Е. Working electrodes for low-temperature C02- sensors //Ionics. V.l. 1995. P.228- 235 .
7. Dobrovolsky Yu.A., Leonova L S., Nadhina S.E., Panina N. G. Low-temperature proton conductivity in hydrated and non-hydrated tin dioxide //Solid State Ionics. V.l 19. 1999. P.275-279.
8. ЗюбинаТ.С, Добровольский Ю.А., Надхина СЕ. Квантово-химиЧеское моделирование взаимовлияния протонов при движении по поверхности кристалла диоксида олова //Журнал неорганической химии. Т.44.1999. С.571-576.
9. Надхина С.Е., Букун Н.Г., Михайлова A.M. Химическая и электрохимическая интеркаляция TiS2 ионами Си+ и Ag+ //Сборник материалов 5-го международного совещания «Фундаментальные проблемы ионики твердого тела». Черноголовка, 2000. С. 135.
10. Зюбина Т.С, Укше А.Е., Леонова Л.С, Добровольский Ю.А., Надхина СЕ. Протонный перенос в диоксиде олова: квантово-химическое рассмотрение //Сборник материалов 5-го международного совещания «Фундаментальные проблемы ионики твердого тела». Черноголовка, 2000. С18.
11. Домашнев Д.И., Добровольский Ю.А., Леонова Л.С, Надхина СЕ. Поведение распределенных систем CsHSO,rSn02 //Сборник материалов 5-го международного совещания «Фундаментальные проблемы ионики твердого тела». Черноголовка, 2000. С.83.
12. Надхина СЕ., Малов Ю.И. Инжекция ионов меди в сульфиды переходных металлов из твердых электролитов //Тезисы докладов 6-й Всесоюзной конференции по электрохимии. Москва, 1982. С220.
13. Надхина С.Е., Вершинин Н.Н., Малов Ю.И. Электрохимическое исследование смешанных сульфидов CuxAgyS //Тезисы докладов 8-й Всесоюзной конференции по физической химии и электрохимии ионных расплавов и твердых электролитов. Ленинград, 1983. С.104-106.
14. Леонова Л.С, Ермолаева СИ., Добровольский Ю:А., Укше Е.А., НаДхина СЕ. Использование суперионных сенсоров для определения концентрации ССЬ в газовой среде //Тезисы Всесоюзного совещания «Микроэлектронные датчики в машиностроении». Ульяновск, 1990. С46.
15. Сазонов Е.И., Ганин В.В., Надхина С.Е., Добровольский Ю.А., Дерлюкова Л.Е. Детектирование диоксида серы в газовых средах //Тезисы Всесоюзного совещания «Микроэлектронные датчики в машиностроении». Ульяновск, 1990. С.35.
16. Леонова Л:С, Надхина СЕ;, Ермолаева СИ., Добровольский Ю.А. Использование суперионных сенсоров для определения •' концентрации СОг в газовой фазе //Тезисы 5-й Украинской конференции по электрохимии. Электрохимическая экология. Т.2. Ужгород, 1990. С.32-33.
17. Leonova L.S., Dobrovolsky Ytl.A., Nadhina S.E. The Effect of working electrode composition on the properties of low-temperature СОг sensor. //1-st Euroconference on Solid State Ionics. Zakynthos. Ionian Sea. Greeece, 1994. P.33.
0 комментариев