Химические свойства лантана
Лантан
| 57 | |
| La | 2 9 18 18 8 2 |
| ЛАНТАН | |
| 138,905 | |
| 5d16s2 | |
Самое знаменательное в элементе №57, несомненно, то, что он возглавляет шеренгу из 14 лантаноидов – элементов с чрезвычайно сходными свойствами. Лантан и лантаноиды – всегда вместе: в минералах, в нашем представлений, в металле. На Всемирной выставке в Париже в 1900 г. были впервые продемонстрированы образцы некоторых чистых, как считалось, лантаноидов. Но можно не сомневаться, что в каждом образчике, независимо от ярлыка, присутствовали и лантан, и церий, и неодим с празеодимом, и самые редкие из лантаноидов – тулий, гольмий, лютеций. Самые редкие, если не считать «вымершего» и воссозданного в ядерных реакциях элемента №61 – прометия. Впрочем, будь у прометия стабильные изотопы, он тоже присутствовал бы в любом образце любого редкоземельного элемента.
Лишь в последние десятилетия развитие науки и техники достигло того уровня, при котором человечество смогло поставить себе на службу индивидуальные качества каждого (или почти каждого) из лантаноидов, хотя, как и прежде, одним из самых массовых и дешевых редкоземельных продуктов остается мишметалл – «природный сплав» лантана и лантаноидов... Поэтому было бы логично посвятить лишь половину этого рассказа непосредственно элементу №57, а другую половину – редкоземельной «команде» в целом. Разумеется, каждый из лантаноидов – как химический индивидуум – заслуживает самостоятельного рассказа; здесь же – об их «предводителе» и об общем для всех них. Кроме лантана и лантаноидов, к редкоземельным элементам относят скандий и иттрий.
Лантан без лантаноидов
Как ни грустно сознавать, герой нашего рассказа – личность вполне заурядная. Это металл, обыкновенный по внешнему виду (серебристо-белый, покрытый сероватой окисной пленкой) и по физическим свойствам: температура плавления 920, кипения 3469°C; по прочности, твердости, электропроводности и прочим характеристикам металл лантан всегда оказывается в середине таблиц. Обыкновенен лантан и по химическим свойствам. В сухом воздухе он не изменяется – окисная пленка надежно защищает от окисления в массе. Но если воздух влажен (а в обычных земных условиях он влажен почти всегда), металлический лантан постепенно окисляется до гидроокиси. La(OH)3 – основание средней силы, что опять-таки характерно для металла-«середнячка».
Что еще можно сказать о химических свойствах лантана? В кислороде при нагревании до 450°C он сгорает ярким пламенем (при этом выделяется довольно много тепла). Если же прокаливать его в атмосфере азота, образуется черный нитрид. В хлоре лантан загорается при комнатной температуре, а с бромом и иодом реагирует лишь при нагревании. Хорошо растворяется в минеральных кислотах, с растворами щелочей не реагирует. Во всех соединениях лантан проявляет валентность 3+. Словом, металл как металл – и по физическим свойствам, и по химическим.
Единственная, пожалуй, отличительная черта лантана – характер его взаимодействия с водородом. Реакция между ними начинается уже при комнатной температуре и идет с выделением тепла. Образуются гидриды переменного состава, поскольку одновременно лантан поглощает водород – тем интенсивнее, чем выше температура.
Так же взаимодействуют с водородом и лантаноиды. Один из них – церий – даже используют как газопоглотитель в электровакуумной промышленности и в металлургии.
Здесь мы подошли к одной из важных частей нашего рассказа, к теме «Лантан и церий», и в связи с ней – к истории лантана.
По распространенности в природе, по масштабам производства, по широте использования лантан уступает своему ближайшему аналогу – первому из лантаноидов. «Родоначальник» и – вечно второй, таково положение лантана в его семействе. И когда редкоземельные элементы по совокупности свойств стали делить на две подгруппы, лантан был отнесен в подгруппу, название которой дали в честь церия... И открыт лантан был после церия, как примесь к церию, в минерале церите. Вот эта история, история об учителях и учениках.
В 1803 г. 24-летний шведский химик Йене Якоб Берцелиус вместе со своим учителем Хизингером исследовал минерал, известный теперь под названием церита. В этом минерале была обнаружена открытая Гадолином в 1794 г. иттриевая земля и еще одна редкая земля, очень похожая на иттриевую. Ее назвали цериевой. Почти одновременно с Берцелиусом цериевую землю открыл знаменитый немецкий химик Мартин Клапрот.
К работе с этим веществом Берцелиус вернулся через много лет, будучи уже именитым ученым. В 1826 г. Карл Мозандер – ученик, ассистент и один из близких друзей Берцелиуса – исследовал цериевую землю и заключил, что она неоднородна, что в ней, помимо церия, содержится еще один, а может быть и не один, новый элемент. Но, чтобы проверить это предположение, нужно было много церита. Доказать сложность цериевой земли Мозандеру удалось лишь в 1839 г.
Интересно, что годом раньше неизвестный среди химиков студент Эрдманн нашел в Норвегии новый минерал и назвал его в честь своего учителя Мозандера – мозандеритом. Из этого минерала также были выделены две редкие земли – цериевая и новая.
Новый элемент, обнаруженный в церите и мозандерите, по предложению Берцелиуса назвали лантаном. Название с намеком: оно происходит от греческого лбнибнейн – скрываться, забываться. Лантан, содержащийся в церите, успешно скрывался от химиков в течение 36 лет!
Долгое время считали, что лантан двухвалентен, что он – аналог кальция и других щелочноземельных металлов, а его атомный вес равен 90...94. В правильности этих цифр не сомневались до 1869 г. Менделеев же увидел, что во II группе периодической системы редкоземельным элементам нет места и поставил их в III группу, приписав лантану атомный вес 138...139. Но правомерность такого перемещения еще надо было доказать. Менделеев предпринял исследование теплоемкости лантана. Полученная им величина прямо указывала на то, что этот элемент должен быть трехвалентным...
Металлический лантан, разумеется, далеко не чистый, впервые был получен Мозандером при нагревании хлористого лантана с калием.
В наше время в промышленных масштабах получают лантан чистотой более 99%. Проследим, как это делается, но прежде познакомимся с главными минералами лантана и первыми стадиями сложнейшего процесса разделения редкоземельных элементов.
Уже упоминалось, что в минералах лантан и лантаноиды неизменно сопутствуют друг другу. Есть минералы селективные, в которых доля того или иного редкоземельного элемента больше, чем обычно. Но нет минералов чисто лантановых или чисто цериевых, не говоря уже о других лантаноидах. Примером селективного лантанового минерала может служить давидит, в котором до 8,3% La2O3 и лишь 1,3% окиси церия. Но получают лантан преимущественно из монацита и бастнезита, как, впрочем, и церий, и все остальные элементы цериевой подгруппы.
Монацит – тяжелый блестящий минерал, обычно желто-бурый, но иногда и других цветов, поскольку постоянством состава он не отличается. Точнее всего его состав описывает такая странная формула: (РЗЭ)PO4. Она означает, что монацит – фосфат редкоземельных элементов (РЗЭ). Обычно в монаците 50...68% окислов РЗЭ и 22...31,5% P2O5. А еще в нем до 7% двуокиси циркония, 10% (в среднем) двуокиси тория и 0,1...0,3% урана. Эти цифры со всей очевидностью, показывают, почему так тесно переплелись пути редкоземельной и атомной промышленности.
Смешанный металл редких земель – мишметалл – и смесь их окислов начали применять в конце прошлого века, а в начале нынешнего в связи с ними был продемонстрирован выдающийся образец международного воровства. Немецкие суда, доставлявшие грузы в Бразилию, собираясь в обратный путь, заполняли трюмы песком с пляжей Атлантического побережья этой страны, причем из определенных мест. Капитаны заявляли, что песок – это просто балласт, необходимый для большей устойчивости судна. В действительности же они, выполняя заказы германских промышленников, крали ценное минеральное сырье – прибрежные пески штата Эспириту-Санту, богатые монацитом...
Монацитовые россыпи распространены по берегам рек, озер и морей на всех континентах. В начале века (данные за 1909 г.) 92% мировой добычи редкоземельного сырья, и прежде всего монацита, приходилось на долю Бразилии. Спустя десять лет центр тяжести переместился на тысячи километров к востоку (или к западу, смотря как считать) – в Индию. После 1950 г. в связи с развитием атомной промышленности гегемоном среди капиталистических стран в добыче и переработке редкоземельного сырья стали Соединенные Штаты.
Разумеется, нашей стране и другим странам социалистического содружества пришлось развивать свою редкоземельную промышленность, изыскивать свои сырьевые ресурсы.
Проследим же в общих чертах путь от монацитового песка до лантана.
Хотя песок и называют монацитовым, монацита в нем немного – доли процента. К примеру, в известных монацитовых россыпях Айдахо (США) тонна песка содержит лишь 330 г монацита. Поэтому прежде всего получают монацитовый концентрат.
Первая стадия концентрирования происходит уже на драге. Плотность монацита 4,9...5,3, а обычного песка – в среднем 2,7 г/см3. При такой разнице в весе гравитационное разделение не представляет особого труда. Но, кроме монацита, в тех же песках есть другие тяжелые минералы. Поэтому, чтобы получить монацитовый концентрат чистотой 92...96%, применяют комплекс гравитационных, магнитных и электростатических методов обогащения. В результате попутно получают ильменитовый, рутиловый, цирконовый и другие ценные концентраты.
Как и всякий минерал, монацит надо «вскрыть». Чаще всего монацитовый концентрат обрабатывают для этого концентрированной серной кислотой. Распространен также щелочной способ вскрытия монацита. Образующиеся сульфаты редкоземельных элементов и тория выщелачивают обычной водой. После того как они перейдут в раствор, в осадке остаются кремнезем и не отделившаяся на предыдущих стадиях часть циркона.
На следующей стадии разделения извлекают короткоживущий мезоторий (радий-228), а затем и сам торий – иногда вместе с церием, иногда отдельно. Отделение церия от лантана и смеси лантаноидов не особенно сложно: в отличие от них, он способен проявлять валентность 4+ и в виде гидроокиси Ce(OH)4 переходить в осадок, тогда как его трехвалентные аналоги остаются в растворе. Отметим только, что операция отделения церия, как, впрочем, и предыдущие, проводится многократно – чтобы как можно полнее «выжать» дорогой редкоземельный концентрат.
После того как выделен церий, в растворе больше всего лантана (в виде нитрата La(NO3)3, так как на одной из промежуточных стадий серная кислота была заменена азотной, чтобы облегчить дальнейшее разделение). Из этого раствора и получают лантан, добавляя аммиак, нитраты аммония и кадмия. В присутствии Cd(NO3)2 разделение более полно. С помощью этих веществ все лантаноиды переходят в осадок, в фильтрате же остаются лишь кадмий и лантан. Кадмий осаждают сероводородом, отделяют осадок, а раствор нитрата лантана еще несколько раз очищают дробной кристаллизацией от примесей лантаноидов.
В конечном счете обычно получают хлорид лантана LaCl3. Электролиз расплавленного хлорида дает лантан чистотой до 99,5%. Еще более чистый лантан (99,79% и выше) получают кальциетермическим способом. Такова классическая традиционная технология.
Как видим, получение элементарного лантана – дело сложное.
Разделение лантаноидов – от празеодима до лютеция – требует еще больших затрат сил и средств, и времени, разумеется. Поэтому в последние десятилетия химики и технологи многих стран мира стремились создать новые, более совершенные методы разделения этих элементов. Такие методы – экстракционные и ионообменные – были созданы и внедрены в промышленность. Уже в начале 60-х годов на установках, работающих по принципу ионного обмена, достигли 95%-го выхода редкоземельных продуктов чистотой до 99,9%.
К 1965 г. внешнеторговые организации нашей страны могли предложить покупателям все лантаноиды в виде металлов чистотой выше 99%. Кроме прометия, разумеется, хотя радиоактивные препараты этого элемента – продукты ядерного распада урана – тоже стали вполне доступны.
В каталоги «Техснабэкспорта» вошли также около 300 химически чистых и особо чистых соединений лантана и лантаноидов. Это свидетельство высокого уровня развития советской редкоземельной промышленности.
Но вернемся к лантану.
Коротко о применении лантана и его соединений
В качестве легирующего металла чистый лантан почти не применяют, используя для этого более дешевый и доступный церий или мишметалл, – легирующее действие лантана и лантаноидов практически одинаково.
Выше упоминалось, что иногда лантан из смеси извлекают методом экстракции, используя разную растворимость некоторых (в основном комплексных) соединений редкоземельных элементов в органических растворителях. Но бывает, что в качестве экстрагента используют сам элемент №57. Расплавленным лантаном экстрагируют плутоний из жидкого урана. Здесь еще одна точка соприкосновения атомной и редкоземельной промышленности.
Намного шире используют окись лантана La2O3. Этот белый аморфный порошок, нерастворимый в воде, но растворимый в кислотах, стал важным компонентом оптических стекол. Фотообъективы знаменитой фирмы «Кодак» содержат от 20 до 40% La2O3. Благодаря добавкам лантана удалось уменьшить размеры объектива при той же светосиле, намного улучшить качество цветной съемки. Известно, что во время второй мировой войны лантановые стекла применяли в полевых оптических приборах. Лучшие отечественные фотообъективы, например «Индустар-61ЛЗ», тоже сделаны из лантанового стекла, а одна из лучших наших любительских кинокамер так и называется «Лантан»... В последнее время лантановое стекло идет также на изготовление лабораторной посуды. Окись лантана придает стеклу не только ценные оптические свойства, но и большую термостойкость и кислотоупорность.
Вот, пожалуй, все главное, что можно рассказать о лантане без лантаноидов, хотя от принципа «без» кое-где нельзя было не отступить...
Лантан и его команда
Сравнение лантана и лантаноидов со спортивной командой, возможно, кому-то покажется надуманным. Однако это сравнение ничуть не крамольнее таких известных определений, как «семейство лантаноидов» или «химические близнецы». Судите сами: у лантана и его команды единая форма (серебристо-белого цвета) и, как у хоккеистов, у всех есть защитная амуниция (из окисных пленок). Всем им природой отпущено примерно поровну (сходство предельно велико), но, как и в спорте, в силу разных причин «способности» реализуются в не одинаковой мере: одни «играют» лучше, другие хуже... И конечно, у каждого члена этой команды свои излюбленные «финты» и «приемы» – ферромагнитность гадолиния, например.
И по химическим свойствам лантаноиды все-таки не близнецы – иначе не удалось бы их разделить. Как в хорошей спортивной команде, они едины в главном и индивидуальны в частностях. Что же касается числа участников, то в разных играх разное число игроков, 14 – в пределах нормы...
Правда, было время, когда в эту «команду» рекомендовали почти полсотни кандидатов. Число открываемых лантаноподобных элементов росло с катастрофической быстротой. В составленном профессором Н.А. Фигуровским списке ложно открытых элементов больше всего лжелантаноидов. Ошибок не избежали даже крупные ученые – Мозандер, Лекок де Буабодран, Ауэр фон Вельсбах, Крукс, Урбен.
Непериодичность свойств лантана и его команды, выпадающей из строгой последовательности периодической системы, доставляла неприятности Менделееву. Но со временем все разрешилось. Вынести лантаноиды за пределы основной части таблицы первым предложил профессор Пражского университета Богуслав Францевич Браунер.
«Надо быть таким знатоком «редких земель», каков Б.Ф. Браунер, чтобы разобраться в этом сложном, трудном и еще едва ли сколько-либо законченном предмете, в котором проверка затруднена не только своеобразностью и сходственностью многих начальных отношений, но и трудностями в получении самого природного материала», – писал Менделеев в 1902 г.
«Что касается систематики элементов редких земель и их места в периодической системе, то в настоящее время можно с уверенностью считать, что скандий, иттрий и лантан стоят в четных рядах III группы, как это следует из их атомных весов и объема их окисей... Прочие элементы редких земель образуют, вероятно, междупериодическую группу или узел в системе, где они следуют друг за другом по величине атомных весов». Это слова Браунера из статьи «Элементы редких земель», написанной для предпоследнего (1903 г.) прижизненного издания менделеевских «Основ химии».
Распутать «узел в системе» окончательно удалось только после того, как в основу менделеевской таблицы был положен новый, физически более точный критерий – заряд атомного ядра. Тогда стало ясно, что между лантаном и танталом могут поместиться всего 15 элементов, причем последний должен быть аналогом циркония. Этот элемент – гафний – был открыт Костером и Хевоши в 1923 г.
Последний (по атомным номерам) лантаноид, лютеций, был обнаружен раньше – в 1907 г.
Причины общности свойств лантана и лантаноидов естественно искать в строении электронных оболочек их атомов.
По законам квантовой механики электроны могут вращаться вокруг ядер не по любым орбитам. Они как бы распределяются по слоям – оболочкам. Емкость этих оболочек, максимальное число электронов в них, определяется формулой ne = 2N2, где ne – число электронов, a N – номер оболочки, считая от ядра. Отсюда следует, что на первой оболочке может быть всего два электрона, на второй – восемь, на третьей – восемнадцать, на четвертой – тридцать два и т.д.
Уже в четвертом периоде таблицы Менделеева, начиная со скандия, «очередные» электроны попадают не в наружный четвертый слой, а в предыдущий. Именно поэтому у элементов с атомными номерами от 12 до 30 разница в свойствах не такая резкая, как у более легких элементов. Подобная же картина наблюдается в пятом периоде. И здесь, начиная с иттрия, новые электроны заполняют не пятую, а предпоследнюю, четвертую оболочку – образуется еще один ряд так называемых переходных металлов.
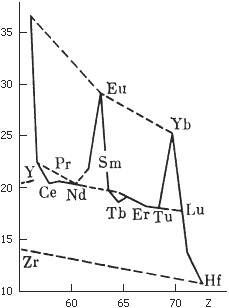
Рис. 3. Кривая атомных объемов редкоземельных элементов. На ней два максимума, образуемых элементами, проявляющими валентность 2+; напротив, элементы, которые могут быть четырехвалентными, имеют минимальные атомные объемы
Перенеся эту аналогию на шестой период, было бы логично предположить, что, начиная с лантана (он аналог скандия и иттрия), и здесь будет происходить то же самое. Электроны, однако, не считаясь с нашей логикой, заполняют здесь не предпоследнюю, а третью снаружи оболочку, благо на ней есть вакансии. Согласно формуле ne = 2N2, на этой оболочке – четвертой от ядра – может быть 32 электрона. Сюда, за редким исключением, и попадают «новые» электроны очередных лантаноидов. А поскольку химические свойства элемента определяются прежде всего строением наружных электронных оболочек, свойства лантаноидов оказываются еще более близкими, чем свойства переходных металлов.
Как и положено элементам III группы, лантаноиды обычно трехвалентны. Но некоторые из них могут проявлять и другую валентность: церий, празеодим и тербий – 4+; самарий, европий и иттербий – 2+.
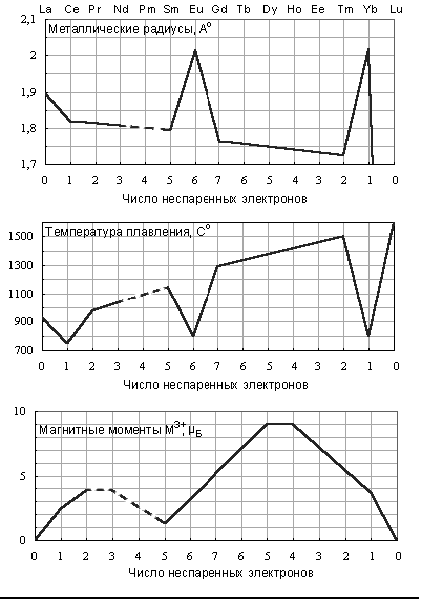
Аномальные валентности лантаноидов исследовал и объяснил немецкий химик Вильгельм Клемм. По рентгеновским спектрам он определил основные параметры их кристаллов и атомные объемы. На кривой атомных объемов явно выражены максимумы (европий, иттербий) и менее резко – минимумы (церий, тербий). Празеодим и самарий тоже выпадают, хотя и не так сильно, из ряда, определяемого плавно ниспадающей кривой. Поэтому первый «тяготеет» к малообъемным церию и тербию, а второй – к крупным европию и иттербию. Элементы с большими атомными объемами крепче удерживают электроны, и потому бывают лишь трех- или даже двухвалентными. В «малообъемных» атомах, напротив, один из «внутренних» электронов заключен в оболочке недостаточно прочно – потому атомы церия, празеодима и тербия могут быть четырехвалентными.
В работах Клемма дано и физическое обоснование давно сложившегося разделения редкоземельных элементов на две подгруппы – цериевую и иттриевую. В первую входят лантан и лантаноиды от церия до гадолиния, во вторую – иттрий и лантаноиды от тербия до лютеция. Отличие между элементами двух этих групп – направление спинов у электронов, заполняющих главную для лантаноидов четвертую оболочку.
Спины – собственные моменты количества движения электронов – у первых имеют один и тот же знак; у вторых же половина электронов имеет спины одного знака, а половина – другого.
Но хватит об аномалиях, объяснимых только с помощью квантовой механики, – вернемся к закономерностям.
Когда речь идет о лантаноидах, закономерности тоже порой кажутся алогичными. Пример тому – лантаноидное сжатие.
Лантаноидным сжатием называют открытое норвежским геохимиком Гольдшмидтом закономерное уменьшение размеров трехвалентного иона редкоземельных элементов – от лантана к лютецию. Казалось бы, все должно быть наоборот: в ядре атома церия на один протон больше, чем в ядре атома лантана; ядро празеодима больше, чем ядро церия, и так далее. Соответственно растет и число электронов, вращающихся вокруг ядра. И если представить атом таким, как его обычно рисуют на схемах, – в виде маленького диска, окруженного вытянутыми орбитами невидимых электронов, орбитами разных размеров, то, очевидно, прибыль электронов должна была бы увеличить размеры атома в целом. Или, если отбросить наружные электроны, число которых может быть неодинаковым, такая же закономерность должна наблюдаться в размерах трехвалентных ионов лантана и его команды.
Истинное положение вещей иллюстрирует диаграмма лантаноидного сжатия. Радиус трехвалентного иона лантана равен 1,22 Ǻ, а такого же иона лютеция – всего 0,99 Ǻ. Все не по логике, а как раз наоборот. Однако до физического смысла явления лантаноидного сжатия докопаться нетрудно и без квантовой механики, достаточно лишь вспомнить основные законы электромагнетизма.
Заряд ядра и число электронов вокруг него растут параллельно. Сила притяжения между разноименными зарядами тоже растет; более тяжелое ядро сильнее притягивает электроны, укорачивает их орбиты. А поскольку в атомах лантаноидов наиболее насыщены электронами глубинные орбиты, электрическое притяжение оказывает еще более сильное действие.
Близость ионных радиусов и общность химических свойств – вот главные причины совместного присутствия лантаноидов в минералах.
О минералах редких земель
О главном из них – монаците – рассказано выше. Второй по важности редкоземельный минерал – бастнезит – во многом похож на него. Бастнезит тоже тяжелый, тоже блестящий, тоже не постоянен по окраске (чаще всего светло-желтый). Но химически с монацитом его роднит только большое содержание лантана и лантаноидов. Если монацит – фосфат, то бастнезит – фторокарбонат редких земель, его состав обычно записывают так: (La, Ce)FCO3. Но, как часто бывает, формула минерала не полностью отражает его состав. В данном случае она указывает лишь на главные компоненты: в бастнезите 36,9...40,5% окиси церия и почти столько же (в сумме) окислов лантана, празеодима и неодима. Но, конечно, в нем есть и остальные лантаноиды.
Кроме бастнезита и монацита, практически используют, хотя и ограниченно, еще несколько редкоземельных минералов, в частности гадолинит, в котором бывает до 32% окислов РЗЭ цериевой подгруппы и 22...50% – иттриевой. В некоторых странах редкоземельные металлы извлекают при комплексной переработке лопарита и апатита.
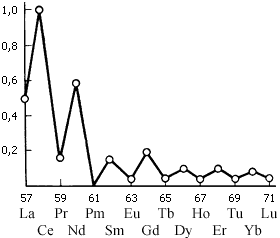
Рис. 4. Относительное содержание лантаноидов в земном коре. Закономерность: четные распространены больше нечетных
Всего известно около 70 собственно редкоземельных минералов и еще около 200 минералов, в которые эти элементы входят как примеси. Это свидетельствует о том, что «редкие» земли вовсе не такие уж редкие, а это старинное общее название скандия, иттрия и лантана с лантаноидными – не более чем дань уважения прошлому. Они не редки – церия в земле больше, чем свинца, а самые редкие из редкоземельных распространены в земной коре намного больше, чем ртуть. Все дело в рассеянности этих элементов и сложности отделения их один от другого. Но, конечно, лантаноиды распространены в природе не одинаково. Элементы с четными атомными номерами встречаются значительно чаще, чем их нечетные соседи. Это обстоятельство, естественно, сказывается на масштабах производств и ценах на редкоземельные металлы. Самые труднодоступные лантаноиды – тербий, тулий, лютеций (заметьте, все это лантаноиды с нечетными атомными номерами) – стоят дороже золота и платины. А цена церия более 99%-ной чистоты – всего 55 рублей за килограмм (данные 1970 г.). Для сравнения укажем, что килограмм мишметалла стоит 6...7 рублей, а ферроцерия (10% железа, 90% редкоземельных элементов, в основном церия) – всего пять. Масштабы использования РЗЭ, как правило, пропорциональны ценам...
Лантаноиды в практике
Осенью 1970 г. Ученый совет Института минералогии, геохимии и кристаллохимии редких элементов АН СССР собрался на расширенное заседание с довольно необычной повесткой дня. Обсуждались возможности редкоземельных элементов «в свете проблем сельского хозяйства».
Вопрос о влиянии этих элементов на живые организмы возник не случайно. С одной стороны, известно, что редкие земли часто входят как примесь в состав важнейших для агрохимии минералов – фосфоритов и апатита. С другой стороны, выявлены растения, могущие служить биохимическими индикаторами лантана и его аналогов. Так, например, в золе листьев южного ореха гикори до 2,5% редкоземельных элементов. Повышенная концентрация этих элементов обнаружена также в сахарной свекле и люпине. Содержание редкоземельных элементов в почве тундр достигает почти 0,5%.
Маловероятно, чтобы эти распространенные элементы не влияли на развитие растений, а возможно, и организмов, стоящих на других ступенях лестницы эволюции. Еще в середине 30-х годов советский ученый А.А. Дробков исследовал влияние редких земель на разные растения. Он экспериментировал с горохом, репой и другими культурами, вводил редкие земли вместе с бором, марганцем или без них. Результаты опытов говорили, что редкие земли нужны для нормального развития растений... Но прошло четверть века, прежде чем эти элементы стали относительно доступны. Окончательный ответ на вопрос о биологической роли лантана и его команды еще предстоит дать.
Металлурги в этом смысле значительно обогнали агрохимиков. С лантаном и его командой связано одно из самых значительных событий последних десятилетий в черной металлургии.
Высокопрочный чугун обычно получали, модифицируя его магнием. Физический смысл этой добавки станет ясным, если вспомнить, что в чугуне 2...4,5% углерода в виде чешуйчатого графита, который и придает чугуну главный его технический недостаток – хрупкость. Добавка магния заставляет графит перейти в более равномерно распределяющуюся в металле шаровидную или глобулярную форму. В результате значительно улучшается структура, а с ней и механические свойства чугуна. Однако легирование чугуна магнием требует дополнительных затрат: реакция идет очень бурно, расплавленный металл брызжет во все стороны, в связи с чем приходилось сооружать для этого процесса специальные камеры.
Редкоземельные металлы действуют на чугун аналогично: «убирают» окисные примеси, связывают и выводят серу, способствуют переходу графита в глобулярную форму. И при этом не требуют специальных камер – реакция протекает спокойно. А результат?
На тонну чугуна вводят всего 4 кг (0,4%) сплава ферроцерия с магнием, и прочность чугуна увеличивается вдвое! Такой чугун во многих случаях можно использовать вместо стали, в частности при изготовлении коленчатых валов. Мало того, что высокопрочный чугун на 20...25% дешевле стальных отливок и в 3...4 раза дешевле стальных поковок. Стойкость против истирания у чугунных шеек валов оказалась в 2...3 раза выше, чем у стальных. Коленчатые валы из высокопрочного чугуна уже работают в тепловозах и других тяжелых машинах.
Редкоземельные элементы (в виде мишметалла и ферроцерия) добавляют и в сталь разных сортов. Во всех случаях эта добавка работает как сильный раскислитель, превосходный дегазатор и десульфатор. В некоторых случаях редкими землями легируют... легированную сталь. Хромоникелевые стали трудно прокатывать – всего 0,03% мишметалла, введенные в такую сталь, намного увеличивают ее пластичность. Это облегчает прокатку, изготовление поковок, обработку металла резанием.
Редкоземельные элементы вводят и в состав легких сплавов. Известен, например, жаропрочный сплав алюминия с 11% мишметалла. Добавки лантана, церия, неодима и празеодима позволили в три с лишним раза поднять температуру размягчения магниевых сплавов и одновременно повысили их коррозионную стойкость. После этого сплавы магния с редкоземельными элементами стали применять для изготовления деталей сверхзвуковых самолетов и оболочек искусственных спутников Земли.
Редкоземельные добавки улучшают свойства и других важных металлов – меди, хрома, ванадия, титана... Не удивительно, что металлурги год от года все шире используют редкоземельные металлы.
Лантан и его аналоги нашли применение и в других областях современной техники. В химической и нефтяной промышленности они (и их соединения) выступают в качестве эффективных катализаторов, в стекольной – как красители и как вещества, придающие стеклу специфические свойства. Разнообразно применение лантаноидов в атомной технике и связанных с нею отраслях. Но об этом – позже, в разделах, посвященных каждому из лантаноидов. Укажем только, что даже созданный искусственно прометий нашел применение: энергию распада прометия-147 используют в атомных электрических батарейках. Одним словом, время безработицы редкоземельных элементов закончилось давно и бесповоротно.
Не надо считать, однако, что все проблемы, связанные с «узлом» в периодической системе, уже разрешены. В наши дни особенно актуально звучат слова Дмитрия Ивановича Менделеева о «редких землях»: «Тут скопилось за последние годы очень много нового»... Однако считать, что познано все и вся, что редкоземельная тематика себя исчерпала, могут только дилетанты. Специалисты же, напротив, уверены, что познание лантана и его команды только начинается, что эти элементы еще не раз удивят научный мир. А может, – не только научный.
Реакторный яд
Природный лантан состоит из двух изотопов с массовыми числами 138 и 139, причем первый (его доля всего 0,089%) радиоактивен. Он распадается путем К-захвата с периодом полураспада 3,2·1011 лет. Изотоп лантан-139 стабилен. Между прочим, он образуется в атомных реакторах при распаде урана (6,3% массы всех осколков). Этот изотоп считается реакторным ядом, поскольку он довольно активно захватывает тепловые нейтроны, что характерно и для лантаноидов. Из искусственных изотопов лантана наибольший интерес представляет лантан-140 с периодом полураспада 40,22 часа. Этот изотоп применяют в качестве радиоактивного индикатора при изучении процессов разделения лантана и лантаноидов.
Какое из трех?
Элементы, следующие за лантаном, называют редкоземельными, или лантанидами, или лантаноидами. Какое из этих названий наиболее оправданно? Термин «редкие земли» появился в XVIII в. Теперь его относят к окислам скандия, иттрия, лантана и его аналогов; первоначально же этот термин имел более широкий смысл. «Землями» вообще называли все тугоплавкие окислы металлов. По отношению к элементам с атомными номерами от 57 до 71 это справедливо: температура плавления La2O3 – около 2600°C. В чистом виде многие из этих «земель» редки и поныне. Но о редкости редкоземельных элементов в земной коре говорить уже не приходится...
Термин «лантаниды» ввели для того, чтобы показать, что следующие четырнадцать элементов идут за лантаном. Но тогда с равным успехом фтор можно назвать кислородидом (или оксидом) – он же следует за кислородом, а хлор – сульфидом... Но в понятия «сульфид», «фосфид», «гидрид», хлорид» и так далее химия издавна вложила другой смысл. Поэтому термин «лантаниды» большинство ученых считают неудачным и пользуются им все реже.
«Лантаноиды» – более оправданно. Окончание «оид» указывает на подобие. «Лантаноиды» – значит «лантаноподобные». Видимо, этим термином и следует пользоваться для обозначения 14 элементов – аналогов лантана.
«Новая история»
В истории лантана и лантаноидов можно выделить два отрезка времени, особенно насыщенных открытиями и спорами. Первый из них относится к концу XIX в., когда лантаноиды открывали и «закрывали» так часто, что в конце концов это стало даже не интересно... Второй бурный период – 50-е годы XX в., когда развитие атомной техники помогло получать большие количества редкоземельного сырья и стимулировало новые исследования в этой области. Именно тогда наметилась тенденция получать и применять редкоземельные элементы не в смеси, а каждый по отдельности, используя их специфические свойства. Не случайно за 15 лет (с 1944 по 1958 г.) количество научных публикаций, посвященных лантаноидам, выросло в 7,6 раза, а по некоторым индивидуальным элементам и того больше: по гольмию, например, – в 24, а по тулию – в 45 раз!
Маскируясь под крахмал
Одно из соединений лантана – его основной ацетат – ведет себя как крахмал, если к нему добавляют иод. Белый гель принимает ярко-синюю окраску. Этим свойством аналитики иногда пользуются для открытия лантана в смесях и растворах.
Двухвалентен лишь формально
Установлено, что во всех соединениях лантан проявляет одну и ту же валентность – 3+. Но как тогда объяснить существование серо-черного дигидрида LaH2 и желтого сульфида LaS? Установлено, что LaH2 – это относительно устойчивый полупродукт реакции образования LaH3 и что в обоих гидридах лантан трехвалентен. В молекуле дигидрида есть металлическая связь La – La. С сульфидом все объясняется еще проще. Это вещество обладает высокой электропроводностью, что заставляет полагать наличие в нем ионов La3+ и свободных электронов. Кстати, LaH2 тоже хорошо проводит ток, в то время как LaH3 – полупроводник.
Похожие работы
... Гадолина - первого исследователя минерала иттербита. Элемент, содержащийся в гадолиниевой земле (Gadolinia), получил название гадолиний (Gadolinium); в чистом виде он получен в 1896 г. Тербий, Terbium, Тb (65) История открытия этого элемента довольно запутана. Она начинается с черного минерала, найденного в 1788 г. близ деревни Иттерби в Швеции и получившего название гадолинита. В 1797 г. ...
... в промышленность. Уже в начале шестидесятых годов на установках, работающих по принципу ионного обмена, достигли 95 % - ного выхода редкоземельных продуктов чистотой до 99.9 %. НЕПЕРИОДИЧНОСТЬ СВОЙСТВ. Вынести лантаноиды за пределы основной части таблицы первым предложил профессор Пражского университета Богуслав Францевич Браунер. Распутать "узел в системе" окончательно удалось только после того, ...
... H2O + Cl2 NaOH + CeO2 = Na2CeO3 + H2O а соединения со степенью окисления II (Eu, Sm, Yb) – восстановительные, причем окисляются даже водой: 2SmCl2 + 2H2O = 2SmOHCl2 + H2 Лантаноиды очень реакционноспособны и легко взаимодействуют со многими элементами периодической системы: в кислороде сгорают при 200–400 °С с образованием Э2O3, а в атмосфере азота при 750–1000 °С образуют ...
... хлоридом аммония в вакууме по методике, разработанной авторами [ 98, 108 ]. Глава III Исследование механизма электровосстановления ионов самария в хлоридных и хлоридно - фторидных расплавах. Исследование процесса электровосстановления ионов Sm3+ вольтамперометрическим методом при стационарных и нестационарных режимах поляризации ...

0 комментариев