Механические свойства биологических тканей
Рассмотрим важнейшие механические свойства биологических тканей, благодаря которым осуществляются разнообразные механические явления
– такие, как функционирование опорно-двигательного аппарата, процессы деформаций тканей и клеток, распространение волн упругой деформации, сокращения и расслабление мышц, движение жидких и газообразных биологических сред. Среди этих свойств выделяют:
– упругость – способность тел возобновлять размеры (форму или объем) после снятие нагрузок;
– жесткость – способность материала противодействовать внешней нагрузкой; эластичность – способность материала изменять размеры под действием внешних нагрузок;
– прочность – способность тел противодействовать разрушению под действием внешних сил;
– пластичность – способность тел хранить (полностью или частично) изменение размеров после снятия нагрузок;
– хрупкость – способность материала разрушаться без образования заметных остаточных деформаций;
– вязкость – динамическое свойство, которое характеризует способность тела противодействовать изменению его формы при действии тангенциальных напряжений;
– текучесть – динамическое свойство среды, которое характеризует
способность отдельных его слоев перемещаться с некоторой скоростью в пространстве относительно других слоев этой среды.
Механические свойства мышц
Основная функция мышц состоит в преобразовании химической энергии в механическую работу или силу. Главными биомеханическими показателями, характеризующими деятельность мышцы, являются: а) сила, регистрируемая на ее конце (эту силу называют натяжением или силой тяги мышцы) и б) скорость изменения длины.
При возбуждении мышцы изменяется ее механическое состояние; эти изменения называют сокращением. Оно проявляется в изменении натяжения и длины мышцы, а также других ее механических свойств (упругости, твердости и др.).
Механические свойства мышц сложны и зависят от механических свойств элементов, образующих мышцу (мышечные волокна, соединительные образования и т.п.), и состояния мышцы (возбуждения, утомления и пр.).
Понять многие из механических свойств мышцы помогает упрощенная модель ее строения – в виде комбинации упругих и сократительных компонентов. Упругие компоненты по механическим свойствам аналогичны пружинам: чтобы их растянуть, нужно приложить силу. Работа силы равна энергии упругой деформации, которая может в следующей фазе движения перейти в механическую работу. Различают: а) параллельные упругие компоненты (ПарК) – соединительнотканные образования, составляющие оболочку мышечных волокон и их пучков, и б) последовательные упругие компоненты (ПосК) – сухожилия мышцы, места перехода миофибрилл в соединительную ткань, а также отдельные участки саркомеров, точная локализация которых в настоящее время неизвестна.
Сократительные (контрактильные) компоненты соответствуют тем участкам саркомеров мышцы, где актиновые и миозиновые миофиламенты перекрывают друг друга. В этих участках при возбуждении мышцы происходит механическое взаимодействие между актиновыми и миозиновыми филаментами, приводящее к изменению натяжения и длины мышцы.
Поскольку каждая миофибрилла состоит из большого числа (n) последовательно расположенных саркомеров, то величина и скорость изменения длины миофибриллы в п раз больше, чем у одного саркомера. Сила, развиваемая каждым из них, одинакова и равна силе, регистрируемой на конце миофибриллы (подобно тому, как равны силы в каждом из звеньев цепи, к концам которой приложены растягивающие силы). Эти же самые n саркомеров, соединенные параллельно (что соответствует большему числу миофибрилл), дали бы кратное увеличение в силе, но при этом скорость изменения длины мышцы была бы той же, что и скорость одного саркомера. Поэтому при прочих равных условиях увеличение физиологического поперечника мышцы привело бы к увеличению ее силы, но не изменило бы скорости укорочения, и наоборот, увеличение длины мышцы сказалось бы положительно на скорости сокращения, но не повлияло бы на ее силу.
Покоящаяся мышца обладает упругими свойствами: если к ее концу приложена внешняя сила, мышца растягивается (ее длина увеличивается), а после снятия внешней нагрузки восстанавливает свою исходную длину. Зависимость между величиной нагрузки и удлинением мышцы непропорциональна (не подчиняется закону Гука)
Сначала мышца растягивается легко, а затем даже для небольшого удлинения надо прикладывать все большую силу (иногда мышцу в этом отношении сравнивают с вязаными вещами: если растягивать, скажем, трикотажный шарф, то вначале он легко изменяет свою длину, а затем становится практически нерастяжимым).
Если мышцу растягивать повторно через небольшие интервалы Времени, то ее длина увеличится больше, чем при однократном «содействии. Это свойство мышц широко используется в практике при выполнении упражнений на гибкость (пружинистые движения, повторные махи и т.п.).
Длина, которую стремится принять мышца, будучи освобожденной от всякой нагрузки, называется равновесной (или свободной). При такой длине мышцы ее упругие силы равны нулю. В живом организме длина мышцы всегда несколько больше равновесной и поэтому даже расслабленные мышцы сохраняют некоторое натяжение.
Для мышц характерно также такое свойство, как релаксация – снижение силы упругой деформации с течением времени. При отталкивании в прыжках с места сразу после быстрого приседания прыжок будет выше, чем при отталкивании после паузы в низшей точке подседа: после паузы упругие силы, возникшие при быстром приседании, вследствие релаксации не используются.
Структура кожи и ее механические свойстваДо недавнего времени кожа привлекала недостаточное внимание исследователей. Ситуация стала меняться сравнительно недавно. Последние исследования привели к лучшему пониманию особенностей этого органа.
Схематическое изображение разреза нормальной человеческой кожи приведено на рис. 4. В большинстве областей тела человека толщина кожи составляет несколько миллиметров. Кожа состоит из трех слоев: наружного – эпидермиса, основного или собственно дермы и подкожной жировой клетчатки.
Верхний слой – эпидермис /52/ состоит из многослойного ороговевшего эпителия, имеющего толщину от 0,1 до 1,5 мм. В тех участках, где кожа малоподвижна и подвергается значительным механическим воздействиям, эпидермис значительно толще. На стопах, ладонях и красной кайме губ толщина эпидермиса составляет 0,2–0,9 мм. На веках он очень тонок. Общая площадь эпидермиса – 1,5–2 м2. Масса – около 0,5 кг. Эпидермис состоит из нескольких слоев клеток. Наружный роговой слой эпидермиса состоит из мертвых клеток (чешуек), богатых белком кератином, которые постоянно слущиваются с поверхности кожи. Кератин может составлять 85% всех белков в слое. Ниже находится роговой слой. Из-за плотной упаковки он имеет значительную прочность и играет роль механического барьера. Толщина рогового слоя в разных участках кожи различна (обычно, от 10 до 20 мкм). Наибольшей толщины (до 600 мкм) он достигает в эпидермисе кожи ладоней и подошв. У мужчин роговой слой толще, чем у женщин. С возрастом этот слой истончается.
Под эпидермисом располагается дерма, которая обуславливает цвет кожи Дерма распадается на два слоя: поверхностный, в котором имеются кровеносные сосуды и нервы, и более глубокий слой, в котором находятся белковые волокна, обеспечивающие эластичность кожи. Волокна, в основном, содержат белки коллаген и эластин. Коллагеновые волокна прочны на разрыв и мало эластичны. Модуль упругости для них более 10х106 Н/м2.Эластиновые волокна, состоящие из эластина, менее прочны на разрыв, чем коллагеновые, но значительно более эластичны. Они могут растягиваться до 170% от длины покоя без остаточной деформации. Эластин сходен по механическим свойствам с резиной, имеет модуль упругости такого же порядка: (1–5)*105 Н/м2. Коллагеновые и эластиновые фибриллы, заключенные в мукополисахаридный гель, представляют более гомогенную по составу структуру, чем эпидермис.
Дерма плавно переходит в подкожную или жировую клетчатку. Она состоит из переплетающихся волокон, собранных в рыхлые толстые пучки, промежутки между которыми заполнены жировыми клетками. Подкожно-жировой слой располагается по телу неравномерно. Толщина его зависит от многих факторов: возраста, пола, питания, образа жизни и т.д. Клетчатка служит для защиты тела от травм, от переохлаждения, а также представляет собой питательный запас организма.
Наличие в коже многих слоев, обладающих своими собственными характеристиками, определяет гетерогенность ее механических свойств. Анизотропия некоторых механических характеристик обусловливает различное поглощение механической энергии в каждом из слоев, что проявляется в особенностях распространения механических волн на границе раздела этих слоев, обладающих разными вязко упругими свойствами.
Слоистое строение кожи затрудняло интерпретацию результатов исследования кожи. Теоретические модели не могли адекватно объяснить экспериментальные результаты исследований механических свойств кожи вследствие её сложной структуры. Аналогичные трудности возникали и при исследованиях методом вдавливания.
Попытка обойти возникающие трудности была предпринята недавно голландскими учеными при исследовании кожи задней стороны локтя. Они использовали инденторы разных диаметров: 1 мм, 0,5 мм 0,1 мм и 0,02 мм.
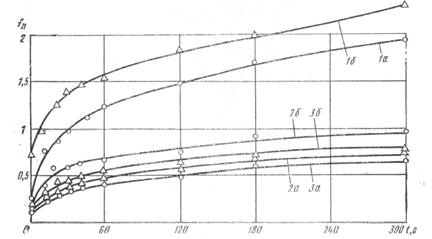
Предполагалось, что зависимость глубины погружения h от прикладываемого усилия для индентора диаметром 0,02 мм отражает твердость рогового слоя, 0,5 мм – дермы и 1 мм – подкожного слоя. На рис. 6 приведен график зависимости F/R от глубины погружения. Эти зависимости линейные в полном соответствии с уравнением (4) и, по-видимому, подтверждают предположения авторов. Упругость эпидермиса по величине больше упругости дермы, которая, в свою очередь, больше упругости подкожной клетчатки.
Состояние кожи изменяется как при возникновении патологии, так и с возрастом /7, 55–58/. По общему мнению, заметные возрастные изменения проявляются после 30–40 лет. При этом гистологически найдены следующие признаки: истончение эпидермиса после 60 лет, уменьшение содержания трансэпидермальной воды, уменьшение толщины кожи /57/ утолщение рогового слоя, истончение дермы. В то же время авторы /17/ путём исследования ультразвуком установили, то толщина кожи остаётся неизменной вплоть до 70 лет. С возрастом, по их мнению, изменяется эластичность кожи, что приводит к уменьшению первоначальной фазы эластических деформаций.
Как уже было указано выше, в работе /69/ в качестве количественного критерия оценки упругости кожи предложено использовать время возврата какой либо точки обследуемого участка кожи к исходной форме после импульсного деформирования. Это предложение основано на определении упругости, как свойства тела восстанавливать свою форму после действия силы. На основе экспериментальных исследований разработанного авторами устройства были сделаны следующие выводы: воспроизводимость результатов измерений не хуже 10%; упругость кожи практически не зависит от силы деформирующего воздействия: разброс параметров лежит в пределах воспроизводимости результатов измерений.
Типичные результаты измерения времени возврата деформированного участка кожи лба к исходной форме с использованием разработанного авторами устройства. Как видно из рис. 7, в процессе возвращения поверхности кожи к исходной форме можно выделить две стадии. Первая (быстрая) стадия характеризуется параметром А – характерным временем возврата кожи к исходной форме. Величина А, по мнению авторов, является основным количественным параметром, характеризующим упругость кожи. Вторая стадия (медленная) характеризуется величиной остаточных деформаций (параметр В) и временем окончательного возвращения поверхности кожи к первоначальной форме. Как следует из графиков, более молодая кожа (кривая а) характеризуется большей скоростью возврата к исходной форме и меньшей величиной остаточных деформаций. Анализ результатов измерений показал, что величина относительных колебаний упругости кожи в зависимости от возраста обследуемого (от 15 до 55 лет) достигал 5-кратного значения. При сравнении упругости кожи в различных областях тела у одного и того же пациента было выявлено, что параметры А и В варьируют в пределах ± 10%.
Одно из объяснений возрастных изменений упругости кожи состоит в предположении, что изменяется состояние сети эластичных волокон дермы. Другое объяснение – увеличивается количество сшивок внутри коллагеновых волокон /58/. Наличие сшивок подтверждается увеличением доли нерастворимой части кожи.
В течении всей жизни человека медленно, но неуловимо проявляются внешние признаки старения. Эти внешние признаки, в первую очередь, связаны с изменениями микрорельефа поверхности кожи (морщины). Микрорельеф кожи, во многом, определяет как внешний вид человека, так и тактильное восприятие его другими людьми (зрительное восприятие, приятность на ощупь).
Поэтому неудивителен интерес к объективному количественному описанию микрорельефа кожи человека, зависимостей микрорельефа от возраста и изменений его под действием лекарств и косметических средств.
Термин «микрорельеф» для кожи аналогичен по своей сути широко используемому в технике термину «шероховатость». Шероховатость – это совокупность неровностей с относительно малыми расстояниями между соседними точками измерений.
В своей основе методы определения микрорельефа кожи аналогичны методам определения шероховатостей поверхностей твёрдых тел /70/, хотя и с учетом свойств кожи.
Одним из старых методов является метод слепков. Метод состоит из следующих стадий: изготовление негативных реплик (отпечатков); получение с них позитивных копий (слепков) из полимеризующихся мелкодисперсных химических композиций (обычно на основе эпоксидных смол или полиметилметакрилата); собственно регистрацию позитивной реплики и анализ полученных результатов. Применительно к коже этот метод подробно разобран в работе /71/. Там же тщательно описаны достоинства и недостатки материалов, используемых для изготовления отпечатков и слепков. Запись профиля с позитивной реплики может выполняться стандартными методами с помощью механических или оптических профилометров (промышленных или разработанных специально для медицинских целей). В зависимости от условий могут анализироваться как отдельные (единичные) профили поверхностей (глубины и ширины борозд), так и их пространственные характеристики (плотность, ориентация, симметрия). Методики обработки результатов измерений продолжают совершенствоваться с применением современной техники (лазерной профилометрии, трёхмерной компьютерной обработкой негатива /72, 73/).
К числу недостатков этого метода следует отнести многоэтапный процесс измерения и наличие погрешностей при контакте материалов с кожей на этапе создания негативной реплики.
В значительной мере этих недостатков лишены ставшие популярные оптико-электронные методы изучения микрорельефа кожи /69/. В работе /69/ для измерения микрорельефа использовался оптический щуп. Последний представлял собой оптико-электронный прибор, позволяющий измерять рельеф исследуемой поверхности оптическим излучением. Регистрация информации о рельефе поверхности исследуемого участка кожи осуществлялся поточечно посредством механического сканирования. Разработанное устройство было использовано для изучения возрастных изменений кожи. Результаты отдельных измерений приведен на рис. 8. Из рисунка видно, что средняя величина рельефа поверхности колеблется в пределах 10–30 мкм как вдоль морщины, так и поперёк.
Эластические свойства сосудовКак указывалось ранее, артерии и вены вносят лишь незначительный вклад в общее сопротивление кровотоку, который осуществляется через сосудистое русло. Поэтому мы обычно не придаем большого значения тому влиянию, которое оказывает изменение их диаметра на кровоток через системные органы. В то же время эластические свойства артерий и вен являются весьма важным фактором, влияющим на деятельность сердечно-сосудистой системы, так как эти сосуды могут функционировать как резервуары, и в них могут быть накоплены существенные количества крови.
Эластические свойства сосудов или отделов сосудистой системы часто характеризуются такой величиной, как растяжимость (С), которая отражает, насколько изменяется их объем (Д V) в ответ на определенное изменение трансмурального давления (АР):
![]()
![]()
Трансмуральное давление представляет собой разность между внутренним и внешним давлением на сосудистую стенку.
Эластические свойства вен важны для их функции по депонированию крови. Как видно по кривым зависимости давления от объема на рис. 7–7, вены более растяжимы, чем артерии. Так как вены столь растяжимы, что даже небольшие изменения периферического венозного давления могут вызвать перемещение существенного объема циркулирующей крови в периферический венозный пул или из него. Переход в вертикаль – нос положение тела, например, увеличивает венозное давление в нижних конечностях и способствует накоплению крови (создание пула) в этих сосудах, что соответствует перемещению из точки А в точку В на рис. 7–7.
К счастью, данный процесс может быть уравновешен активным сужением вен. Пунктирная линия на рис. 7–7 отражает взаимозависимость между венозным давлением и объемом, которая отмечается при сужении вен в результате сокращения гладкой мускулатуры вен. В суженных венах объем крови может соответствовать норме (точка С) или даже быть ниже нормы (точка D), несмотря на более высокое, чем венозное давление. Сужение периферических вен само по себе способно повышать периферическое венозное давление и перемещать кровь из венозного резервуара.
Эластические свойства артерий позволяют им функционировать в качестве резервуара в промежутке между сокращениями сердца. Артерии играют важную роль в превращении пульсирующего потока крови, изгоняемого из сердца, в постоянный поток через сосудистое русло системных органов. С этой точки зрения, артерии выполняют функцию буфера. В начале фазы быстрого изгнания объем артериальной крови увеличивается, так как кровь поступает в 1 аорту быстрее, чем она проходит в просвет системных артериол. Таким образом, часть той работы, которую сердце выполняет при выбросе крови, уходит на растяжение эластических стенок артерий. Ближе к концу систолы и на протяжении диастолы, артериальный объем уменьшается, поскольку кровоток, выходящий из артерий, превышает кровоток, поступающий в аорту. Находящаяся в растянутом состоянии артериальная стенка сокращается и при этом утрачивает накопленную потенциальную энергию. Данная энергия, перешедшая из одной формы в другую, и обеспечивает работу по продвижению крови через периферическое сосудистое русло во время диастолы. Если бы артерии представляли собой жесткие трубки, не способные аккумулировать энергию за счет эластического растяжения, артериальное давлением немедленно падало бы до нуля при окончании процесса каждого сердечного выброса.
Физиология крови
Кровь, лимфа, тканевая, спинномозговая, плевральная, суставная и другие жидкости образуют внутреннюю среду организма. Внутренняя среда отличается относительным постоянством своего состава и физико-химических свойств, что создает оптимальные условия для нормальной жизнедеятельности клеток организма.
Впервые положение о постоянстве внутренней среды организма сформулировал более 100 лет тому назад физиолог Клод Бернар. Он пришел к заключению, что «постоянство внутренней среды организма есть условие независимого существования», т.е. жизни, свободной от резких колебаний внешней среды.
В 1929 г. Уолтер Кэннон ввел термин гомеостаз. В настоящее время под гомеостазом понимают как динамическое постоянство внутренней среды организма, так и регулирующие механизмы, которые обеспечивают это состояние. Главная роль в поддержании гомеостаза принадлежит крови. В 1939 г. Г.Ф. Ланг создал представление о системе крови, в которую он включил периферическую кровь, циркулирующую по сосудам, органы кроветворения и кроверазрушения, а также регулирующий нейрогуморальный аппарат.
Объем и физико-химические свойства крови
Объем крови – общее количество крови в организме взрослого человека составляет в среднем 6 – 8% от массы тела, что соответствует 5 – 6 л. Повышение общего объема крови называют гиперволемией, уменьшение – гиповолемией.
Относительная плотность крови – 1,050 – 1.060 зависит в основном от количества эритроцитов. Относительная плотность плазмы крови – 1.025 – 1.034, определяется концентрацией белков.
Вязкость крови – 5 усл. ед., плазмы – 1,7 – 2,2 усл. ед., если вязкость воды принять за 1. Обусловлена наличием в крови эритроцитов и в меньшей степени белков плазмы.
Осмотическое давление крови – сила, с которой растворитель переходит через полунепроницаемую мембрану из менее в более концентрированный раствор. Осмотическое давление крови вычисляют криоскопическим методом путем определения точки замерзания крови (депрессии), которая для нее равна 0,56 – 0,58 С. Осмотическое давление крови в среднем составляет 7,6 атм. Оно обусловлено растворенными в ней осмотически активными веществами, главным образом неорганическими электролитами, в значительно меньшей степени – белками. Около 60% осмотического давления создается солями натрия (NаСl).
Осмотическое давление определяет распределение воды между тканями и клетками. Функции клеток организма могут осуществляться лишь при относительной стабильности осмотического давления. Если эритроциты поместить в солевой раствор, имеющий осмотическое давление, одинаковое с кровью, они не изменяют свой объем. Такой раствор называют изотоническим, или физиологическим. Это может быть 0,85% раствор хлористого натрия. В растворе, осмотическое давление которого выше осмотического давления крови, эритроциты сморщиваются, так как вода выходит из них в раствор. В растворе с более низким осмотическим давлением, чем давление крови, эритроциты набухают в результате перехода воды из раствора в клетку. Растворы с более высоким осмотическим давлением, чем давление крови, называются гипертоническими, а имеющие более низкое давление – гипотоническими.
Онкотическое давление крови – часть осмотического давления, создаваемого белками плазмы. Оно равно 0,03 – 0,04 атм, или 25 – 30 мм рт. ст. Онкотическое давление в основном обусловлено альбуминами. Вследствие малых размеров и высокой гидрофильности они обладают выраженной способностью притягивать к себе воду, за счет чего она удерживается в сосудистом русле, При снижении онкотического давления крови происходит выход воды из сосудов в интерстициальное пространство, что приводит к отеку тканей.
Кислотно-основное состояние крови (КОС). Активная реакция крови обусловлена соотношением водородных и гидроксильных ионов. Для определения активной реакции крови используют водородный показатель рН – концентрацию водородных ионов, которая выражается отрицательным десятичным логарифмом молярной концентрации ионов водорода. В норме рН – 7,36 (реакция слабоосновная); артериальной крови – 7,4; венозной – 7,35. При различных физиологических состояниях рН крови может изменяться от 7,3 до 7,5. Активная реакция крови является жесткой константой, обеспечивающей ферментативную деятельность. Крайние пределы рН крови, совместимые с жизнью, равны 7,0 – 7,8. Сдвиг реакции в кислую сторону называется ацидозом, который обусловливается увеличением в крови водородных ионов. Сдвиг реакции крови в щелочную сторону называется алкалозом. Это связано с увеличением концентрации гидроксильных ионов ОН и уменьшением концентрации водородных ионов.
В организме человека всегда имеются условия для сдвига активной реакции крови в сторону ацидоза или алкалоза, которые могут привести к изменению рН крови. В клетках тканей постоянно образуются кислые продукты. Накоплению кислых соединений способствует потребление белковой пищи. Напротив, при усиленном потреблении растительной пищи в кровь поступают основания. Поддержание постоянства рН крови является важной физиологической задачей и обеспечивается буферными системами крови. К буферным системам крови относятся гемоглобиновая, карбонатная, фосфатная и белковая.
Буферные системы нейтрализуют значительную часть поступающих в кровь кислот и щелочей, тем самым препятствуя сдвигу активной реакции крови. В организме в процессе метаболизма в большей степени образуется кислых продуктов. Поэтому запасы щелочных веществ в крови во много раз превышают запасы кислых, Их рассматривают как щелочной резерв крови.
Гемоглобиновая буферная система на 75% обеспечивает буферную емкость крови. Оксигемоглобин является более сильной кислотой, чем восстановленный гемоглобин. Оксигемоглобин обычно бывает в виде калиевой соли. В капиллярах тканей в кровь поступает большое количество кислых продуктов распада. Одновременно в тканевых капиллярах при диссоциации оксигемоглобина происходит отдача кислорода и появление большого количества щелочно реагирующих солей гемоглобина, Последние взаимодействуют с кислыми продуктами распада, например угольной кислотой. В результате образуются бикарбонаты и восстановленный гемоглобин, В легочных капиллярах гемоглобин, отдавая ионы водорода, присоединяет кислород и становится сильной кислотой, которая связывает ионы калия. Ионы водорода используются для образования угольной кислоты, в дальнейшем выделяющейся из легких в виде Н2О и СО2.
Карбонатная буферная система по своей мощности занимает второе место. Она представлена угольной кислотой (Н2СО3) и бикарбонатом натрия или калия (NaНСО3, КНСО3) в пропорции 1/20. Если в кровь поступает кислота, более сильная, чем угольная, то в реакцию вступает, например, бикарбонат натрия. Образуются нейтральная соль и слабодиссоциированная угольная кислота. Угольная кислота под действием карбоангидразы эритроцитов распадается на Н2О и СО2, последний выделяется легкими в окружающую среду. Если в кровь поступает основание, то в реакцию вступает угольная кислота, образуя гидрокарбонат натрия и воду. Избыток бикарбоната натрия удаляется через почки. Бикарбонатный буфер широко используется для коррекции нарушений кислотно-основного состояния организма.
Фосфатная буферная система состоит из натрия дигидрофосфата (NаН2РО4) и натрия гидрофосфата (Nа2НРО4). Первое соединение обладает свойствами слабой кислоты и взаимодействует с поступившими в кровь щелочными продуктами. Второе соединение имеет свойства слабой щелочи и вступает в реакцию с более сильными кислотами.
Белковая буферная система осуществляет роль нейтрализации кислот и щелочей благодаря амфотерным свойствам.: в кислой среде белки плазмы ведут себя как основания, в основной – как кислоты.
Буферные системы имеются и в тканях, что способствует поддержанию рН тканей на относительно постоянном уровне. Главными буферами тканей являются белки и фосфаты.
Поддержание рН осуществляется также с помощью легких и почек. Через легкие удаляется избыток углекислоты. Почки при ацидозе выделяют больше кислого одноосновного фосфата натрия, а при алкалозе – больше щелочных солей: двухосновного фосфата натрия и бикарбоната натрия.
Свертывающие механизмы
Свертывание крови (гемокоагуляция) – это жизненно важная защитная реакция, направленная на сохранение крови в сосудистой системе и предотвращающая гибель организма от кровопотери при травме сосудов.
Основные положения ферментативной теории свертывания крови были разработаны А. Шмидтом более 100 лет назад.
В остановке кровотечения участвуют: сосуды, ткань, окружающая сосуды, физиологически активные вещества плазмы, форменные элементы крови, главная роль принадлежит тромбоцитам. И всем этим управляет нейрогуморальный регуляторный механизм.
Физиологически активные вещества, принимающие участие в свертывании крови и находящиеся в плазме, называются плазменными факторами свертывания крови. Они обозначаются римскими цифрами в порядке их хронологического открытия. Некоторые из факторов имеют название, связанное с фамилией больного, у которого впервые обнаружен дефицит соответствующего фактора. К плазменным факторам свертывания крови относятся: Iф – фибриноген, IIф – протромбин, IIIф – тканевой тромбопластин, IVф – ионы кальция, Vф – Ас-глобулин (ассеlеrаnсе – ускоряющий), или проакцелерин, VIф – исключен из номенклатуры, VIIф – проконвертин, VIIIф – антигемофильный глобулин А, IXф – антигемофильный глобулин В, или фактор Кристмаса, Xф – фактор Стюарта – Прауэра, XIф – плазменный предшественник тромбопластина, или антигемофильный глобулин С, XIIф – контактный фактор, или фактор Хагемана, XIIIф – фибринстабилизирующий фактор, или фибриназа, XIVф – фактор Флетчера (прокалликреин), XVф – фактор Фитцджеральда – Фложе (высокомолекулярный кининоген – ВМК).
Методы определения вязкости жидкостейОпределение вязкости биологических жидкостей и, особенно, вязкости крови имеет существенное диагностическое значение. Разнообразные приборы, применяемые для этой цели называют вискозиметрами. Они подразделяются на два основных типа: капиллярные и ротационные.
В капиллярных вискозиметрах (вискозиметр Оствальда, Гесса) вязкость оценивается по объему жидкости, протекающему в единицу времени через капиллярную трубку под действием перепада давлений. Зная геометрические параметры капилляра, величину вязкости ньютоновских жидкостей можно расчитать по уравнению Пуазейля.
Для определения вязкости неньютоновских жидкостей (в частности, крови) предпочтительнее использовать ротационные вискозиметры. В них исследуемая жидкость помещается в зазор между двумя вращающимися цилиндрами. При этом измеряют угол поворота внутреннего цилиндра, определяют угловую скорость, а затем вязкость. Достоинством такого метода является возможность определять не только значение вязкости, но и ее зависимость от скорости сдвига. Следует помнить, что вязкость крови, определенная при помощи визкозиметра, иногда существенно отличается от вязкости крови в организме.
Похожие работы
... школа, 1988. 10. Артюхов В.Г., Ковалева Т.А., Шмелев В.П. Биофизика. Воронеж: Воронежский гос. ун-т 1994. 11. Антонов В.Ф. Биофизика. VI.: Арктос-Викапресс, 2000. 12. Дополнительная 13. Механика и биомеханика 14. Никитин E. VI. Теоретическая механика. VI.: Наука. 1968. Александер Р. Биомеханика. VI.: Мир. 1970. 15. Журавлева А.И., Iраевская И.Д. Спортивная медицина и лечебная ...
... , форменных элементов (эритроциты, лейкоциты, тромбоциты и др.) существенно повышают восприимчивость и чувствительность жидких сред организма к внешнему воздействию различных физических факторов, в том числе низкоэнергетического лазерного излучения. В биологических жидкостях имеются специфические фотоакцепторы, реагирующие на лазерное излучение определенной длины волны. Кроме того, энергетической ...
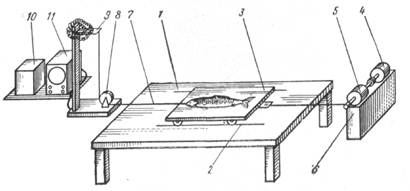
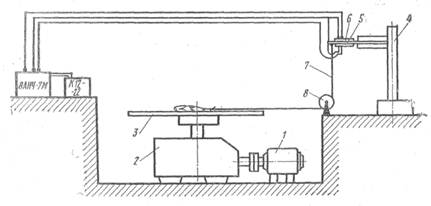
... силы взаимодействия между рыбой и рабочими органами машин, поскольку изменяется площадь контакта, обусловливающая силы трения. До настоящего времени структурно-механические характеристики в основном оцениваются органолептическим методом. Рыбу сдавливают пальцами и оценивают ее консистенцию. Не достатком такого метода оценки структурно-механических характеристик мышечной ткани является его ...
... в различных областях, поэтому почти всегда удается найти такую область, в которой один из сигналов достаточно хорошо отделен и пригоден для интегрирования. Особая сложность количественного анализа биологических жидкостей и тканей, которые могут содержать сотни компонентов в очень большом интервале концентраций, в том, что обычно заранее не известно, до какой глубины необходимо проводить анализ и ...
0 комментариев