Немировский А.М.
Глубокое знакомство с литературными источниками, посвященными ионометрии, выявляет фатальную склонность авторов использовать закон Нернста для объяснения абсолютно всех явлений ионометрического эксперимента. Упоминание о законе считается почти правилом хорошего тона. Однако хорошие манеры в некоторых случаях не могут исправно объяснять наблюдаемые эффекты. В связи с этим меня заинтересовала проблема взаимодействия законов ионометрии и электродинамики. На мой взгляд, ионометристы пренебрегают законами электродинамики, углубляясь только в химическую сторону дела.
Рассмотрим следующий пример. Допустим, что нам предстоит работать с нитратным ионоселективным электродом на ПВХ-матрице. Однако нам стало известно, что среда, в которой предстоит делать измерения, взаимодействует с пластификатором мембраны, внося свой вклад в общий потенциал электрода. Как быть? Надеяться на то, что можно описать такую систему с помощью уравнения Никольского не приходится, так как электродноактивное вещество и пластификатор вряд ли связаны химическим массообменом. С другой стороны, нет повода считать, что потенциалы от потенциалопределяющего иона и пластификатора просто складываются.
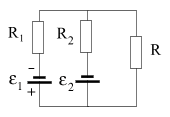
Для случаев такого рода я предлагаю модель параллельно соединенных источников э.д.с. В этой модели часть потенциалопределяющих реакций рассматриваются в виде источников э.д.с. в том виде, как это принято в электродинамике:
где
e 1 - э.д.с. источника тока, организованного потенциалопределяющим ионом;
e 2 - э.д.с. источника тока, организованного альтернативной электрохимической реакцией;
R1 и R2 - внутренние сопротивления источников тока;
R - сопротивление измерительного прибора.
Используя правила Кирхгофа для расчетов в замкнутых электрических цепях, получим следующую систему уравнений:
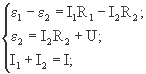
где I - сила тока на участке цепи с сопротивлением R.
Если R>>R1+R2, то измеряемое прибором напряжение равно
![]()
Так как мы договорились о том, что e 1 вызывается потенциалопределяющим ионом, то
![]()
или
![]()
Из этого следует, что потенциал (э.д.с.) параллельной реакции уменьшает наклон электродной функции (S) при условии, что этот потенциал не зависит от концентрации потенциалопределяющего иона! Тому есть экспериментальные подтверждения, достаточно вспомнить нитратселективные электроды на основе четвертичных аммониевых солей, хлоридные электроды на основе смеси сульфидов и хлоридов серебра и т.д.
Развивая гипотезу о параллельных электродинамических процессах, рассмотрим другой пример. Допустим, что анализируемый раствор состоит из смеси солей основного и мешающего ионов, причем механизмы потенциалобразования этих ионов различны. (Представить такое сложно, но можно.) Тогда
![]()
где B1 и B2 - константы,
Этот пример интересен тем, что если строить калибровку по основному иону в растворе мешающего, то это никак не будет влиять на линейность калибровки. Кроме того, приведенный пример допускает существование таких электрохимических систем, в которых влияние мешающего иона в большей мере сказывается на абсолютном значении потенциала, нежели на наклоне электродной функции. Это является очень важным аналитическим фактом, расширяющим возможности метода добавок. (Как известно, в методе добавок малое влияние мешающих ионов на наклон электродной функции является очень важным.) Не нужно говорить о том, что классическая модель (уравнение Никольского) не предполагает таких вариантов, так как мешающий ион влияет на результаты анализа следующим образом:
U = const + S * lg ( C + KCm ),
где С и Сm - концентрации основного и мешающего ионов;
К - коэффициент селективности.
Однако гипотезы гипотезами, но существуют ли приметы, подтверждающие правильность приведенных выше рассуждений? Кроме того, правомерно ли использовать правила Кирхгофа для реальных химических источников электричества.
Сразу же скажу о том, что мною были проведены опыты на батарейках фирмы "TOSHIBA". Измерение напряжения параллельно соединенных батареек показало, что правила Кирхгофа справедливы. В таблице приведены результаты проведенных опытов.
| R1, МОм | R2, МОм | e 1, В | e 2, В | U, В | Uтеорич.,В |
| 8,09 | 8,17 | 1624,5 | 1614,4 | 1619,4 | 1619,5 |
| 1624,5 | 3274,3 | 2445 | 2445,3 | ||
| 1624,5 | 4898,7 | 3252,9 | 3253,5 | ||
| 3,33 | 8,17 | 1624,1 | 1614,3 | 1621,1 | 1621,3 |
| 1624,1 | 3274,2 | 2101,1 | 2101,9 | ||
| 1624,1 | 4898,7 | 2570,7 | 2572,3 | ||
| 0,942 | 0,788 | 1619,4 | 1658,6 | 1641,2 | 1640,7 |
| 1619,4 | 3282,8 | 2526,1 | 2525,1 | ||
| 1619,4 | 4906,6 | 3410,9 | 3409,3 | ||
| 0,01067 | 0,0952 | 1588,1 | 1655,1 | 1594,8 | 1594,9 |
| 1588,1 | 3275,9 | 1759,5 | 1758,2 | ||
| 1588,1 | 4898,6 | 1924,1 | 1921,7 |
Что же касается моих гипотез, то стоит вспомнить о том, как современная ионометрия объясняет наличие ионоселективных электродов с наклоном электродной функции отличного от теоретического. Объяснение следующее: чем больше массообмен иона с мембраной, тем больше отличие в значении наклона электродной функции. Однако эта версия не всегда справедлива, так как некоторые стеклянные электроды, так же как и электроды с ПВХ-мембранами, имеют недостаточный наклон, хотя массообмен их несопоставим. Моя гипотеза объясняет этот факт менее противоречиво, так как допускает наличие параллельного электрохимического процесса, который не связан с основным процессом химически.
Вторым серьезным следствием моей гипотезы является то обстоятельство, что при нетеоретическом наклоне коэффициент селективности к мешающим ионам претерпевает изменения. Дело в том, что коэффициент селективности перестает быть постоянным в рамках уравнения Никольского. Экспериментального подтверждения этого я не имею, но о таких эффектах мне рассказывали. Если кто-нибудь имеет экспериментальные данные об этом явлении, то я буду рад организовать совместную работу.
В заключении я хочу вкратце изложить преимущества, которые дает новая гипотеза.
Гипотеза о влиянии параллельного электродинамического процесса на ионометрические измерения объясняет наличие у электродов нетеоретического наклона электродной функции.
Гипотеза предсказывает возможные погрешности при использовании уравнения Никольского для учета влияния мешающих ионов.
В некоторых случаях гипотеза не исключает иного влияния мешающих ионов на потенциал ионоселективного электрода, нежели предполагает уравнение Никольского.
Список литературы
Для подготовки данной работы были использованы материалы с сайта http://www.novedu.ru/
Похожие работы
... . (Следует пояснить, что неподвижная фаза должна представлять собой инертный сорбент не являющийся электрическим проводником, насыщенный экстрагентом.) Исходя из предлагаемой теории, потенциал хроматографической системы будет развиваться во времени в 3 этапа. I этап. По мере продвижения фронтов хорошо и плохо удерживаемого компонентов, последний занимает все большую площадь поверхности ...
0 комментариев