Министерство образования Республики Беларусь
УО «Полоцкий государственный университет»
Контрольная работа
по дисциплине «Тепломассообмен»
Примеры решения задач по курсу технической термодинамики
Новополоцк 2010
Задача № 1
Газовая смесь G, заданная объемными долями и занимающая исходный объем V1, нагревается при постоянном давлении от температуры t1 до температуры t2, а потом охлаждается при постоянном объеме до исходной температуры t1. Определить конечное давление и объем смеси, величину работы и теплоты, участвующие в процессах, и изменение энтропии 1 кг смеси. Показать оба процесса в pv- и TS-диаграммах (без масштаба).
Дано: G=22 кг, V1=20 м3, t1=125 ºС, t2=375 ºС, N2=50%, СО2=20%, Н2=30%
Решение
Молярная масса газа
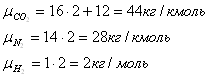
Молярная масса смеси
![]()
![]()
Где ri-объемные доли
μi-молярная масса компонента
Газовая постоянная смеси
![]()
Начальная температура
![]()
Начальное давление
![]()
Абсолютная температура после нагревания
![]()
Конечное давление
![]()
Конечный объем смеси
![]()
Для определения количества теплоты подведенной к газовой смеси в процессе её изобарного нагрева, найдем изобарные мольные теплоемкости при нагреве:
![]()
Углекислый газ
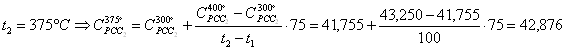
![]()
![]()
Азот
![]()
![]()
![]()
Водород
![]()
![]()
![]()
Изобарная мольная теплоемкость смеси:
![]()
Массовая теплоемкость
![]()
Количество подведенной теплоты
![]()
Работа при изобарном нагреве
![]()
Изменение энтропии в изобарном процессе нагрева смеси
![]()
Охлаждение при V=const
Изохорная мольная теплоемкость смеси найдется из уравнения:
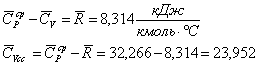
Объемная теплоемкость смеси
![]()
Количество отводимой теплоты:
![]()
Работа изохорного процесса L=0, т.к. объем не меняется.
Для расчета изменения энтропии найдем массовую изохорную теплоемкость смеси
![]()
И тогда
![]()
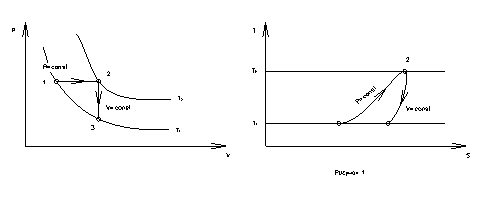
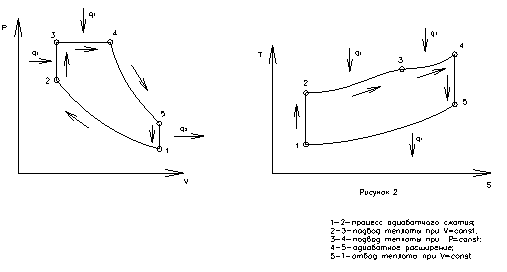
Процессы в pv- и ТS- диаграммах см. на рисунке 1.
Задача №2
Для теоретического цикла поршневого двигателя внутреннего сгорания с изохорно-изобарным подводом теплоты определить параметры состояния, р, v, t характерных точек цикла, полезную работу и термический КПД по заданным значениям начального давления р1 и температуры t1, степени сжатия ε, степени повышения давления λ и степени предварительного расширения ρ. Рабочим телом считать воздух, полагая теплоемкость его постоянной. Изобразить цикл ДВС в pv- и TS-диаграммах (без масштаба). Определить также КПД цикла Карно, проведенного в том же интервале температур t1-t4, что и цикл ДВС.
Дано: р1=98 кПа, t1=30 ºС, ε=16, λ=1,5, ρ=1,5.
Решение
Изобразим цикл ДВС в pv- и TS-диаграммах см. рисунок 2.
Параметры точки 1.
Давление р1=98 кПа, температура Т1=273+30=303 К.Удельный объем найдем из уравнения состояния р1v1=RT1, где R=287 Дж/кг·ºС- газовая постоянная воздуха.
![]()
Параметры точки 2.
Степень сжатия ![]() , поэтому
, поэтому ![]() .
.
Температура в конце адиабатного сжатия
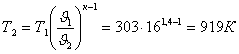
Давление в конце адиабатного сжатия
![]()
Параметры точки 3.
Удельный объем ![]()
Степень повышения давления ![]() поэтому абсолютное давление
поэтому абсолютное давление
![]()
Для идеального газа по закону Шарля ![]() поэтому абсолютная температура
поэтому абсолютная температура
![]()
Параметры точки 4.
Абсолютное давление р3=р4=7193,25 кПа.
Степень предварительного расширения ![]() поэтому удельный объем
поэтому удельный объем ![]()
По закону Гей-Люссака для идеального газа ![]() поэтому абсолютная температура
поэтому абсолютная температура ![]()
Параметры точки 5.
Удельный объем ![]() .
.
Давление в конце адиабатного расширения определим из уравнения адиабаты ![]() , отсюда
, отсюда
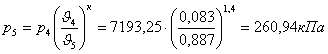 .
.
По закону Шарля ![]() отсюда абсолютная температура
отсюда абсолютная температура
![]()
Работа цикла определяется как разность между работой расширения и работой сжатия.
Работа сжатия
![]()
Работа расширения
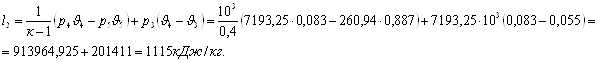
Работа цикла есть алгебраическая сумма l1 и l2
L = l1 - l2 = -442+1115 = 673 кДж/кг
Количество подведенной теплоты:
В процессе 2-3 ![]()
В процессе 3-4 ![]()
Количество отведенной теплоты
![]()
Теплота полезно используемая в цикле
![]()
Термический КПД цикла
![]()
Термический КПД цикла Карно по условиям задачи
![]()
Задача №3
Показать сравнительным расчетом целесообразность применения пара высоких начальных параметров и низкого конечного давления на примере паросиловой установки, работающей по циклу Ренкина, определив располагаемое теплопадение, термический КПД цикла и удельный расход пара для двух различных значений начальных и конечных параметров пара. Указать конечное значение степени сухости х2 (при давлении р2). Изобразить схему простейшей паросиловой установки и дать краткое описание ее работы.
Дано: 1-вариант: р1=2,0 МПа, t1=300ºС, р2=70кПа
2-вариант: р1=8,0 МПа, t1=480ºС, р2=3кПа
Решение
Для решения задачи используем is-диаграмму водяного пара.
Теплосодержание пара, соответствующее начальному состоянию i1=3250 кДж/кг.
Теплосодержание пара, поступающего в конденсатор. i2=2405 кДж/кг.
Температура кипящей воды при Р2=70 кПа t’2=90 ºС.
Принимая теплоемкость воды Св=4,19 кДж/(кг·ºС), найдем энтальпию кипящей воды i’2=Cв·t´2=4,19·90=377,1 кДж/кг.
Конечная степень сухости пара χ2=0,89.
Располагаемый теплоперепад
![]()
Термический КПД цикла Ренкина
![]()
Удельный расход пара
![]()
Вариант №2
Из is-диаграммы i1=3351 кДж/кг; i2=1975 кДж/кг; t´Н2 =10 ºС, Св=4,19 кДж/(кг·ºС), поэтому энтальпия кипящей воды i’2=10·4,19=41,9 кДж/кг. Следовательно,
![]()
![]()
![]()
Вывод: Применение пара высоких начальных параметров и низкого конечного давления приводит к повышению термического КПД цикла Ренкина и снижению удельного расхода пара на единицу работы.
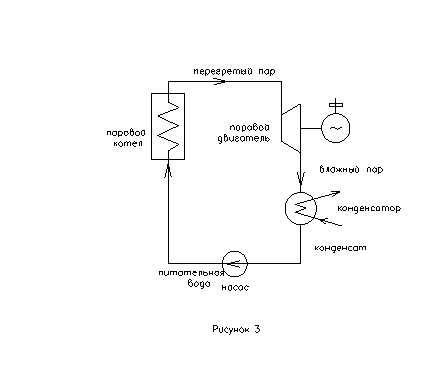
Схему простейшей паросиловой установки можно увидеть на рисунке 3. Она включает в себя паровой котел, паровой двигатель, конденсатор и насос.
Паровой котел представляет собой устройство, в котором производится сжигание топлива, и теплота образующихся газообразных продуктов сжигания используется для превращения поступающей в него воды в перегретый пар. Паровой двигатель является основным элементом всей установки, поскольку именно в нем потенциальная энергия пара используется для совершения полезной работы. Большей частью эта работа состоит во вращении ротора электрического генератора.
Конденсатор представляет собой трубчатый теплообменник, внутренняя поверхность трубок которого охлаждается циркуляционной водой, за счет чего на наружной поверхности их происходит конденсация отработавшего пара. Скапливающийся внизу конденсат откачивается насосом, который повышает его давление до необходимой величины и подает обратно в котел.
Задача №4
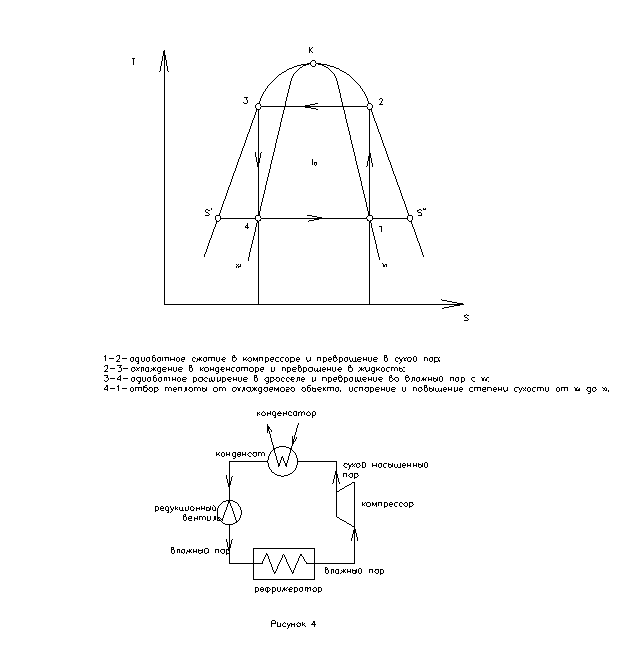
Определить холодильный коэффициент паровой аммиачной установки (с дросселем) по известной температуре влажного пара NH3 на входе в компрессор t1 и температуре сухого насыщенного пара NH3 за компрессором t2. По заданной холодопроизводительности Q определить также массовый расход аммиака и теоретическую мощность привода компрессора. Изобразить схему установки и ее цикл в TS-диаграмме.
Дано: t1=-15 ºС, t2=30 ºС, Q=150 кВт.
Решение
Холодопроизводительность аммиака, т.е. количество теплоты, поглощаемой 1 кг аммиака от охлаждаемого объекта:
![]()
где r = 1312,6 кДж/кг – скрытая теплота парообразования аммиака при t = -15 ºС.
Значение степеней сухости х1 и х4 найдем аналитически, используя постоянство энтропии в обратном адиабатном процессе.
Для процесса 1-2:
![]()
Где из таблицы для насыщенного пара NH3![]() - энтропия кипящего аммиака при t=-15 ºС;
- энтропия кипящего аммиака при t=-15 ºС;
![]() - энтропия сухого насыщенного пара аммиака при t=-15 ºС;
- энтропия сухого насыщенного пара аммиака при t=-15 ºС;
![]() - энтропия сухого насыщенного пара аммиака при t=+30ºС.
- энтропия сухого насыщенного пара аммиака при t=+30ºС.
Тогда
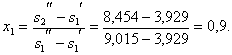
Для процесса 3-4: ![]()
Где из таблицы ![]() - энтропия сухого кипящего аммиака при t=+30ºС.
- энтропия сухого кипящего аммиака при t=+30ºС.
Тогда
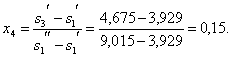
Следовательно, q0 = 1312,6 · (0,9 - 0,15) = 984,45 кДж/кг.
Тепловая нагрузка конденсатора, т.е. количество теплоты, отводимой с охлаждающей водой:
q = i2 - i3 = r2,
где r2=1145,5 кДж/кг – скрытая теплота парообразования NH3 при t=30 ºС.
Следовательно, q = r2 = 1145,5 кДж/кг.
Работа, затраченная в цикле:
l0= q - q0 = 1145,5-984,45 = 161,05 кДж/кг.
Холодильный коэффициент:
![]()
Расход аммиака:
![]()
Теоретическая мощность привода компрессора:
![]()
Схему установки и ее цикл в TS- диаграмме см. рисунок 4.
Литература
1. Э.И. Гончаров «Техническая термодинамика. Учебно-методический комплекс для студентов специальности 1-700402 «Теплогазоснабжение, вентиляция и охрана воздушного бассейна», Новополоцк: ПГУ 2004г.
Похожие работы
... , или термодинамическое равновесие, при котором движение частиц хаотично. Максимальная энтропия означает полное термодинамическое равновесие, что эквивалентно хаосу. Часто второе начало термодинамики преподносится как объединенный принцип существования и возрастания энтропии. Принцип существования энтропии формулируется как математическое выражение энтропии термодинамических систем в условиях ...
... сравнение величин температур определяется по переходу тепла от рабочего тела к термометру. То есть, второе начало – это слишком общее свойство, которое не играет никакой практической роли в технической термодинамике. А из одного «закона сохранения энергии» невозможно вывести такие значимые формулы, как: КПД цикла Карно и формулу Майера. Невозможно также доказать, что в идеальном цикле изменение ...
... в другую. Процессы переноса теплоты представляют собой процессы обмена внутренней энергией между элементами рассматриваемой системы в форме теплоты. Общая характеристика и формулировка второго закона термодинамики Естественные процессы всегда направлены в сторону достижения системой равновесного состояния (механического, термического или любого другого). Это явление отражено вторым законом ...
... цикл с идеальным газом в диаграмме Т – s 1.7 Определение характеристик термодинамического состояния водяного пара Неизвестные величины в состояния 1, 2, 3, 4 определяются с помощью таблицы «Теплофизические свойства воды и водяного пара» или с помощью масштабной диаграммы h – s. Состояние 1 В соответствии с исходными данными табл.1 известны: V1 = 2,6 м3; Р1 = 4000 кПа = 40 бар Т1 = 573 К; ...


0 комментариев