МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РФ
МОСКОВСКАЯ ГОСУДАРСТВЕННАЯ АКАДЕМИЯ ТОНКОЙ ХИМИЧЕСКОЙ ТЕХНОЛОГИИ ИМЕНИ М.В. ЛОМОНОСОВА
Кафедра Химии и Технологии
Основного Органического Синтеза
Аттестационная работа по теме:
«Разделение смеси бензол – циклогексан – этилбензол – н-пропилбензол экстрактивной ректификацией»
на соискание степени бакалавра по направлению 550800
«Химическая Технология и Биотехнология»
Зам. заведующего кафедройА.В. Тимошенко
д.т.н., проф.
Руководители:
д.т.н., проф.А.В. Тимошенко
асп. Л.В. Иванова
СоискательА.В. Макашова
Москва 2004
Список сокращений
МБ – материальный баланс
ТБ – тепловой баланс
Т – температура, оС
ЭА – экстрактивный агент
РА – разделяющий агент
ЭР – экстрактивная ректификация
Б – бензол
ЦГ – циклогексан
ЭБ – этилбензол
ПБ – н-пропилбензол
NЭА –уровень подачи экстрактивного агента
NF – уровень подачи питания
ПЖР – парожидкостное равновесие
Введение
Процесс ректификации играет ведущую роль среди процессов разделения промышленных смесей. Большая энергоемкость процесса делает поиск оптимальных схем разделения актуальной задачей химической технологии. В промышленности разделению подвергаются многокомпонентные смеси как простых зеотропных, так и сложных азеотропных смесей. В последнем случае в связи с термодинамико-топологическими ограничениями получение чистых продуктов обычной ректификацией невозможно. Для решения этой проблемы предложен ряд методов, одним из которых является экстрактивная ректификация с использованием разделяющего агента. Данный метод достаточно прост в аппаратурном оформлении и не требует значительных энергозатрат по сравнению с другими методами разделения азеотропных смесей.
На сегодняшний день сложилась классификация схем экстрактивной ректификации, согласно которой разделяющий агент применяется на разных этапах разделения. Таким образом, возникает поливариантность организации процесса и необходимость исследования каждого варианта с целью выявить наименее энергоемкий.
В данной работе рассматриваются традиционные схемы разделения азеотропных смесей, состоящих из простых двухсекционных колонн. Цель работы заключается в разработке энергосберегающего процесса экстрактивной ректификации азеотропной смеси.
Литературный обзор Методы разделения азеотропных смесей
В различных отраслях промышленности используют разнообразные жидкие и газовые смеси, подлежащие разделению на чистые компоненты или фракции различного состава. Разделение таких смесей проводят в комплексах, основанных на процессе ректификации.
Если смесь образует азеотроп, то ее разделение на практически чистые компоненты методом обычной ректификации становится очень трудно. В данном случае необходимо использовать специальные методы ректификации:
1) разделение в комплексе колонн, работающих под разными давлениями;
2) экстрактивную ректификацию;
3)азеотропную и гетероазеотропную ректификацию.
Азеотропным смесям присущи термодинамико-топологические ограничения на выделение конечных фракций заданного состава. Основой для преодоления ограничений служит принцип перераспределения полей концентраций между областями разделения [1–3]. Этот принцип может быть реализован с использованием однородных и неоднородных (с включением экстракции, адсорбции, абсорбции, химических и др. методов разделения) разделительных комплексов. В первом случае процесс ректификации может быть организован так, что на одном из этапов осуществляется выделение азеотропной фракции, которая затем подвергается разделению с использованием специальных методов. Если это фракция двух и более компонентов, то можно использовать экстрактивную ректификацию или разделение азеотропного состава под разными давлениями. Если фракция содержит более двух компонентов, появляется возможность применить для разделения методы, использующие кривизну разделяющего многообразия [3, 4]. В работах [2, 5] предложен общий подход к синтезу схем ректификации многокомпонентных неидеальных (включая азеотропные) смесей, основанный на понятии области ректификации. Авторами [6–8] предложены некоторые подходы к синтезу технологических схем ректификации многокомпонентных смесей, содержащих один бинарный азеотроп. При этом используется метод разделения азеотропной смеси под разными давлениями.
Разделение азеотропных смесей в комплексах, работающих под разным давлениемПрименение данного метода рассматриваются авторами [6-9]. Для разделения азеотропных смесей используются комплексы (рис.1), работающие под разным давлением, которые позволяют преодолеть ограничения физико-химического характера и получать продукты требуемой чистоты.
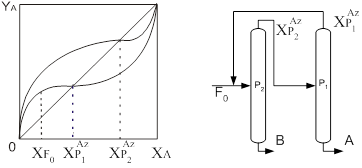
Рис.1. Разделение азеотропных смесей в комплексах, работающих под разным давлением
В таких случаях используется изменение состава азеотропной смеси с изменением температуры (при изменении давления) [11]. Изменение состава азеотропа, приходящееся на один градус температуры, согласно правилу Вревского, зависит от разности молярных теплот испарения компонентов. Следовательно, рассматриваемый метод разделения тем эффективнее, чем больше отличаются теплоты испарения компонентов разделяемой смеси. Обычно теплоты испарения значительно различаются у веществ различной химической природы. Но практическое применение метода ограничено, т.к. интервал изменения давления, в свою очередь, ограничен температурами хладагентов, используемых для конденсации паров в дефлегматорах, и теплоносителей, применяемых в кубах ректификационных установок.
Азеотропная ректификацияМетод азеотропной ректификации применим как для смесей с малым коэффициентом относительной летучести, так и для азеотропообразующих смесей (в том числе при составах, близких к азеотропу). При азеотропной ректификации разделяющий агент образует с каким-либо компонентом разделяемой смеси азеотроп с иным соотношением компонентов, нежели в исходной смеси, если последняя является азеотропообразующей. В качестве разделяющих агентов могут применяться вещества, образующие гомоазеотропы с компонентами исходной смеси (это могут быть азеотропы с максимумом или минимумом температур кипения), либо гетероазеотропы, представляющие собой тройные смеси разделяемых компонентов А и В с разделяющим агентом РА. Во всех случаях один из компонентов разделяемой смеси в колонне азеотропной ректификации может быть получен в практически чистом виде [10].
Наиболее сложным и энергоемким в схемах азеотропной ректификации является узел разделения азеотропной смеси.
Несколько проще разделение смеси с помощью разделяющего агента, образующего гетероазеотроп (рис.2). Последний после конденсации образует два жидких слоя с разными соотношениями разделяемых компонентов в них. Это различие в составах двух слоев позволяет использовать колонну меньшей эффективности (высоты) по сравнению с образованием гомоазеотропа. Температура кипения гетероазеотропа всегда ниже, чем у компонентов разделяемой смеси. Расслаивание и декантацию гетероазеотропной смеси осуществляют во флорентийском сосуде, позволяющем раздельно выводить слои легкой и тяжелой жидкости.
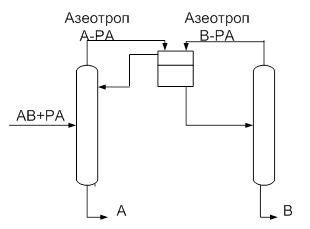
Рис.2. Принципиальная схема разделения гетероазеотропной смеси
Разделение азеотропных смесей методом экстрактивной ректификацииНаиболее часто на практике для преодоления теродинамико-топологических ограничений на выделение конечных фракций заданного состава используют метод экстрактивной ректификации.
Этот метод основан на увеличении движущей силы процесса разделения за счет изменения условий равновесия между жидкостью и паром, достигаемого путем добавления к заданной смеси специально подобранных веществ – разделяющих агентов. Если необходимо разделить на достаточно чистые компоненты трудноразделимую бинарную смесь, к такой смеси добавляют специально подобранный компонент (обычно труднолетучий), избирательно растворяющий один из компонентов исходной смеси и мало растворяющий другой. Иными словами, введение в систему третьего компонента заметно снижает упругость паров растворяемого компонента бинарной смеси, увеличивая тем самым коэффициент относительной летучести разделяемой смеси.
Выбор разделяющего агентаПри выборе разделяющих агентов для процессов азеотропной и экстрактивной ректификации должны учитываться свойства системы, подлежащей разделению. Прежде всего, в исходной системе должны быть определены требования, предъявляемые к разделяющему агенту. В основном, разделяющие агенты, используемые в процессах азеотропной и экстрактивной ректификации должны удовлетворять следующим требованиям:
1) избирательность, т.е. изменение относительной летучести компонентов заданной смеси в желательном направлении;
2) легкость регенерации из смесей с компонентами системы, подвергаемой разделению;
3) легкое отделение от продукта;
4) безопасность в обращении, доступность и дешевизна;
5) инертность по отношению к компонентам заданной смеси, термостабильность, неспособность вызывать коррозию аппаратуры.
Наиболее сложной задачей является выбор разделяющих агентов, удовлетворяющих первому требованию, тогда как последующие требования относятся к числу обычных технологических вопросов.[11,12]
Количественный эффект от использования разделяющего агента, при прочих равных условиях, определяется его концентрацией в колонне. Поэтому в случае непрерывной ректификации на линии равновесия наблюдается скачок концентраций в паровой фазе, обусловленный изменением концентрации экстрактивного агента в жидкости при подаче в колонну исходной смеси.
Помимо избирательного растворения одного из компонентов разделяемой смеси, экстрактивный агент должен удовлетворять ряду требований; основные из этих требований следующие [11,12]:
— он не должен образовывать азеотропов с компонентами исходной смеси (чтобы его можно было без затруднений в последствии отделить от них с целью его регенерации и получения чистых компонентов);
— он должен существенно отличаться от компонентов исходной смеси по температуре кипения, т.е. быть значительно более труднолетучим, чем ВКК исходной смеси, или (это бывает реже) значительно более легколетучим, чем низкокипящий компонент исходной смеси (что позволяет его выделить без больших энергетических и капитальных затрат).
Метод экстрактивной ректификации заключается в проведении процесса ректификации с практически нелетучими разделяющими агентами, или имеющими значительно меньшую относительную летучесть, чем компоненты заданной смеси. В процессах экстрактивной ректификации практически весь разделяющий агент отводится с кубовой жидкостью, а в дистиллат обычно попадает в очень небольших количествах. Разделяющий агент подается в ректификационную колонну на некотором расстоянии от ее верха и стекает вместе с флегмой. Образование азеотропных смесей разделяющим агентом с компонентами исходной смеси нежелательно во избежание загрязнения дистиллата разделяющим агентом.
Однако в некоторых случаях для экстрактивной ректификации применяются разделяющие агенты, образующие азеотропную смесь с компонентом, отбираемым в виде дистиллата. Такой процесс называется азеотропно-экстрактивной ректификацией.
Классификация схем экстрактивной ректификацииК настоящему времени сложилась классификация схем экстрактивной ректификации. Условно все технологические схемы можно разделить на две основные группы [13]. К первой группе схем относятся схемы с применением ЭА в первой колонне и выделением азеотропобразующего компонента на первом этапе (рис.3а, в).
Ко второй группе схем относятся структуры, в которых первоначально происходит фракционирование исходной смеси и отделение зеотропной и азеотропной составляющих друг от друга (рис. 3б). Далее каждая из них разделяется в последовательности простых двухсекционных колонн и в комплексе экстрактивной ректификации соответственно. В этом случае ЭА может применяться на любой стадии разделения, кроме первой.
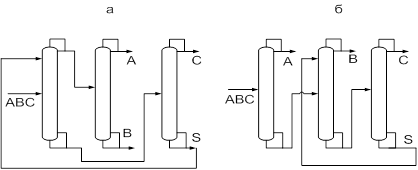
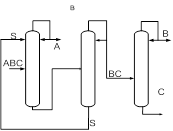
Рис.3. Разделение смеси АВС методом экстрактивной ректификации (а),(в) – с применением ЭА в первой колонне, (б) – с фракционированием исходной смеси
В целом, эти два класса схем охватывают все возможные варианты разделения. Схемы из первого класса для ректификации смесей с низкой размерностью концентрационного пространства можно использовать как элементы разделения смесей во второй группе схем для смесей более высокой размерности.
Экстрактивный агент должен направляться только в ту колонну (колонны), где его применение необходимо для разделения смеси. Поэтому иногда целесообразно применение последовательно соединенных комплексов экстрактивной ректификации (рис.4 а).
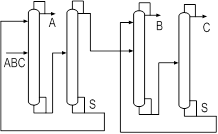
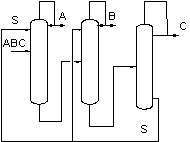
А б
Рис. 4. Схемы экстрактивной ректификации трехкомпонентной смеси при выделении в первой колонне индивидуального азеотропообразующего компонента
В случае сложного портрета ПЖР с несколькими азеотропами появляется необходимость подачи ЭА одновременно в две колонны комплекса (рис. 4 б). Такую организацию процесса следует всегда сопоставлять с двумя последовательно связанными комплексами ЭР для выявления наиболее эффективного решения.
Применение экстрактивной ректификации для разделения промышленных смесейМетоды экстрактивной ректификации в настоящее время применяются для решения разнообразных задач по разделению жидких смесей, а также для интенсификации процессов разделения. Нефть и природный газ широко применяются в химической промышленности и этим вызвана необходимость разделения смесей близкокипящих углеводородов. Последнее время находят все большее применение комбинированные РА, что позволяет понизить температуру кипения кубовой жидкости (это имеет существенное значение, если температуры кипения компонентов заданной смеси и РА сильно различаются).
Процесс экстрактивной ректификации почти никогда не используются самостоятельно, а являются стадиями технологических процессов разделения смесей. Широко применяется для выделения ароматических углеводородов из природных смесей и смесей с неорганическими компонентами, выделения и очистки 1.3-диоксолана, разделения углеводородов С4-С5 и т.д.
Выделение бутадиена из смесей углеводородов С4 [12]Методом ЭР решается одна из крупных промышленных проблем – выделение бутадиена из смесей углеводородов С4. Процессы экстрактивной ректификации играют важнейшую роль в общем комплексе производства бутадиена. Существует два пути получения бутадиена на основе метода ЭР. Первый путь – непосредственное выделение бутадиена из газов крекинга; второй – выделение бутадиена из смесей, получающихся при последовательном каталитическом дегидрировании бутана и бутиленов.
По условиям разделения оба эти способа в принципе равноценны. Различаются эти методы лишь относительным содержанием компонентов в исходных смесях.
Рассмотрим метод выделения бутадиена из смесей, получающихся при двухстадийном каталитическом дегидрировании бутана.
Смеси, из которых выделяется бутадиен, содержат (после отделения низкокипящих компонентов — например, водорода, метана, этана) вещества, приведенные в табл.1 в порядке возрастания температуры кипения.
Бутадиен с бутаном образует азеотроп, который при давлении 8 ат содержит 21 мол.% бутана. Это обстоятельство заставило обратиться к методу экстрактивной ректификации. Наилучшими разделяющими агентами были признаны фурфурол, ацетон и фенол в смеси с водой. Бутилены получаются со степенью чистоты 95—98%.
Принципиальная схема установки разделения бутан-бутиленовых смесей представлена на рис.5.
Таблица 1. Температуры кипения разделяемых веществ
| Углеводороды | Температура кипения, С | Углеводороды | Температура кипения, С |
| Пропилен | -47,70 | Бутан | -0,50 |
| Пропан | -42,07 | Транс-бутилен 2 | 0,88 |
| Метилацетилен | -23,20 | Цис-бутилен-2 | 3,72 |
| Изобутан | -11,73 | Винилацетилен | 5,1 |
| Изобутилен | -6,9 | Этилацетилен | 8,7 |
| Бутилен – 1 | -6,26 | Диацетилен | 9,8 |
| Бутадиен-1,3 | -4,41 | Диметилацетилен | 26,99 |
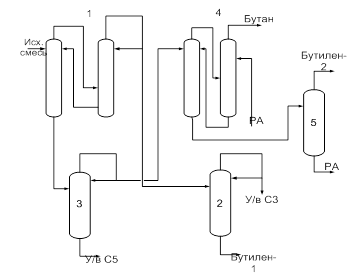
Рис.5. Схема процесса разделения бутан-бутиленовых смесей:
1-ректификационная система; 2, 3, 5- колонны; 4-система экстрактивной ректификации
Первая стадия процесса — выделение и очистка бутиленов, а также получение практически чистого бутана. В смеси присутствуют небольшие количества соединений с температурами кипения ниже и выше, чем температуры кипения углеводородов С4. Эту смесь подают в ректификационную систему 1, состоящую из двух последовательных колонн. В этой системе производится выделение бутилена-1 путем четкой ректификации. Вместе с бутиленом-1 в виде азеотропа с бутаном отгоняется бутадиен. В дистиллате содержатся также в небольших количествах углеводороды Сз и наиболее легкие углеводороды С4 изобутан и изобутилен. Этот дистиллат подается в колонну 2 для отгонки углеводородов С3. Полученная в этой колонне в виде кубовой жидкости смесь направляется в систему выделения бутадиена, в которой бутилен-1 отгоняется в смеси бутиленов, направляемой на вторую стадию дегидрирования.
Кубовая жидкость ректификационной системы 1 поступает в колонну 3, для выделения пентана и других высококипящих примесей, которые в процессе ректификации концентрируются в кубовой жидкости. Полученную в качестве дистиллата смесь бутиленов и бутана подают в систему экстрактивной ректификации 4, состоящую из двух последовательных колонн. В качестве разделяющего агента применяют фурфурол, содержащий ~6 вес. % воды. В виде дистиллата в процессе экстрактивной ректификации получается бутан, возвращаемый на дегидрирование. Бутилены отводятся в смеси с разделяющим агентом из куба. Эту смесь подают в отгонную колонну 5, в которой отгоняются бутилены, а разделяющий агент отбирают из куба в промежуточную емкость, из которой он возвращается в систему экстрактивной ректификации.
При использовании в качестве исходного сырья для выделения бутадиена газов крекинга бутилен-сырец содержит значительные количества изобутана и изобутилена, которые отгоняются вместе с бутиленом-1. Из этой смеси изобутилен удаляется путем поглощения 65% серной кислоты на холоду с последующей полимеризацией при нагревании. Оставшиеся же изобутан и бутилен-1 разделяются путем экстрактивной ректификации.
Вторая стадия процесса заключается в выделении и очистке бутадиена, а также регенерации непревращенных бутиленов для возвращения их в стадию дегидрирования.
Регулирование процесса осуществляется за счет того, что устанавливаются постоянные расходы исходной смеси, флегмы и разделяющего агента и температура последнего, а регулируемым параметром является нагрев куба. Соотношение расходов разделяющего агента и подаваемой смеси углеводородов составляет около 12 : 1 по объему.
Следует остановиться на вопросах, связанных с длительным использованием разделяющего агента. Хотя фурфурол является термостойким веществом, но в присутствии воды, бутадиена и других углеводородов при повышенных температуре и давлении может происходить его полимеризация и взаимодействие с непредельными углеводородами, в частности с бутадиеном. Это вызывает потери фурфурола и необходимость удаления образующихся продуктов реакции.
Другими источниками потерь являются утечки через неплотности в вентилях и насосах, а также попадание фурфурола в продукты разделения. Общие потери, зависящие от температуры, объема системы и концентрации углеводородов, весьма невелики и составляют 0,01—0,02% от расхода циркулирующего фурфурола. По данным заводских балансов, из этого количества ~60% приходится на полимеризацию, а 40% —на механические потери. [12]
Процесс удаления примесей из олефинов [14]В данной работе предлагается способ очистки олефинов от примесей, особенно таких как этилен и пропилен, которые традиционно получаются в процессах нефтепереработки. Для удаления примесей предлагается использовать экстрактивную ректификацию. Предпочтительно экстрактивный агент – это полярная жидкость, при 1 атм. имеющая температуру кипения около 38оС, содержащая 75 %вес. воды, спирта или нечто подобное. Авторы предлагают использование данного метода в широком интервале давлений (6,8-340,2атм.).
Рассмотрим применение данного метода более подробно.
Газовый поток после реактора, в котором происходит каталитическое получение олефинов, частично конденсируется в емкости при температуре 38оС и давлении 2,7 атм. Это паровой поток, содержащий различные углеводородные продукты содержит эитлен и пропилен, а также различные примеси (1,28% воды, 1,85% окисленных углеводородов, 0,995% из которых – диметиловый эфир, 0,32% – ацетальдегид). Паровой поток из емкости при давлении 2,7 атм. и 38оС поступает в нижнюю часть отпарной колонны, состоящей из 10 тарелок. На верх колонны подают жидкий поток воды при 4оС и 2,7 атм. Верхний продукт колонны содержит 0,95% воды и 0,81% окисленных углеводородов. Диметиловый эфир присутствует в паровом потоке в количестве 0,71%, ацетальдегид – 0,1%. Далее паровой продукт колонны сжимается до давления 20,4 атм. и с температурой 135,33оС направляется в колонну экстрактивной ректификации, состоящую из 39 тарелок и кипятильника. В качестве экстрактивного агента используется вода, которая поступает на первую тарелку колонны с температурой 32оС. Верхний паровой продукт колонны содержит углеводороды и удаляется с температурой 32,5оС и давлением 20,4 атм. Этот поток содержит 0,14% воды и менее 1 ppm окисленных углеводородов, включая диметиловый эфир и ацетальдегид.
О критериях оптимизации технологических схемПод оптимизацией понимают деятельность научных, проектных и производственных коллективов, направленную на создание производства, дающего наилучшие результаты в принятых условиях.
При выборе метода оптимизации необходимо учитывать критерий оптимизации, который является количественной мерой, позволяющей сравнивать все технологически осуществимые процессы и определять оптимальный вариант работы объекта.
Критерии оптимизации выбираются для всего производства, т.е. для всей системы. Однако чаще всего приходится сталкиваться с оптимизацией части технологического процесса (аппарат, комплекс аппаратов, цех или завод, входящий в комбинат). Следовательно, решаются частные задачи оптимизации.
В частных задачах оптимизации, когда требуется получить экстремальное значение какого-либо параметра работы отдельного аппарата, речь идет о некоторых экстремальных свойствах самого объекта оптимизации, которые обусловлены химическими или физико-химическими свойствами проходящего в данном объекте процесса.
Следовательно, в таких случаях критерием оптимальности служат технологические характеристики, которые косвенно оценивают экономичность работы агрегата (время пребывания реакционной смеси, выход продукта, конечная концентрация, температура и т.д.). В качестве критериев оптимизации могут быть использованы различные экономические (себестоимость продукции, приведенные затраты, средняя прибыль и т.п.) и технологические (качество продуктов, разделительный потенциал и т.п.) критерии. Тот или иной критерий выбирают исходя из поставленной задачи. Выбранный критерий должен соответствовать некоторым требованиям [11]:
1. он должен характеризовать эффективность процесса с точки зрения конечной схемы производства;
2. должен быть количественным и однозначным;
3. должен иметь физический смысл, чтобы можно было найти его значение для модельного процесса;
4. должен обладать простой и лёгкостью вычисления.
Ни один из существующих критериев не может отвечать всем требованиям. Наибольшему числу соответствует экономический критерий, но его расчет весьма трудоемок. Поэтому, для предварительных оценок часто используют другие критерии. В данной работе представлен один из таких критериев – энергозатраты, которые, для большого числа смесей изменяются пропорционально приведённым затратам. Для процесса ректификации энергозатраты определяются количеством тепла, подведенного в куб колонны, и могут быть определены по формуле:
Qi = riDi (Ri+1)
для i - ой колонны
![]()
для j - ой схемы
![]()
где: F– функция для определения оптимальной схемы
ri – мольная теплота испарения жидкости, кипящей в кубе;
Di – поток дистиллята;
R – флегмовое число для i - ой колонны;
z – число возможных схем разделения;
n – число ректификационных колонн.
Таким образом, расчет критерия энергозатрат сводится к расчету флегмового числа.
Таким образом, сама постановка задачи оптимизации предполагает наличие:
- объекта и выявление цели оптимизации. При этом устанавливается экстремальное значение только одной величины;
-возможности выбора значений некоторых параметров оптимизируемого объекта. При этом объект должен обладать определенными степенями свободы, т.е. при воздействии внешних факторов на систему изменять ее первоначальное состояние в соответствии с заданными требованиями;
- количественной оценки оптимизируемой величины, позволяющей выявить влияние управляющих воздействий.
Модели ПЖРВыбор модели, адекватно описывающей фазовое равновесие системы, является важным и необходимым шагом при решении массообменного процесса. На сегодняшний день разработано достаточно большое число методов математического моделирования различных типов парожидкостного равновесия. В настоящей работе на основании общих рекомендаций по применению были выбраны три группы математических моделей, имеющих различное представление о структуре раствора и межмолекулярных взаимодействиях:
· Модели локальных составов (Wilson, NRTL, UNIQUAC);
· Уравнения состояния (SRK, Peng Robinson);
· Групповая модель (UNIFAC).
Рассмотрим их более подробно.
Модели локальных составовКонцепция локальных составов позволяет учитывать структуру раствора, свойства чистых веществ и межмолекулярные взаимодействия разных типов (слабые неспецифические и сильные специфические). Согласно этой теории раствор рассматривается как упорядоченная структура. Для бинарной смеси можно выделить молекулы двух сортов, при этом молекула одного вида находится в окружении молекул другого вида. Зависимость между концентрациями компонентов внутри такого образования с общей молярной концентрацией компонентов в растворе описывается соотношением, учитывающим вероятность возникновения связей между разноименными молекулами.
Модель Вильсона[15,16,17,]Уравнение Вильсона было первым уравнением, в котором была применена концепция локального состава. Основная идея ее состоит в том, что из-за разницы в межмолекулярных взаимодействиях локальный состав вблизи конкретной молекулы в растворе будет отличаться от состава жидкости. Для бинарной пары два параметра связаны со степенью, в которой каждая молекула влияет на состав своего локального окружения. Выражение для коэффициента активности представлено ниже:
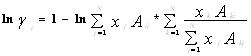
где :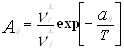 , (aij, °K);
, (aij, °K);
![]() – мольный объем жидкости компонента i.
– мольный объем жидкости компонента i.
Параметры aij представляет энергию взаимодействия между молекулами i и j.
Уравнение Вильсона может быть использовано в довольно широком интервале температур, несмотря на то, что его параметры в явном виде не включают температурную зависимость. Эта модель также дает хорошие результаты для смесей, содержащих полярные компоненты.
К недостаткам модели можно отнести то, что уравнение Вильсона не может описывать локальные максимумы или минимумы коэффициента активности, а также не подходит для описания равновесия с частично смешивающимися жидкими фазами.
Модель NRTL [18,19]Уравнение NRTL (non-random two-liquid – неслучайное двужидкостное) было разработано Реноном и Праузницем с целью использовать концепцию локального состава в тех случаях, когда уравнение Вильсона неспособно к предсказанию разделения фаз жидкость – жидкость. Модель NRTL дает хорошие результаты для широкого круга систем, в частности для смесей в высокой степени неидеальных и для частично несмешивающихся систем.
Выражение для коэффициента активности имеет вид:
![]()
![]() , (когда единицей измерения является °K)
, (когда единицей измерения является °K)
![]()
Для каждой бинарной пары требуется три параметра (![]() ,
, ![]() ,
, ![]() ), которые могут быть расширены включением в них температурной зависимости.
), которые могут быть расширены включением в них температурной зависимости.
Уравнение UNIQUAC (universal quasi-chemical – универсальное квазихимическое) было развито Абрамсом и Праусницем на основании статистически-механических положений и решеточной квазихимической модели Гуггенхайма. Каждую молекулу характеризует два параметра: объем ![]() и площадь (поверхность)
и площадь (поверхность) ![]() .
.
Избыточная энергия Гиббса (и соответственно логарифм коэффициента активности) делится на комбинаторную и остаточную части. Комбинаторная часть зависит только от размеров и форм отдельных молекул, она не содержит бинарных параметров. Остаточная часть, которая учитывает энергетические взаимодействия, имеет два регулируемых бинарных параметра. Выражение для коэффициента активности имеет следующий вид:
![]()
![]()

![]()
![]()
![]()
![]()
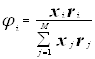
![]()
![]()
![]()
где ![]() ,
, ![]() – объем и площадь Ван-дер-Ваальса молекулы i
– объем и площадь Ван-дер-Ваальса молекулы i
С и R – комбинаторный и остаточный вклады в коэффициент активности жидкости.
Для каждой бинарной пары необходимы два параметра: Uij и Uji, которые используются в вычислениях остаточной части коэффициента активности. По желанию параметры могут быть расширены включением температурной зависимости.
Уравнение UNIQUAC адекватно описывает широкий ряд систем, оно применяется для неэлектролитических смесей, содержащих полярные или неполярные компоненты, также подходит для частично смешивающихся систем.
Уравнения состояния [23,24]Уравнения состояния применимы для широкого диапазона температур и давлений. Они могут быть использованы для расчетов всех термодинамических свойств, таких как К-значения, энтальпия, энтропия и плотность. Стандартным состоянием как для жидкости, так и для пара является идеальный газ, а отклонения от идеального поведения определяются расчетом коэффициентов фугитивности для обеих фаз.
Модель SRKВ 1972 г. для улучшения предсказания парового давления чистых компонентов и парожидкостного равновесия многокомпонентных смесей Соав предложил следующую температурную зависимость:
![]()
![]()
где ![]() – приведенная температура, Т/Тс
– приведенная температура, Т/Тс
![]() – ацентрический фактор
– ацентрический фактор
Константы в уравненииях были получены из преобразования данных по паровому давлению для ограниченного числа обычных углеводородов. Эти пределы использования уравнения состояния СРК ограничены неполярными компонентами.
Уравнение состояния Соав-Редлих-Квонга – это модификация уравнения состояния Редлиха-Квонга (которое основано на уравнении Ван-дер-Ваальса). Соав заменил член ![]() более общей температурной зависимостью а(Т). Выражение получило следующий вид:
более общей температурной зависимостью а(Т). Выражение получило следующий вид:
![]()
где ![]()
![]()
![]() ,
, ![]() – критические температура и давление для i-го компонента
– критические температура и давление для i-го компонента
![]()
![]()
![]()
![]()
![]()
![]() – ацентрический фактор для компонента i
– ацентрический фактор для компонента i
![]() – константа бинарного взаимодействия для компонентов i и j
– константа бинарного взаимодействия для компонентов i и j
Введение члена альфа позволило улучшить предсказание парового давления для чистых компонентов. Комбинированная формула для вычисления α(Т) с введенным членом ![]() означает улучшение предсказания свойств смеси.
означает улучшение предсказания свойств смеси.
Использование формулировки Соава для предсказания свойств смеси включает в себя два этапа. Во-первых, для каждого из компонентов подбирается ацентрический фактор компонента (wi) таким образом, чтобы точно предсказать давление паров компонента. Во-вторых, из экспериментальных данных для бинарных систем с компонентами i и j, для которых достигается фазовое равновесие, определяется параметр kij.
Модель Peng-RobinsonУравнение состояния Пенга-Робинсона было опубликовано в 1976 году и является модификацией уравнения Редлиха-Квонга. Во многих отношениях оно похоже на уравненеие SRK, но все же он разработано для улучшения предсказания плотности жидкости
![]()
Введением дополнительных членов было достигнуто улучшение предсказания давления пара чистых компонентов и улучшение предсказания свойств смесей.
Использование уравнения Пенга-Робинсона включает в себя два шага, аналогичные предыдущей модели.
Групповые моделиГрупповые модели основаны на предположении об аддитивности вкладов различных химических групп в термодинамические свойства компонентов и смесей. Наибольшее распространение получила модель UNIFAC. Именно её мы использовали для создания псевдоэкспериментальных данных парожидкостного равновесия. Рассмотрим модель более подробно.
Модель UNIFAC [25,26,27]Метод UNIFAC (universal functional activity coefficient – универсальный функциональный коэффициент активности) был разработан в 1975 году Фреденслундом, Джонсом и Праузницем. Данный метод рассчитывает величины коэффициентов активности на основе концепции группового вклада. Предполагается, что взаимодействия между двумя молекулами являются функцией взаимодействий между группами. Данные межгруппового взаимодействия получаются путем обработки экспериментальных данных для пар компонентов. Число функциональных групп ограничено.
Метод UNIFAC основан на модели UNIQUAC, которая представляет избыточную энергию Гиббса (и логарифм коэффициента активности) как комбинацию двух эффектов. Таким образом, используется уравнение:
![]()
Комбинационный член ![]() рассчитывается непосредственно по уравнению UNIQUAC с использованием параметров площади и объема Ван дер Ваальса, рассчитанных по индивидуальным структурным группам :
рассчитывается непосредственно по уравнению UNIQUAC с использованием параметров площади и объема Ван дер Ваальса, рассчитанных по индивидуальным структурным группам :
![]()
где:
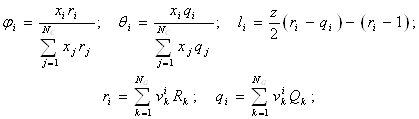
NC – число компонентов;
NG – число различных групп в смеси;
z – согласованное число для пространственной решетки, равное 10;
![]() – число функциональных групп типа k в молекуле i;
– число функциональных групп типа k в молекуле i;
Rk – параметр объема для функциональной группы k;
Qk – параметр площади для функциональной группы k;
xi – мольная доля компонента i в жидкой фазе.
Материальный баланс процесса экстрактивной ректификацииЭкстрактивная ректификация отличается от обычной тем, что в колонну кроме исходной смеси и флегмы вводят разделяющий агент, причем его расход чаще всего значительно превышает расходы других материальных потоков, что влечет за собой соответствующее изменение материального и теплового балансов процесса ректификации.
Ректификационная колонна состоит из 3 основных частей:
1) регенерационная, которая располагается выше точки ввода разделяющего агента и предназначена для очистки отбираемого дистиллата от разделяющего агента путем обычной ректификации;
2) укрепляющая, располагается между точками ввода исходной смеси и разделяющего агента. В ней происходит обогащение восходящего пара компонентами, отбираемыми в виде дистиллата;
3) исчерпывающая, расположенная ниже точки ниже ввода исходной смеси. Предназначена для выделения из истекающей жидкости компонентов, отбираемых в виде дистиллата.
В регенерационной части колонны мольные доли РА в паре(![]() ), в жидкости (
), в жидкости (![]() ) и (хр)д связаны условием материального баланса по уравнению (1):
) и (хр)д связаны условием материального баланса по уравнению (1):
D![]() = L
= L![]() + П(хр)д,где (хр)д концентрация РА в дистиллате(1)
+ П(хр)д,где (хр)д концентрация РА в дистиллате(1)
Если (хр)д = 0, то ![]() =
= ![]()
![]() (2)
(2)
Для произвольного сечения укрепляющей части экстрактивной колонны, если РА не содержит компонентов исходной смеси, то МБ по произвольному компоненту выражается уравнением:
Dn+1 yn+1=LnXn+ПXд илиуn+1 =![]() xn+
xn+ ![]() xд(3)
xд(3)
где D, G, L и П- молярные расходы пара, разделяющего агента, жидкости и дистиллата; n -номер тарелки считая сверху вниз. [12]
Это уравнение выражает зависимость между концентрациями любого компонента в паре и жидкости, проходящих через произвольное сечение укрепляющей части колонны экстрактивной ректификации.
Материальный баланс произвольного участка исчерпывающей части колонны, включая куб, выражается уравнением:
Lm=Dm-1+G+Wk(4)илиy =![]()
![]() -
-![]() (5)
(5)
где Wk- молярныйрасход компонентов заданной смеси, отбираемой в виде кубового остатка; m- номер тарелки (снизу вверх).
где ![]() - приведенное флегмовое число исчерпывающей части колонны для экстрактивной ректификации.
- приведенное флегмовое число исчерпывающей части колонны для экстрактивной ректификации.
В кубе имеет место скачкообразное возрастание концентрации РА, поскольку величина Wkвсегда составляет лишь часть величины W для произвольной тарелки. При подаче в колонну исходной смеси в виде жидкости скачкообразное изменение концентрации РА происходит также на тарелке питания. В этом случае концентрация РА в укрепляющей части больше, чем в исчерпывающей. Соответственно с этим изменяются и условия равновесия между жидкостью и паром.
В зависимости от распределения концентрации РА по высоте колонны изменяется и температура. Наивысшую температуру кипения имеет кубовая жидкость с максимальной в ней концентрацией РА. Затем на ближайших к кубу тарелках температура резко понижается и далее по мере приближения к точке ввода РА температура продолжает медленно уменьшаться. Обусловлено это, с одной стороны, понижением температуры кипения в связи с возрастанием концентрации отгоняемого компонента, а с другой стороны,- уменьшением гидравлического сопротивления части колонны, находящейся выше рассматриваемого сечения. Выше точки ввода РА температура резко понижается в связи с резким уменьшением его концентрации. При подаче в колонну исходной смеси в виде жидкости вблизи тарелки питания происходит резкое изменение температуры, обусловленное скачкообразным изменением концентрации РА. [12]
Постановка задачи
Целью данной работы является поиск оптимальной схемы экстрактивной ректификации смеси бензол-циклогексан-этилбензол-н-пропилбензол, содержащей один бинарный азеотроп. Для этого необходимо выполнить:
· параметрическую оптимизацию традиционных схем экстрактивной ректификации;
· сравнение полученных результатов и выбор энергосберегающего решения.
Расчетно-экспериментальная часть Программный комплекс PRO/ II
Данная программа предназначена для проектно-поверочного расчета и поверочного расчета химико-технологических процессов и, в частности, процесса ректификации. Программа включает широкий набор методов, позволяющих создавать модели для широкого круга систем, использующихся в различных отраслях химической промышленности. В программе совместно с термодинамическими методами могут также быть использованы транспортные свойства индивидуальных соединений и их смесей. Последние включают в себя вязкости паров и жидкости, теплопроводности паров и жидкости и диффузию жидкости. Расчет поверхностного натяжения на границе пар-жидкость, хотя это и не транспортное свойство, также относится к этой группе. Транспортные свойства находят применение в строгих расчетах теплопередачи, расчетах перепадов давления, расчетах колонн с ситчатыми тарелками и насадочных колонн.
Требования к аппаратным средствам
Для работы программы PRO/II требуется: IBM совместимый компьютер с процессором 80386 и выше, имеющий 4 и более мегабайта оперативной памяти. Операционная система MS Windows версия 3.1, Windows-95 или более поздняя версия.
Выходные данные программыОтчет по колонне включает в себя: суммарные данные по колонне. Суммарные данные по колонне содержат температуры, давления, расходы, тепловые нагрузки по каждой тарелке, информацию по потокам сырья и продуктов и общие тепловой и материальный балансы. По умолчанию расходы выводятся в мольных единицах. Путем выбора соответствующего варианта может быть выведен дополнительный суммарный отчет в массовых, объемных или газовых объемных единицах: молекулярные веса, реальные плотности, реальные объемные расходы и транспортные свойства, энтальпии потоков и стандартные плотности жидкости, К.П.Д. тарелок и/или К.П.Д. тарелок для отдельных компонентов, диаграмма температур, давлений, мольных расходов, расходов сырья, и продуктов и тепловых нагрузок нагревателей/холодильников, суммарная нагрузка тарелок, отчет по составам, таблица извлечения компонента, отчет по сепаратору, отчет по теплообменнику.
Выбор исходной смеси и экстрактивного агентаВ качестве объекта исследования была выбрана четырехкомпонентная смесь бензол – циклогексан – этилбензол – н-пропилбензол, содержащая один бинарный азеотроп на стороне бензол – циклогексан. Для разделения азеотропной пары применяется анилин, его применение рекомендовано авторами [12]. В табл.2 представлены физико-химические свой ства чистых компонентов и параметры азеотропа.
Таблица 2
Свойства чистых компонентов
| Вещество | Ткип, ◦С | Тплавл., ◦С | Ткрит, ◦С | Ркрит, кг/см2 | Плот-ность, кг/м3 | Молекулярная масса, г/моль |
| Бензол | 80,09 | 5,53 | 288,90 | 49,92 | 883,92 | 78,11 |
| Циклогексан | 80,72 | 6,54 | 280,39 | 41,54 | 782,65 | 84,16 |
| Этилбензол | 136,20 | -94,95 | 344,00 | 36,80 | 870,96 | 106,17 |
| н-Пропилбензол | 159,24 | -99,60 | 365,20 | 32,63 | 865,62 | 120,19 |
| Анилин | 184,35 | -6,02 | 425,85 | 54,14 | 1025,5 | 93,13 |
Таблица 3
Параметры бинарного азеотропа бензол-циклогексан [28]
| Ткип1,оС | Ткип2,оС | Ткип смеси,оС | Конц1, вес% | Тип азеотропа |
| 80,09 | 80,74 | 28,4(128) * | 49,4 мол% | гом |
| 80,09 | 80,74 | 33,1(155) | 49,8 мол% | гом. |
| 80,10 | 80,75 | 39,99(–) | 51,1 мол% | гом |
| 80,09 | 80,74 | 48,3(287) | 49,3 мол% | гом |
| 80,09 | 80,74 | 50,4(307) | 51,2 мол% | гом |
| 80,09 | 80,74 | 63,7(495) | 52,6 мол% | гом |
| 80,09 | 80,74 | 69,8(602) | 53,1 мол% | гом |
________________
*В скобках указано давление при котором проводилось измерение
Мы рассмотрели тройную смесь, разделяемую в комплексе экстрактивной ректификации при давлении 0,3 кг/см2. В концентрационном симплексе мы определили ход альфа линий (рис. 6). Значения альфа линий представлены для пары компонентов 12, где 1 – циклогексан, 2 – бензол.
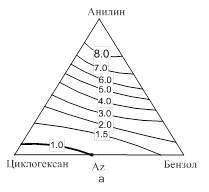
Рис. 6. Ход альфа-линий в смеси циклогексан-бензол-анилин при 0,3 кг/см2
В данном случае на рис. 6 единичная альфа линия делит симплекс на две области. Область α<1 прилегает к легкокипящему циклогексану. Здесь максимальным коэффициентом распределения обладает бензол, что делает невозможным выделение чистого циклогексана при нахождении состава питания в данной области.
В области α>1 циклогексан обладает максимальным коэффициентом распределения и может быть выделен в качестве дистиллата экстрактивной колонны. Поэтому нами был выбран эквимолярный состав исходного питания, при котором хРА=0,8 (F:РА=1:4), где значение коэффициента относительной летучести α ≈ 8 (>2).
Тепловой баланс процесса экстрактивной ректификации
В качестве критерия оптимизации традиционного варианта организации процесса экстрактивной ректификации мы использовали суммарные энергетические затраты в кипятильниках колонн:
![]() , (6)
, (6)
где N – число колонн в технологической схеме.
Причем, энергетические затраты в кубе каждой колонны рассчитываются, исходя из общего теплового баланса.
Для колонны экстрактивной ректификации традиционной схемы уравнение теплового баланса имеет вид:
![]() ,(7)
,(7)
где QF = F*CF*TF – количество тепла, поступающее с потоком исходной смеси;
QЭА = PЭА*СЭА*ТЭА – количество тепла, поступающее в колонну с потоком экстрактивного агента;
QD = D*CD*TD – количество тепла, отводимое из колонны с потоком дистиллята;
QW = W*CW*TW – количество тепла, отводимое из колонны с кубовым потоком;
Qконд = D(R+1)r – количество тепла, отводимое при конденсации потоков дистиллята и флегмы.
Откуда затраты тепла в кипятильнике:
Qкип = QD + QW + Qконд – QF – QЭА(8)
Qкип = D*CD*TD + W*CW*TW + D(R+1)r – F*CF*TF – PЭА*СЭА*ТЭА (9)
При заданных количестве, составе питания и качестве продуктов поток дистиллята определяется из общего материального баланса колонны и является фиксированной величиной. Следовательно, теплосодержание верхнего продукта QD есть величина практически постоянная. Величина кубового потока также определяется из материального баланса и зависит от F:ЭА. Следовательно, теплосодержание нижнего продукта QW зависит от расхода разделяющего агента. Величина QF в уравнении (8) является постоянной, поскольку все расчеты мы проводили при фиксированном количестве исходной смеси заданного состава, поступающей в колонну при температуре кипения.
Таким образом, величина энергетических затрат в кубе экстрактивной колонны в рассматриваемом случае зависит в основном от флегмового числа, температуры и расхода подаваемого в колонну экстрактивного агента.
Как известно, флегмовое число в колонне заданной эффективности определяется, с одной стороны, природой разделяемой смеси, а с другой – положением тарелки питания, поскольку в зависимости от точки подачи исходной смеси в колонне формируется определенный профиль концентраций компонентов (траектория ректификации).
В колонне ЭР на формирование профиля оказывает существенное влияние и уровень ввода ЭА.
Температура подачи в колонну ЭА оказывает неоднозначное влияние на величину энергозатрат. С одной стороны, как видно из уравнения (9), чем выше температура ЭА, тем меньше на первый взгляд, Qкип. Однако поскольку ЭА подают в верхнее сечение колонны и при этом увеличивается его концентрация на верхних тарелках, то для получения дистиллята заданного качества потребуются более высокие значения флегмового числа, что в свою очередь приводит к росту Qкип.
Для колонны регенерации ЭА уравнение теплового баланса имеет вид:
QF + Qкип = QD + QW + D(R+1)r.(10)
Откуда Qкип = QD + QW + D(R+1)r – QF(11)
Обозначения те же, что и в уравнении (7)
В данном случае количество и состав исходной смеси и продуктовых потоков определяется общим материальным балансом схемы. Поэтому величина энергозатрат зависит в основном от флегмового числа, которое в свою очередь в колонне заданной эффективности определяется положением тарелки питания.
Таким образом, основными параметрами, определяющими энергоемкость традиционной схемы экстрактивной ректификации, состоящей из двух колонн, при заданных количестве, составе и температуре исходной смеси и заданном качестве продуктовых потоков являются:
— для колонны экстрактивной ректификации: взаиморасположение тарелок подачи в колонну исходной смеси и экстрактивного агента, температура и расход ЭА;
— для колонны регенерации экстрактивного агента: уровень ввода исходной смеси.
Выбор адекватной модели ПЖРИз литературных данных нами были получены данные по парожидкостному равновесию для следующих бинарных составляющих: бензол – этилбензол; этилбензол – н-пропилбензол; бензол – н-пропилбензол; бензол – циклогексан. Фазовое равновесие остальных бинарных пар были рассчитаны, используя групповую модель UNIFAC. Экспериментальные и псевдоэкспериментальные данные, а также результаты их сравнения представлены в табл. 4.
В качестве критерия сравнения для статистической обработки результатов было выбрано среднее относительное отклонение описания паровой фазы, δ:
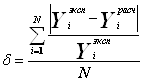 ,(12)
,(12)
где N – количество экспериментальных точек фазового равновесия.
Таблица 4.
Результаты моделирования парожидкостного равновесия бинарных составляющих
| Смесь | δ, % | ||||
| NRTL | UNIQUAC | Wilson | SRK | PR | |
| бензол-этилбензол | 1,261 | 4,343 | 3,460 | 0,755 | 0,182 |
| бензол-циклогексан | 0,332 | 0,249 | 0,256 | 0,070 | 0,363 |
| бензол-пропилбензол | 1,025 | – | 0,090 | 0,361 | 0,176 |
| этилбензол-пропилбензол | 0,052 | – | 0,053 | 0,537 | 0,317 |
| циклогексан-этилбензол | 0,038 | 0,027 | 0,038 | 0,148 | 0,280 |
| бензол-анилин | 0,006 | 0,015 | 0,014 | 0,034 | 0,171 |
| циклогексан-анилин | 0,012 | 0,033 | 0,019 | 0,163 | 0,299 |
| этилбензол-анилин | 0,037 | 0,058 | 0,055 | 0,127 | 0,369 |
Из табличных данных видно, что во всех случаях значение критерия сравнения не превышает 1%, исключение составляет лишь описание фазового равновесия бинарной составляющей бензол-этилбензол моделями UNIQUAC и Wilson. Однако при более подробном рассмотрении можно сказать о приоритете модели NRTL над всеми остальными. Только эта модель обеспечивает минимальное отклонение описания паровой фазы в 50% случаев, в то время как все оставшиеся – всего лишь в 12%. Исходя из этого, примем для дальнейшего описания фазового равновесия системы модель локальных составов NRTL.
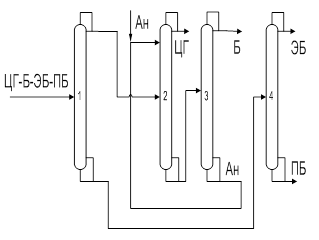
Определение оптимальных рабочих параметров экстрактивной ректификации по схеме с использованием разделяющего агента в первой колоннеПринципиальная технологическая схема ректификации азеотропной смеси циклогексан-бензол–этилбензол–н-пропилбензол с использованием анилина в качестве разделяющего агента приведена на рис.7.
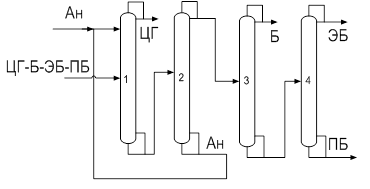
Рис. 7. Технологическая схема ЭР с применением ЭА в первой колонне
Технологическая схема представляет собой последовательность из четырех ректификационных колонн. Две первые колонны составляют традиционный комплекс экстрактивной ректификации, необходимый для разделения азеотропообразующей пары компонентов. Согласно классификации схем экстрактивной ректификации данный вариант организации процесса относится к группе схем с использованием разделяющего агента на первом этапе и, следовательно, выделением азеотропообразующего компонента в первой колонне.
Рассмотрим работу установки более подробно. В колонне 1 осуществляется разноуровневая подача: разделяющий агент подается в верхнюю часть, а исходная смесь – в среднюю часть колонны. Под действием ЭА происходит изменение относительной летучести компонентов исходной смеси, в результате в качестве дистиллята отбирается практически чистый высококипящий компонент – циклогексан. Кубовая жидкость, содержащая анилин и бензол, направляется на разделение в колонну 2. В колонне регенерации экстрактивного агента анилин выделяется в качестве нижнего продукта и возвращается в верхнюю часть колонны 1, образуя рецикл. Верхний продукт колонны 2, содержащий бензол, этилбензол и пропилбензол далее разделяется в последовательности простых двухсекционных колонн, работающих в режиме первого заданного разделения.
Нами была проведена параметрическая оптимизация комплекса экстрактивной ректификации с целью снижения энергозатрат на разделение.
Первоначально мы определили оптимальную совокупность рабочих параметров колонны экстрактивной ректификации. Известно, что энергоемкость разделения в колонне экстрактивной ректификации при фиксированных количестве, составе и температуре исходной смеси и заданном количестве продуктовых потоков зависит от температуры и расхода ЭА, а также от уровня ввода исходной смеси и разделяющего агента.
Расчет проводили на 100 моль/час исходной смеси, содержащей бензол-циклогексан-этилбензол-н-пропилбензол, эквимолярного состава. Эффективность колонн задавали равной 20 т.т. Качество продуктовых фракций – 99%мольн. целевого компонента, за исключением фракции регенерированного анилина (содержание экстрактивного агента 99,9%мольн.).
На первом этапе, закрепив соотношение исходной смеси и экстрактивного агента (1:2), мы исследовали влияние температуры подачи анилина на энергетические затраты. Диапазон исследуемых температур закрепили в интервале 60–100 °С с шагом 10 °С. Для каждой из установленных температур определили оптимальное положение тарелок питания и ввода экстрактивного агента. Результаты расчета приведены в табл.5.
Таблица 5.
Изменение энергозатрат в зависимости от температуры подачи экстрактивного агента. F:ЭА = 1:2
| Температура подачи ЭА, °С | NЭА/NF | Флегма колонны 1 | Энергозатраты, ГДж/ч |
| ||
| Колонны 1 | Суммарные |
| ||||
| 100 | 4/11 | 1,450 | 2,558 | 37,326 | ||
| 90 | 4/11 | 0,983 | 2,561 | 37,285 | ||
| 80 | 4/10 | 0,642 | 2,642 | 37,375 | ||
| 70 | 5/14 | 0,261 | 2,675 | 37,596 | ||
| 60 | 4/12 | 0,172 | 2,905 | 37,805 | ||
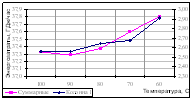
Рис.8. Изменение энергозатрат в зависимости от температуры подачи ЭА
Видно, что при изменении температуры подачи ЭА оптимальное положение уровня подачи ЭА практически не изменяется. Флегмовое число уменьшается с уменьшением температуры. Это связано с тем, что при более высокой температуре возрастает концентрация анилина в укрепляющей секции колонны и для получения циклогексана заданного качества требуется возвращать в колонну больший поток флегмы. Зависимость суммарных энергозатрат от температуры имеет экстремальный характер – минимальные знергозатраты наблюдаются при температуре подачи ЭА 90 0С, что видно из рисунка 8.
Изменение энергозатрат на разделение при разных температурах подачи экстрактивного агента можно объяснить, рассмотрев уравнение теплового баланса (9). Члены уравнения Qконд и QЭА зависят от ТЭА. С одной стороны, с ростом температуры анилина происходит увеличение флегмового числа и затрат на конденсацию (Qконд), а с другой стороны, увеличивается количество тепла, приносимое потоком ЭА в колонну (QЭА). Очевидно, что увеличение Qконд приводит к росту энергопотребления в кубе, а увеличение QЭА — к его снижению. По полученным результатам для экстрактивной колонны можно сказать, что снижение энергозатрат за счет увеличения теплосодержания ЭА практически во всех случаях, превышает их рост за счет увеличения затрат на конденсацию.
Далее мы рассмотрели зависимость энергозатрат на разделение от температуры и расхода ЭА, определив на предыдущем этапе оптимальные уровни подачи входящих потоков экстрактивной колонны, а также температуру ввода разделяющего агента, закрепив их, мы исследовали влияние расхода ЭА на энергозатраты. Результаты представлены в табл. 6 и на рис. 9.
Таблица 6. З
Зависимость энергозатрат от расхода ЭА при температуре его подачи 90ºС. Уровни подачи NЭА/NF = 4/11
| Расход ЭА, моль/час | Флегма колонны 1 | Энергозатраты,ГДж/ч | |
| Колонны 1 | Суммарные | ||
| 50 | 1,420 | 2,315 | 24,400 |
| 60 | 1,500 | 2,316 | 23,140 |
| 70 | 1,519 | 2,318 | 22,870 |
| 80 | 1,521 | 2,321 | 22,890 |
| 90 | 1,514 | 2,329 | 22,960 |
| 100 | 1,515 | 2,338 | 22,950 |
Из приведенных данных видно, что энергозатраты экстрактивной колонны не чувствительны к изменению расхода ЭА. В общем, уменьшение расхода разделяющего агента со 100 до 50 моль/час приводит к колебаниям значений суммарных энергозатрат на
разделение в пределах 6%. Однако для всей схемы в целом наблюдается экстремальная зависимость энергозатрат с минимумом при расходе ЭА, равным 70 моль/час.
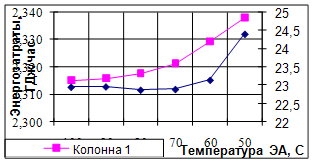
Рис.9. Зависимость энергозатрат от расхода ЭА при температуре его подачи 90 оС
Появление минимума на зависимости суммарных энергозатрат от расхода ЭА можно легко объяснить, если рассмотреть изменение численного соотношения величин QЭА, QW и Qконд в уравнении теплового баланса (8) С уменьшением расхода анилина увеличивается флегмовое число и, соответственно, энергозатраты на конденсацию. Наряду с этим уменьшается количество тепла, приносимое в колонну с потоком экстрактивного агента. Это приводит к росту Qкип. С другой стороны, за счет уменьшения кубового потока происходит снижение QW, а следовательно и Qкип.
Далее мы проделали подобную процедуру для каждого значения температуры ЭА и определили оптимальный расход экстрактивного агента, при котором наблюдаются минимальные нагрузки на кипятильники колонн. Результаты представлены в табл. 7.
Таблица 7. Зависимость энергозатрат от расхода ЭА при разных температурах подачи ЭА
| Температура подачи ЭА, °С | Опт. расход ЭА, моль/час | Флегма колонны 1 | Энергозатраты,ГДж/ч | |
| Колонны 1 | Суммарные | |||
| 100 | 60 | 1,724 | 2,338 | 22,967 |
| 90 | 70 | 1,519 | 2,318 | 22,870 |
| 80 | 70 | 1,328 | 2,341 | 22,967 |
| 70 | 70 | 1,113 | 2,334 | 21,914 |
| 60 | 70 | 0,991 | 2,344 | 22,738 |
В общем, флегмовое число уменьшается с уменьшением температуры. Минимальные энергозатраты наблюдаются при оптимальном расходе 70 моль/час и температуре подачи ЭА 700С. Далее мы определили величину минимального и оптимального расхода разделяющего агента от его температуры и положения тарелок питания. При этом для каждого набора параметров фиксировали энергозатраты на разделение. Результаты представлены в табл. 8.
Таблица 8.
Зависимость величины минимального и оптимального расхода ЭА от его температуры и положения тарелок питания
| NЭА/NF | Расход ЭА, моль/час | Флегма Т1 при опт. расходе | Энергозатраты при опт. расходе ЭА, ГДж/час | Энергозатраты при мин. расходе ЭА, ГДж/час | |||
| Опт. | Мин. | Колонна 1 | Суммарные | Колонна 1 | Суммарные | ||
| ТЭА=600С | |||||||
| 4/10 | 80 | 50 | 1.750 | 2.357 | 22.912 | 2.357 | 22.936 |
| 4/11 | 80 | 50 | 1,728 | 2,339 | 22,893 | 2,337 | 22,978 |
| 4/12 | 50 | 50 | 1,765 | 2,457 | 23,333 | 2,457 | 23,333 |
| 5/10 | 50 | 50 | 1,870 | 2,457 | 23,333 | 2,457 | 23,333 |
| 5/11 | 60 | 50 | 1,764 | 2,372 | 23,217 | 2,371 | 23,255 |
| 5/12 | 50 | 50 | 1,770 | 2,378 | 23,239 | 2,378 | 23,239 |
| ТЭА=700С | |||||||
| 4/10 | 60 | 50 | 1,544 | 2,358 | 22,880 | 2,356 | 22,962 |
| 4/11 | 70 | 50 | 1,521 | 2,340 | 22,869 | 2,338 | 22,940 |
| 4/12 | 70 | 50 | 1,563 | 2,374 | 22,906 | 2,370 | 22,996 |
| 5/10 | 100 | 50 | 1,555 | 2,425 | 23,051 | 2,455 | 23,330 |
| 5/11 | 70 | 50 | 1,550 | 2,372 | 23,196 | 2,371 | 23,250 |
| 5/12 | 60 | 50 | 1,558 | 2,378 | 23,210 | 2,378 | 23,238 |
| ТЭА=800С | |||||||
| 4/10 | 60 | 50 | 1,349 | 2,360 | 22,885 | 2,359 | 22,920 |
| 4/11 | 60 | 50 | 1,327 | 2,342 | 22,860 | 2,342 | 22,867 |
| 4/12 | 50 | 50 | 1,370 | 2,377 | 22,889 | 2,377 | 22,889 |
| 5/10 | 70 | 50 | 1,451 | 2,455 | 23,306 | 2,453 | 23,376 |
| 5/11 | 90 | 50 | 1,348 | 2,373 | 23,194 | 2,373 | 23,221 |
| 5/12 | 90 | 50 | 1,357 | 2,380 | 23,207 | 2,378 | 23,284 |
| ТЭА=900С | |||||||
| 4/10 | 60 | 50 | 1,171 | 2,360 | 22,822 | 2,358 | 22,883 |
| 4/11 | 60 | 50 | 1,146 | 2,340 | 22,870 | 2,341 | 22,841 |
| 4/12 | 50 | 50 | 1,191 | 2,375 | 22,850 | 2,376 | 22,850 |
| 5/10 | 90 | 50 | 1,263 | 2,452 | 23,261 | 2,449 | 23,335 |
| 5/11 | 90 | 50 | 1,160 | 2,370 | 23,180 | 2,370 | 23,210 |
| 5/12 | 90 | 50 | 1,170 | 2,378 | 23,188 | 2,378 | 23,204 |
| ТЭА=1000С | |||||||
| 4/10 | 50 | 50 | 1,003 | 2,359 | 22,843 | 2,359 | 22,843 |
| 4/11 | 70 | 50 | 0,991 | 2,344 | 22,738 | 2,342 | 22,827 |
| 4/12 | 50 | 50 | 1,023 | 2,376 | 22,860 | 2,376 | 22,860 |
| 5/10 | 50 | 50 | 1,095 | 2,452 | 23,226 | 2,452 | 23,226 |
| 5/11 | 60 | 50 | 0,992 | 2,371 | 23,155 | 2,371 | 23,177 |
| 5/12 | 50 | 50 | 0,999 | 2,379 | 23,183 | 2,379 | 23,183 |
Как видно из таблицы 8, минимальные энергозатраты в кипятильниках колонн обеспечиваются при следующих значениях рабочих параметров: температуре подачи ЭА 1000С, расходе ЭА 70 моль/час, уровнях подачи экстрактивного агента и исходной смеси на 4 и 11 тарелки соответственно.
Заметим, что независимо от температуры подачи ЭА оптимальные уровни подачи экстрактивного агента и исходной смеси находятся на 4 и 11 (10-ой для Т=900С) тарелках соответственно.
Далее рассмотрим изменение энергозатрат в колонне регенерации от положения тарелки питания при различных температурах подачи экстрактивного агента. Результаты представим в табл. 9.
Таблица 9. Зависимость энергозатрат в колонне регенерации от положения тарелки питания
| Температура, оС | Оптимальная тарелка питания | Энергозатраты, ГДж/час |
| 100 | 11 | 22,550 |
| 90 | 11 | 22,208 |
| 80 | 11 | 22,871 |
| 70 | 11 | 22,942 |
| 60 | 11 | 23,020 |
Как видно из табл. 9, с изменением температуры экстрактивного агента положение оптимальной тарелки питания в колонне регенерации не меняется.
Таким образом, мы провели параметрическую оптимизацию схемы экстрактивной ректификации. В итоге нами был получен набор оптимальных параметров работы технологической схемы, при котором энергопотребление минимально:
· температура подачи ЭА 100 оС;
· оптимальный расход ЭА 70 моль/ч (F:ЭА = 1:0,7);
· NЭА/NF = 4/11;
· тарелка питания колонны регенерации - 11;
Определение оптимальных рабочих параметров экстрактивной ректификации по схеме с использованием разделяющего агента во второй колонне
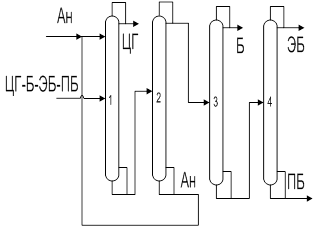
Рассмотрим технологическую схему разделения четырехкомпонентной азеотропной смеси с использованием тяжелолетучего экстрактивного агента, представленную на рис. 10.
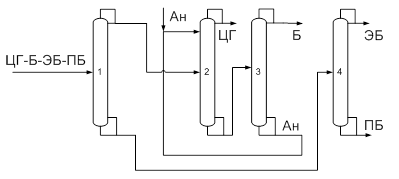
Рис. 10. Принципиальная схема разделения четырехкомпонентной азеотропной смеси
Исходная смесь, содержащая циклогексан, бензол, этилбензол, н-пропилбензол, поступает на разделение в колонну 1, где происходит отделение зеотропной и азеотропной составляющих друг от друга. Верхним продуктом колонны 1 является фракция азеотропообразующих компонентов – циклогексан-бензол, а кубовым продуктом – смесь этилбензола и н-пропилбензола, которая далее разделяется в простой двухсекционной колонне 4. Разделение смеси циклогексан – бензол происходит с применением традиционного комплекса экстрактивной ректификации с тяжелолетучим разделяющим агентом (анилин). Азеотропную смесь подают в середину колонны 2, а экстрактивный агент – в верхнюю её часть. Таким образом, происходит выделение циклогексана в качестве дистиллата колонны 2. Оставшуюся смесь бензола и анилина разделяют в колонне регенерации 3, бензол отбирают с верха колонны, а экстрактивный агент – с низа и направляют на рецикл в колонну 2.
Рассматриваемая технологическая схема относится ко второй группе схем экстрактивной ректификации, в которой первоначально происходит фракционирование смеси, а разделяющий агент применяется во второй колонне.
Снижение энергозатрат на разделение рассмотренной технологической схемы можно добиться нахождением оптимальных параметров работы её экстрактивного комплекса (при фиксированных количестве, составе и температуре исходной смеси и заданном качестве продуктовых потоков необходимо определить оптимальные температуру, расход ЭА, а также уровни ввода исходной смеси и разделяющего агента).
Все расчеты проводили на 100 кг/ч четырехкомпонентной смеси эквимолярного состава. Качество продуктовых фракций задавали равным 99% мольн. целевого компонента, экстрактивного агента – 99,9%. Разделяемую смесь подавали в колонну при температуре кипения.
На первом этапе мы исследовали влияние на энергозатраты температуры подачи в колонну ЭР при фиксированном соотношении исходная смесь : ЭА = 1 : 2.
Мы рассчитали энергозатраты при температурах подачи ЭА в колонну 60, 70, 80, 90 и 100 °С. При этом для каждой температуры определили положение тарелок питания, при котором энергопотребление в кубе минимально. Результаты расчета приведены в табл.10 и рис. 11.
Таблица 10.
Изменение энергозатрат в зависимости от температуры подачи экстрактивного агента. F: ЭА = 1:2
| Температура подачи ЭА, 0С | NЭА/NF | Флегмовое число колонны 2 | Энергозатраты, ГДж/час | |
| колонны 2 | суммарные | |||
| 100 | 4/11 | 1.01 | 2.13 | 11.17 |
| 90 | 4/11 | 0.58 | 2.17 | 11.21 |
| 80 | 5/11 | 0.33 | 2.33 | 11.36 |
| 70 | 4/12 | 0.25 | 2.59 | 11.63 |
| 60 | 4/11 | 0.18 | 2.83 | 11.86 |
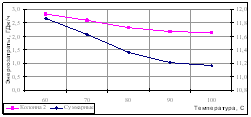
Рис. 11.Изменение энергозатрат в зависимости от температуры подачи ЭА
Видно, что оптимальное положение тарелок подачи исходной смеси и ЭА практически не изменяется с изменением температуры последнего. Флегмовое число с увеличением ТЭА растет. Это связано с тем, что при более высокой температуре возрастает концентрация ЭА в укрепляющей секции колонны и для получения циклогексана заданного качества требуется возвращать в колонну больший поток флегмы. В данном случае суммарные энергозатраты и энергозатраты в кубе колонны 2 растут с уменьшением температуры, что видно из рисунка 11.
Далее мы рассмотрели зависимость энергозатрат на разделение в зависимости от температуры подачи ЭА и расхода ЭА. В табл. 11 и рис 12 представлена зависимость энергозатрат для фиксированной температуры и уровней подачи ЭА и питания.
Таблица 11.
Зависимость энергозатрат от расхода ЭА при температуре его подачи 100ºС. Уровни подачи NЭА/NF = 4/11
| Расход ЭА, моль/час | Флегма колонны 2 | Энергозатраты, ГДж/ч | |
| Колонны 2 | Суммарные | ||
| 50 | 1,49 | 1,92 | 10,41 |
| 60 | 1,48 | 1,87 | 10,37 |
| 70 | 1,31 | 1,80 | 10,32 |
| 80 | 1,23 | 1,75 | 10,32 |
| 90 | 1,18 | 1,75 | 10,35 |
| 100 | 1,15 | 1,76 | 10,40 |
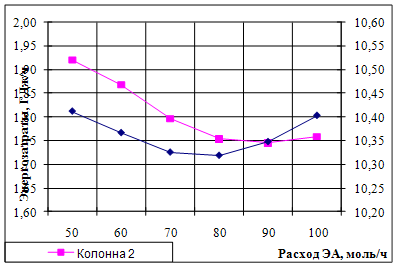
Рис.12. Зависимость энергозатрат на разделение в зависимости от температуры подачи ЭА
Видно, что существует оптимальное количество подаваемого разделяющего агента. Для температуры 100 С оно составляет 80 моль/час. Появление минимума на зависимости энергозатрат подробно обсуждалось в предыдущем случае. Далее рассмотрим изменение энергопотребления от расхода ЭА при различных температурах. Результаты представим в табл. 12.
Таблица 12.
Зависимость энергозатрат на разделение от ТЭА и расхода ЭА, NЭА/NF=4/11
| Температура подачи ЭА, оС | Опт расход ЭА, моль/час | Флегмовое число колонны 2 | Энергозатраты, ГДж/час | |
| колонны 2 | суммарные | |||
| 100 | 80 | 1.23 | 1.75 | 10.32 |
| 90 | 80 | 1.04 | 1.75 | 10.32 |
| 80 | 80 | 0.86 | 1.75 | 10.32 |
| 70 | 70 | 0.84 | 1.73 | 10.27 |
| 60 | 60 | 0.66 | 1.67 | 10.17 |
Видно, что при различных ТЭА значение оптимального расхода РА практически не изменяется. При уменьшении температуры от 100 до 60 0С флегмовое число уменьшается, достигая минимального значения при 100 0С. Оптимальный расход ЭА равен 60 моль/час.
Рассмотрим зависимость расхода ЭА и энергозатрат от уровней подачи ЭА и смеси.
Таблица 13. Зависимость величины минимального и оптимального расхода ЭА от его температуры и положения тарелок питания
| NЭА/NF | Расход ЭА, моль/час | Энергозатраты в кубе, ГДж/ч | ||
| Оптимальный | Минимальный | при опт. расходе | при мин. расходе | |
| Т= 100 0С | ||||
| 4/10 | 60 | 50 | 10.163 | 10.169 |
| 4/11 | 80 | 50 | 10.318 | 10.411 |
| 4/12 | 90 | 50 | 10.677 | 11.299 |
| 5/10 | 60 | 50 | 10.158 | 10.159 |
| 5/11 | 80 | 50 | 10.315 | 10.378 |
| 5/12 | 100 | 50 | 10.666 | 11.193 |
| Т=900С | ||||
| 4/10 | 60 | 50 | 10.164 | 10.170 |
| 4/11 | 80 | 50 | 10.319 | 10.412 |
| 4/12 | 100 | 50 | 10.669 | 11.299 |
| 5/10 | 50 | 50 | 10.159 | 10.159 |
| 5/11 | 80 | 60 | 10.315 | 10.378 |
| 5/12 | 100 | 60 | 10.667 | 11.192 |
| Т= 800С | ||||
| 4/10 | 60 | 50 | 10.164 | 10.173 |
| 4/11 | 80 | 50 | 10.319 | 10.422 |
| 4/12 | 100 | 50 | 10.670 | 11.300 |
| 5/10 | 60 | 50 | 10.160 | 10.161 |
| 5/11 | 80 | 50 | 10.319 | 10.422 |
| 5/12 | 100 | 50 | 10.667 | 11.193 |
| Т=700С | ||||
| 4/10 | 60 | 50 | 10.164 | 10.174 |
| 4/11 | 80 | 50 | 10.319 | 10.423 |
| 4/12 | 100 | 50 | 10.670 | 11.343 |
| 5/10 | 60 | 50 | 10.162 | 10.161 |
| 5/11 | 80 | 50 | 10.317 | 10.389 |
| 5/12 | 100 | 60 | 10.667 | 11.193 |
| Т=600С | ||||
| 4/10 | 60 | 50 | 10.165 | 10.177 |
| 4/11 | 80 | 50 | 10.321 | 10.423 |
| 4/12 | 100 | 50 | 11.300 | 13.487 |
| 5/10 | 60 | 50 | 10.162 | 10.164 |
| 5/11 | 80 | 50 | 10.317 | 10.389 |
| 5/12 | 100 | 50 | 10.668 | 11.193 |
При снижении температуры расположение тарелок подачи не изменяется (5/10), оптимальный расход равен 60 моль/час. Минимальные суммарные энергозатраты достигаются при температуре 100 0С.
Рассмотрим изменение энергозатрат на разделение от положения тарелки питания в колонне регенерации при различных температурах подачи экстрактивного агента. Результаты представим в табл. 14.
Таблица 14.
Зависимость энергозатрат в колонне регенерации от положения тарелки питания
| Температура, оС | № тарелки питания | Энергозатраты, ГДж/ч |
| 100 | 4 | 10.752 |
| 90 | 4 | 10.763 |
| 80 | 4 | 10.744 |
| 70 | 4 | 10.759 |
| 60 | 4 | 10.745 |
При различных температурах уровень подачи остается неизменным. Оптимальная тарелка питания в колонне регенерации 4.
Таким образом, данная технологическая схема имеет минимальное энергопотребление при следующих рабочих параметрах:
· температура подачи ЭА 100 оС;
· оптимальный расход ЭА 60 моль/ч (F:ЭА =1:0,6);
· NЭА/NF = 5/10;
· тарелка питания колонны регенерации - 4.
Сравнение результатовНами был проведен сравнительный анализ традиционных схем разделения четырехкомпонентной азеотропосодержащей смеси методом экстрактивной ректификации. Эти схемы различаются по структуре: в одной из них экстрактивный агент подается в первую колонну, что позволяет выделить компонент азеотропной пары на первом этапе, в другой – первоначально происходит фракционирование смеси на зеотропную и азеотропную составляющую, а затем их разделение.
Каждая из предложенных технологических схем была подвергнута параметрической оптимизации с целью снижения энергозатрат на разделение. Результаты оптимизации представлены в табл. 15.
Таблица 15.
Сравнение технологических параметров схем экстрактивной ректификации
| Параметры | Схема с применением ЭА в первой колонне | Схема с предварительным фракционированием |
| Температура подачи ЭА, оС | 100 | 100 |
| Оптимальный расход ЭА, моль/ч | 70 | 60 |
| NЭА/NF | 4/11 | 5/10 |
| Тарелка питания колонны регенерации | 11 | 4 |
| Суммарные энергозатраты, ГДж/ч | 24,55 | 10,75 |
Из приведенных данных видно, что оптимальные параметры работы экстрактивной колонны для двух схем весьма близки. Поэтому можно утверждать, что значительная экономия энергозатрат в случае схемы с предварительным фракционированием исходной смеси достигается за счет структурных особенностей. Выделение зеотропной составляющей на первом этапе значительно облегчает дальнейшее разделение смеси. Суммарные энергозатраты различаются более чем на 50% (54,25%).
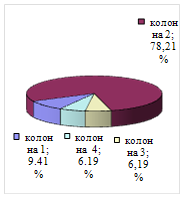
Рассмотрим структуру энергозатрат более подробно (рис 13).
В случае схемы с применением ЭА в первой колонне наибольшее энергопотребление приходится на кипятильник колонны регенерации. Это связано с высоким требованием к чистоте разделяющего агента (99,9%). Для схемы с предварительным фракционированием максимальные энергозатраты наблюдаются в колонне разделения ЭБ и ПБ.
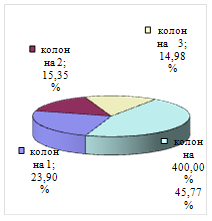
б
Рис.13. Структура энергозатрат (а) - схема с предварительным фракционированием; (б) - схема с применением ЭА в первой колонне
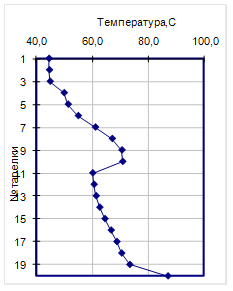
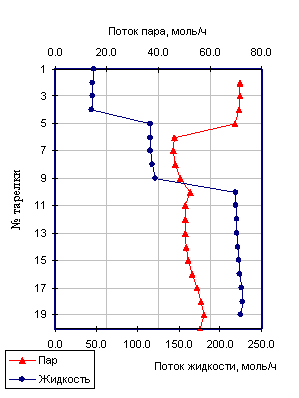
Далее на рис14. представлены профили температуры и скоростей жидкости и пара по высоте колонны при оптимальных технологических параметрах.
На представленных зависимостях отчетливо видны скачки изменения температуры и расходов пара и жидкости, соответствующие разноуровневой подаче ЭА и питания в экстрактивной колонне.
Схема разделения с применением ЭА в первой колонне | Схема с применением ЭА во второй колонне |
|
|
|
|
в |
г |
Рис.14. Температурные профили (а, б) и скорости потоков пара и жидкости (в, г) для различных схем ЭР
Выводы· В ходе работы были рассмотрены традиционные схемы экстрактивной ректификации: схема с использованием ЭА в первой колонне и схема с предварительным фракционированием исходной смеси. Для каждой структуры найден оптимальный набор параметров.
Для схемы с использованием ЭА в первой колонне:
-температура подачи ЭА 100 оС;
-оптимальный расход ЭА 70 моль/ч;
-уровни подачи ЭА и питания в экстрактивную колонну – 4/11 тарелки;
-тарелка питания в колонне регенерации – 11 тарелка.
Для схемы с предварительным фракционированием:
-температура подачи ЭА 100 оС;
-оптимальный расход ЭА 60 моль/ч;
- уровни подачи ЭА и питания в экстрактивную колонну – 5/10 тарелки;
-тарелка питания в колонне регенерации – 4 тарелка.
· При фиксированном суммарном числе ступеней разделения оптимальной является схема с предварительным фракционированием исходной смеси.
Список литературы
1. Серафимов Л.А. Технология разделения азеотропных смесей (дополнительная глава) в кн. Свентославский В. Азеотропия и полиазеотропия. - М.: “Химия”, 1968, 186 с.
2. Жаров В.Т., Серафимов Л.А. Физико-химические основы дистилляции и ректификации. - М.: - “Химия”, 1975, 240 с.
3. Серафимов Л.А., Фролкова А.К. Фундаментальный принцип перераспределения полей концентраций между областями ректификации как основа создания технологических комплексов // Теор. осн. хим. технологии. - т.31, №2, 1997, с.184-193.
4. Гришунин А.В., Балашов М.И., Серафимов Л.А. Синтез комплексов ректификационных колонн для разделения трехкомпонентных азеотропных смесей с использованием принципов переходимости разделяющих многообразий // Разделение жидких неидеальных смесей, труды Алтайского политехнического института, Барнаул, 1974, с.45-49.
5. Петлюк Ф.Б., Серафимов Л.А. Многокомпонентная ректификация, теория и расчет.-М.:, Химия, 1983, 304 с.
6. Тимошенко А.В., Серафимов Л.А., Синтез технологических схем ректификации многокомпонентных смесей с одним бинарным азеотропом // Теор. осн. хим. технологии.-1999, т.33, №1, с.47-53.
7. Тимошенко А.В. Серафимов Л.А. Синтез и дискриминация технологических схем ректификационного разделения с использованием критерия энергозатрат. - В сб. “Наукоемкие химические технологии” III международная конференция, Тверь, 1995, с. 65
8. Тимошенко А.В., Серафимов Л.А., Тимофеев В.С., Глушаченкова Е.А. Синтез и анализ технологических схем для разделения трехкомпонентных азеотропных смесей. - в сб. “Наукоемкие химические технологии”, IV международная конференция, Волгоград, 1996, с.84
9. Гельперин И.Н, Новикова К.Е./ Журнал прикладной химии – 1961. Т 34. -№ 9. - С 11-16.
10. Айнштейн В.Г., Захаров М.К., Носов Г.А., Захаренко В.В., Зиновкина Т.В., Таран А.Л., Костаян А.Е. «Общий курс процессов и аппаратов химической технологии» т.2 Москва «Логос» «Высшая школа» 209023 г. 1758с.
11. Тимофеев В.С., Серафимов Л.А «Принципы технологии основного органического и нефтехимического синтеза», Москва «Высшая школа» 2003 г, 536 с
12. Коган В.Б. «Азеотропная и экстрактивная ректификация» Издательство «Химия» Ленинградское отделение 1971 г, 432 с
13. Фролкова А.К. Теоретические основы разделения многокомпонентных многофазных систем с использованием функциональных комплексов – Дисс. на соискание ученой степени д.т.н., Москва, МИТХТ, 2000.
14. Hendriksen, Dan E.; (Phillipsburg, NJ) ; Cheng, Minquan; (Evansville, IN) ; Kuechler, Keith H.; (Friendswood, TX) ; Lumgair, David R.; (Craddockville, VA) ; Nicoletti, Michael P.; (Houston, TX) ; Shutt, Richard; (Tervuren, BE), ExxonMobil Chemical Company ,US, Serial No.: 943695, August 31, 2001
15. Holmes, M. H. and van Winkle, M., 1970, Wilson Equation Used to Predict Vapor Compositions, Ind. Eng. Chem., 62(1), 2231.
16. Orye, R. V. and Prausnitz, J. M., 1965, Multicomponent Equilibria with the Wilson Equation, Ind. Eng.Chem., 57(5), 1826.
17. Wilson, G. M., 1964, VaporLiquid Equilibrium XI. A New Expression for the Excess Free Energy of Mixing, J. Amer. Chem. Soc., 86, 127.
18. Renon, H. and Prausnitz, J. M., 1968, Local Composition in Thermodynamic Excess Functions for Liquid Mixtures, AIChE J., 14, 135144.
19. Harris, R. E., 1972, Chem. Eng. Prog., 68(10), 57.
20. Abrams, D. S. and Prausnitz, J. M., 1975, Statistical Thermodynamics of Mixtures: A New Expression for the Excess Gibbs Free Energy of Partly or Completely Miscible Systems, AIChE J., 21, 116-128.
21. Anderson, T. F. and Prausnitz, J. M., 1978, Application of the UNIQUAC Equation to Calculation of Multicomponent Phase Equilibria. 2. LiquidLiquid Equilibria, Ind. Eng. Chem. Proc. Des. Dev., 17, 561-567.
22. Maurer, G. and Prausnitz, J. M., 1978, On the Derivation and Extension of the UNIQUAC Equation, Fluid Phase Equilibria, 2, 91-99.
23. Abbott, M. M., 1973, Cubic Equations of State, AIChE J., 19(3), 596-601.
24. Peng, D. Y., and Robinson, D. B., 1976, A New Two-constant Equation of State for Fluids and Fluid Mixtures, Ind. Eng. Chem. Fundam., 15, 58-64.
25. Skjold-Jørgensen, S., Kolbe, B., Groehling, J., and Rasmussen, P., 1979, VaporLiquid Equilibria by UNIFAC Group Contribution. Revision and Extension, Ind. Eng. Chem. Proc. Des. Dev., 18(4), 714-722.
26. Gmehling, J., Rasmussen, P., and Fredenslund, Aa., 1983, Vapor-Liquid Equilibria by UNIFAC Group Contribution. Revision and Extension, Ind. Eng. Chem. Proc. Des. Dev., 22(10), 676-678.
27. Hansen, H.K., Rasmussen, P., Fredenslund, Aa., Schiller, M., and Gmehling, J., 1991, VaporLiquid Equilibria by UNIFAC Group Contribution. 5. Revision and Extension, Ind. Eng. Chem. Res., 30(10), 2352-2355.
28. Огородников С.К., Лестова Т.М., Коган В.Б. «Справ. Азеотропные смеси» Изд. «Химия» 1971г. 848с
 а
а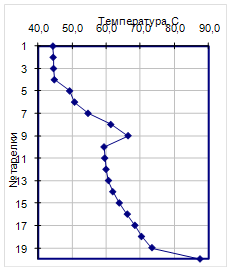 б
б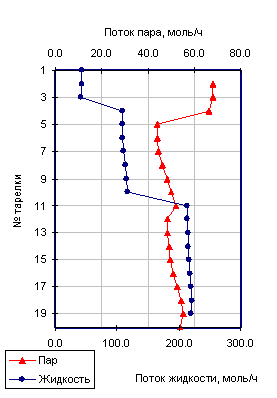
0 комментариев