Муниципально образовательное учреждение средняя образовательная школа №39
Четвертной проект на тему:
«Строение и свойства железа»
Выполнил:
Проверил:
Хабаровск 2007г.
Содержание
1. Введение……………………………………………………3
2. Свойства и использование железа. Доменная печь…………..…..4
3. Список литературы…………………………………………………..8
Введение
Железо - один из самых распространенных металлов в земной коре. Люди научились извлекать железо из руды и обрабатывать его около 4 тыс. лет назад.
Содержание железа в земной коре составляет 4,65%, а в целом наша планета состоит из железа почти на 35%. В основном оно сосредоточено в земном ядре.
В природе железо встречается в виде оксидов (соединений с кислородом) железных рудах. Две основные железные руды – это гематит и магнетит. Гематит – одна из основных железных руд. Этот минерал часто образует комки, похожие на почки, - конкреции.
С XIV в. для выплавки чугуна из железной руды, смешанной с коксом, стали применять доменные печи. Чугун – это почти чистое железо с примесью углерода, который включается в железо в доменной печи при сгорании кокса. Углерод придает чугуну твердость.
Со второй половины XIX в. все больше чугуна начали перерабатывать в сталь. Сталь содержит меньше углерода, чем чугун, и поэтому она более пластична и устойчива к резким ударным нагрузкам. При выплавке стали углерод частично удаляют из чугуна путем продувания кислорода через расплав и добавляют в сталь разные металлы, каждый из которых придает ей особые свойства.
Свойства и использование железа. Доменная печь.
Железную руду, кокс и известняк помещают в шахту доменной печи. Руда содержит оксид железа, кокс получают нагреванием угля без доступа воздуха, а известняк состоит из карбоната кальция. Горячий воздух подается в нижнюю часть доменной печи. По мере сгорания кокса содержащийся в нем углерод вступает в реакцию с кислородом воздуха, в ходе которой образуется оксид углерода. Горящий кокс нагревает сырье в нижней части печи до температуры выше 1600 градусов по Цельсию. При такой температуре кислород, содержащийся в оксиде железа, вступает в реакцию оксидом углерода. В результате получается диоксид углерода, а из руды высвобождается практически чистое железо(чугун) и стекает на дно печи. Расплавленный чугун выливают из нижней части печи каждые 3-4 часа. Известняк взаимодействует с песком, глиной и другими содержащимися в руде примесями, образуя так называемый шлак. Расплавленный шлак, будучи легче чугунного расплава, скапливается на поверхности металла и время от времени удаляется из печи через специальное отверстие – летку.
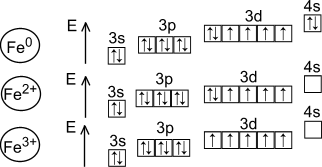
Железо – VIII В группы. Электронная конфигурация его тома:1s 2s 2p 3s 3p 4s 3d .Это металл, простое вещество – восстановитель средней силы. Основные степени окисления железа в соединениях:+2,+3. оксид железа (II) FeO – основный оксид, его гидратная форма Fe(OH)2 - нерастворимое основание, обладает восстановительными свойствами. Оксид железа (III)Fe2O3 – основный оксид с признаками амфотерного оксида. Его гидроксид Fe(OH)3- амфотерный гидроксид с преобладанием основных свойств. Соединения железа(III) – слабые окислители. Из соединений железа они наиболее химически инертны.Чистое железо, не содержащее примесей, - прочный и пластичный металл, который легко куется и прокатывается. Железо притягивается магнитом. Плотность металла 7,87 г/см³, относится к тяжелым металлам(черная металургия). Температура плавления 1535 градусов по Цельсию, кипения – 3200 градусов по Цельсию.
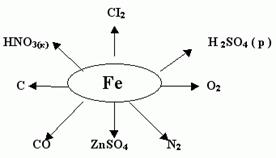
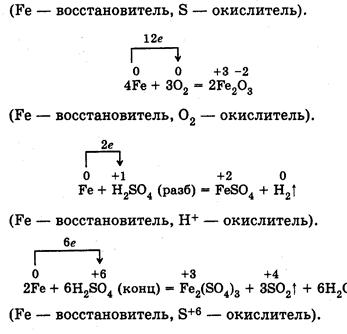
С простыми веществами железо реагирует только при высокой температуре: сгорает на воздухе с образованием оксида Fe2O3, хлором окисляется Fe +3 .
2Fe+3Cl2=2FeCl3 - хлорид железа (III).
При нагревании с серой образуется сульфид железа (II)FeS,с углеродом – карбид железа Fe3C.
В разбавленных растворах хлороводородной (соляной) и серной кислот железо растворяется с образованием соединений Fe(II):
Fe+2HCl=FeCl2+H2é.
Разбавленная азотная и концентрированная серная кислота окисляют железо до Fe+3:
Fe+4HCl=Fe(NO3)3+NO+2H2O,
2Fe+6H2SO4=Fe2(SO4)3+3SO2+6H2O.
Концентрированная азотная кислота пассивирует железо, создавая на поверхности защитную оксидную пленку.
Железо вытесняет малоактивные металлы из растворов их солей:
Fe+CuSO4=FeSO4=Cu.
Гидроксид железа (II) окисляется кислородом воздуха:
4Fe(OH)2+O2+2H2O=4Fe(OH)3.
Соединения железа (III) – оксид и гидроксид – обладют амфотерными свойствами. Так, оксид реагирует при нагревании с основными оксидами:
Fe2O3+CaO=Ca(FeO2)2.
Свежеосажденный гидроксид железа (III) легко растворяется в кислотах:
Fe(OH)3+3HNO3=Fe(NO3)3+3H2O.
В щелочах Fe(OH)3 растворяется только при длительном кипячении:
Fe(OH)3+NaOH=Na[Fe(OH)4].
Железо (III) образует многочисленные комплексные соединения: гидратные комплексы при гидролизе. Качественными реакциями на ионы Fe+3 и Fe+3 также являются реакции с образованием окрашенных комплексных соединений:
Fe+2
FeSO4+K3[Fe(CN)6]=KFe[Fe(CN)6]â+K2SO4
4FeCl3+3K4[Fe(CN)6]=Fe4[Fe(CN)6]3â+12KCl
Взаимопереходы ионов железа при передаче электронов:
Fe+2 Fe+3
обусловливают работу дыхательных ферментов (цитохромов) , в частности, гемоглобина, переносящего кислород от органов дыхания ко всем клеткам организма.
 | |||
![]()
Список литературы
1. «Химия и научно-технический прогресс», И.Н.Семенов, А.С.Максимов, А.А.Макареня, Москва “Просвещение” 1999г. .(для учеников 10-11 классов)
2. «Энциклопедический словарь юного химика», Москва 2000г.
3. «Необычные свойства обычных металлов», В.А.Займовский, Т.Л.Колупаева, библиотека “Квант”
Похожие работы
... всасываемости яда хвощей при сопутствующем кормлении осоками (обычно осоки бывают сильно засорены хвощами), ранящими слизистую оболочку кишечника. Не исключается и возможность того, что растения, вызывающие механические повреждения, открывая доступ инфекции, могут обусловить развитие местных гнойных или гнилостных процессов или даже общее заражение организма. Ботанические сведения. Семейство ...
... Масло нейтрализует кислотность крови и повышенную кислотность желудочного сока, компенсирует общее истощение организма, способствует «наращиванию мяса», укрепляет тело, применяется как глистогонное средство. Полезные свойства кунжута дополняются и еще одним, очень важным. Он является основным источником извести в человеческом организме, в которой обычно ощущается острый недостаток. Считается, что ...
... с железом и его соединениями, а также способами устранения. И в следующей главе мы будем рассматривать, способы проведения уроков в школе по этой теме. ГЛАВА 3. ИЗУЧЕНИЕ ТЕМЫ «ЖЕЛЕЗО И ЕГО СОЕДИНЕНИЯ» НА УРОКЕ ПО ХИМИИ В СРЕДНЕЙ ШКОЛЕ 3.1 План урока Железо: его строение и свойства “Век девятнадцатый, железный, Воистину жестокий век! Тобою в мрак ночной, беззвездный Беспечный брошен ...
... государственный индустриальный университетФакультет электротермических технологийКафедра электрометаллургии стали и ферросплавов Дипломная работа на тему: Термодинамические характеристики расплавов на основе железа Руководитель: Воробьев Анатолий Александрович Исполнитель: Бородин Игорь Сергеевич студент группы ЭМ- ...
0 комментариев