Семейство хеморепеллентов, семафорины
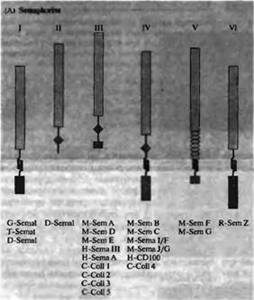
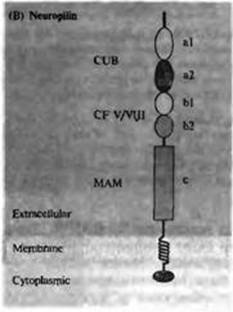
Другими белками, которые играют роль хеморепеллентов, являются семафорины, большое семейство секреторных и трансмембранных белков (рис. 1А). Первоначально они были идентифицированы как факторы, управляющие ростом аксона у кузнечиков, и были признаны хеморепеллентами. Затем был обнаружен и выделен в чистом виде гомолог этого белка у позвоночных, коллапсин-1, который, как было показано, приводит к ретракции конусов роста в культуре клеток. Он также способен управлять на длинных дистанциях ростом аксона, вызывая его отклонения. Нейропилины являются высококонсервативным семейством рецепторов к семафоринам (рис. 1В).
Модуляция ответов на хеморепелленты и хемоаттрактантыНа пути передачи сигналов, которые обеспечивают ответы клетки на хемоаттрактанты и хеморепелленты, можно влиять при помощи кальций-зависимых протеинкиназ и протеинкиназ, зависящих от концентрации циклических нуклеотидов. Например, в культуре спинальных нейронов Xenopus активация пути циклических нуклеотидов более благоприятна для сигналов аттракции; ингибирование этих путей приводит к отталкиванию конуса роста. Таким образом, источник нетрина-1 притягивает конус роста культивированных спинальных нейронов Xenopus. Однако при добавлении ингибитора протеинкиназы А конусы роста поворачивали прочь от источника нетрина. С другой стороны, конусы роста Xenopus в нормальных условиях направляются прочь от источника коллапсина-1; эти отталкивающие эффекты становятся привлекающими после активации сигнальных путей, связанных с цГМФ. В среде с низким содержанием кальция исчезают все типы ответов (как привлекающие, так и отталкивающие), а скорость роста возрастает.
|
|
| Рис. 1АВ. Семафорины и нейропилин обеспечивают хемоаттракцию и хемоотталкивание на близких и дальних дистанциях. (А) Домен sema (полоски) характеризует все шесть классов семафоринов которые включают секреторные (II и III) и связанные с мембраной (I, IV-VI) формы. Внеклеточные регионы также содержат домены, напоминающие иммуноглобулины (кружочки), повторы тромбосподина I типа (овалы), и домены, богатые щелочными аминокислотами (полоски). Цитоплазматические домены короткие и имеют большую вариабельность. (В) Нейропилин — рецептор семафорина. Во внеклеточном регионе домены a1 и а2 (также называемые CUB последовательностями) схожи с доменами комплементарных факторов С1а и C1s, протеином костного морфогенеза 1 и несколькими металлопротеиназами. Домены b1 и b2 повторяют домены факторов свертывания V и VIII. С область содержит МАМ домен, последовательности которого обнаружены в тирозинфосфатазе Ми, А5/нейропилине и метал лоэндопептидазе меприне. Короткий цитоплазматический конец остается высококонсервативным от вида к виду. |
Механизмы управления конусов роста, описанные до сих пор, направляют аксон к его конечной цели. Однако проблема того, как каждый аксон подходит к своей клетке-мишени, остается открытой. Путь, по которому ганглиозные клетки сетчатки иннервируют свои клетки-мишени в области передних бугров покрышки, является примером того, какие сигналы обеспечивают достижение правильного паттерна иннервации. Во время развития аксоны ганглиозных клеток задней или височной (temporal) части сетчатки направляются для иннервации в переднюю часть тектума, а клетки передней (nasal) части сетчатки направляются для иннервации задней части тектума (рис. 2).
|
|
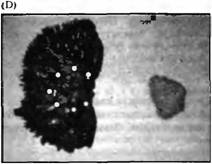
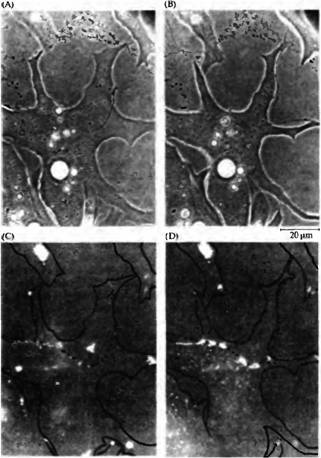
| Рис. 1CD. (С и D) Семафорим III (Sema3A) — хемореппелент дальней дистанции для сенсорных аксонов. Спинальный ганглий эмбриона крысы (слева на каждой панели) культивировали в течение 48 часов рядом с агрегатами COS клеток. Белыми кружками показаны контуры ганглия. Для того чтобы вызывать рост сенсорных волокон малого диаметра в среду был добавлен ФРН. (С) Контрольные COS клетки. Аксоны растут в виде венчика. (D) COS клетки, секретирующие рекомбинантный Sema3A. Sema3A отталкивает аксоны. |
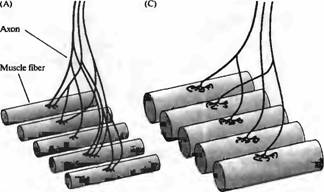
В элегантной серии экспериментов Бонхоеффер с коллегами продемонстрировали, что аксоны определяют территории своей иннервации посредством отталкивающих взаимодействий, которые предотвращают вторжение аксонов височной зоны в область задней части тектума. Ганглиозные клетки височной сетчатки были помещены в культуру, где рядом с ними находились поверхности, покрытые мембранами, выделенными либо из передней, либо из задней области тектума. В этих условиях аксоны отталкивались мембранами из задней части тектума и росли преимущественно в направлении мембран своих естественных мишеней, мембран передней части тектума. Любопытно, что аксоны сетчатки, не имея подобного выбора, быстро растут в направлении любого субстрата, как из передней, так и из задней части тектума.
Молекулы, ответственные за такие отталкивающие взаимодействия, принадлежат к семейству рецепторов, связанных с тирозинкиназой (известных как Eph киназы), а также их лигандов (называемых эфринами, ephrines). Эфрин-А2 и эфрин-5 экспрессируются в тектуме во время образования ретинотектальных связей, и их концентрация постепенно увеличивается в направлении спереди назад. Рецептор к Eph-АЗ экспрессируется на аксонах клеток сетчатки соответственно назотемпоралыюму градиенту. При заключении в липидные пузырьки и добавлении в среду, омывающую аксоны клеток височной части сетчатки, эфрины А2 и А5 вызывают отделение конусов роста от субстратов и их ретракцию. Эфрины и семейство Eph рецепторов, связанных с тирозинкиназой, действуют во всех частях развивающейся нервной системы, влияя на нахождение пути аксоном, миграцию клеток, образование связей между ними, в основном демонстрируя сходный отталкивающий механизм.
Одного рострокаудального градиента недостаточно для того, чтобы аксоны клеток сетчатки правильно достигли своего окончательного месторасположения в тектуме. Более поздние изменения в рострокаудальных проекциях основываются как на определенно расположенных химических сигналах, так и на механизмах, зависящих от активности нейронов
Образование синапсовКак только конус роста достигает своей мишени, он должен установить синаптический контакт, часто имеющий специфическое расположение на клетке-мишени. Анализ механизмов, благодаря которым формируются такие четкие связи в пределах ЦНС, является основной проблемой. Предпочтительным препаратом для изучения образования синаптических связей является нервно-мышечное соединение в скелетной мышце позвоночных.
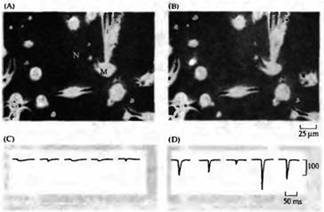
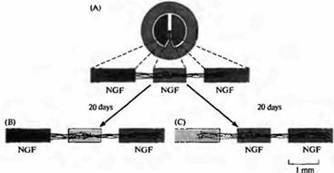
Накопление рецепторов к ацетилхолинуИсследования Фишбаха, Кохена, Шанге, Салпетера, Штайнбаха, Пу, Кидокоро и других показали, что на ранних периодах развития рецепторы АХ распределены диффузно вдоль поверхности неиннервированных мышечных волокон с плотностью около нескольких сотен рецепторов на квадратный миллиметр. По мере того как конус роста мотонейрона приближается к мышечному волокну, в клетке-мишени возникают деполяризующие потенциалы в ответ на выделение АХ из конуса роста (рис. 3.). После контакта частота спонтанного выделения квантов АХ быстро возрастает, как и величина синаптического потенциала, возникающего в ответ на стимуляцию аксона. Таким образом, в течение минут формируется функциональная сииаптическая связь.
На первом этапе синаптической специализации происходит накопление рецепторов АХ (AChRs) непосредственно под терминалью аксона. Этот процесс начинается через несколько часов после первоначального контакта. Через день-два плотность рецепторов под терминалью составляет несколько тысяч на квадратный миллиметр. Примерно в то же самое время в областях синапсов начинает накапливаться ацетилхолинэстераза и становятся заметны пучки матрикса пластинки в области синаптической щели. Дальнейшая дифференцпровка нервно-мышечного соединения происходит постепенно, в течение нескольких последующих недель развития. У многих видов субъединица рецептора АХ заменяется на субъединицу, что приводит к формированию из эмбрионального рецептора рецептора взрослого типа (глава 3). Распределение рецепторов также меняется: концентрация под терминалью аксона постепенно увеличивается, достигая у взрослых уровня примерно 104 рецепторов на 1 мкм2, а плотность рецепторов вне синаптической зоны мышечных волокон уменьшается до уровня меньше чем 10 рецепторов на I мкм2. Метаболическая стабильность рецепторов АХ также меняется. До иннервации рецепторы мембраны имели период полужизни порядка 1 дня; рецепторы АХ в иннервированных волокнах удивительно стойкие, их период полужизни составляет около 10 дней.
| Рис. Быстрое образование действующих синаптических связей между аксонами мотонейронов и мышечными клетками. (А, В) Фазово-контрастные фотографии растущих нервных отростков (N) и веретеновидных миоцитов (М) в нервно-мышечной культуре клеток Xenopus в начале (А) и в конце (В) электрической регистрации. (С, D) Whole-cell patch-clamp миоцитов. Можно зарегистрировать спонтанные синаптические токи уже через Î минуту после контакта (С), которые увеличиваются на несколько порядков к 18-й минуте (D). |
|
Изменения также происходят в терминали аксона, приводя в течение нескольких недель к образованию активных зон. Эти и многие другие исследования показывают, что образование синапса не является простым событием по принципу «все или ничего». Хотя функциональная синаптическая передача может устанавливаться довольно быстро, дифференцировка пре- и постсинаптических характерных свойств — более долгий процесс, идущий на протяжении нескольких недель развития, и он основан на обмене разнообразными молекулярными сигналами между нервной терминалью и мышечным волокном. Детальные морфологические и физиологические эксперименты показывают, что конусы роста соприкасаются с поверхностью мышечной клетки в произвольном месте, игнорируя сушествуюшие кластеры рецепторов АХ, и быстро приводят к формированию новых агрегатов рецепторов (рис. 4.).
Таким образом, терминали аксона должны высвобождать некий сигнал, который индуцирует накопление рецепторов АХ на мышечной клетке. Этот сигнал является специфическим для холинергических нейронов; при прорастании нехолинергических нейронов в мышечные клетки они не вызывают изменений в распределении рецепторов АХ. Однако сигналом к этому не является сам АХ; накопление рецепторов АХ под терминалями аксона происходит в культурах клеток в присутствии кураре и бунгаротоксина, которые блокируют взаимодействие АХ с его рецепторами. В экспериментах, изначально предназначенных для идентификации сигналов, контролирующих регенерацию нервно-мышечного соединения , был идентифицирован белок, названный агрином, который высвобождался терминалями двигательного нерва и приводил к накоплению рецепторов АХ, холинэстеразы и других компонентов постсинаптического аппарата в синаптических областях.
Вызванная агрином синаптическая дифференцировкаАгрин существует в нескольких изоформах, которые возникают вследствие альтернативного сплайсинга одного гена. Мотонейроны, мышечные клетки и шванновские клетки экспрессируют агрин, но только у мотонейронов агрин находится в такой изоформе, которая способна вызывать постсинаптическую дифференцировку. Агрин является большой молекулой (heparan sulfate proteoglyсап), домены которой взаимодействуют с ламииином, белками, связывающими гепарин, дистрогликаном, гепарином и интегринами (рис. 5). Способность индуцировать образование постсинаптической специализации в основном зависит от С-концевого домена.
Ведущая роль агрина в формировании нервно-мышечного соединения наиболее очевидна у мышей, у которых при помощи гомологичной рекомбинации выключена экспрессия гена агрина. При таком выключении гена мышечные волокна выглядят нормально и аксон растет в направлении развивающихся мышц, однако нервно-мышечные соединения не образуются.
|
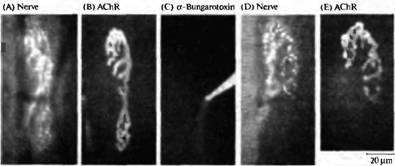
| Рис. 4. Аксоны вызывают агрегацию рецепторов ацетилхолина в областях контакта с мышечными клетками. Фазово контрастные (A. В) и флуоресцентные (С, D) микрофотографии нервно-мышечной культуры клеток Xenopus. Рецепторы ацетилхолина окрашены при помощи родамин бунгаротоксина. (А, С) До и сразу после контакта на миоците имеются спонтанно образованные кластеры рецепторов АХ. (В, D) Через 24 ч спонтанно образовавшиеся области рецепторов АХ исчезли и образовались новые области непосредственно в области аксонального контакта. |
Подобный же фенотип наблюдается у мышей, у которых выключен синтез мышечно-специфического рецептора тирозинкиназы MuSK. Это наводит на мысль, что MuSK формирует часть рецептора к агрину и что вызванное агрином аутофосфорилирование MuSK запускает внутриклеточный сигнальный каскад, который приводит к формированию необходимых компонентов в постсинапсе (рис. 6). Одним из наиболее важных компонентов является рапсин (rapsyn), белок, который, как считается, играет роль в передаче сигналов между рецепторами АХ, MuSK, дистрогликанами и членами Src семейства цитоплазматических рецепторов тирозинкиназ. Таким образом, в нервно-мышечном соединении мутантных мышей с дефицитом рапсина происходит накопление MuSK и выборочная экспрессия гена рецептора АХ в ядре, а также формируются некоторые характерные для синапса свойства, однако не происходит накопления рецепторов АХ.
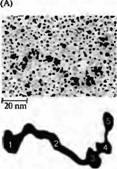
| Рис. 5. Агрин представляет собой гепаран-сульфат протеогликана большой массы (400-600 кДа). Его домены взаимодействуют с ламинином, гепаран сульфат протеогликанами (HSPGs), гепарином, дистрогликаном, интегрином, гепаринсвязывающими белками и рецепторами агрина, которые вызывают агрегацию рецепторов АХ. (А) Электронная микрофотография агрина после rotatory shadowing. (В) Схематическая диаграмма структурных и связывающихся доменов агрина цыпленка. EG — домен, подобный эпидермальному фактору роста; FS — домен, подобный фолиостатину; LE — домен, подобный ламинину EGF; LG — домен, подобный ламинину G; SEA — последовательность, обнаруженная в белках спермы морского ежа, энтерокиназах и агрине; S/T — домены, богатые серином и/или треонином. Также показаны области связывания. Глобулярные (1, 3-5) и вытянутые (2) области молекулы можно увидеть в части А. |
|
Среди белков, которые накапливаются в ответ на изменения в синапсе под действием агрина, находится ARIA, член семейства белков нейрегулинов (neuregulin) и белки рецепторов нейрегулинов erbВ2, erbВЗ и erbВ4. Активация erbВ рецепторов в мышце приводит к экспрессии синаптических субъединиц рецептора АХ.
Гораздо меньше известно о дифференцировке пресинаптической нервной терминали. Эксперименты МакМахана показали, что молекулы, прочно связанные с синаптической базальной мембраной во взрослой мышце, могут вызывать формирование активных зон в регенерирующих аксонах. Отсутствие пресинаптической специализации у мутантных мышей с дефицитом агрина и MuSK может говорить о том, что во время развития пресинаптическая дифференцировка управляется ретроградными сигналами с мышечных клеток в ответ на выделение агрина. Одним из таких ретроградных сигналов, связанных с базальной пластинкой, является ламинин2; он накапливается во время изменений в постсинапсе в ответ на агрин, и у мутантных мышей, у которых имеется дефицит ламинина2, имеются явные аномалии пресинаптической дифференцировки.
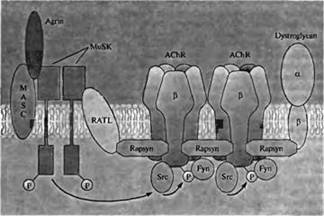
| Рис. 6. Взаимодействие агрина с MuSK запускает дифференцировку постсинаптических образований в мышечной клетке, где начинают накапливаться рецепторы АХ, рапсин и дистрогликаны Связывание агрина с MuSK требует корецептора неидентифицированного типа (MASK) и приводит к аутофосфорилированию тирозина MuSK и активации внутриклеточных киназ Src и Fyn. Активированный MuSK захватывает рапсин посредством неидентифицированного трансмембранного белка, RATL. Рапсин, в свою очередь, захватывает дистрогликан и рецепторы АХ, которые фосфорилируются по остаткам тирозина в -субъединице. Через взаимодействие с дистрогликаном происходит накопление большого количества дополнительных синаптических факторов (не показано). |
|
Выводы
У позвоночных в период эмбриогенеза происходит диффузия протеинов из Шпемановских организационных центров, что приводит к формированию нервной пластинки, края которой загибаются вверх и формируют нервную трубку.
Клетки, расположенные в стенках нервной трубки, быстро делятся. Постмитотические нейроны и клетки-предшественники глии мигрируют в различных направлениях с вентральной поверхности нервной трубки и образуют ЦНС.
Миграция нейронов происходит вдоль радиально расположенных глиальных клеток и клеточных путей, обозначенных различными метками на поверхности клеток и компонентами экстраклеточного матрикса.
Конечное идентифицирование клеток определяется их происхождением и индукционными взаимодействиями с другими клетками.
Гомеотические гены являются управляющими генами, которые контролируют и координируют экспрессию групп других генов и, таким образом, определяют формирование различных частей тела.
Литература:
1. Gilbert, S.F. 2000. Developmental Biology, 6th Ed. Sinauer Associates, Sunderland, MA.
2. Levi-Montalcini, R. 1982. Developmental neuro-biology and the natural history of nerve growth factor. Anny. Rev. Neurosci. 5: 341-362.
3. Lumsden, A, and Krumlauf, R. 1996. Patterning the vertebrate neuroaxis. Science 274: 1109-1115.
4. McAllister, A.K., Katz, L. C., and Lo, D.C. 1999. Neurotrophins and synaptic plasticity. Annu. Rev. Neurosci. 22: 295-318.
Похожие работы
... вопрос: существуют ли факторы, подобные ФРН, в ЦНС? В самом деле, в экстракте из ЦНС был обнаружен протеин, названный мозговым нейротрофическим фактором (МНФ, brain-derived neurotrophic factor, BDNF), который способствует выживанию нейронов дорзального спинного ганглия (ДСГ) в культуре и спасает их от гибели, если вводится in vivo эмбрионам во время периодов естественной гибели нейронов. Очистка ...

0 комментариев