Лабораторная работа № 3
Определение кристаллохимических формул магнитных материалов по данным
мессбауэровской спектроскопии
I. Цель работы
Освоить расчет кристаллохимических формул магнитных материалов при различном числе обменных связей железа, за счет разупорядочения в структуре, изоморфных примесей и вакансий катионов.
II. Введение
Явление нарушения прямых и косвенных обменных магнитных взаимодействий за счет изоморфных замещений, вакансий и разупорядочения катионов в кристаллической структуре широко распространены как в техногенных магнитоупорядоченных материалах, так и в минералах. При этом возникают неэквивалентные положения ионов железа, которые могут отличаться как по изомерному сдвигу, квадрупольному расщеплению, так и магнитным полям на ядрах Fe57. Примерами могут служить ферриты различного состава, где за счет изоморфных замещений существенно меняются их магнитные характеристики, например в ферритах-шпинелях состава (Fe3-xMex), сплавы на основе железа и немагнитных элементов, например Fe1-xМех, Fe3-хМех, минералы сульфидов из группы пирротина Fe1-хS, в которых за счет различного числа и расположения вакансий рвутся обменные связи и возникают неэквивалентные положения ионов железа с магнитными полями на ядрах Fe57, зависимыми от числа вакансий во второй координационной сфере. Из-за этого определение состава таких соединений часто сопряжено со значительными трудностями. Определенную помощь в ряде случаев при расчете кристаллохимических формул может оказать мёссбауэровская спектроскопия. На примере ферромагнитного магнитного сплава сендаста ниже приведена технология таких расчетов.
III. Физическая сущность методика определения кристаллохимических формул
Известно [1, 2], что во многих случаях по мессбауэровским параметрам определяется координация ионов железа. С другой стороны, между координационными числами и формульными коэффициентами существуют обратные соотношения. Так, в структурах типа АВ к.ч.А = к.ч.В, в структурах АВ2 к.ч.А/к.ч.В =2:1, в общем случае АmВn к.ч.А/к.ч.В=n/m. Особенно успешно такие расчеты реализуются, когда вследствие изоморфных замещений или дефектов рвутся обменные магнитные связи и изменяется состав координационного окружения как в зюссите, или за счет вакансий как, например, у пирротина.
Эти два положения были рассмотрены нами и применены для расчета кристаллохимической формулы исследуемого твердого раствора Fe- Si.
Мёссбауэровский спектр образца природного аналога сендаста (Рис.1), снятый при комнатной температуре, имеет сложную сверхтонкую структуру с двумя наиболее ярко выраженными секстетами, соответствующими двум магнитным подрешеткам от ионов железа с различным числом атомов Fe (4 и 8) в первой координационной сфере [3].
Таблица 1
Химический состав природного аналога сендаста
|
Природный аналог сендаста |
Элементы |
∑ |
||||
|
Fe |
Si |
Ti |
V |
Ni |
||
|
Содержание, % |
86,34 |
13,52 |
0,002 |
0,23 |
0,09 |
100,10 |
|
Кристаллохимическая формула рассчитанная по х/а |
Fe3,04V0,1Si0,95 или (Fe, V)3,05Si0,95 |
|||||
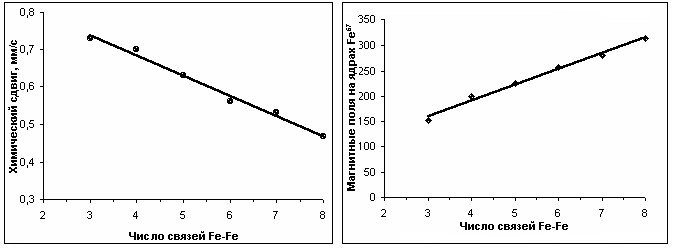
Дополнительные секстеты, присутствующие в спектрах природного зюссита, обусловлены возникновением неэквивалентных положений атомов железа, имеющих различное число (2, 3, 5, 7) обменных связей Fe-Fe, образующихся за счет статистического распределения части атомов Fe и Si. Мёссбауэровские параметры зюссита приведены в таблице 2. Зависимость химического изомерного сдвига от числа связей (Рис. 2) линейна. Уменьшение изомерного сдвига с ростом числа связей Fe-Fe в структуре объясняется увеличением их ковалентности. Линейную зависимость от числа связей Fe-Fe имеют также магнитные поля на ядрах Fe57 (Рис. 3). С ростом числа связей величина магнитного поля увеличивается, что вполне закономерно.
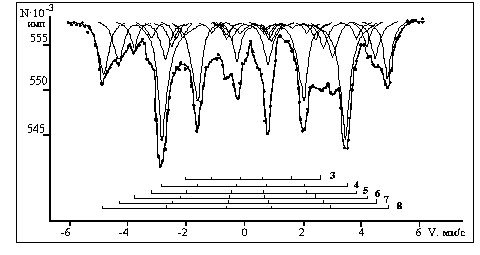
Рис. 1. Мессбауэровский спктр зюссита (3-8 число обменных связей Fe-Fe).
Таблица 2
Мессбауэровские параметры зюссита
|
№№ п.п. |
Число связей между центральным ионом Fe полиэдра и лигандами |
Изомерный химический сдвиг d, мм/c |
Квадрупольный сдвиг D, мм/с |
Магнитные поля на ядрах Fe57, кЭ |
Ширина линии Г, мм/с |
Площади секстипле- тов % отн. |
|
1 |
8 |
0,47 |
0,04 |
315 |
0,35 |
21,2 |
|
2 |
7 |
0,53 |
0 |
280 |
0,35 |
14,7 |
|
3 |
6 |
0,56 |
-0,05 |
258 |
0,35 |
10,8 |
|
4 |
5 |
0,63 |
-0,10 |
225 |
0,35 |
3,6 |
|
5 |
4 |
0,70 |
-0,05 |
200 |
0,35 |
39,9 |
|
6 |
3 |
0,73 |
-0,01 |
152 |
0,35 |
9,8 |
|
|
При этом по величине магнитного поля на ядрах устанавливается число немагнитных атомов в окружении железа, а по площади соответствующей составляющей мёссбауэровского спектра формульные коэффициенты железа. Пользуясь соотношением между к.ч. и формульными коэффициентами, устанавливаются формульные коэффициенты немагнитных элементов, или вакансий [4,5]. Поскольку формулу сендаста можно представить в виде FeS1+Х, по площадям секстетов можно определить долю неэквивалентных ионов железа каждого типа y, приходящихся на атом железа. Так как во второй координационной сфере у каждого атома железа в структуре сендаста имеется 8 соседей, то при одной оборванной связи на этот атом будет приходиться 0,125 единиц немагнитных атомов, а на у атомов 0,125у единиц. Таким образом, находятся формульные коэффициенты х немагнитных атомов, приходящиеся на у неэквивалентных атомов железа. В общем случае кристаллохимическая формула таких соединений записывается как:
Fey1(0) Fey2(1) (Me )x2 Fey3(2) (Me)x3 ...Feyn(n-1) (Me,)xn , (1)
где верхним индексом в скобках указано число оборванных связей Fe-Fe за счет немагнитных атомов или вакансий в окружении атома железа. где: у - формульные коэффициенты неэквивалентных атомов железа; х - формульные коэффициенты приходящихся на них немагнитных атомов. При этом у1+ у2+ у3+... +уi = 1; х1+х2+ х3+...+хj = Х.
Для непосредственно изученного образца природного аналога сендаста формула запишется как:
Fe0,637(0)Fe0,441(1) (Si,V)0,055 Fe0,324(2) (Si,V)0,081Fe0,108(3) (Si,V)0,041 Fe1,196(4) (Si,V)0,598 Fe0,294(5) (Si,V)0,184 (2)
Приведенная к виду Fe3(Si,V)0,959 , эта формула достаточно хорошо совпадает с рассчитанной формулой по данным химического анализа - Fe3,04,V0,01 Si 0,95 (табл.1).
Другим примером применения методики, является расчет, когда оборванные магнитные вязи возникают за счет вакансий катионов в структуре минерала, например в пирротинах различных модификаций [4]. На рис. 4. показаны возможные неэквивалентные положения ионов железа в модификациях пирротина 4С, 5С, 6С, 11С.
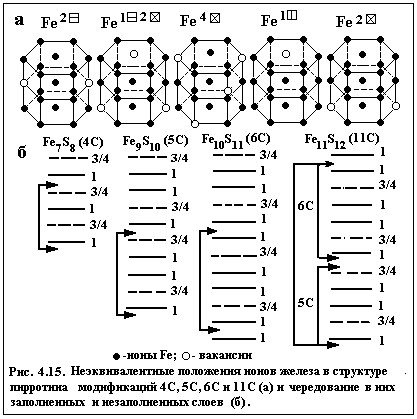
Рассчитанные значения вклада в магнитные поля на ядрах Fe57 от связи каждого типа позволили найти теоретические значения полей на ядрах атомов железа при любом числе и расположении вакансий в его катионном окружении. Это особенно важно при изучении гексагональных пирротинов, в которых вакансии могут быть как упорядочены, так и неупорядочены, вследствие чего их число в ближайшем катионном окружении атомов железа может быть различным. Расчет значений магнитных полей представлен в таблице 3.
Таблица 3
Магнитные поля на ядрах атомов железа при различном числе вакансий в их второй
координационной сфере
|
№ п/п |
Число и расположение вакансий |
Магнитные поля на ядрах Fe57, кэ |
Модификация пирротина |
||
|
Троилит |
Моноклин-ный пирротин |
Гексагональ-ный пирротин |
|||
|
1 |
0 |
308 |
|||
|
2 |
1 |
||||
|
3 |
2 |
302 |
302 |
4с, 5c, 6c, 11c |
|
|
4 |
3 |
299 |
|||
|
5 |
1 |
290,5 |
5c, 6c, 11c |
||
|
6 |
1 |
287,5 |
|||
|
7 |
1 |
287,3 |
|||
|
8 |
1 |
284,5 |
|||
|
9 |
1 |
284,3 |
|||
|
10 |
1 |
281,3 |
|||
|
11 |
2 |
273 |
|||
|
12 |
2 |
270 |
|||
|
13 |
1 |
269,8 |
|||
|
14 |
2 |
267 |
|||
|
15 |
2 |
266,5 |
5c, 6c, 11c |
||
|
16 |
2 |
263,5 |
|||
|
17 |
2 |
260,5 |
|||
|
18 |
2 |
249 |
249 |
4c, 5c, 11c |
|
|
19 |
3 |
245,8 |
|||
|
20 |
3 |
242,8 |
|||
|
21 |
3 |
228,3 |
|||
|
22 |
4 |
225 |
225 |
4c,5c, 11c |
|
Примечание:
![]() - вакансия находится с атомами железа в одной плоскости;
- вакансия находится с атомами железа в одной плоскости;
![]() - вакансия находится вдоль оси «c» в смежной плоскости;
- вакансия находится вдоль оси «c» в смежной плоскости;
![]() -вакансия находится в смежной плоскости с углом Fe-S - Fe 135°.
-вакансия находится в смежной плоскости с углом Fe-S - Fe 135°.
Расчет ограничен 4-мя вакансиями во второй координационной сфере атомов железа, поскольку в моноклинном пирротине это максимальное их число, и вероятность, что в неупорядоченном гексагональном пирротине в катионном окружении их может быть больше, мала, так как железистость гексагональных пирротинов больше по сравнению с моноклинным. Полученные данные позволяют установить состав пирротина любого типа.
Мёссбауэровские спектр пирротина представляют сумму секстетов, каждый из которых обусловлен ионами железа с определенным числом вакансий во второй координационной сфере. Неэквивалентные положения Fe характеризуются своими магнитными полями на ядрах. Разложив экспериментальный спектр с помощью компьютерной обработки на составляющие секстеты, по значению магнитных полей на ядрах неэквивалентных ионов железа по таблице 3 можно установить, сколько вакансий в их катионном окружении и как они расположены. Поскольку формулу каждого пирротина можно представить в виде FeS1+Х, по площадям секстетов можно определить долю неэквивалентных ионов железа каждого типа y, приходящихся на атом железа. Так как во второй координационной сфере у каждого атома железа в структуре пирротина имеется 20 соседей, то при одной вакансии среди них на этот атом будет приходиться 0,05 вакансии, а на у атомов 0,05у вакансий. Таким образом, находятся формульные коэффициенты вакансий х, приходящиеся на у неэквивалентных атомов железа. Формулу пирротина можно записать в виде:
Fey1(1c ) c x1 Fey2(2c ) c x2 … Feyi(nc ) c xj, S1+X, (3)
где: у - формульные коэффициенты неэквивалентных атомов железа; х - формульные коэффициенты приходящихся на них вакансий. При этом у1+ у2+ у3+...+уi = 1; х1+х2+ х3+...+хj = Х.
Полученные кристаллохимические формулы позволяют определить состав пирротина в атомных % компонентов, а также дать распределение железа по неэквивалентным позициям.
Правильность методологического подхода определения состава показана на примере упорядоченного гексагонального пирротина Fe9 S10, спектр которого приведен на рисунке 5.
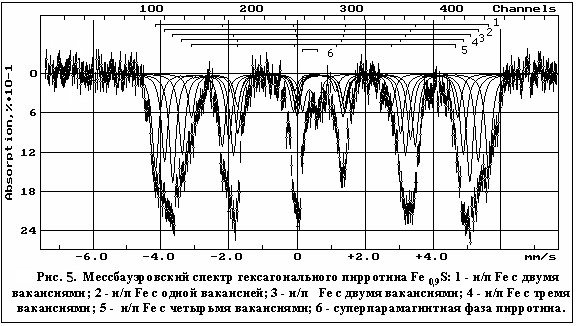
В гексагональном пирротине Fe9S10 (рис. 5) теоретическое отношении ионов Fe различного типа выражается отношением:
Fe(1![]() ) : Fe(2
) : Fe(2![]() ) : Fe(2
) : Fe(2![]() ) : Fe(2
) : Fe(2![]() , 1
, 1![]() ) : Fe(4
) : Fe(4![]() ) = 0,5 : 1,5 : 1,5 : 0,5 : 0,5. (4)
) = 0,5 : 1,5 : 1,5 : 0,5 : 0,5. (4)
Выполнив расчеты формульных коэффициентов неэквивалентных ионов Fe и соответствующих им вакансий, получим формулу пирротина в виде:
Fe (1![]() )0, 1(1) c 0,005(5) Fe(2
)0, 1(1) c 0,005(5) Fe(2![]() )0,3(3) c 0,003(3) Fe (2
)0,3(3) c 0,003(3) Fe (2![]() )0,3(3) c0,03(3) Fe (2
)0,3(3) c0,03(3) Fe (2![]() ,1
,1![]() ) c 0,16(6)
) c 0,16(6)
Fe(4![]() )0,1(1) c 0,02 S1+X , а в кратком виде Fe S1,111, или Fe 0,9 S. (5)
)0,1(1) c 0,02 S1+X , а в кратком виде Fe S1,111, или Fe 0,9 S. (5)
Аналогично можно рассчитать теоретические соотношения концентраций неэквивалентных ионов Fe и соответствующие им соотношения в мёссбауэровском спектре, по которым по можно вывести формулы пирротинов модификаций Fe10 S11 и Fe11S12 [ 4-6].
3. Порядок проведения работы
1. Открыть мёссбауэроский спектр PrtM для математической обработки из папки «Примеры спектров», «Лабораторная работа №3».
2. Ввести калибровку.
3. Задать модель разложения спектра и запустить программу обработки.
3. Открыть последовательно окна «Результаты», «Таблица» и распечатать результат.
4. Записать в таблицу 4 значения площадей секстетов и магнитных полей.
5. Определить формульные коэффициенты неэквивалентных ионов железа, исходя из формулы пирротина FeS1+x.
6. Установить по полученным магнитным полям и таблицей 3 количество оборванных связей у ионов Fe.
7. Определить коэффициенты пересчета для определения формульных коэффициентов вакансий и записать в таблицу.
8. Определить формульные количества вакансий и записать в таблицу.
9. Выбрать интервал для корректировки модели и произвести обработку спектра
10. Записать расширенную формулу пирротина и сокращенную и записать в таблицу.
11. Сравнить полученную формулу с теоретической и сделать вывод.
12. Оформить лабораторную работу.
Таблица 4
Результаты поэтапного расчета кристаллохимической формулы пирротина по данным
мёссбауэровской спектроскопии
|
№№ секстетов. |
Площади секстетов % отн |
Магнитные поля на ядрах Fe57 |
Формульные коэффициенты неэквивалентных ионов Fe |
Количество оборванных связей у ионов Fe |
Коэффициенты пересчета для определения формульных коэффициентов вакансий |
Формульные коэффициенты вакансий. |
|
1 |
||||||
|
2 |
||||||
|
3 |
||||||
|
Расширенная кристаллохимическая формула пирротина |
||||||
|
Сокращенная формула пирротина |
||||||
V. КОнтрольные вопросы
В каких случаях применима методика определения кристаллохимических формул материалов? Чем отличается кристаллохимическая формула вещества от химической? Какие мёссбауэровские параметры используются при расчете кристаллохимических формул? Что такое координационное число катионов? Какова последовательность операций при определении кристаллохимических формул? Какую информацию можно получить из мёссбауэровских спектров?ЛИТЕРАТУРА:
1. Menil F. Systematic trends of 57Fe Mössbauer isomer shifts in (FeOn) and (FeFn) polyhedra. Evidence of a new correlation between the isomer shift and the inductive effect of the competing bond T-X (- Fe) (where X is O or F and T element with a formal positive charge) // J. Phys. and Chem. Solids. 1985. Vol. 46. No 7. P. 763-789.
2. Бенкрофт Г., Меддок Р., Барнс Р. Применение эффекта Мессбауэра к минералогии силикатов. 1. Силикаты железа с известной структурой // Физика минералов, М., Мир, 1971, с. 179-204.
3. Первая находка зюссита на Земле / М.И. Новгородова, Р.Г. Юсупов, М.Т.Дмитриева, В.В.Коровушкин и др. // ДАН СССР, 1983, т. 271, № 6, с. 1480-1483.
4. Коровушкин В.В. Определение состава минералов группы пирротина с количественным распределением ионов железа по неэквивалентным позициям с помощью ЯГР-спектроскопии / Инструкция НСОММИ № 18 ЯГР, М., ВИМС, 1989, 19 с.
5. Коровушкин В.В., Якубовская Н.Ю., Шипко М.Н. Применение мессбауэровской спектроскопии для расчета кристаллохимических формул некоторых минералов и сплавов // Тезисы Всесоюзной конф. «Прикладная мессбауэровская спектроскопия», Казань, 1990, с.126.
6. Коровушкин В.В. ЯГР-спектроскопия в практике геолого-минералогических работ. (Лабораторные и технологические исследования минерального сырья: Обзор) / М., АО «Геоинформмарк». 1993, 39 с.
0 комментариев