Равновесие реакции образования метанола. Процесс получения метанола основан на взаимодействии водорода и окиси углерода:
2Н2 + СО « СНзОН + 21,67 ккал
Реакция может протекать как в прямом, так и в обратном направлениях.
В соответствии с законом действующих масс скорость любой химической реакции пропорциональна произведению концентраций
реагирующих веществ. Тогда скорости прямой и обратной реакций выразятся уравнениями
u1 = k1 [Н2]2 [СО] u2 = к2 [СНзОН]
где [Hz], [СО] и [СНзОН]—концентрации водорода, окиси углерода и метанола; k1, kz—константы скорости прямой и обратной реакций, значения которых зависят от температуры/
При условии равновесия скорости прямой и обратной реакций становятся равными
k1 [Н2]2 [СО] = к2 [СНзОН] откуда:
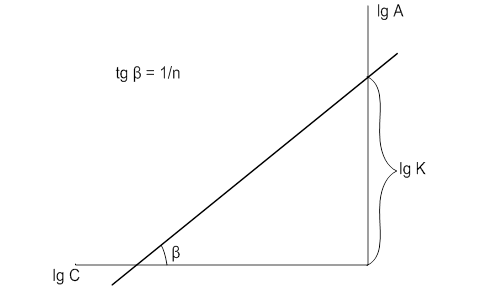
![]()
где К—константа равновесия реакции.
Значение константы равновесия необходимо для расчета равновесного выхода метанола. Равновесный выход—это теоретический максимальный выход метанола, который может быть получен из водорода и окиси углерода, .взятых при данных концентрациях, температуре и давлении процесса. Константу равновесия можно определить как теоретическим, так и экспериментальным путем.
Константа равновесия может быть представлена в различных единицах измерения.
Давление. В технических расчетах обычно пользуются выражением константы равновесия через парциальное давление компонентов.
При повышении давления и понижении температуры равновесие сдвигается в сторону увеличения выхода метанола. В промышленных условиях синтез метанола осуществляется из газовой смеси, содержащей кроме водорода и окиси углерода также двуокись углерода. Поэтому при расчете равновесия синтеза метанола из смеси газов Н2—СО—COz необходимо учитывать следующую реакцию:
СО2 + Н2(г)—> СО + Н2О — 9,8 ккал ;
Равновесный выход метанола, степень превращения окиси и двуокиси углерода в значительной мере меняются в зависимости от давления, температуры, отношения Н2: СО и содержания двуокиси углерода в газе. Влияние давления и температуры на равновесный выход метанола определено для следующего состава газа: 1,25 объемн.% СОа; 10,6 объемн.% СО; 74,2 объемн.% Нд;-13,95 объемн.% (CH4+Nz).
Давление. При повышении давления выход метанола почти прямо пропорционально увеличивается и резко возрастает степень превращения окиси/и двуокиси углерода (при 380°С):
Давление, кгс/см2 .......... 50 100 200 300 400
Выход СНэОН, объемн. %...... 0,37 1,56 5,54 9,31 11,68
Следует заметить, что с увеличением давления более резкий рост равновесного выхода метанола наблюдается при повышенных температурах. Так, при изменении давления от 50 до 300 кгс/см5 равновесный выход метанола при 280 °С увеличивается в 2,4 раза а дри 380 °С — в 2,3 раза (отношение Hz : СО =4 : 1).
Температура. С повышением температуры равновесный выход
метанола понижается. Наиболее резкое понижение наблюдается при температурах выше 340°С. В этих условиях (при 300 кгс/см2) начинает снижаться степень превращения окиси и двуокиси угле рода в метанол, причем более резко окиси углерода:
Температура, °С ....... 250 300 340 360 380 400
Выход метанола, объемн. %. . 15,44 14,81 12,88 11,37 9,31 7,40 Степень превращения, %
СО ........... 99,75 97,20 87,52 78,96- 66,19 53,29
СОз ........... 98,00 89,80 77,00 71,50 66,61 64,00
При давлении 50 кгс/см2 и повышении температуры от 180 дс 300 °С равновесный выход метанола снижается более чем в 7 pa;
(отношение Н2 :СО=3,6, содержание двуокиси углерода 6,0 объемн. %). При этом степень превращения окиси и двуокиси углерода в метанол уменьшается с 75,3 до 14,6%.
При повышении отношения На: СО степени превращения окиси и двуокиси углерода возрастают, причем степень превращения СО2 в большей мере, а равновесный выход метанола снижается. Влияние отношения На : СО на равновесны? выход метанола определено для такого состава газа: 1,25 объемн.% С02; 84,8 объемн. %); 13,95 объемн. % (CI^+Nz). При 300 кгс/см2 и 380 °С равновесный выход метанола и степень превращения окислов углерода в зависимости от отношения Нг: СО меняются следующим образом:
Отношение На:СО . ......... 2 4 8 10 14
Выход СНдОН, объемн. %,..... 17,25 13,80 8,39 7,05 5,40
Степень превращения, %
СО ............... 44,50 60,39 66,85 67,80 67,97
СОа .............. 19,50 45,71 70,52 76,15 82,39
\При увеличении содержания окиси углерода в газе, т. е. уменьшении отношения На: СО, равновесный выход метанола возрастает пропорционально при 50 кгс/см2 и 6 объемн. % СОз). Так, при 8 объемн. % СО, равновесный выход метанола составляет 5,71 объемн. %, при 16 объемн. % СО—11,41 объемн. %, а при 24 объемн, % СО—16,82 объемн. % СНзОН.
Двуокись углерода. Реакция восстановления двуокиси углерода водородом до окиси углерода в промышленных условиях синтеза метанола протекает практически до равновесного состояния, и пренебрегать ею при расчете равновесных выходов метанола нельзя. 'При повышении содержания двуокиси углерода в газе равновесный выход метанола меняется незначительно. Степень превращения
окислов углерода в метанол при этом снижается с 42,2% при 6 обьемн.% СО2 до 32,7% при 12 объемн.% СО2.
Инертные компоненты. В промышленных условиях синтез метанола протекает в присутствии инертных к данному процессу газов (метан, азот). Они в реакции не участвуют и не оказывают прямого влияния на равновесие реакции образования метанола. Однако наличие их в газе снижает парциальное (эффективное) давление реагирующих веществ, что ведет к уменьшению равновесного выхода метанола. Поэтому концентрацию инертных компонентов необходимо поддерживать на минимальном уровне.
На основании изложенного следует отметить, что синтез метанола на цинк-хромовом катализаторе, который работает при 360—380 °С, целесообразно проводить только при давлениях выше 200 кгс/см2. На низкотемпературных катализаторах, эксплуатируемых в температурном интервале 220—280°С, возможна работа при давлениях ниже 100 кгс/см2, причем, чем ниже температура, тем ниже может быть и давления синтеза.
Кинетика синтеза метанола. В гомогенных условиях (без катализатора) скорость взаимодействия окиси углерода и водорода ничтожно мала, и получить метанол в больших количествах невозможно. Для увеличения скорости реакции взаимодействия исходных компонентов используют вещества, которые, способствуя ускорению процесса, сами к концу реакций остаются химически неизменными. Для оценки этого ускорения, или иначе активности катализатора, необходимо знать скорость химического взаимодействия реагирующих компонентов. Если реакция протекает в гомогенных условиях, то скорость ее зависит от температуры, давления и концентрации реагирующих веществ. В гетерогенном, каталитическом процессе скорость реакции будет определяться также типом катализатора и состоянием его поверхности. Синтез метанола является гетерогенным каталитическим процессом, протекающим на границе раздела твердой (поверхность катализатора) и газообразной (смесь окиси углерода и водорода) фаз. До начала реакции окись углерода и водород концентрируются на поверхности катализатора (происходит адсорбция СО и Hz). Суммарный процесс синтеза метанола состоит из следующих стадий: диффузия исходных веществ к поверхности катализатора;
адсорбция этих веществ да поверхности катализатора; химическое взаимодействие адсорбированных молекул СО и Н2 до метанола;
удаление (десорбция) образовавшегося метанола с поверхности катализатора. Скорость процесса образования метанола будет равна скорости реакции в зависимости от начальных условии (температуры, давления, концентрации веществ, времени контакта газа с катализатором) позволило вывести кинетическое уравнение. Последнее используют при моделировании процесса и разработке промышленных реакторов.
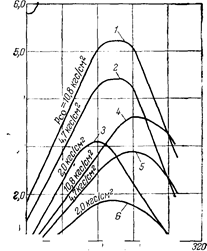
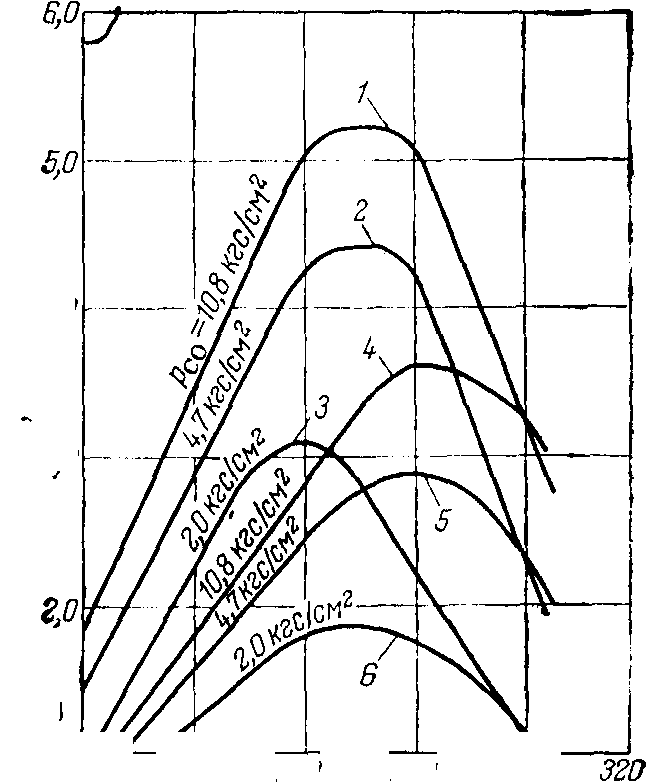
Проведенные на электронно-вычислительной машине расчеты по кинетическому уравнению показали, что оно хорошо описывает процесс образования метанола.
На катализаторе СНМ-1 и может быть использовано для расчета промышленных реакторов, работающих при 50 Krc/C можно определить оптимальные параметры процесса и равновесные условия. Наибольший выход метанола наблюдается при 255— 270° С, что согласуется с экспериментальными данными. С уменьшением парциального давления окиси углерода (повышение отношения Н2:СО) максимум активности катализатора смещается в сторону более низких температур.
При подготовке данной работы были использованы материалы с сайта http://www.studentu.ru
Похожие работы
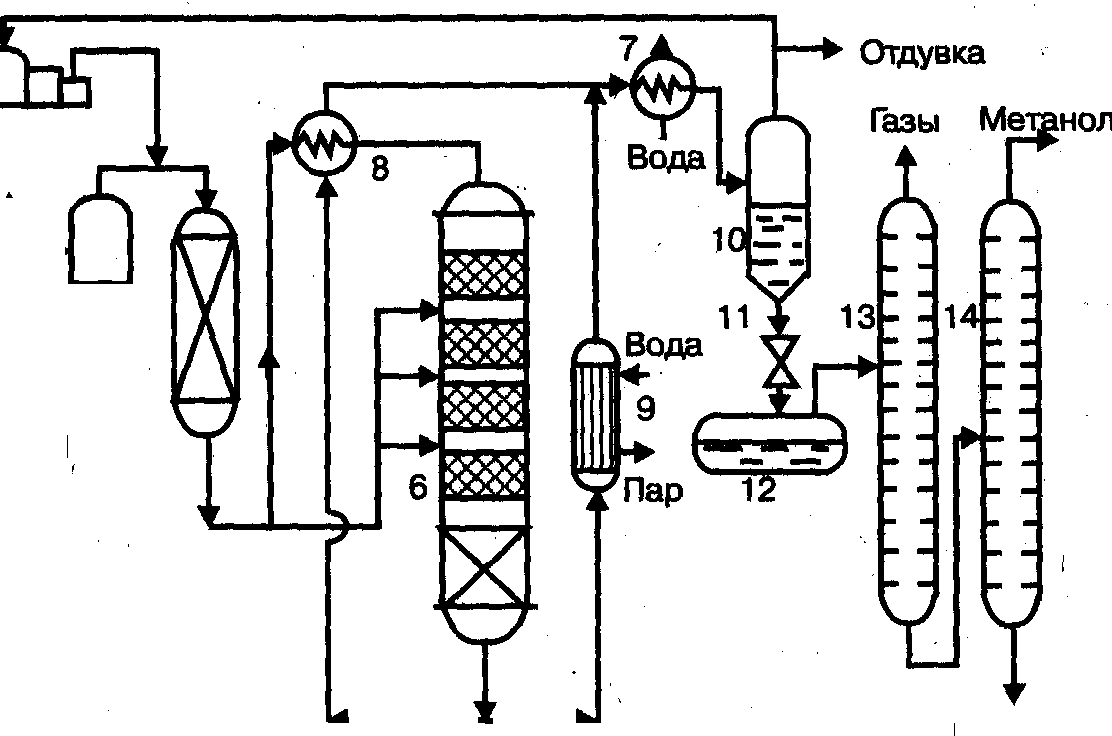
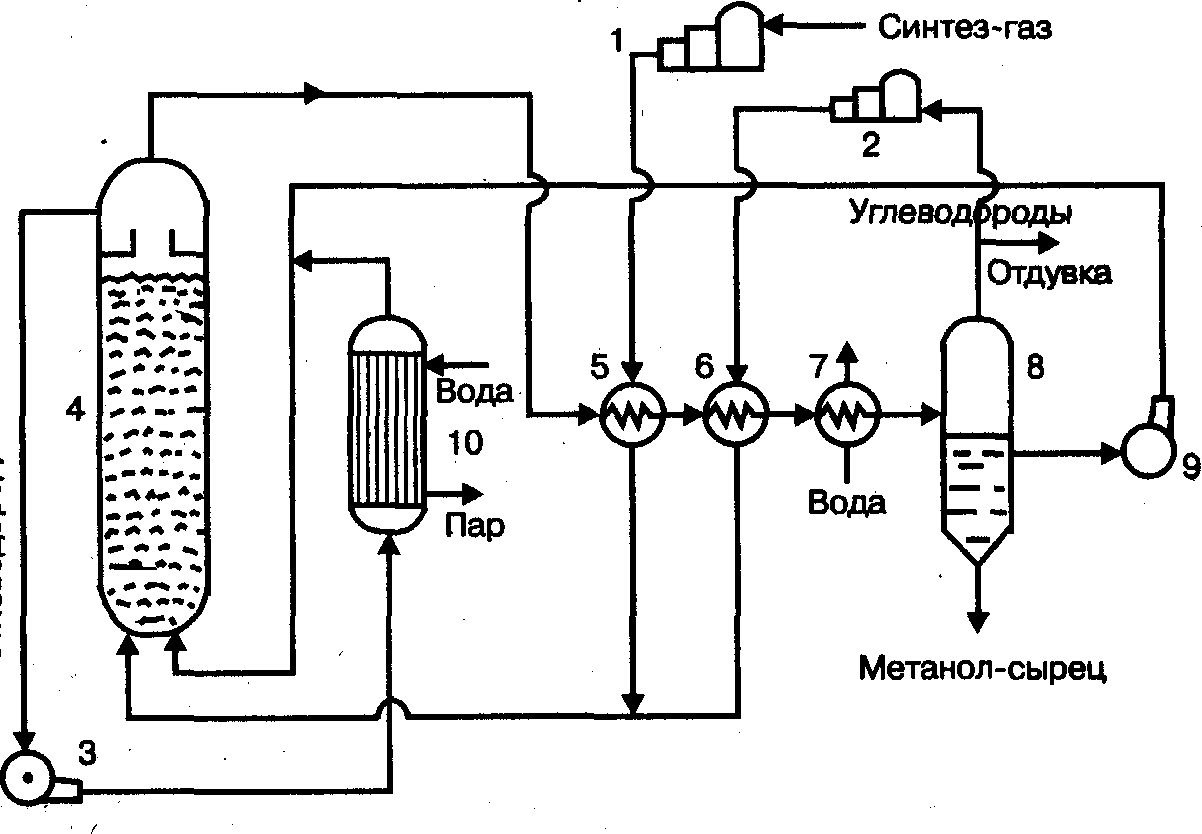
... с циркуляционным газом, который поджимается до рабочего давления в компрессоре 2. Газовая смесь проходит через адсорбер. Высшие спирты Рис. 1. Технологическая схема производства метанола при низком давлении: 1 — турбокомпрессор, 2 — циркуляционный компрессор, 3, 7 —холодильники, 4 — сепаратор, 5 — адсорбер, 6 — реактор адиабатического действия, б — ...
... и красный уголок. Все рассмотренные помещения соединяются между собой с помощью коридоров, лестничных клеток, галерей и тамбуров. 11. БЕЗОПАСНОСТЬ И ЭКОЛОГИЧНОСТЬ ПРОЕКТА ПРОИЗВОДСТВА ФОРМАЛИНА Химическое производство относится к отрасли промышленности, которая представляет потенциальную опасность профессиональных заболеваний и отравлений работающих. Число отравлений и профессиональных ...
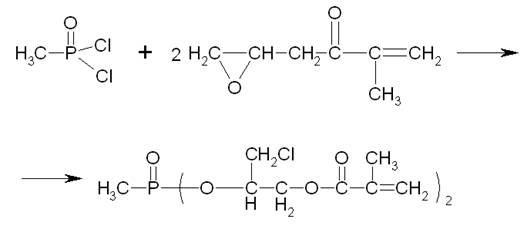
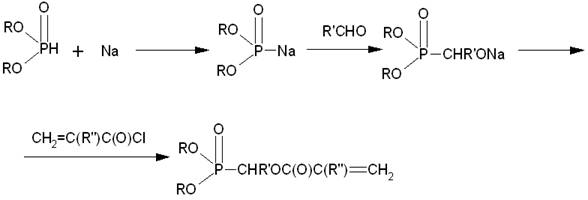
... бесспорно положительным, поскольку при нагревании модифицированных этим соединением полимеров не выделяется вредных веществ. Таким образом, рекомендуемое производство является перспективным для получения малотоксичных полимерных материалов пониженной горючести. Методы получения фосфорсодержащих (мет)акрилатов (литературный обзор) Применение фосфорсодержащих (мет)акрилатов Многие ...
... промышленных сточных вод. Цель регенерации – с одной стороны, десорбция адсорбированных молекул (при регенеративной очистке воды) или деструктивное их разрушение и, с другой стороны, восстановление адсорбционной способности активного угля. Для удаления органических веществ с поверхности активного угля используют вытеснительную десорбцию, смещение равновесного состояния системы с помощью изменения ...
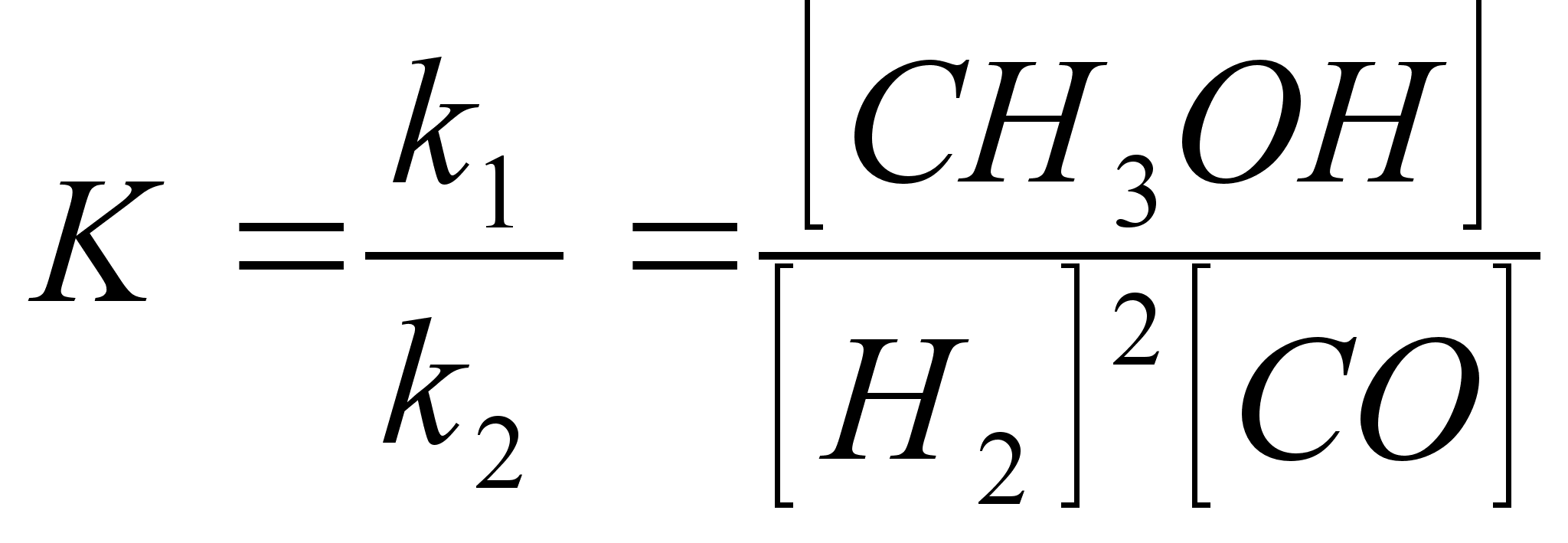



0 комментариев