Московский Государственный Университет
Химический факультет
Моделирование процессов разряда-ионизации серебра на поверхности твердого электрода
Курсовая работа
по аналитической химии
студента 213 группы
Ляхова Антона Борисовича.
Научный руководитель -
к. х. н., доцент А. И. Каменев.
Преподаватель -
к. х. н., старший преподаватель
А. Г. Борзенко.
Москва, 1997.
Введение
Метод инверсионной вольтамперометрии позволяет изучать процессы разряда-ионизации металлов. Основные теоретические положения вольтамперометрии были изложены в работах Делахея - Берзинса и Никольсона - Шейна. Брайниной был предложен ряд теоретических соотношений, позволяющих оценить степень обратимости и скорость процессов разряда-ионизации. Для проверки этих теоретических соотношений в качестве модельного примера обратимого процесса использовано серебро (I), но аппаратурное оснащение не позволяло накопить большой массив данных для получения надежных оценок кинетических параметров. Для изучения кинетики электрохимического растворения металлов предложены различные твердые электроды, однако в литературе отсутствуют данные по изучению электродных процессов с применением углеситалловых электродов.
В литературе приведены различные модели, описывающие обратимое растворение металла с поверхности твердого электрода. Однако сравнительный анализ этих моделей не проводился. Между тем, представляло интерес сравнить эти модели и экспериментально полученные вольтамперные кривые, а также рассмотреть особенности процесса разряда-ионизации серебра на углеситалловом электроде.
Целью работы было проведение сравнительного анализа моделей обратимого растворения металла с поверхности твёрдого электрода, а также сравнение этих моделей с экспериментально полученными вольтамперными кривыми.
Литературный обзор
Процессы электрохимического растворения металлов
Электродный процесс состоит из ряда последовательных стадий:
1. Подвод вещества из объема раствора в зону реакции.
2. Электрохимическая реакция.
3. Отвод продуктов.
Поэтому скорость электрохимического процесса может лимитироваться либо массопереносом вещества - обратимый процесс, либо разрядом-ионизацией - необратимый процесс, либо тем и другим.
Предположим, что перенос электрона происходит быстро и процесс контролируется только скоростью диффузии (конвекцией и миграцией можно пренебречь). В случае использования плоского электрода массоперенос вещества к электроду можно считать линейным. Поэтому основное уравнение диффузии ( второй закон Фика [2] ) можно записать, как
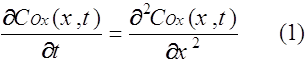 для окисленной формы и
для окисленной формы и
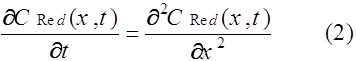 для восстановленной формы.
для восстановленной формы.
Для описания токов, связанных с электродными реакциями, необходимо решить уравнения (1), (2). Впервые эту задачу решили Шевчик и Рендлс. Рендлс применил для решения графический метод. Аналитический метод, избранный Шевчиком, заключается в применении преобразования Лапласа. После обратного преобразования получается выражение для потока вещества Ox от поверхности электрода.
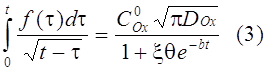
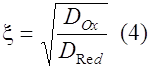
В окончательной форме интегральное уравнение (3), после перехода к безразмерным координатам z = t/b, выглядит следующим образом:
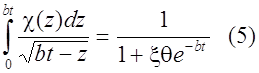
Решение (5) дает зависимость (bt) от bt при данном . Эта функция определяет форму вольтамперных кривых для обратимого процесса. bt связано с потенциалом
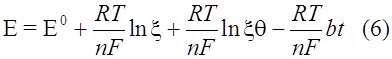
т.е. (bt) можно представить как ([E - E0]n) или i(E).
Из уравнения (5) следует, что
![]()
Уравнения (3) и (5) решали различными способами.
Мацуда и Аябе [1] получили следующее аналитическое решение уравнения (5)
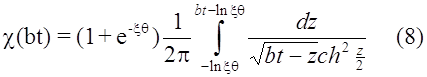
Гохштейн [6] решил уравнение (15) также в аналитическом виде
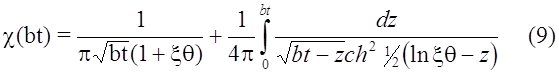
Интегралы в функциях (8), (9) авторы работ [1,6] раскрыли как интегральное уравнение Абеля и вычислили его значения по формуле Маклорена.
Никольсон и Шейн [7] решили уравнение (5) численным методом в виде интеграла Римана-Стилтжета
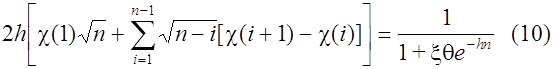
Рейнмут [8] выразил (5) в виде ряда:
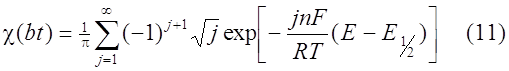
Найденная любым из приведенных способов функция определяет форму вольтамперных кривых в случае обратимого электродного процесса. Уравнение тока пика легко получили на основе уравнения (7) и графика функции (8 - 11). Это выражение известно как уравнение Рендлса - Шевчика:
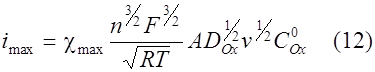
В случае > 6 во всех решениях max = 0.447. Для температуры 25 °С это выражение сводится к зависимости
![]()
Левая полуширина пика, используемая как критерий обратимости, в этой модели для обратимого процесса составляет 0.056/n, В.
Делахеем и Берзинсом [9] была найдена функция, определяющая форму вольтамперной кривой в случае обратимого растворения объемного осадка металла (активность осадка принимается равной 1). В этом случае краевое условие принимает вид
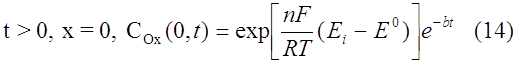 Выражение для тока выглядит как
Выражение для тока выглядит как
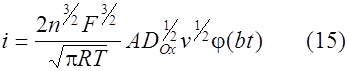 , где
, где 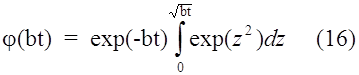
z является вспомогательной переменной. Функция (16) имеет максимум, равный 0.541 при bt = 0.924. Соответствующий ток пика при 25 °С составляет
![]()
Левая полуширина пика в этой модели для обратимого процесса составляет 0.016n, В.
Никольсон [11] установила зависимость i(E) для растворения отдельного незаполненного монослоя металла с поверхности плоского электрода. При этом уравнение Нернста записывается как
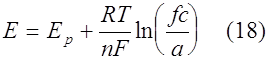
a = m/ms (19)
a - активность осадка
m - количество металла на электроде,
ms - количество металла на единицу активности,
f - коэффициент активности,
Еp - равновесный потенциал, соответствующий а0 и с0
Активность а является в данном случае функцией времени
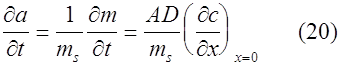
Схема решения такая же, как и в предыдущем случае. Уравнение вольтамперной кривой в интегральной форме в этой модели выглядит так:
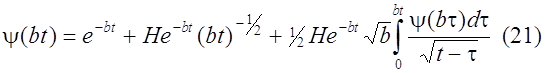
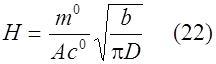
Точки первой производной (bt) описывают форму кривой i(E) и
i = nFm0b(bt) (23)
Это уравнение эквивалентно уравнению
i = q0b(bt) (24)
При Н > 100 максимум функции (bt) определяется как
[-(bt)max] = 0.298 ± 0.002 (25)
При /max > 0.1 выполняется условие
(bt)2 - (bt)1 = ln ( H2 / H1) (26)
Левая полуширина пика составляет 0.040n, В.
В работах Брайниной [ 3, 4, 12 - 14 ] была решена задача растворения металла с электрода при следующих допущениях [15]:
1. Раствор содержит избыток фонового электролита, миграцией ионов можно пренебречь.
2. Подвод ионов металла к поверхности плоского электрода в катодной стадии и отвод в анодной осуществляется путем полубесконечной конвективной или естественной диффузии.
3. Поток ионов металла вблизи поверхности электрода зависит от скорости электродной реакции.
Также было принято предположение о существовании двух энергетических состояний металла на электроде. Первое энергетическое состояние - микрофаза - характерно для малых количеств осадка на электроде. В этом случае его активность а, определяемую общим соотношением
![]()
при малых Q можно представить как
![]()
т.е. активность осадка прямо пропорциональна его количеству на электроде.
Во втором энергетическом состоянии - макрофаза - активность перестает зависеть от Q и равна активности объемной фазы, т.е.
а = а=d/M.
Уравнения (1), (2) были решены со следующими граничными условиями:
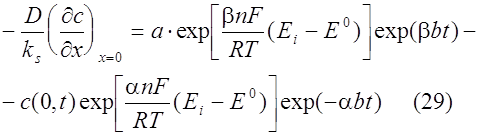
В каждый момент времени t активность определяется уравнением:
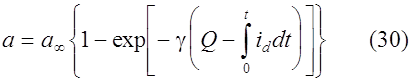
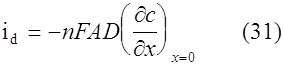
Выражение для потенциала электрода выглядит так:
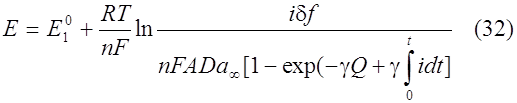
- толщина диффузионного слоя, которая для вращающегося дискового электрода равна [5]
![]()
Решение этого уравнения дает зависимость тока электрохимического растворения металла от времени или потенциала
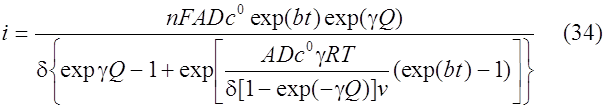
Экспериментальная часть
Аппаратура, реактивы
Использовалась трёхэлектродная ячейка Н-образной формы: индикаторный электрод - цилиндрический углеситалловый (площадь поверхности 0.126 см2), может вращаться со скоростью 2000 об/мин, электрод сравнения - платиновая фольга, площадь поверхности 0,3 см2, вспомогательный электрод - платиновая проволока, диаметр 0.3 мм, длина 0,5 см.
Концентрация ионов Ag+ во всех опытах составляла 1,8*10-6 M, фоновым электролитом являлся 1M раствор KNO3, подкисленный азотной кислотой до pH=2. В ячейку вводили 5 мл фона.
Анодные инверсионные вольтамперные кривые электрохимического растворения серебра получались с использованием анализатора вольтамперометрического АВА-1, сопряжённого с компьютером IBM PC (процессор Intel 80386SX) с помощью интерфейсной платы L-154.
Вычисления на ЭВМ
В процессе сравнительного анализа теоретических моделей обратимого электрохимического растворения металла необходимо было составить подробные таблицы функций, описывающих эти модели. Большинство из этих функций содержат интегралы, которые, как известно из математического анализа, не могут быть представлены в аналитическом виде. Поэтому эти интегралы вычисляли приближённо с помощью ЭВМ. Все определённые собственные (в смысле Римана) интегралы вычисляли по формуле Симпсона [10]. Все вычисления производили на компьютере IBM PC по программам, написанным на языке Borland C++.
Модели процессов обратимого электрорастворения серебра
Модель Делахея-Берзинса описывает форму вольтамперной кривой в случае обратимого растворения объемного осадка металла (активность осадка принимается равной 1) (уравнения (15), (16)).
Была составлена таблица значений этой функции. Максимум j=0.541 при bt=0.924. График этой функции приведен на рис. 1:
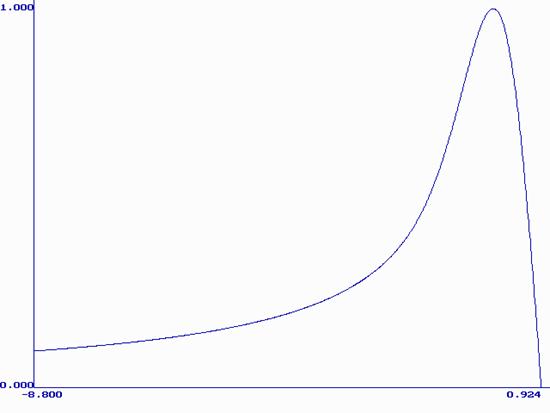
Рис. 1. Нормированная вольтамперная кривая обратимого электрохимического растворения металла (модель Делахея-Берзинса).
Модель Никольсона-Шейна описывается уравнением (9). Модель не учитывает образования новой фазы на поверхности электрода. Графики этой функции при различных xq приведены на рис. 2. Можно заметить, что при ln(xq) ³ 6.5 форма кривой не зависит от значения xq. Потенциал при увеличении xq смещается в область больших по величине значений.
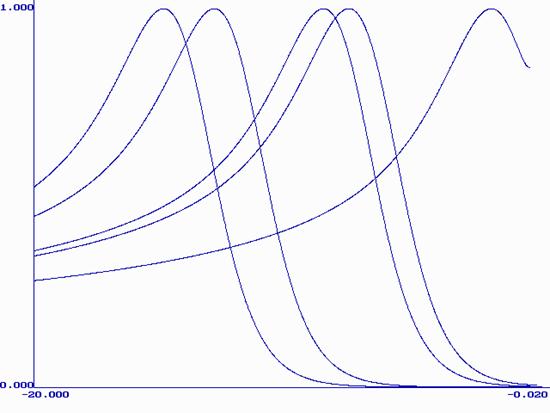
Рис. 2. Нормированные по высоте пиков графики функции (9) при следующих значениях ln(xq): 1(1), 6.5(2), 7.5(3), 11.8(4), 13.8(5).
Модель М. Никольсон описывает форму вольтамперной кривой при растворении монослоя металла с поверхности твердого электрода. Кривая описывается уравнением (21) в интегральной форме. Форму вольтамперной кривой описывает первая производная функции y(bt).
Были составлены таблицы значений y¢(bt) при разных значениях H. На рис. 3 приведены нормированные (все максимумы сведены в точку (0;1)) графики функции y¢(bt) при H=0.1, 1, 3, 10, 100, 1000, 10000, 170000. Из этого рисунка видно, что при больших H форма кривой становится постоянной. Высота максимума при H³100 почти не меняется (0.298±0.002), а потенциал максимума смещается в область более положительных значений согласно уравнению (26):
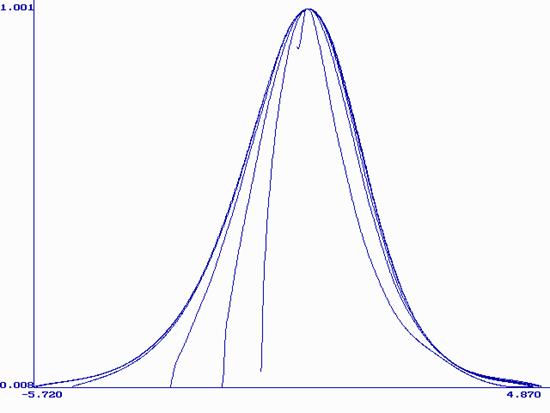
Рис. 3. Нормированные графики функции y¢(bt) при следующих значениях H: 0.1(1), 1(2), 3(3), 10(4), 100(5), 1000(6), 10000(7), 170000(8).
Модель Брайниной основывается на предположении о существовании двух энергетических состояний металла на электроде. Первое энергетическое состояние - микрофаза - характерно для малых количеств металла на электроде, активность зависит от его количества. Во втором состоянии - макрофазе активность перестает зависеть от количества металла и равна активности объемной фазы.
На рис. 4 приводится вольтамперная кривая, полученная при подстановке в уравнение (34) следующих значений параметров: n=1, F=96485 Кл/моль, A=0.126 см2, D=1.54*10-5 см2/c, c0 = 1.8*10-9 моль/см3, s=1,3*10-3 см, g=10-6 Кл-1, gQ=1, R=8,314 Дж/моль*К, T=298 K, v=0.1 В/с, соответствующих условиям эксперимента.
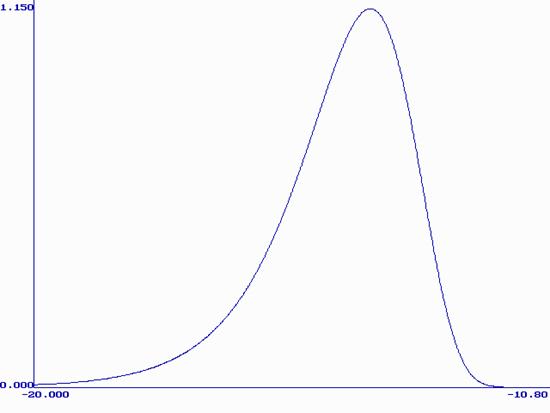
Рис. 4. Вольтамперная кривая, полученная при подстановке в уравнение (34) параметров, соответствующих условиям эксперимента.
В табл. 1-3 приведены некоторые параметры, характеризующие форму пиков для следующих моделей: 1 (Делахея-Берзинса), 2.1 - 2.5 (Никольсона-Шейна), 3.1 - 3.8 (М. Никольсон), 4 (Брайниной), 5 (эксперимент).
Таблица 1
КООРДИНАТЫ МАКСИМУМОВ ФУНКЦИЙ:
| N | Модель | bt | знач. функ. | коэфф. | i, мкА |
| 1 | Модель Делахея-Берзинса | 0.92 | 0.541 | 3.312 | 1.792 |
| 2 | Модель Никольсона-Шейна при | ||||
| 2.1 | ln(xq)=1 | 1.99 | 0.465 | 2.962 | 1.376 |
| 2.2 | ln(xq)=6.5 | 7.61 | 0.446 | 2.962 | 1.322 |
| 2.3 | ln(xq)=7.5 | 8.61 | 0.446 | 2.962 | 1.322 |
| 2.4 | ln(xq)=11.8 | 12.91 | 0.446 | 2.962 | 1.322 |
| 2.5 | ln(xq)=13.8 | 14.91 | 0.446 | 2.962 | 1.322 |
| 3 | Модель М. Никольсон при | ||||
| 3.1 | H=0.1 | 0.23 | 0.703 | 1.974 | 1.387 |
| 3.2 | H=1 | 0.99 | 0.456 | 1.974 | 0.900 |
| 3.3 | H=3 | 1.79 | 0.363 | 1.974 | 0.717 |
| 3.4 | H=10 | 2.87 | 0.321 | 1.974 | 0.634 |
| 3.5 | H=100 | 5.12 | 0.300 | 1.974 | 0.592 |
| 3.6 | H=1000 | 7.42 | 0.298 | 1.974 | 0.588 |
| 3.7 | H=10000 | 9.72 | 0.296 | 1.974 | 0.584 |
| 3.8 | H=170000 | 12.55 | 0.296 | 1.974 | 0.584 |
| 4 | Модель Брайниной | 13.90 | 1.150 | --- | 1.150 |
| 5 | Эксперимент | 13.11 | 1.611 | --- | 1.611 |
Таблица 2
ПОЛУШИРИНЫ ПИКОВ:
| N | левая | правая | прав/лев | общая |
| 1 | 1.240 | 0.639 | 0.5153 | 1.879 |
| 2.1 | 5.555 | нет | нет | нет |
| 2.2 | 5.731 | 2.202 | 0.3842 | 7.933 |
| 2.3 | 5.731 | 2.202 | 0.3842 | 7.933 |
| 2.4 | 5.731 | 2.202 | 0.3842 | 7.933 |
| 2.5 | 5.731 | 2.202 | 0.3842 | 7.933 |
| 3.1 | нет | 0.92 | нет | нет |
| 3.2 | 0.82 | 1.25 | 1.5244 | 2.07 |
| 3.3 | 1.24 | 1.32 | 1.0645 | 2.56 |
| 3.4 | 1.49 | 1.36 | 0.9128 | 2.85 |
| 3.5 | 1.57 | 1.37 | 0.8726 | 2.94 |
| 3.6 | 1.59 | 1.36 | 0.8553 | 2.95 |
| 3.7 | 1.59 | 1.37 | 0.8616 | 2.96 |
| 3.8 | 1.59 | 1.37 | 0.8616 | 2.96 |
| 4 | 1.461 | 0.984 | 0.6735 | 2.445 |
| 5 | 1.49 | 1.01 | 0.6779 | 2.50 |
Таблица 3.
КАСАТЕЛЬНЫЕ В ТОЧКАХ, ОПРЕДЕЛЯЮЩИХ
ПОЛУШИРИНУ (все функции нормированы):
| N | правая | левая |
| 1 | Y = -1.5258*X + 1.4744 | Y = 0.3176*X + 0.8937 |
| 2.1 | нет | Y = 0.0451*X + 0.7505 |
| 2.2 | Y = -0.3242*X + 1.2140 | Y = 0.0421*X + 0.7412 |
| 2.3 | Y = -0.3242*X + 1.2140 | Y = 0.0421*X + 0.7412 |
| 2.4 | Y = -0.3242*X + 1.2140 | Y = 0.0421*X + 0.7412 |
| 2.5 | Y = -0.3242*X + 1.2140 | Y = 0.0421*X + 0.7412 |
| 3.1 | Y = -1.0830*X + 1.4964 | нет |
| 3.2 | Y = -0.4684*X + 1.0855 | Y = 1.4535*X + 1.6919 |
| 3.3 | Y = -0.4618*X + 1.1096 | Y = 0.6127*X + 1.2597 |
| 3.4 | Y = -0.4840*X + 1.1582 | Y = 0.4316*X + 1.1431 |
| 3.5 | Y = -0.4918*X + 1.1738 | Y = 0.3770*X + 1.0919 |
| 3.6 | Y = -0.4966*X + 1.1754 | Y = 0.3650*X + 1.0804 |
| 3.7 | Y = -0.4924*X + 1.1746 | Y = 0.3689*X + 1.0866 |
| 3.8 | Y = -0.4924*X + 1.1746 | Y = 0.3689*X + 1.0866 |
| 4 | Y = -0.8394*X + 1.3266 | Y = 0.3834*X + 1.0601 |
| 5 | Y = -0.589*X + 1.060 | Y = 0.253*X + 0.876 |
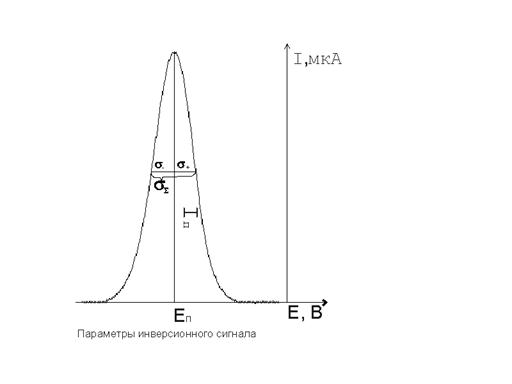
Рис. 5. Приводимые в таблицах параметры пиков (условно).
Из приведенных данных видно, что наиболее близко эксперименту по потенциалам соответствуют модели 4, 3.8, 2.4 (табл. 1) . По высотам наиболее близки к экспериментальным данным модели 1, 4 (табл. 1). Исходя из полуширин пиков и уравнений касательных в точках, определяющих полуширину, форму экспериментальной кривой лучше описывают модели 3.8, 4 (табл. 2, 3). Из всего вышесказанного следует, что наиболее точно эксперимент описывают модели 1, 2.4, 3.8, 4, представленные на рис. 6-8. Соответствующие параметры пиков представлены в табл. 4.
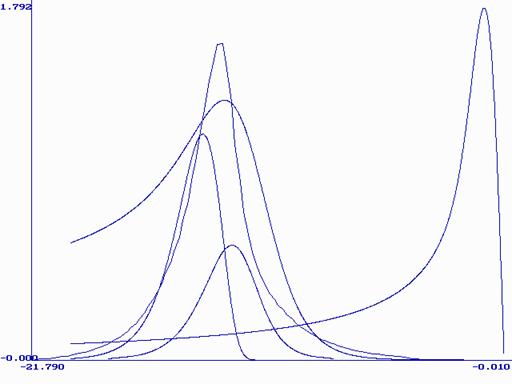
Рис. 6. Теоретические вольтамперные кривые моделей: 1(1), 2.4(2), 3.8(3), 4(4), и экспериментальная кривая(5).
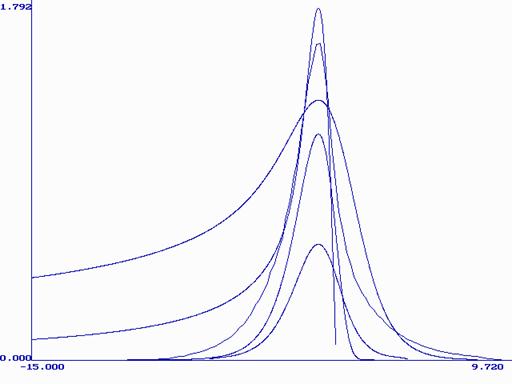
Рис. 7. Теоретические вольтамперные кривые моделей: 1(1), 2.4(2), 3.8(3), 4(4), и экспериментальная кривая(5), максимумы совмещены.
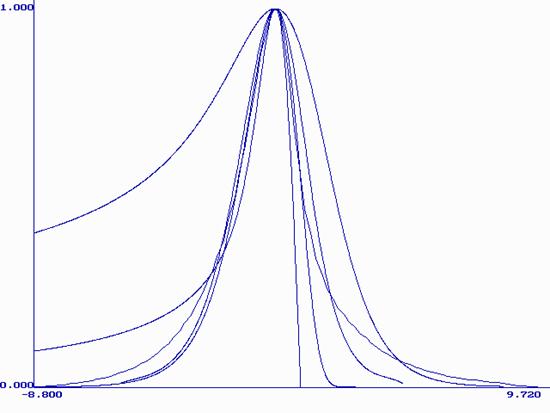
Рис. 8. Нормированные теоретические вольтамперные кривые моделей: 1(1), 2.4(2), 3.8(3), 4(4) и экспериментальная кривая(5).
Таблица 4
| Некоторые параметры пиков, иллюстрирующие их соответствие экспериментальным данным. | |||||
| Модель | 3.8 | 4 | эксп. | 1 | |
| Высота пика, мкА | 0.584 | 1.150 | 1.611 | 1.792 | |
| Левая полуширина пика, s-, bt | 1.37 | 0.984 | 1.01 | 0.639 | |
| Правая полуширина пика, s+, bt | 1.59 | 1.461 | 1.49 | 1.240 | |
| Отношение левой/правой полуширин | 0.862 | 0.673 | 0.677 | 0.515 | |
Таким образом, на основании проведенного сравнительного анализа можно сделать предположение, что процесс разряда-ионизации Ag на углеситалловом электроде близок к обратимому. Рассмотренные теоретические зависимости показали, что нельзя однозначно описать эксперимент ни моделью монослойного покрытия, ни моделью объёмного осадка, поэтому можно предположить, что на поверхности электрода одновременно присутствуют две фазы: адсорбированный монослой и объёмные зародыши металла.
Выводы
1. Проведен сравнительный анализ моделей Делахея-Берзинса, Никольсона-Шейна, М. Никольсон и Брайниной, описывающих обратимое электрохимическое растворение металла с поверхности твёрдого электрода.
2. Получены экспериментальные анодные инверсионные вольтамперные кривые растворения серебра и проведено их сравнение с существующими теоретическими моделями.
3. Высказано предположение, что процесс разряда-ионизации серебра, протекающий на углеситалловом электроде, существенно не отличается от обратимого.
Список литературы
1. Matsuda H., Ayabe Y. // Z. Elektrochem. 1955. B.59. №2. P.494.
2. Дамаскин Б.Б., Петрий О.А. Электрохимия. М.: Химия. 1987. 265 с.
3. Брайнина Х. З., Ярунина Г. В. // Электрохимия. 1966. Т.2. №7. С.781.
4. Брайнина Х. З. // Электрохимия. 1966. Т.2. №8. С.901.
5. Галюс З. Теоретические основы электрохимического анализа. М.: Мир. 1974. 552с.
6. Гохштейн Я. П. // Докл. АН СССР. 1959. Т.126. ¹3. С. 598.
7. Nicholson R. S., Shain I. // Anal. Chem. 1964. V.36. ¹3. P.706.
8. Reinmuth W.H. // Anal. Chem. 1962. V.34. №7. P.1446.
9. Делахей П. Новые приборы и методы в электрохимии. М.: Инлитиздат. 1957. 510 с.
10. Ильин В. А., Садовничий В. А., Сендов Бл. Х. Математический Анализ, Т. 1. М.: Изд-во Моск. Ун-та. 1985. 662 с.
11. Nicholson M. M. // J. Am. Chem. Soc. 1957. V.79. №1. P.7.
12. Брайнина Х. З., Кива Н. К., Белявская В. Б. // Электрохимия. 1965. Т.1. №3. С.311.
13. Брайнина Х. З. // Электрохимия. 1966. Т.2. №9. С. 1006.
14. Брайнина Х. З. Инверсионная вольтамперометрия твердых фаз. М.: Химия. 1972. 192 с.
15. Брайнина Х. З., Нейман Е. Я. Твердофазные реакции в электроаналитической химии. М.: Химия. 1982. 264 с.
Похожие работы
... химия не только обеспечила эти области эффективными методами анализа, но и послужила основой разработки многих новых технологических процессов. Основные этапы развития аналитической химии Многие практические приемы аналитической химии и аналитические методики были известны в глубокой древности. Это, прежде всего пробирное искусство, или пробирный анализ, который выполнялся «сухим» путем, т. ...
... соответствует знак (+) на пересечении строки 8 и столбца Ж. Можно дать и более подробную характеристику межпредметных связей - на уровне подразделов и примеров, а также перечни методов и понятий, но в настоящей статье такие детали вряд ли целесообразны. В таблице цифрами обозначены следующие разделы курса АХ: 1 - метрологические основы химического анализа; 2 - теория и практика пробоотбора; 3 - ...
... АНАЛИЗА 4.1. Теории кислотно-основных индикаторов Кроме использования органических соединений для образования металлокомплексов, образования окрашенных соединений органические реагенты используются очень широко в аналитической химии в качестве индикаторов методов кислотно-основного титрования. Индикатор – это вещество, которое проявляет видимое изменение в точке эквивалентности или вблизи ...
... ;à НbО2- + ННb + СО2 Кислотно-основные свойства лигандов, связанных с комплексообразователем, часто выражены более ярко, чем кислотно-основные свойства свободных лигандов. 4. Комплексные соединения в аналитической химии 4.1 Качественный анализ катионов Первая группа катионов В первую аналитическую группу катионов входят ионов калия K+, натрия Na+, аммония NH4+ и магния Mg2+. ...
0 комментариев