Органической химии.
тема:
"Реакции электрофильного замещения в ароматическом ряду"
Оглавление:
| Электрофильное замещение в бензольном кольце | 2 |
| Правила ориентации электрофильного замещения в бензольном кольце | 4 |
| Реакция Фридела-Крафтса | 8 |
| Галогенирование | 10 |
| Сульфирование | 11 |
| Нитрование | 13 |
Электрофильное замещение в бензольном кольце.
В реакциях электрофильного замещения в бензольном кольце атом водорода замещается на электрофильный реагент при сохранении ароматического характера исходного соединения:
.
Механизм электрофильного замещения можно записать так:
.
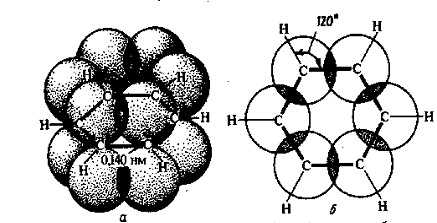
1-я стадия: образование п-комплекса. В этом случае образуется слабая связь между п-электронным облаком бензольного кольца и электрофильным реагентом с дефицитом электронной плотности при сохранении ароматического секстета. Электрофильный реагент располагается обычно перпендикулярно плоскости кольца вдоль его оси симметрии. Эта стадия протекает быстро и не влияет на скорость реакции. Существование п-комплекса доказывается методом УФ-спетроскопии.
.
2-я стадия: образование б-комплекса. Эта стадия медленная и практически не обратимая. Образуется ковалентная б-связь между электрофилом и атомом углерода бензольного кольца, при этом атом углерода переходит из spІ в spі-валентное состояние с нарушением ароматического секстета и образованием циклогексадиенильного катиона (иона бензоления). Катион бензоления вместе с противоионом образуют ионное соединение, хорошо проводящее электрический ток. В ионе бензоления все атомы углерода расположены в одной плоскости, а заместители у spі-гибридизованного атома углерода перпендикулярно ей.
.
Электрофильный реагент присоединяется за счет двух электронов п-электронного облака бензольного кольца с нарушением ароматического секстета. Устойчивость циклогексадиенильного катиона обусловлена делокализацией положительного заряда с образованием мезомерной частицы, в которой четыре п-элект-рона делокализованы в поле пяти ядер.
Истинное строение иона бензоления промежуточное между тремя предельными структурами, реально не существующими (п,р-сопряжение), положительный заряд локализован преимущественно в о- и п-положениях к месту присоединения электрофила.
Придельные структуры б-комплекса:
.
Мезоформулы:
.
Бензолениевые ионы мало устойчивы и высокореакционны, но существуют длительное время в сильной кислоте или сильнокислой среде, где противоион не обладает нуклеофильными свойствами и не будет отщеплять протон.
3-я и 4-я стадии: образование второго п-комплекса и ароматизация. б-комплекс может превращаться в новый мало устойчивый п-комплекс, который под воздействием основания, обычно противоиона, депротонируется. При этом восстанавливается ароматическая система: атом углерода переходит из spі в spІ-валентное состояние и замыкается ароматический секстет.
.
б-комплекс п-комплекс
.
Первые две стадии электрофильного замещения у ароматических соединений аналогичны электрофильному присоединению к алкенам, а 3-я и 4-я стадии отличаются. Вместо присоединения нуклеофильного реагента к карбокатиону отщепляется протон. Так как образуется энергетически более устойчивая ароматическая система (1) по сравнению с диеновой (2):
.
Правила ориентации электрофильного замещения в бензольном кольце.
Все заместители делятся на два типа: первого рода (о- и п-ориентанты) и второго рода (м-ориентанты).
.
Заместители первого рода, кроме Alk-группы, более электроотрицательны, чем углерод, поэтому они уменьшают электронную плотность кольца по механизму отрицательного индуктивного эффекта (-I-эффект). Однако в большинстве заместителей первого рода атом, связанный с бензольным кольцо, имеет неподеленную пару электронов, способную вступать в р,п-сопряжение (+М-эффект). Относительная сила -I и +М-эффектов и определяет реакционную способность соединения.
Заместители второго рода более электроотрицательны, чем углерод (-I-эффект) и, кроме NR -группы, имеют п-связи, способные вступать в сопряжение с бензольным кольцом.
| Орто-, пара-ориентанты | Мета-ориентанты |
| Активирующие: -O -NH2, -NHR, -NR2 -OH, -OR -NHCOR -SH, -SR -Alk, -Aч Дезактивирующие: -F, -Cl, -Bч, -I | Дезактивирующие -NR3 -NO2 -SO3H -COR -CHO -COOH, -COOR -CN -CCl3 -CF3 -CH2NO2 и др. |
Существуют два метода для определения реакционной способности соединений и места преимущественного вступления в кольцо: статистический и динамический.
1.Статистический подход - основан на учёте положения: электрофильный реагент, обладающий дефицитом электронной плотности, будет преимущественно атаковать те положения кольца, где электронная плотность максимальна.
о,п-ориентанты: если в кольце присутствует заместитель с неподелённой электронной парой, для которого +М-эффект (р,п-) больше -I-эффекта, тогда все положения кольца имеют повышенную электронную плотность по сравнению с бензолом. Реакционная плотность такого соединения выше незамещённого бензола. Наибольший избыточный заряд сосредотачивается в о- и п-положениях к заместителю, куда и вступает преимущественно электрофильный реагент.
.
м-ориентанты уменьшают электронную плотность кольца, но особенно сильно в о- и п-положениях. Поэтому преимущественно электрофильный реагент вступает в м-положения, выбирая места наименьшей дезактивации.
.
2.Динамический подход. Различие в действии ориентантов является следствием их влияния на стабильность образующегося в промежуточной стадии бензолениевого иона (б-комплекса). Чем выше устойчивость интермедиата, тем меньше энергия активации.
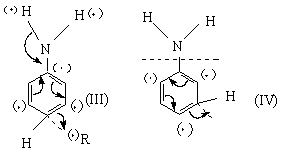
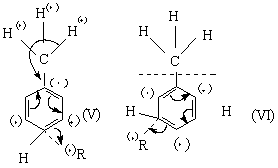
о,п-ориентанты. Ориентация в о- и п-положения к заместителю первого рода предпочтительнее, б-комплекс более устойчив вследствии сильно делокализации заряда 6 в делокализации заряда принимает участие группа ОН. Соответственно уменьшается свободная энергия активации переходного состояния в стадии образования б-комплекса. В случае вступления электрофила в м-положение стабилизация за счёт группы ОН невелика.
.
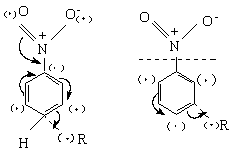
м-ориентанты. Анализ предельных структур б-комплексов показывает, что второй заместитель будет преимущественно вступать в м-положение к заместителю второго рода. Потому что только в этом случае заместитель не будет мешать делокализации положительного заряда в трех позициях кольца б-комплекса. Образование б-комплекса с положением электрофила в о- и п-положениях мало вероятно, так как положительный заряд локализован лишь в двух положениях кольца.
.
Правила ориентации имеют относительный характер и указывают лишь на преимущественное место вступления второго заместителя. Чаще всего образуются все три изомера в том или ином соотношении.
Ориентация в дизамещённых производных бензола.
Если в кольце уже есть два заместителя, то реакционная способность и место вступления третьегозаместителя определяется распределением электронной плотности в кольце с учётом их I- и М-эффектов. Действию электрофила подвержены положения с наибольшей электронной плотностью или приводящие к наиболее устойчивому б-комплексу.
В кольце два заместителя одного рода:
а) Два о, п-ориентанта. В этом случае наибольшая реакционная способность наблюдается у соединений с м-положением заместителя (согласованная ориентация).
б) Два м-ориентанта. Такие соединения проявляют низкую реакционную способность, однако из трёх изомеров наибольшую активность проявляют м-изомеры (согласованная ориентация).
Реакция Фриделя-Крафтса.
Реакция Фриделя-Крафтса - алкилирование или ацилирование ароматических соединений в присутствии катализаторов - кислот Льюиса (AlCl3, BF3, FeCl3) или минеральных кислот (HF, H3PO4 и др.). В качестве алкилирующих средств используются алкилгалогенидыб алкены и спирты, а в качестве ацилирующих - ацилгалогениды:
Алкилирование:
Ацилирование:
Алкилирование:
Алкилгалогениды наиболее распространенные алкилирующие средства.
Образование электрофильного реагента: центральный атом катализатора образует б-комплекс, в котором связь углерод - галоген сильно ослаблена и легко разрывается с образованием ионной пары:
CH3-CH2-Cl + AlCl3 [CH3CH2-Cl-AlCl3] CH3CH2 + AlCl4
Активность алкилгалогенидов уменьшается в ряду: AlkF > AlkCl > > AlkBч > AlkI (в порядке уменьшения сродства галогена к атому алюминия). На активность алкилгалогенидов влияет строение алкильной цепочки: третичные более активны, чем вторичные, которые активнее первичных, это обусловлено устойчивостью образующихся карбокатионов.
Реакция электрофильного замещения обратима:
.
Реакцией Фриделя-Крафтса приводит к образованию изомеров. Например, алкилирование бензола н-пропилхлоридом приводит к образованию 70% изопропилбензола (кумола):
C6H6 + CH3CH2CH2Cl C6H6-CH-CH3 + C6H6CH2CH2CH3
70% CH3 30%
Это можно объяснить перегруппировкой первичного н-пропильного катиона в изопропильный:
H
CH3CH2CH2-Cl-AlCl3 [CH3-CH-CH2 CH3-CH-CH3] AlCl4
Алкены и спирты так же широко используются в реакциях Фриделя-Крафтса. Например, для получение кумола применяют пропилен:
CH3
C6H6 + CH2=CH-CH3 C6H6-CH-CH3
Алкилирование идёт, если галогенид алюминия содержит следы галогеноводорода (сокатализатора):
HX + AlX3 H [AlX4]
CH3CH=CH2 + H [AlX4] [CH3-CH-CH3] AlX4
Алкены вступают в реакцию алкилирования и в присутствии минеральных кислот (HF или H3PO4):
CH3-CH=CH2 + H3PO4 [CH3-CH-CH3] H2PO4
Спирты тоже участвуют в алкилировании в присутствии кислот Льюиса или минеральных кислот:
R-O + BF3 R [HOBF3]
H
В реакцию Фриделя-Крафтса вступают и алкильные производные бензола. Реакция неселективна% кроме моноалкилированного соединения образуется ди- и полиалкилзамещённые:
Моноалкилзаменщённые более реакционноспособны, чем бензол (Alk-группа - заместитель первого рода), и легче вступают в реакции электрофильного замещения. Реакция Фриделя-Крафтса обратима, при нагревании происходит перегруппировка о- и п-диалкилбензолов в термически более устойчивый м-диакилбензол. В реакцию Фриделя-Крафтса не вступают соединения с заместителями второго рода, дезактивирующими кольцо.
Галогенирование.
1.Хлорирование бензола: реакция экзотермическая , по этому введение галогена осуществляется в присутствии катализатора (кислот Льюиса) в жидкой фазе, без нагревания. Наиболее часто используют хлорид железа (III).
2Fe + 3Cl2 2FeCl3
Cl-Cl + FeCl3 Cl Cl FeCl3 Cl-Cl-FeCl3 [ Cl ][FeCl4]
Реакция протекает в инертном растворителе.
Бензольное кольцо атакуется неионизированным комплексом, а разрыв связи Hal-Hal идёт на стадии образования бензолениевого катиона. Отсутствие изотопного эффекта указывает на то, что стадия образования б-комплекса самая медленная стадия процесса.
При избытке хлора хлорирование может проходить по ступенчатой схеме. Вместе с хлорбензолом образуется о- и п-дихлорбензолы.
Сульфирование.
В качестве реагентов при сульфировании используется серная кислота и олеум. Сульфирование обратимо и может сопровождаться образованием продуктов вторичного замещения - диарилсульфона:
Aч-H + HOSO2OH AчSO OH + H2O
AчSO2OH + HAч AчSO2Aч + H2O
Сульфон не образуется при избытке серной кислоты, избыток серной кислоты используют потому, что при уменьшении её концентрации резко уменьшается скорость сульфирования, начинает преобладать обратная реакция - гидролиз.
В качестве сульфирующего реагента может выступать оксид серы (YI). Образование оксида серы (YI) может происходить в результате автопротолиза серной кислоты:
H
HOSO2OH + H-OSO2OH HOSO2O-H + OSO2OH
HOSO2O-H H2O + HOS H3O + S
H O
Высокая электрофильность серы обусловлена высокой полярностью связе S-O. Это приводит к тому, что в стадии образования б-комплекса у серы освобождается свободная орбиталь, способная образовать б-связь с двумя п-электронами кольца.
Сульфирование:
.
При сульфировании все стадии процесса обратимы. В случае сульфирования олеумом, в котором нет сильного основания - воды, способствующего отщеплению протона от б-комплекса, скорость определяется стадией отщепления протона, присутствует изотопный эффект. Если сульфируют купоросным маслом, в котором есть вода, то самой медленной является стадия образования б-комплекса, изотопный эффект отсутствует.
Нитрование.
Нитрование может происходить под действием разных нитрующих реагентов: концентрированной или разбавленной азотной кислоты; нитрующей смеси (смеси азотной и серной кислот); смеси нитрата калия и серной кислоты: KNO3 + H2SO4 KHSO4 + HNO3; смеси азотной кислоты с уксусным ангидридом:
O O O
CH3-C-O-C-CH3 + HO:NO2 CH3-C-O-NO2 (ацетилнитрат)
Электрофильную атаку бензольного кольца осуществляет нитроний-катион, образующийся из нитрующей смеси:
HNO3 + 2H2SO4 NO2 + H3O + 2HSO4
Нитрование происходит по обычному механизму, изотопный эффект отсутствует:
Катион нитрония, атомы азота находятся в sp-гибридизации, не содержит свободных орбиталей. В п-комплексе он располагается вдоль оси симметрии бензольного кольца, сохраняя sp-гибридизацию. В стадии б-комплекса атом азота переходит в sp¤-гибридизацию.
Похожие работы
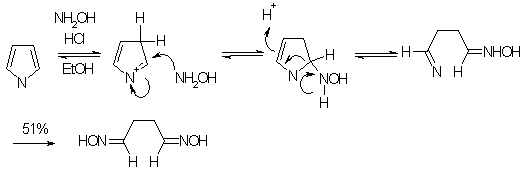
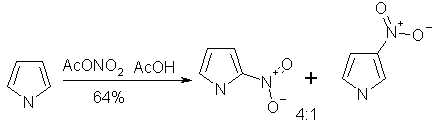
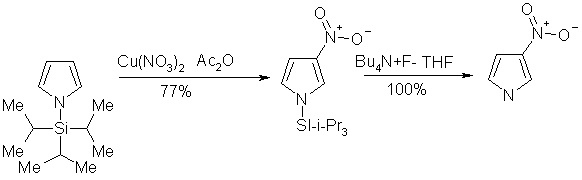
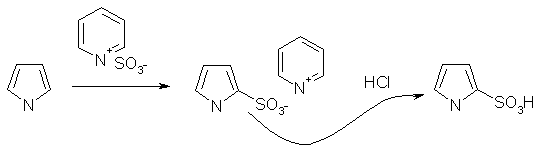
... продуктами олигомеризации и полимеризации. Наиболее гладко пиррол моноалкилируется сопряженными енонами, содержащими уходящую группу в β-положении. 1.2.2 Электрофильное замещение тиофена Как и следовало ожидать, для тиофена характерны реакции, свойственные ароматическим соединениям типа бензола. Тиофен галогенируется, нитруется, сульфируется и ацилируется аналогично фурану и пирролу ...
... ) В ряду ароматических углеводородов часто применяют тривиальные названия, например, метилбензол иначе называют толуолом. По международной номенклатуре (правила ИЮПАК) все ароматические углеводороды объединяют названием – арены. Соответственно, их одновалентные остатки, образованные отнятием водорода от углеродных атомов ядра (одновалентные ароматические радикалы), называют арилами и обозначают - ...
тия цепных процессов с низким расходом энергии. Реакции замещения по радикальному типу изображаются следующими общими схемами: или Кинетическое описание данной реакции: 2. Типы реакции замещения в бензольном кольце При гомолитическом замещении бензольное кольцо атакуется нейтральным радикалом, существующем как кинетически независимая частица, либо возникающем только в ...
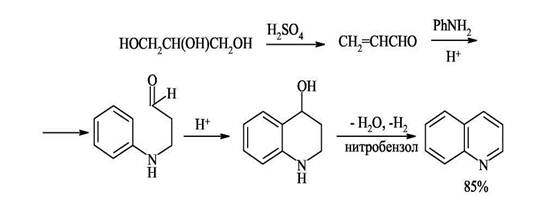
... по карбонильной функции бензальдегида (в мягких условиях альдимины получают с высокими выходами). 2) циклизация альдиминов под действием сильных кислот. Этот способ удачно дополняет два рассмотренных ранее метода синтеза изохинолинов, поскольку при его применении образуются замещённые изохинолины, которые не удаётся синтезировать другими путями. При замене ароматических альдегидов ...
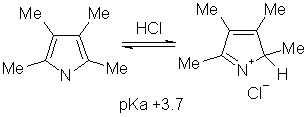
0 комментариев