В.А. Руднов
Необходимость более отчетливой регламентации антибактериальной терапии (АБТ) сепсиса связана с несколькими обстоятельствами: – высоким риском развития неблагоприятного исхода при неадекватном выборе препарата; – принятием решения в условиях дефицита времени; – распространенной в ОРИТ системой дежуранства и различным уровнем подготовки врачей в области терапии инфекций; – наличием доказательств из фармакоэпидемиологических исследований, свидетельствующих об ошибках и нерациональном назначении антибиотиков [1–3].
В последние годы с целью преодоления отмеченных недостатков и совершенствования подходов к терапии данного патологического процесса появился ряд международных и отечественных Рекомендаций и Руководств [4–6].
В отличие от других разделов фармакотерапии сепсиса большинство положений АБТ основаны не на доказательствах высокого уровня, а являются рекомендациями экспертов. Подобная ситуация не является недостатком организации исследований, а отражает сложность сепсиса, как патологического процесса, и особенности антибиотиков, как фармакологических средств, по целому ряду позиций. С целью улучшения восприятия и ускорения внедрения в клиническую практику современных подходов по АБТ сепсиса мы посчитали необходимым конкретизировать в настоящей публикации ряд ключевых положений. Время начала антибактериальной терапии Согласно существующим консенсусным рекомендациям Surviving Sepsis Campaign, объединивших 11 международных Ассоциаций различных медицинских специальностей, АБТ при тяжелом сепсисе должна быть начата в течение первого часа после постановки диагноза и взятия материала для бактериологического исследования [5].
В основу данной рекомендации положены проспективные и ретроспективные исследования, продемонстрировавшие существенно более высокую летальность в случае неадекватного выбора первоначальной схемы АБТ или при запоздалом начале терапии у пациентов с сепсисом и бактериемией, а также госпитальной и внебольничной пневмонией тяжелого течения [1–2].
Быстрая интерпретация тяжести инфекционного процесса может быть выполнена с помощьюиспользования диагностических критериев сепсиса ACCP/SCCM, критериев органной дисфункции (SOFA, MODS, Baue et al.) и/или экспресс–теста на содержание прокальцитонина, уровень которого выше 2 нг/мл, как правило, соответствует сепсису с органной дисфункцией (табл. 1). Алгоритмы выбора схемы антибиотикотерапии Для выбора оптимальной схемы эмпирической АБТ следует принимать во внимание локализацию первичного очага, место возникновения сепсиса (внебольничный, госпитальный, госпитальный в ОРИТ), уровень устойчивости возбудителей госпитальных инфекций (ГИ) к антибиотикам в конкретном отделении, наличие/отсутствие бактериемии. На сегодняшний день в большинстве крупных поливалентных медицинских центров частота грамположительного (Гр+) и грамотрицательного (Гр–) сепсиса оказалась приблизительно равной. Это произошло в результате увеличения роли в патологии таких бактерий, как Streptococcus spp ., Staphylococcus и Enterococcus spp . Инвазивность лечения и рост численности лиц со сниженной антиинфекционной защитой увеличили долю инфекций, вызванных условно–патогенными микроорганизмами, в особенности, S. epidermidis . Среди популяции различных видов стафилококка–возбудителей сепсиса наблюдается неуклонное увеличение метициллин (оксациллин)–резистентных штаммов. Исчезновение доминирующей роли грамотрицательных микроорганизмов сопровождается изменениями этиологической структуры внутри этой группы. Выросла сепсиса, вызываемого неферментирующими грамотрицательными бактериями ( Pseudomonas aeruginosa и Acinetobacter spp .), а также Klebsiella pneumonia продуцентов ? –лактамаз расширенного спектра (БЛРС), а в некоторых лечебных учреждениях – Enterobacter cloacae . Как правило, эти микроорганизмы выступают в роли возбудителей госпитального сепсиса у пациентов ОРИТ. Повышение их значимости в развитии тяжелых инфекций связано с увеличением пропорции больных на длительной ИВЛ и излишне широким использованием в клинической практике цефалоспоринов 3–го поколения и аминогликозидов. Увеличение продолжительности жизни лиц, перенесших критические состояния, популярность схем комбинированной антибиотикотерапии и новые препараты ультраширокого спектра действия обусловили появление прежде крайне редко встречающихся в патологии микробов, таких как Enterococcus faecium , Stenothrophomonas maltophilia , С hryseobacterium spp . и др.. В целом этиологическая структура возбудителей ГИ и уровень их устойчивости к АБП в различных стационарах и отделениях (в особенности в ОРИТ) имеет свое «лицо». Поэтому построение алгоритма АБТ с учетом этиологии и особенностей резистентности к антибактериальным средствам является самым оптимальным подходом. Однако, к сожалению, существование реальных баз данных в ЛПУ, основанных на хорошо организованных микробиологических исследованиях, является пока, скорее, исключением, чем системой. В сложившейся ситуации остается рекомендовать ориентироваться на результаты многоцентровых национальных исследований [7–9].
Взаимосвязь между локализацией очага инфекции и характером микрофлоры, запускающей инфекционно–воспалительный процесс, и местом его развития отображена в таблице 2. Обязательный ракурс оценки состояния пациента – наличие/отсутствие факторов риска смерти у пациента с сепсисом . Под фактором риска смерти понимают какую–либо клинико–лабораторную характеристику (особенность состояния пациента), являющуюся самостоятельным статистически значимым фактором, повышающим риск развития неблагоприятного исхода. В этом отношении наибольшее значение имеют: локализация инфекционного очага, шок и тяжесть ПОН, место возникновения сепсиса (госпитальный, внебольничный), особенности бактериемии (первичная, вторичная, род или вид возбудителя). Эти данные были получены как при рассмотрении когортных исследований, так и в результате выполнения post hoc анализа значительного объема контролируемых испытаний по оценке эффективности отдельных лекарственных средств при сепсисе. В частности, было доказано, что локализация инфекционного очага в брюшной полости и легких сопровождается более высокой смертностью, чем при его нахождении в мочевыводящих путях или коже и мягких тканях при идентичных значениях индексов тяжести состояния пациента [10].
Летальность при вторичной бактериемии превышает таковую при первичной и катетер–ассоциированном сепсисе. А выживаемость при грамотрицательном сепсисес бактериемией ниже, чем при грампозитивном [11].
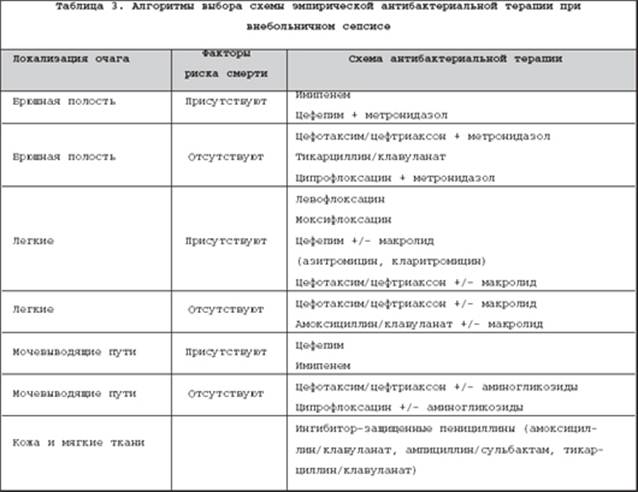
Кроме того, шансы на выживание снижаются у пожилых и престарелых больных, а также у лиц с декомпенсированной хронической сопутствующей патологией (ХПН, ХСН, ХОБЛ, сахарный диабет). В целом алгоритмы выбора схемы АБТ при сепсисе с обозначенных позиций представлены в таблицах 3–4. Подразделение АБТ в зависимости от риска развития неблагоприятного исхода при внебольничном сепсисе обусловлено стремлением максимального снижения вероятности ошибки по выбору препарата и более быстрой эрадикации возбудителя у пациентов в критическом состоянии. Помимо этого, в отношении обозначенных схем выбора в настоящее время имеется обширная клиническая практика, отдельные когортные и контролируемые исследования, свидетельствующие об их высокой эффективности при сепсисе. Вместе с тем, учитывая отчетливую тенденцию к росту устойчивости синегнойной палочки к карбапенемам, следует ограничивать их применение для терапии внебольничного сепсиса в отделениях с высоким уровнем распространенности ГИ и резистентности к ним данного микроорганизма. Анализ применения появившихся в последние годы в арсенале отечественных специалистов респираторных фторхинолонов (левофлоксацин, моксифлоксацин) продемонстрировал их преимущество в плане снижения относительного риска смерти по сравнению с цефалоспоринами 2–3–й генерации в комбинации с макролидами [16].
В силу отсутствия клинических преимуществ и значимого повышения риска нефротоксического действия необходимо отказаться от рутинного добавления аминогликозидов к ? –лактамным АБП как при эмпирической, так и целенаправленной терапии у пациентов с сепсисом (табл. 4) [17].
В общей группе больных не выявлено различий по частоте развития резистентности к АБП, а также бактериальной или грибковой колонизации и суперинфекции. В то время как нефротоксичность при комбинированной АБТ оказалась статистически значимо выше – показатель относительного риска – RR=0,36 (0,28–0,47). С чем могло быть связано такое расхождение между результатами, полученными в эксперименте и в реальной клинической практике? Для АМГ характеренвысокий объем распределения в организме, обусловливающий низкую концентрацию в тканях, в частности, в легких. По–видимому, в этих условиях их содержание в тканях не достигает тех значений минимально подавляющих концентраций (МПК), которые необходимы для эрадикации бактерий. С эти обстоятельством, вероятно, также связано отсутствие доказательств торможения развития устойчивости возбудителей к АБП при добавлении АМГ в схему терапии. Более того, неоправданно широкое использование АМГ привело к росту устойчивости к ним ключевых возбудителей госпитальных инфекций в ОРИТ [14–15].
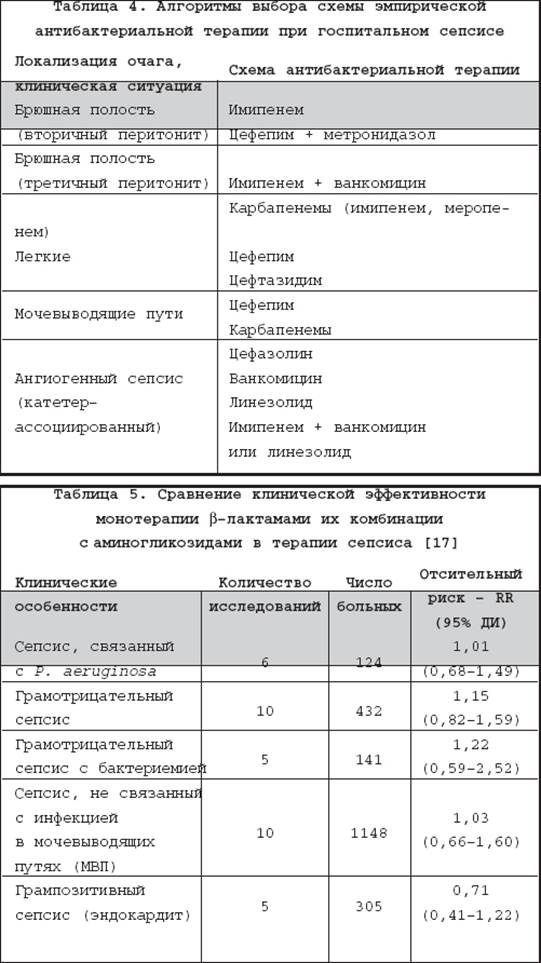
Логика ориентации на факторы риска смерти при выборе схемы АБТ не может в полной мере быть распространена на госпитальный сепсис в силу большей приоритетной значимости ситуации с локальным уровнем чувствительности ключевых возбудителей к АБП. Именно он должен определять выбор между препаратами разных групп или внутри одной из них. Из–за весьма существенного роста резистентности возбудителей ГИ круг потенциально эффективных препаратов в последние годы заметно сузился. Принимая во внимание результаты многоцентровых исследований в России, можно заключить, что наиболее надежная эмпирическая терапии госпитального сепсиса может быть связана с достаточно узким кругом препаратов – карбапенемами и цефепимом. Назначение ципрофлоксацина без знания особенностей по резистентности в конкретном отделении сопряжено с риском неудач. Добавление ванкомицина или линезолида будет оправданным при ангиогенном сепсисе (АС) или вентилятор–ассоциированной пневмонии (ВАП) в отделениях с высоким уровнем распространения MRSA или у пациентов с нейтропенией. На этиологическую структуру АС влияет несколько факторов: длительность катетеризации, место стояние катетера (верхняя полая или бедренная вена), проводимая АБТ, распространенность MRSA или MRSE в конкретном ОРИТ. При катетеризации более 10 суток и/или нахождении катетера в бедренной вене возрастает риск АС, связанного с P. aeruginosa, Enterococcus spp . и MRSA . Если эти факторы ассоциируют с тяжелым состоянием пациента (шок, ПОН), представляется обоснованной эмпирическая терапия в варианте имипенем (Тиенам) + ванкомицин или линезолид . Подчеркнем, что в результате субпопуляционного анализа установлена идентичная клиническая эффективность монотерапии ? –лактамами и их комбинации с аминогликозидами, в том числе и при сепсисе, связанном с P. aeruginosa (табл. 5) [17].
Возможности проведения деэскалационного режима антибактериальной терапии при сепсисе и септическом шоке Стабилизация гемодинамики, регресс СВР и органной дисфункции при условии надежной идентификации возбудителя и характера его чувствительности к АБП являются необходимыми предварительными условиями для рассмотрения возможности через 3–4 дня перехода на АБП более узкого спектра при первоначальном старте с карбапенемов или с комбинации антибиотиков, перекрывающий спектр возможных патогенов. Переход на антибиотик с более узким спектром действия по результатам бактериологического исследования оправдан как с позиций контроля резистентностипроблемных возбудителей, так и экономии материальных средств. Эффективность и безопасность подобной стратегии недавно была подтверждена в проспективных контролируемых исследованиях, которые касались пациентов с госпитальным сепсисом, осложнившим течение пневмонии. Об исходной тяжести сепсиса свидетельствуют следующие характеристики: 44% больных были в состоянии шока, а 83,5% – требовалось проведение ИВЛ [20].
В качестве стартового режима в данном случае использовался имипенем. Непременными условиями для деэскалационной стратегии использования АБП являются надежность лаборатоных данных и отсутствие бактериемии, связанной с K . pneumonia , Acinetobacter spp ., Enterobacter spp. Дело в том, что в отношении тяжелых инфекций различной локализации с бактериемией, вызванных данными микроорганизмами, существуют исследования, результаты которых демонстрируют значительно более высокую выживаемость при терапии имипенемом , чем цефалоспоринами 3–4–й генерации при чувствительности к ним « in vitro » [12–13].
Поэтому проводить деэскалацию при старте с карбапенемов в данных клинических ситуациях нельзя. Более того, оправдан переход на данный класс АБП при отсутствии клинического эффекта и начальной терапии цефалоспоринами. Путь введения антибактериальных препаратов Всасывание лекарственных веществ у септических больных при внутримышечных инъекциях существенно снижается из–за нарушения периферического кровообращения, метаболического ацидоза, ограниченной подвижности, снижении мышечного тонуса. Более того, наблюдается увеличение объема распределения препаратов при гипергидратации и проведении длительной, активной инфузионной терапии. В результате действия перечисленных факторов снижается концентрация антибиотиков в очаге инфекционного воспаления. В этой связи при сепсисе должен использоваться исключительно внутривенный путь введения АБП. Режим дозирования Развитие тяжелого сепсиса, как правило, сочетается с дисфункцией почек (нередко и печени) и требует более скрупулезного отношения к режиму дозирования АБП. В условиях быстро меняющейся ситуации полезен динамический контроль уровня клиренсакреатинина, который и позволит сделать правильный расчет дозировок АБП на конкретный момент времени. Применения максимально возможных доз требует сепсис, вызванный синегнойной палочкой. Бактерицидность ? –лактамных антибиотиков зависит от времени превышения концентрации препарата в крови/тканях над МПК (минимально подавляющие концентрации) в отношении возбудителей сепсиса. С этих позиций показано определенное преимущество при их введении в виде постоянной внутривенной инфузии после первой нагрузочной дозы в виде болюса [18 и др.].
Такой подход оправдан прежде всего при госпитальном сепсисе, связанном с проблемными микроорганизмами, для которых характерен более высокий уровень МПК ( K . pneumonia , Acinetobacter spp ., P. aeruginosa ). Применения максимально возможных доз антибиотиков требует сепсис, вызванный синегнойной палочкой. Длительность антибактериальной терапии В настоящее время, в свете рассмотрения сепсиса в качестве системной воспалительной реакции (СВР) инфекционного генеза и накапливающихся клинических данных, длительность АБТ для многих его клинических форм должна быть пересмотрена в сторону сокращения. Следует признать устаревшими рекомендации по проведению АБТ до полной нормализации температуры тела или числа лейкоцитов в крови или предлагающие минимальный срок – 10–14 дней [19].
Представляется, что длительность АБТ во многих случаях могла бы быть ограничена 7–10 днями . В первую очередь это касается пациентов с хирургическим сепсисом, у которых выполнена радикальная санация очага инфекта. В основе индивидуального принятия решения должны лежать клинико–инструментальные данные, свидетельствующие о регрессе признаков воспаления в первичном очаге, купировании синдрома системного воспаления, отсутствии признаков присоединения суперинфекции. При госпитальной пневмонии важным подспорьем может служить динамическая количественная оценка возбудителя в нижних дыхательных путях. Отсутствие эффекта от оптимально избранной схемы при внебольничном сепсисе прежде всего является основанием для пересмотра хирургической тактики и поиска не санированных очагов инфекта или рассмотрения альтернативных источников поддержания СВР. В случае госпитального сепсиса, в дополнение к отмеченному, особое внимание необходимо уделить повторному анализу микробиологического диагноза в аспекте «колонизация – инфекция» и заключению о характере чувствительности к АБП.


Список литературы
1. Ibrahim E.H.,Sherman G., Ward S. et al. Chest 2000; 118:146–155.
2. Leibovici L.,Shraga I., Drucker M. et al. J Intern Med 1998;244:379–386.
3. Руднов В.А., Ложкин С.Н., Галеев Ф.С. и др. Клиническая микробиология и антимикробная химиотерапия 2003; 5, №2:144–152.
4. Bochud P.Y.,Glauser M.P., Calandra T. Intensive Care Med. 2001; 27(suppl 1): 33–48.
5. Dellinger R.P., Carlet J.M., Masur H. et al. Suviving Sepsis Campaign guidelines for management of sepsis and septic shock. Crit Care Med 2004 32,4:858–873.
6. Сепсис в начале XXI века.Классификация, клинико–диагностическая концепция и лечение. Патолого–анатомическая диагностика: Практическое руководство.–М.:Издательство НЦССХ им. А.Н.Бакулева РАМН, 2004.–130 с.
7. Сидоренко С.В.,Страчунский Л.С., Ахметова Л.И. и др. Антибиотики и химиотер.1999; 44:7–16.
8. Страчунский Л.С.,Решедько Г.К., Эйдельштейн М.В. и др. Клиническая микробиология и антимикробная химиотерапия 2003; 5, №3:259–274.
9. Страчунский Л.С.,Решедько Г.К., Стецюк О.У. и др. Клиническая микробиология и антимикробная химиотерапия 2003; 5, №1: 36–46.
10. Renaud B. et al. Am J Respir Crit Care Med 2001;163:1584–1590
11. Opal S. et al. Crit Care Med 1999;27:1608 –1615
12. Cisneros J. Clin Infect Dis 1996;22:102 – 108
13. Chow J. Ann Intern Med 1991;115:585–591
14. Бейкин Я.Б. Шилова В.П.,Руднов В.А., Розанова С.М. и др. Микробный пейзаж и антибиотикотеризстентность госпитальной флоры реанимационных отделений Екатеринбурга. Инф.письмо. Екатеринбург, 2004.
15. Решедько Г.К. Микробиологические основы клинического применения аминогликозидов в стационарах России. Автореф дисс... докт мед наук. Смоленск. 2004, 43с.
16. Gleason P., Meeehan T., Fine J. Arch Intern Med 1999; 159:2562–2572.
17. Paul M., Benuri – Silbiger I.,Soares–Veiser K.,Leibovici L. BMJ,doi:10.1136/bmj.308028.520995.63(published 2 March 2004)
18. Craig A.W.,Ebert S.C. Antimicrob Agents Chemother 1992;36:2577–2583.
19. Бочоришвили В.Г. Сепсисология с основами инфекционной патологии.– Тбилиси.:Мецниереба, 1988.–806с.
20. Alvarez–Lerma F. et al. Intensive Care Med 2003;29(1S): A250
Похожие работы
... моральные и материальные затраты при производстве инъекций - уменьшение длительности применения антибактериальных препаратов. В 2000 году средний койко-день при осложненном аппендиците составил 22,7 и 2001 году – 19,6. Количество осложнений в 2000 году (90 больных) – 11, в том числе инфильтратов брюшной полости – 7, абсцессов брюшной полости – 2, продолженных перитонитов –2. Количество ...
... повреждениями (жировая эмболия при травме головы и конечностей, стрессовое изъязвление желудочно-кишечного тракта при травме головы и груди, острое повреждение легких при ЧМТ и повреждении органов брюшной полости). В этой связи, основные пути оптимизации интенсивной терапии заключаются в максимально раннем применении методов интенсивной терапии, позволяющих обеспечить адекватную изменившимся ...
... местных гнойных инфекционных осложнений являются флегмона, абсцесс и гнойный затек. Аналогичная ситуация возникает и при других видах инфекционных осложнений, не связанных с хирургическими ранами или травмами. Частным вариантом инфекционных осложнений является катетерассоциированная инфекция. Это специальная форма локальной или генерализованной инфекции, возникающей на фоне нахождения в ...
... также у тех, кому установлены периферические сосудистые катетеры. ИЭ правых клапанов сердца считают более доброкачественным, хирургическое лечение при этом выполняют реже, чем при поражении митрального или аортального клапанов. Тем не менее, риск осложнений повышается особенно существенно, если размер вегетации на трикуспидальном клапане превосходит 20 мм. Известно, что септическая пневмония при ...
0 комментариев