Курсовая работа
Студент гр. ЭУИ-43017к Игнатьев А.В.
Уральский государственный технический университет-УПИ
Екатеринбург 2007
Введение
Свойства титана и области применения его сплавов
Титан имеет атомный номер 22 и расположен в IV переходной группе периодической системы элементов Д.И.Мендлеева. Атомная масса титана – 47,90; атомный объем – 10,7; изотопы – 46, 47, 48, 49, 50.
Титан существует в двух кристаллических модификациях – α и β. Температура полиморфного превращения титана зависит от количества примесей в нем; для чистого металла она равна 882,5°C. Низкотемпературная модификация (α-титан) имеет гексагональную решетку с плотной упаковкой атомов. Высокотемпературная модификация (β-титан) имеет объемно-центрированную кубическую решетку.
Плотность чистого α-титана при 25°C равна 4,507г/см3, β-титана при 900°C – 4,32г/см3, жидкого (технического) при температуре кристаллизации – 4,11г/см3.
Энтропия титана при 25°C равна 7,3ккал/(моль·град), скрытая теплота α→β-томная масса титана мер 22 и расположен в IV переходной группе периодической системы элементов Д.И.Мендлеева. ________________превращения – 0,83ккал/моль, точка плавления 1660°C±4, точка кипения – 3260°C.
Химический состав и механические свойства титановой губки в значительной степени определяются тем способом, которым она получена, а также технологией очистки реакционной массы.
Титан отличается малым сопротивлением ползучести, несмотря на высокую температуру рекристаллизации и плавления. Сплавы на основе титана обладают большей устойчивостью против ползучести, которая еще может быть повышена термической обработкой.
Титан обладает высокой прочностью, твердостью и хорошей пластичностью при малой плотности. По удельной плотности титан превосходит многие конструкционные материалы. Малый коэффициент линейного расширения титана обеспечивает его надежную работу в условиях теплосмен. Отличное сопротивление коррозии позволяет использовать титан для работы во многих агрессивных средах.
Титан можно подвергать всем видам механической обработки, а также сварке различных видов. Поверхность изделий из титана можно упрочнять различными способами и создавать на ней окисную пленку электролитическим путем.
Наряду с преимуществами титан имеет ряд недостатков. Один из них – низкий модуль нормальной упругости, затрудняющий создание жестких и устойчивых конструкций. Но с другой стороны это свойство можно рассматривать и как преимущество, позволяющее снизить величину напряжений, возникающий при знакопеременных нагрузках, а также величину термических напряжений, возникающих при нагреве конструкции. Низкая теплопроводность титана отрицательно сказывается на его эксплуатационных свойствах, ухудшая стойкость при работе в условиях теплосмен. В настоящее время преимущественно применяется не технический титан, а сплавы на его основе.
Титан и сплавы титана активно применяется в авиации и ракетно-космической отрасли. В самолетостроении титан применяют преимуществен для изготовления деталей двигателей, для обшивки корпусов сверхзвуковых самолетов, а также для изготовления некоторых конструкций планеров (особенно в современном гражданском авиастроении).
Другой отраслью, в которой сплавы титана находят активное применение, является химическая промышленность. Такие свойства титана как высокая коррозионная стойкость, низкая смачиваемость жидкостями, а также образование на поверхности защитной окисной пленки, выделяют сплавы титана среди прочих конструкционных материалов для производства элементов химической аппаратуры (холодильники, змеевики, роторы высокоскоростных центрифуг, лопасти и корпуса центробежных насосов для перекачивания растворов хлоридов, слабых растворов соляной кислоты, различных органических кислот).
Широкое применение получила аппаратура из титана в ряде гидрометаллургических производств. Катоды из сплава титана с палладием применяет в промышленном масштабе при производстве марганца.
Из областей, где применение титана не связано с большими масштабами, но дает существенных эффект, следует назвать медицину – изготовление медицинского инструмента, а также внутренних протезов.
Восстановление четыреххлористого титана
С теоретической и практической точек зрения наибольший интерес представляют восстановление четыреххлористого титана магнием или натрием, а также восстановление окислов титана кальцием (гидрохлоридом кальция) и алюминием.
В настоящее время промышленной производство титана основано на восстановлении четыреххлористого титана магнием (магниетермический способ) или натрием (натриетермический способ).
В первом случае для разделения продуктов восстановления титановой губки, магния и хлористого магния – применят в основном способ отгонки магния и хлористого магния от титановой губки при температуре около 1000°C и остаточном давлении в реакторе от нескольких миллиметров ртутного столба в начале процесса до нескольких микронов в конце (так называемый способ вакуумной сепарации).
Во втором случае для разделения продуктов восстановления – титановой губки, хлористого натрия и незначительного количества непрореагировавшего натрия – применяют способ выщелачивания полученного после восстановления реакционной массы слабым раствором соляной кислоты (так называемый гидрометаллургический способ).
Магниетермический способ
Магний – один из наиболее распространенных в природе элементов. Содержание его в земной коре составляет 2,35%. Благодаря крупным месторождениям магниевого сырья, высокопроизводительной технологии получения металла электролизом и сравнительно небольшой стоимости металла, производство магния осуществляется в крупных промышленных масштабах.
Магний отличается высоким сродством к хлору (![]() = 55 ккал/г-атом хлора), которое при 800°C на 12,0 ккал/г-атом хлора (
= 55 ккал/г-атом хлора), которое при 800°C на 12,0 ккал/г-атом хлора (![]() = 43 ккал/г-атом хлора), что вполне достаточно для полного восстановления
= 43 ккал/г-атом хлора), что вполне достаточно для полного восстановления ![]() магнием. Соотношение температур плавления и кипения магния и образующегося в результате восстановления
магнием. Соотношение температур плавления и кипения магния и образующегося в результате восстановления ![]() благоприятно для проведения процесса в интервале температур 720-900°C. Магний и титан практически взаимно не растворимы.
благоприятно для проведения процесса в интервале температур 720-900°C. Магний и титан практически взаимно не растворимы.
Все это, а также технологические особенности процесса восстановления титана делают магний одним из наиболее благоприятных восстановителей для организации крупного производства титановой губки магниетермическим способом.
Патент на получение титановой губки магниетермическим способом был выдан в 1940г в США американскому исследователю Кроллю, проводившему опыты на крупнолабораторной установке.
Титановая губка, получаемая магниетермическим способом, в промышленных условиях содержит обычно 0,03–0,15% O2; 0,01–0,04% N2; 0,02–0,15% Fe2; 0,002–0,005% H2; 0,02–0,12% Cl; 0,01–0,05% Si; 0,01–0,03% C; около 0,01% Al; 0,01% Ni; 0,01% V и другие примеси.
Вместе с TiCl4 в губку вносится около 40% всего азота, более 20% кислорода, около 15% железа и значительная часть углерода. Вместе с магнием в губку вносится около 20% N2, 40% O2, 15% Fe. Около 50–70% железа, содержащегося в титановой губки попадает в нее в результате взаимодействия титана с материалом реактора. Установлено, что большая часть примесей из материала реактора переходит в титан в период вакуумной сепарации, особенно в последний период, когда температура на границе стенок реактора достигает максимальных значений.
Физико-химические основы восстановления
Магниетермическое производство металлического титана основано на использовании реакции:
|
| + |
| = |
| + |
|
| (ж.пар) | (ж.пар) | (тв) | (ж.пар) |
В стандартных условиях эта реакция характеризуется высокими по абсолютной величине и отрицательными по знаку значениями энтальпии и энергии Гиббса:
![]()
![]()
Температурная зависимость константы равновесия не может являться монотонной функцией, поскольку участвующие в реакции исходные и конечные вещества претерпевают фазовые превращения.
По аналогии со сложными реакциями, которые протекают через промежуточные соединения, восстановление титана можно представить как ступенчатое восстановление четыреххлористого титана из его низших хлоридов:
![]()
Протекающие при этом реакции условно можно разбить на две группы:
Реакции восстановления четыреххлористого титана до низших хлоридов и металла:
|
| (1) |
|
| (2) |
|
| (3) |
|
| (4) |
|
| (5) |
|
| (6) |
|
| (7) |
Вторичные реакции взаимодействия четыреххлористого титана с продуктами реакции группы 1. и реакции диспропорционирования низших хлоридов титана:
|
| (8) |
|
| (9) |
|
| (10) |
|
| (11) |
Реакция обычно осуществляется в атмосфере инертного газа. Равновесие процесса магниетермического восстановления четыреххлористого титана устанавливается при исчезающее малой концентрации тетрахлорида.
В начале процесса реакция восстановления протекает на зеркале жидкого магния, которое постепенно покрывается пленкой образующегося хлористого магния, хорошо смачивающего магний. Пленка затрудняет контакт магния с ![]() и препятствует дальнейшему протеканию реакции на зеркале магния. Фронт реакции к этому времени смещается к стенкам реактора, где условия взаимодействия
и препятствует дальнейшему протеканию реакции на зеркале магния. Фронт реакции к этому времени смещается к стенкам реактора, где условия взаимодействия ![]() с магнием наиболее благоприятны вследствие стекания соли с поверхности магния, поднимающегося за счет сил поверхностного натяжения ли капиллярных сил по стенкам реактора или по капиллярам образовавшейся на стенках губки. В дальнейшем, реакции идут в основном на стенках реактора или боковой поверхности губки с ростом ее от боков к центру реактора. Реакция в газовой фазе не идет.
с магнием наиболее благоприятны вследствие стекания соли с поверхности магния, поднимающегося за счет сил поверхностного натяжения ли капиллярных сил по стенкам реактора или по капиллярам образовавшейся на стенках губки. В дальнейшем, реакции идут в основном на стенках реактора или боковой поверхности губки с ростом ее от боков к центру реактора. Реакция в газовой фазе не идет.
Конструкции реакторов и печей восстановления
Восстановление четыреххлористого титана магнием сопровождается выделением большого количества тепла. Энтальпия суммарной реакции в стандартных условиях составляет 123,6 ккал/г-атом титана. В современных реакторах тепловыделение составляет около 100-200тыс.ккал/ч. Значительная часть этого тепла должны быть отведена от реактора.
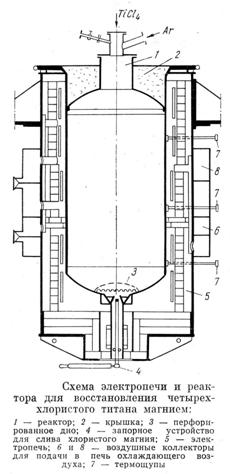
Объемные соотношения титана, магния и хлористого магния в реакторе таковы, что на каждую единицу объема, занимаемого титаном, приходится 2,8 единиц объема магния и 10,4 единицы объема образующегося хлорида магния. Поэтому для более полного использования рабочего объема реактора, хлористый магний в процессе восстановления периодически сливают из реактора.
В качестве реакторов восстановления в промышленных условиях используют цилиндрические реакторы диаметром от 850-1000 до 1300-1500мм и высотой от 1800-2000 до 3000мм. Диаметр реактора восстановления в основном лимитируется требованиями последующего процесса – вакуумной сепарации блока реакционной массы, где повышение диаметра реактора больше определенного значения приводит к ухудшению условий прогрева реакционной масса и отгонки остатков магния и хлористого магния из глубинных слоев титановой губки.
Реакция восстановения ![]() магнием проводится в реакторах из малоуглеродистой стали, из хромоникелевой, хромистой сталей, а также в реакторах из биметалла (наружный слой – хромоникелевая сталь, а внутренний – малоуглеродистая сталь).
магнием проводится в реакторах из малоуглеродистой стали, из хромоникелевой, хромистой сталей, а также в реакторах из биметалла (наружный слой – хромоникелевая сталь, а внутренний – малоуглеродистая сталь).
На практике, учитывая очаговый характер реакций восстановления, в результате которого максимальная температура внезапно резко возрастет то в одной, то в другой зонах реактора, процесс обычно проводят при температуре 750–900°C.
Хромоникелевая сталь более окалиностойка и более устойчива при взаимодействии с парами ![]() в условиях высоких температур, чем малоуглеродистая сталь. Однако температура плавления эвтектики этой стали с титаном ниже, чем с малоуглеродистой сталью, на 900–100°C. Кроме того, находящийся в реакторе жидкий магний хорошо растворяет никель, входящий в состав хромоникелевой стали, загрязняется им и загрязняет титановую губку. Тем не менее, эти стали широко применяются для изготовления реакторов.
в условиях высоких температур, чем малоуглеродистая сталь. Однако температура плавления эвтектики этой стали с титаном ниже, чем с малоуглеродистой сталью, на 900–100°C. Кроме того, находящийся в реакторе жидкий магний хорошо растворяет никель, входящий в состав хромоникелевой стали, загрязняется им и загрязняет титановую губку. Тем не менее, эти стали широко применяются для изготовления реакторов.
Хромистые стали типа 0Х13, Х25Т, обладая средней между малоуглеродистой и хромоникелевой сталью температурой плавления эвтектики с титаном и досочной окалиностойкостью, являются также более устойчивыми против взаимодействия с парами ![]() при высокой температуре, и меньше чем хромоникелевые стали растворяются в расплавленном магнии, поэтому их использование в качестве материала благоприятно.
при высокой температуре, и меньше чем хромоникелевые стали растворяются в расплавленном магнии, поэтому их использование в качестве материала благоприятно.
Большой интерес для изготовления реакторов представляют биметаллы. Использование таких сталей с внутренней поверхностью из малоуглеродистой стали, стали Х25Т или титана несмотря для большую трудность в изготовлении реакторов и несколько большую их стоимость позволяет заметно повысить производительность аппарата и улучшить качество получаемого титана,.
В промышленных условиях используют обычно два типа реакторов – реактор со вставленным внутрь реакционным стаканом, изготовленным из рассмотренных выше материалов, и реактор без реакционного стакана. Реакционный стакан позволяет предохранить корпус реактора от проплавления, применить реактор из нержавеющей стали, а стакан из малоуглеродистой стали. Кроме того он облегчает извлечение реакционной массы из реактора после окончания процесса восстановления. С другой стороны, при использовании стакана образуется зазор между его стенкой и стенкой реактора, который резко ухудшает условия отвода тепла из зоны реакции, сокращает полезный объем реактора, что снижает его производительность. Кроме того, осложняется устройство для слива хлористого магния, в зазоре между стенками могут образовываться низшие хлориды титана. Внутреннюю поверхность такого реактора после каждого процесса необходимо тщательно очищать от хлоридов титана и магния, промывая раствором соляной кислоты. Эта операция трудоемка, вредна для обслуживающего персонала и приводит к повышенному износу реактора.
Недостаток реактора без стакана состоит в большей опасности проплавления корпуса, а также в необходимости более маневренного охлаждения его стенок в процессе восстановления во избежании намораживания на них гарнисажа, что может затруднить транспортировку магния в зону реакции.
Вакуумирование реактора, подача в него четыреххлористого титана и аргона осуществляют через центральную трубу, расположенную на крышке реактора. Хлористый магний сливают из реактора с помощью сифона, выходящего на рабочую площадку через крышку или боковую стенку реактора непосредственно под его фланцем.
Для отведения тепла, образующегося в ходе реакции необходима эффективная система его отвода от реактора. Поддержание области преимущественного протекания реакций в определенной зоне реактора может облегчить решение этой задачи. Расположение этой зоны по высоте реактора можно регулировать, поддерживая уровень расплава в указанной зоне и регулируя слив накапливающегося хлористого магния. Тепло от реактора отводят, как правило, охлаждая зону преимущественного протекания реакции с помощью воздуха, подаваемого в печь от вентиляционной установки. Охлаждающий воздух подают в нескольких точках по окружности печи, форсунки располагают в 2–3 ряда. Вентиляторы включают и подают охлаждающий воздух периодически с помощью автоматической схемы, подающей сигнал о повышении температура в той или иной зоне реактора.
Для нормально протекания процесса при охлаждении зоны реакции обычно необходимо подогревать нижнюю часть реактора. Подогрев необходим для поддержания хлористого магния в жидком состоянии, что обеспечивает расслоение магния и бесперебойную подачу магния в зону реакции, а также облегчает регулярный слив хлористого магния из реактора.
Переохлаждение реактора ниже зоны протекания реакции приводит к замедлению поступления магния в эту зону и к расстройству процесса восстановления, который при этом резко замедляется и идет с образованием большого количества низших хлоридов титана.
Для предотвращения загрязнения титановой губки газами и влагой, адсорбированными на внутренних стенках аппарата, а также кислородом из окисных пленок и гидролизовавшегося хлористого магния, реакционный стакан и реактор перед проведением в них процесса восстановления тщательно очищают.
Технология восстановления
Магний загружают в реактор в твердом состоянии, в виде чушек и крупных слитков (поверхность предварительно очищают от оксидных пленок и шлаковых включений путем травления в растворе соляной кислоты), или в расплавленном состоянии (температура до 800°C).
Реактор с загруженным в него магнием перед установкой в печь вакуумируют и проверяют на герметичность. Затем реактор заполняется осушенным инертным газом (обычно аргоном) и устанавливают в печь восстановления, где реактор разогревается до температуры полного расплавления и некоторого перегрева магния (650–760°C).
После того как весь магний расплавился (740–780°C) начинают подачу в реактор четыреххлористого титана, через центральный патрубок, расположенный в крышке реактора. С наибольшей скоростью четыреххлористый титан подают в аппарат в начальной и средней стадиях процесса, когда в зоне реакции имеется достаточное количество магния. К концу процесса транспорт магния в зону реакции затрудняется, что сопровождается ростом давления в аппарате за счет паров не успевающего прореагировать четыреххлористого титана. Реакция восстановления начинает приобретать очаговый характер, что может привести к местному перегреву и проплавлению стенок реактора. Поэтому скорость подачи ![]() в аппарат в конце процесса постепенно снижается. Окончание процесса восстановления определяется по росту давления в аппарате или расчетным путем по заданному коэффициенту использования магния.
в аппарат в конце процесса постепенно снижается. Окончание процесса восстановления определяется по росту давления в аппарате или расчетным путем по заданному коэффициенту использования магния.
После прекращения подачи ![]() аппарат выдерживают в печи в течении 1ч при 1123°K, затем, как можно более полно, сливают хлористый магний. В печи аппарат охлаждают до 873–923°K, после чего его извлекают и устанавливают в холодильник, где его поверхность орошают вводом или обдувают воздухом для охлаждения до температуры 20-40°C.
аппарат выдерживают в печи в течении 1ч при 1123°K, затем, как можно более полно, сливают хлористый магний. В печи аппарат охлаждают до 873–923°K, после чего его извлекают и устанавливают в холодильник, где его поверхность орошают вводом или обдувают воздухом для охлаждения до температуры 20-40°C.
Охлажденная реакционная масса представляет собой 50-70% губчатого титана, поры которого заполнены магнием и хлористым магнием, 30-35% магния и 15-20% хлористого магния. Среднее содержание в реакционной массе основных компонентов составляет (по массе): Ti–60%, Mg–20-30%, MgC2–10-20%. Содержание металлического магния максимально в нижней части блока, поскольку эта часть магния оказывается как бы заблокированной от взаимодействия с ![]() . Содержание хлористого магния максимально в верхней части блока. Предельно допустимое содержание хлора и магния в очищенной товарной губке не должно быть выше 0,08–0,12% и 0,1–0,5% соответственно.
. Содержание хлористого магния максимально в верхней части блока. Предельно допустимое содержание хлора и магния в очищенной товарной губке не должно быть выше 0,08–0,12% и 0,1–0,5% соответственно.
Присутствие магния и хлористого магния в губчатом титане определяет особенности его поведения на воздухе. Хлористый магний, свободно сообщающийся с атмосферным воздухом, может увлажняться. В свою очередь металлический магний взаимодействует с выделением водорода. Поэтому во избежание ухудшения качества титана контакт реакционной массы с воздухом должен быть исключен или сведен до минимума.
Разделять реакционную массу можно одним из двух принципиальных способов: отгонкой хлористого магния в вакууме при высоких температурах или выщелачиванием реакционной массы в 0,5–1,0%-ном растворе соляной кислоты.
Вакуумная сепарация реакционной массы
Отгонка хлористого магния и магния из реакционной массы при вакуумной сепарации основана на большой разности упругости паров компонентов реакционной массы при высокой температуре. Магний может быть отогнан из реакционной массы при температуре выше температуры кипений магния (1103°C), а хлористый магний – при температуре выше температуре кипения хлористого магния (1418°C). Однако при этих температурах титановая губка интенсивно взаимодействует с материалами, из которых изготовлен реактор, в результате чего качество губки резко ухудшается.
С целью снижения температуры и более полного удаления хлористого магния и магния из реакционной массы процесс проводится при высоком выкууме.
При остаточном давлении около 50 мкм.рт.ст. температура кипения хлористого магния в свободном состоянии составляет около 700°C, а магния – 400°C. Однако в реакционной массе магний и хлористый магний находятся в порах титановой губки, в том числе и в мельчайших порах, расположенных в глубинных слоях губки. Поэтому для ускорения процесса и большей полноты отгонки вакуумную сепарацию обычно проводят при температуре 950–1000°C.
Реакционная масса может подвергаться вакуумной сепарации в виде монолитного блока или в виде стружки. В промышленной практике преимущественно используют процесс сепарации монолитной реакционной массы. При этом легче избежать заметного увлажнения реакционной массы, но несколько труднее отогнать хлористый магний из глубинных слоев блока, затрудняется также удаление отсепарированной губки из реактора.
Реактор с реакционной массой тщательно уплотняют и проверяют на герметичность и откачивают до остаточного давления ниже 0,2мм.рт.ст., после чего включают электрообогрев.
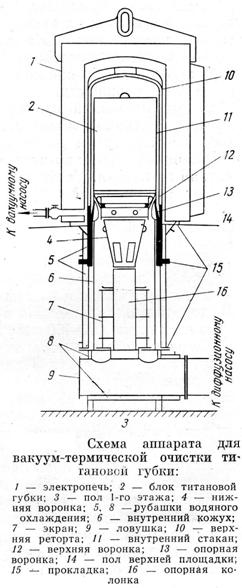
При повышении температуры до 300-350°C из реакционной массы удаляется основное количество влаги, которая содержится в увлажненном хлористом магнии или адсорбируется на внутренних стенках реактора. До этой температуры выделяющаяся влага не окисляет титановой губки, которая покрыта слоем хлористого магния и магния. При температуре выше 480°C вся выделяющаяся влага взаимодействует с титановой губкой, загрязняя ее кислородом и водородом.
При повышении температуры в реакторы выше 600–700°C и остаточном давлении ниже 1мм.рт.ст. начинается бурная возгонка магния и хлористого магния, в результате чего вакуум в аппарате падает, а температура в кондесаторе резко растет. В это время приходится периодически отключать электрообогрев печи, чтобы избежать перегрева кондесатора и забивания вакуумной системы возгонами. Уже через 8–12 часов после начала бурной возгонки основное количество магния и хлористого магния отгоняется от титановой губки. После этого остаточное давление в аппарате начинает быстро падать. С этого момента начинается высокотемпературная выдержка (до 1000°C), в течении которой при постепенном снижении остаточного давления в реакторе до 10–20мкм из губки удаляются остатки хлористого магния.
После определения конца вакуумной сепарации электрообогрев печи отключают, реактор заполняют аргоном и одновременно снижают контрвакуум в печи. После охлаждения аппарата с содержащейся в нем губкой до температуры окружающей среды воздуха его демонтируют. Реактор направляют в отделение переработки губки, а конденсатор – в отделение переплавки кондесата. Выплавленный из конденсата магний возвращают в процесс восстановления, а хлористый магний направляют на электролиз для получения из него хлора и магния, которые возвращаются в процесс.
С точки зрения повышения производительности аппаратов восстановления и вакуумной сепарации представляет интерес совмещение этих двух процессов в одном аппарате. Один из вариантов такого аппарата представляет собой реактор восстановления, над которым располагается конденсатор.
Извлечение титановой губки
Образующаяся в реакторе титановая губка прочно приваривается к его стенкам. Наиболее прочно к стенкам приваривается гарнисажная часть губки. Отделить титановую губка от стенок реактора из нержавеющей стали легче чем от стенок реактора из обычной стали, так как между губкой и материалом реактора образуется прослойка из промежуточного сплава титана с нержавеющей сталью, которая легче отделяется от стенок реактора.
Обычно после окончания процесса вакуумной сепарации и охлаждения блок титановой губки извлекают из него, отделяя гарнисажную губку с помощью пневмомолотков. Затем подрезают центральную кричную часть металла, после чего блок губки извлекают из реактора.
Операция извлечения губки из реактора таким способом – очень тяжелая и трудоемкая. Механические же способы вырезания титановой губки из реактора до настоящего времени не нашли широкого применения вследствии интенсивного окисления титановой губки в процессе резания.
Извлеченный из реактора и очищенный блок титановой губки поступает на разделку (нижняя часть, гарнисаж и поверхностные пленки, которые содержать повышенное количество примесей обрабатываются отдельно).
Основной блок губки – крицу подвергают крупному дроблению. В дальнейшем губку измельчают обычно в системе щековых дробилок, после чего ее рассеивают на фракции.
Полученную титановую губку загружают в герметичную тару, в которой она хранится и транспортируется потребителям. После загрузки губки тару иногда вакуумируют, после чего в нее задают осушенный инертный газ. Эти предосторожности иногда необходимы при длительном хранении для предотвращения увлажнения остатков хлористого магния, содержащихся в титановой губке.
Металлургические расчеты
Заданные условия
В качестве заданных условий примем следующие составы компонентов. Для выполнения металлургических расчетов будем использовать параметры тетрахлорида титана, выпускаемого Sumitomo Titanium Corporation:
|
|
|
|
|
| |
| 99,9% min | 0,001% max | 0,0001% max | 0,001% max | 0,0015% |
Магний будем подавать в виде металлических чушек марки мг98 (ГОСТ 804-93):
| Марка | Mg, не менее, % | Массовая доля примесей, не более, % | |||||||||
| Fe | Si | Ni | Cu | Al | Mn | Zn | Pb | Sn | Любого другого элемента | ||
| Мг98 | 99,98 | 0,002 | 0,003 | 0,0005 | 0,0005 | 0,004 | 0,002 | 0,005 | 0,005 | 0,005 | 0,002 |
Материальный баланс
Для производства 1т титановой губки потребуется пропорционально реакции (исходя из стехиометрии реакции и молекулярных масс вещества):
|
| + |
|
|
| + |
|
| 190 | 49 | 48 | 190 |
Четыреххлористого титана: ![]() ;
;
Магния: ![]() ;
;
Принимая во внимание, что почти все примеси из ![]() переходят в губку получаем:
переходят в губку получаем:
Si: ![]() ;
;
Fe: ![]() ;
;
V: ![]() ;
;
Т.к. суммарная масса примесей, попадающих в 1т титановой губки из четыреххлористого титана составит менее 80г на тонну, будем при расчете ими пренебрегать.
Составляем материальный баланс:
| Материальный баланс | |||||
| Задано | Получено | ||||
| Четыреххлористый титан | 3958кг | 79.5% | Титан | 1000кг | 20.08% |
| Магний | 1021кг | 20.5% |
| 3958кг | 79.50% |
| Невязка | 21кг | 0.42% | |||
| Итого: | 4979кг | 100% | Итого: | 4979кг | 100% |
Тепловой баланс реакции восстановления TiCl4
Для расчета количества энергии, введенной при нагреве исходных компонентов до температуры проведения процесса (1100К) и остывания продуктов реакции до температуры 298,15К воспользуемся «Shomate Equation» [5]:
![]()
Параметры A,B,C,D,E,F,H берем из справочника [5].
Для расчета теплового эффекта реакции воспользуемся справочными значениями энтальпии образования исходных компонентов и продуктов реакции.
| Термодинамические параметры веществ | ||||
| Параметр | TiCl4 | Mg | Ti | MgCl2 |
| A | 106,8573 | 34,30901 | 44,37174 | 92,048 |
| B | 1,049482 | -7,47103E-10 | -44,09225 | -0,000005 |
| C | -0,2843 | 6,14621E-10 | 31,70602 | 4,77E-07 |
| D | 0,024257 | -1,59824E-10 | 0,052209 | 1,14E-07 |
| E | -1,043516 | -1,15201E-11 | 0,036168 | -0,000005 |
| F | -798,5666 | -5,439367 | -12,72011 | -634,343 |
| H | -763,1616 | 4,790011 | 0 | -601,577 |
| H1100-H298.15, кДж/моль | 83,60436175 | 27,510533 | 23,46612676 | 68,48680177 |
| Энтальпия образования ΔH, кДж/моль | -804,2 | 0 | 0 | -641,3 |
Рассчитываем выделение тепла от экзотермии реакции используя энтальпии образования принимающих участие в реакции веществ:
Аналогично, используя параметр H1100-H298.15, вычисляем разницу теплоты получаемых и исходных компонентов (теплота нагрева до 1100К и остывания до 298.15К):
![]()
Таким образом, количество тепла, подлежащее отведению составит: ![]()
Пересчитывая граммы в моли, получаем суммарный тепловой эффект реакции при получении 1кг металлического титана и заполняем таблицу:
| Параметр | TiCl4 | 2Mg | Ti | 2MgCl2 | Сумма |
| масса, г | 3958 | 1021 | 1000 | 3958 | |
| молярная масса, г/моль | 190 | 49 | 48 | 190 | |
| кол-во, моль | 20,83157895 | 20,83673469 | 20,83333333 | 20,83157895 | |
| энтальпия образования, кДж | -16752,75579 | 0 | 0 | -13359,29158 | 3393,464211 |
| H1100-H298.15, кДж | 1741,610862 | 573,2296774 | 488,8776407 | 1426,688218 | -399,2746809 |
| Итого | 3792,738891 |
Составляем тепловой баланс:
| Тепловой баланс получения 1т титана | |||||
| Приход тепла | Отвод тепла | ||||
| Статья | мДж | % | Статья | мДж | % |
| От электроэнергии на расплавление Mg | 573,2296774 | 14,5 | С Титаном | 488,8776407 | 12,3 |
| От экзотермии реакции | 3393,464211 | 85,5 | С MgCl2 | 1426,688218 | 36,0 |
| Теплоотвод | 2051,128029 | 51,7 | |||
| Невязка | 0 | ||||
| Итого: | 3966,693888 | 100,0 | Итого: | 3966,693888 | 100,0 |
Расчет кол-ва аппаратов
Рассчитаем кол-во реакторов для производства 5 000 тонн титановой губки в год. Используем реакторы высотой 3050мм и внутренним диаметром 1360мм.
Цикловая производительность таких реакторов составляет 2000кг титановой губки (одна условная единица). Продолжительность полного цикла – 39 часов [1]. Кол-во товарного металла, получаемого с одного реактора в год составит (365дн * 24ч / 39ч) * 0,9 * 2000кг = 405 тонн.
Таким образом, для получения 5 000 тонн в год необходимо использовать 5 000 / 405 = 13 реакторов.
Т.к. длительность цикла процесса вакуумной сепарации составляет 30 часов, он не является «узким звеном» участка, следовательно, расчет производительность по реакторам восстановления четыреххлористого титана является корректным.
За один цикл аппарат вакуум-термической очистки титановой губки также перерабатывает 2000кг. Учитывая, что его производительность (30 часов) лишь несколько меньше производительности реактора (39 часов), в цеху необходимо использовать 13 таких аппаратов (по одному аппарату-дистиллятору на каждый реактор восстановления).
Заключение
В ходе выполнения курсовой работы приведена аппаратно-технологическая схема процесса восстановления четыреххлористого титана магнием. Приведены схемы и описания действия аппаратов для осуществления реакции. Рассчитан материальный и тепловой балансы процесса, а также такие параметры, для кол-во агрегатов, необходимых для выпуска 5 000 тонн титановой губки в год.
Список литературыМеталлургия титана. Гармата В.А., Гуляницкий Б.С., Крамник В.Ю., Липкес Я.М., Серяков Г.В., Сучков А.Б., Хомяков П.П., Москва, изд. «Металлургия», 1967. 643с
Титан. Гармата В.А., Петрунько А.Н., Галицкий Н.В., Олесов Ю.Г., Сандлер Р.А., Москва, изд. «Металлургия», 1983. 532с.
Магниетермия. Самсонов Г.В., Перминов В.П., Москва, изд. «Металлургия», 1971., 168с
Верятин У.Д., Маширев В.П. и др. «Термодинамические свойства неорганических веществ». Справочник изд.под.ред. Зефирова А.П., Москва, Атомиздат, М., 1965., с.376
«NIST Standard Reference Database Number 69. NIST Chemistry WebBook», National Institute of Standards and Technology, 2005, http://webbook.nist.gov/chemis
0 комментариев