После открытия кислорода, французскому химику Лавуазье удалось выяснить, что горение есть реакция соединения с кислородом. В соответствии латинским наименованием кислорода "oxigenium" реакции соединения с кислородом были названы окислением.
2Mg0 +O20=2Mg+2O-2
Обратный процесс полного или частичного отнятия кислорода от веществ называется восстановлением. При восстановлении оксида элемент, соединённый с кислородом, меняет своё состояние - образует простое вещество, т.е. восстанавливается.
Fe2+3O3-2+2Al0=Al2+3O3-2+2Fe0
Вы заметили, что в этих реакциях изменились степени окисления химических элементов. Химические реакции, в результате которых происходит изменение степеней окисления атомов химических элементов или ионов, образующих реагирующие вешества, называют окислительно-восстановительными реакциями.
В соответствиии с теорией электронного строения атома окисление и восстановление легко объясняется как процесс отдачи или присоединения электронов. В окислительно-восстановительных реакциях электроны не уходят из сферы реакции, а переносятся от одного элемента к другому.
Рассмотрим реакцию взаимодействия магния с кислородом.
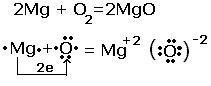
Из схемы видно, что атом магния отдал 2 электрона атому кислорода, за счёт такого перехода химические элементы изменили степени окисления. Протекают два процесса. Процесс отдачи электронов и процесс их присоединения , которые называются соответственно окислением и восстановлением.
Вещества, участвующие в окислительно-восстановительных реакциях, и у которых изменились степени окисления, являются либо окислителямия,либо восстановителями.
Окислитель - это атомы, ионы или молекулы, которые принимают электроны.
Восстановитель - это атомы, ионы или молекулы, которые отдают электроны.
Из уравнения реакции видно, что магний является восстановителем, а кислород - окислителем.
| Запомните! Восстановитель в химической реакции всегда окисляется, окислитель - восстанавливается. |
Важнейшие восстановители и окислители.
| Восстановители | Окислители |
| Металлы, водород, уголь | Фтор, хлор, бром, иод |
| Оксид углерода (II) CO | Перманганат калия KMnO4, манганат калия K2MnO4, оксид марганца (IV)MnO2 |
| Сероводород H2Sоксид серы (IV)SO2 | Бихромат калия K2Cr2O7, хромат калия K2CrO4 |
| HI, HBr, HCl | Азотная кислота HNO3 |
| Хлорид олова (II) SnCl2 | Кислород O2, озон O3, перекись водорода H2O2 |
| Азотистая кислота HNO2 | Серная кислота (конц.) H2SO4 |
| Фосфористая кислота H3PO3 | Оксид меди (II) CuO, оксид серебра Ag2O |
| Хлорид железа (III) FeCl3 | |
| Царская водка (смесь концентрированных соляной и азотной кислот) |
Похожие работы
... Для составления уравнений окислительно-восстановительных реакций обычно используют два метода: 1) метод электронного баланса, 2) электронно-ионный метод. При расчете коэффициентов в окислительно-восстановительных реакциях пользуются правилом электронного баланса: суммарное число электронов, теряемых восстановителем, должно быть равно суммарному числу электронов, приобретаемых окислителем. ...
... , а в нейтральных и щелочных растворах ионы О реагируют с образованием гидроксид-ионов НОН + О = 2ОН . Применяются в основном два метода составления уравнений окислительно-восстановительных реакций: 1) электронного баланса – основан на определении общего количества электронов, перемещающихся от восстановителя к окислителю; 2) ионно-электронный – предусматривает раздельное ...
... HСlO3 Хлораты Хлористая НClO2 Хлориты Хлорноватистая HClO Гипохлориты Хромовая H2CrO4 Хроматы Циановодородная (синильная кислота) слота) HCN Цианиды Основные типы химических реакций Среди разнообразных химических реакций можно выделить два типа, существенно отличающихся друг от друга. К первому типу реакций относятся те, в ходе которых степень окисления ...
... это целый класс реакций окисления органических веществ с участием катализатора, обладающего окислительно-восстановительными свойствами. Этот процесс протекает циклично т. е. состоит из многократных повторений. Колебательные химические реакции были открыты и научно обоснованы в 1951 г. советским учёным Борисом Петровичем Белоусовым. Б.П. Белоусов изучал окисление лимонной кислоты при её реакции с ...
0 комментариев