Можно ли, съев ГМ-продукты, приобрести устойчивость к антибиотикам?
А.Л. Конов, специалист по генетической инженерии растений
Среди проблем, обсуждаемых в связи с возделыванием ГМ-культур, одна из главных — возможность передачи генов от ГМ-растений к другим обитателям биоценоза и микроорганизмам ризосферы, а также от ГМ-продуктов к бактериям желудочно-кишечного тракта человека и животных. О чем же идет речь?
Во-первых, это перенос генов (в основном устойчивости к гербицидам) от ГМ-растений к обычным (прежде всего сорнякам) за счет опыления на полях и делянках. Такой традиционный способ (опыление с образованием потомства) определяют термином «вертикальный перенос». Это — тема отдельного обсуждения, скажем только, что риск перекрестного опыления и, соответственно, обмена генами между разными видами растений различен для разных сельскохозяйственных культур и регионов и в принципе устраним правильными агротехническими приемами и превентивными защитными мерами.
Здесь же речь пойдет о другой проблеме — «горизонтальном» переносе генов (ГПГ) от ГМ-растений к бактериям, а от них — к другим растениям, животным и человеку за счет естественной трансформации, т. е. передачи ДНК от одного организма к другому. Многие ГМ-растения содержат не только «целевые» гены (скажем, устойчивости к патогенам или гербицидам), но и гены устойчивости к селективным агентам, например антибиотикам (подробнее об этом см. «ЭиЖ», 2001, №2, с. 66). Могут ли они из ГМ-растений попасть в микрофлору почв или от ГМ-пищи — к бактериям желудочно-кишечного тракта животных и человека? Каков риск этого? Следует ли его опасаться или важнее обратить внимание на другие риски, связанные не с генной инженерией, а, например, с обычными бактериями или агротехническими мероприятиями?
Перенос переносу рознь. Что же такое ГПГ? Напомним, что вся информация об организме — от бактерии до человека — хранится (точнее, кодируется) в его ДНК. Знаменитая двойная спираль молекулы ДНК состоит всего из 4 оснований: А (аденин), Т (тимин), Г (гуанин) и Ц (цитозин). Две нити ДНК связаны углеводородными «мостиками», соединяющими между собой (по принципу «ключ — замок») соответствующие друг другу по химическому строению «концы» оснований (А — Т и Г — Ц). Допустим, нить ДНК представлена последовательностью: ТТТАТТГТТГЦТ. Разобьем ее на «слова» из трех «букв»: ТТТ АТТ ГТТ ГЦТ — это и есть генетический код, в котором каждое «слово» (триплет, или кодон) кодирует определенную аминокислоту. Так, выбранная последовательность кодирует короткий пептид (небольшой белок) из четырех аминокислот: фенилаланина, изолейцина, валина и аланина. Когда говорят об «экспрессии» генов (реализации в клетке закодированной в ДНК информации), подразумевают, что кодоны считываются специальными ферментами клетки с образованием промежуточной информационной молекулы и-РНК (этап транскрипции), считывание триплетов которой (этап трансляции) происходит в рибосомах с образованием белков.
Эти упрощенно описанные строение и механизм работы генетического аппарата, оказывается, едины для всего живого. Поэтому одновременно существующие в природе формы (не только близкородственные) в принципе могут обмениваться генами. Такой перенос наследственной информации не от родителей к потомству, а между одновременно существующими организмами и назвали ГПГ.
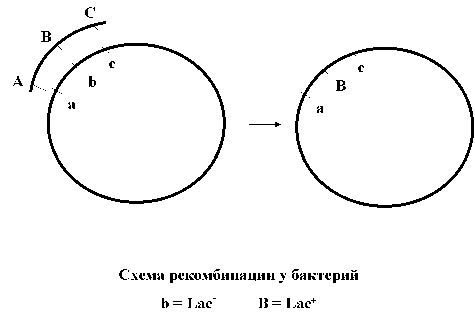
Природные механизмы ГПГ. У бактерий ГПГ — один из важнейших механизмов эволюции (есть у них и половое размножение, но примитивное, без образования гамет и слияния клеток). В Царстве бактерий можно выделить три основных способа ГПГ: трансдукция, конъюгация, трансформация. При трансдукции фрагменты ДНК от бактерии-донора к реципиенту переносят бактериофаги (вирусы, поражающие бактерий). При конъюгации обмен генами происходит в результате контакта между клетками. Наконец, трансформация — это естественный захват бактерией чужеродной ДНК с последующей экспрессией генов этой ДНК, причем, как и при трансдукции, контакт клеток не обязателен. Ученые считают, что вклад трансформации в ГПГ, по сравнению с остальными механизмами, у бактерий невелик. Это важно, ибо единственным способом ГПГ от растений к бактериям в природе оказывается именно трансформация.
ГПГ: опасности мнимые и подлинные. Бактерии несут разные гены устойчивости, которые ученые научились использовать в генной инженерии. Так, ген устойчивости к колорадскому жуку, который защищает ГМ-картофель от вредителя, выделен из бактерии Bacillus thuringiensis, живущей на листьях картофеля и в почве и абсолютно безвредной для человека, а ген устойчивости к антибиотику канамицину (используемый для отбора ГМ-растений) — из всем известной кишечной палочки.
Потребляя овощи и фрукты с собственных грядок, мы уверены, что едим «экологически чистую» пищу. Но даже если мы тщательно вымоем овощи и фрукты, с пищей в организм попадут бактерии, в том числе и те, что могут нести различные гены устойчивости. Между тем обмен генами (природная «генная инженерия») — один из основных механизмов эволюции бактерий. А болезнетворные формы той же кишечной палочки опасны для здоровья человека. Именно за счет трансформации генами других бактерий ее безвредные формы превращаются в патогенные.
Итак, прежде чем оценить риск неконтролируемого переноса гена (трансгена) из растения в бактерии, следует уяснить роль ГПГ в передаче наследственной информации между самими бактериями, обратив особое внимание на перенос болезнетворных генов и генов устойчивости к антибиотикам.
Бактерии и антибиотики. В последние годы ГПГ обнаружен у патогенных микроорганизмов (Salmonella, Acinetobacter, Streptococcus). Особо опасен он между стрептококками и кишечной палочкой. Очевидно, что ГПГ с участием болезнетворных микробов серьезно влияет на возникновение и развитие различных заболеваний. Этот распространенный в природе механизм ныне привлекает пристальное внимание эпидемиологов, которые надеются с его помощью разобраться в прежде необъяснимых вспышках опасных болезней.
Многие микроорганизмы вырабатывают антибиотики. В их числе и такие бактерии, как Streptomycetes spp., Erwinia carotovora, Pseudomonas aureofaciens. По мнению ряда авторов, ГПГ сыграл важную роль в эволюции генов антибиотиков у стрептомицетов и ряда других бактерий.
С другой стороны, многие бактерии обладают генами устойчивости к антибиотикам. Развитие у ряда болезнетворных бактерий устойчивости к нескольким видам антибиотиков большинство ученых связывают именно с ГПГ, при котором та или иная бактерия не только сохранила «свой» ген устойчивости, но и приобрела «чужие». Чем шире применяют антибиотики в медицине, тем больше становится устойчивых к ним микробов.
Так, ген nptII, обеспечивающий устойчивость к канамицину и ряду других антибиотиков, часто используют в ГМ-растениях как маркер — ген, непосредственно не определяющий какой-либо признак, но позволяющий судить о его передаче. (ГМ-растения, содержащие этот ген, прекрасно себя чувствуют в питательной среде, куда добавлен антибиотик. В отличие от них обычные растения, в которых этого гена нет, теряют способность к фотосинтезу и погибают.) Так вот, при оценке гипотетических рисков передачи этого гена от ГМ-растений бактериям не мешало бы учесть, насколько широко он распространен в природе (найден в бактериях из стоков, навоза, речной воды, почв, кишечного тракта человека и животных), где вполне возможен его перенос из одних бактерий в другие.
Но несмотря на это его использование (как и других маркеров) в ГМ-растениях находится под жесточайшим контролем. Не означает ли это, что возможен ГПГ из растений в бактерии?
От растений — к бактериЯм. Попробуем оценить вероятность ГПГ от растений к бактериям, вклад этого процесса в общий ГПГ и понять, опасен ли он. Как уже отмечалось, единственный природный механизм этого процесса — трансформация. Вероятность (а следовательно, и роль в эволюции) ГПГ от растений к бактериям зависит от ряда обстоятельств, которые должны совпасть, чтобы этот перенос произошел в естественной экосистеме:
выход неповрежденной ДНК в окружающую среду;
ее абсорбция частицами почвы для защиты от разрушения ферментами;
наличие «пригодных» для трансформации видов бактерий;
создание необходимых для этого условий;
эффективное поглощение ДНК на поверхности бактериальных клеток;
эффективный перенос ДНК в эти клетки;
интеграция чужеродной ДНК в геном бактерии-реципиента;
экспрессия генов введенной ДНК в клетке-реципиенте.
В последние годы эти этапы подробно рассмотрены. Детально описаны и препятствия ГПГ, причем особое внимание уделено клеточным барьерам — абсорбции ДНК на поверхности бактериальной клетки и т. д. Собрано много данных о возможных примерах взаимного ГПГ между про- и эукариотами в процессе эволюции. Но пока не удалось наблюдать ГПГ от ГМ-растений к бактериям в природных условиях. Действительно, трудно представить, чтобы все перечисленные требования оказались выполненными одновременно, да еще из десятков тысяч растительных генов в бактерию попал бы именно тот, который пытаются «уловить». Означает ли это, что ГПГ от растений к бактериям в принципе невозможен?
Для ответа на этот вопрос провели исследования не в природных условиях, а в специально созданных, способствующих ГПГ. Их результаты собраны в таблице (символ «?» означает, что предсказание не подтверждено в эксперименте):
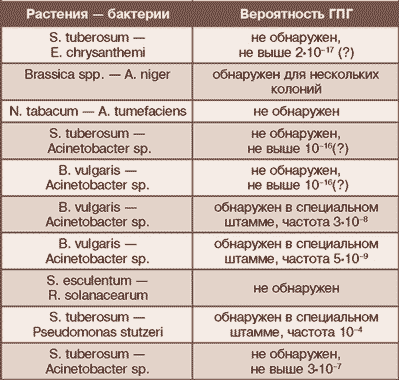 О чем говорят эти данные? В искусственных условиях можно «поймать» ГПГ от растения к бактерии. По мнению исследователей, и в природе он мог происходить и, возможно, даже играл определенную роль в эволюции. Но его вклад в общий ГПГ между организмами пренебрежимо мал.
О чем говорят эти данные? В искусственных условиях можно «поймать» ГПГ от растения к бактерии. По мнению исследователей, и в природе он мог происходить и, возможно, даже играл определенную роль в эволюции. Но его вклад в общий ГПГ между организмами пренебрежимо мал.
Не перенесем ли «Что-нибудь» за обедом? Способность к естественной трансформации пока выявлена всего у 40 представителей Царства бактерий, и лишь несколько из них относятся к кишечной флоре. Специалисты считают, что риска от употребления в пищу ГМ-растений нет. Да и молоко, мясо и яйца от животных, которых кормили ГМ-пищей, эксперты сочли столь же безопасными, как и от животных, получавших обычные корма.
В связи с возможной трансформацией бактерий желудочно-кишечного тракта вернемся к гену nptII, вызывающему устойчивость к антибиотику, пусть и устаревшему. Вероятность его передачи из пищи микробам желудочно-кишечного тракта оценивается примерно так же, как и вероятность ГПГ от растений к бактериям почвы (правда, пока пищу готовят и переваривают, молекулы ДНК испытывают много разрушающих воздействий: механические, термические, ферментативные, так что в итоге уцелеть «перенесенному» гену трудно). Тем не менее в ряде руководств и правил, действующих в генной инженерии, учитывают как возможный перенос генов в микроорганизмы желудочно-кишечного тракта, так и свойства белков — продуктов этих генов. Например, в руководстве «Использование устойчивых к антибиотикам генов-маркеров в трансгенных растениях», выпущенном в 1998 г. специальным ведомством США, оценивающим пищевую безопасность продуктов, указано, что продукт гена nptII (фермент неомицинфосфотрансфераза) нетоксичен и не вызывает аллергии и что употребление в пищу сырых ГМ-томатов, содержащих этот ген, не влияет на терапию с применением канамицина или схожих антибиотиков, например, неомицина (исследование проводили на томатах, но результаты применимы и, скажем, к картофелю — если кто-то любит картошку сырой). Там же отмечено, что наличие упомянутого фермента в кормах безопасно для скота. В итоге сделан вывод о том, что присутствие гена устойчивости к канамицину в ГМ-растениях не вызывает опасений с точки зрения эпидемиологии. Аналогичные выводы содержатся и в подготовленном в 2001 г. докладе Европейской федерации по биотехнологии.
Почему же растет устойчивость к антибиотикам? Итак, пока никто не обнаружил ГПГ от растений к бактериям в природных условиях. Тем не менее он, скорее всего, имел место в эволюции, хотя и гораздо реже, чем ГПГ среди самих прокариот. Во всяком случае, специалисты не исключают такой возможности, но признают, что из-за низкой вероятности процесса и несовершенства методов детектирования мы еще долго не сможем «уловить» его в природе. Но экологическое значение этого исключительно редкого события будет зависеть от селекции перенесенного признака и его последующего распространения.
Нас окружают и в нас живут бактерии, несущие гены устойчивости к разным антибиотикам, включая и те, что вводят в ГМ-растения. Для бактерий обмен генами (в частности, болезнетворными и устойчивости к антибиотикам) — «дело житейское».
Распространенность в природе генов устойчивости к антибиотикам, с одной стороны, и частый ГПГ между разными бактериями при все более широком применении антибиотиков — с другой, порождают устойчивые к нескольким антибиотикам штаммы патогенных микробов. Злоупотребляя антибиотиками, мы создаем устойчивых к ним бактерий. Это заставляет искать все новые классы антибиотиков, отказываясь от прежних. Круг замыкается.
Так что проблемы с устойчивостью к антибиотикам в медицине и ветеринарии связаны с неконтролируемым использованием самих антибиотиков, а не с ГМ-растениями.
Список литературы
Для подготовки данной работы были использованы материалы с сайта http://www.ecolife.ru/
Похожие работы
... инженерию. Необходимо отметить, что если базовый стандарт по химии не предусматривает изучение вопросов биотехнологии, то таковой по биологии содержит наиболее общие её аспекты: достижения генной инженерии и перспективы биотехнологии. 2.2 Межпредметные связи по изучению аспектов биотехнологии в средней школе По программе Р.Г. Ивановой и Л.А. Цветкова в 10 классе предусмотрено изучение темы ...
... исследователями было показано, что белковый сплайсинг является аутокаталитическим процессом и для своего осуществления не требует присутствия ферментов или кофакторов. Однако определить точный механизм сплайсинга белков долгое время не удавалось — процесс происходит очень быстро, и обычными методами обнаружить промежуточные соединения не представлялось возможным. Главная проблема заключалась в ...
... геномов ряда вирусов. Первыми свободно живущими организмами, чьи геномы были полностью прочитаны, стали микоплазма Micoplasma genitalium и бактерия Haemophilus influenzae. Эти микроорганизмы оказались выбраны, т.к. являются патогенами (т.е. вызывают заболевания) человека. Всего на начальном этапе реализации геномных проектов были изучены 8 разных представителей мира микроорганизмов, а к концу ...
... растений, как пшеница и кукуруза. Также открываются пути привнесения дополнительной генетической информации по желанию экспериментатора в целях создания трансгенных растений. Прямой перенос чужеродной ДНК в протопласты возможен также с помощью микроинъекции, трансформации, упаковки в липосомы с последующим их эндоцитозом растительными протопластами, и электропорации (высоковольтных электрических ...



0 комментариев