Федеральное агентство по образованию
Государственное образовательное учреждение высшего профессионального образования
Самарский государственный технический университет
Кафедра: «Органическая химия»
“ Бензимидазол, его производные, синтезы и свойства ”
Курсовая работа
Выполнил: студент
_________________
(подпись)
Руководитель:
_________________
(подпись)
Работа защищена
“___“ __________ 2008г.
Оценка _______
Зав. кафедрой: доцент, д. х. н.
_________________
(подпись)
Самара, 2008 г.
Содержание
1. Введение. 3
1.1. Свойства бензимидазолов. 3
1.2. Практическое применение. 4
1.3. Методика синтеза. 8
2. Литературный обзор. Бензимидазол, его производные, их синтезы и свойства 9
3. Выводы.. 40
Список литературы.. 41
1. Введение
1.1. Свойства бензимидазолов
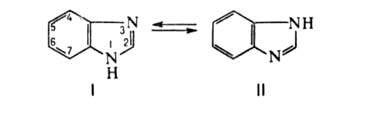
Бензимидазол, мол. м. 118; бесцветные кристаллы, т. пл. 172°С; растворим в воде, спиртах, разбавленных кислотах и щелочах, трудно растворим – в неполярных растворителях. Молекулы ассоциированы благодаря водородной связи — NH...NH=. Положения 4 и 7, а также 5 и 6 равноценны вследствие равновесия между таутомерами I и II:
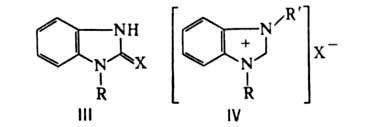
С ионами некоторых металлов (Ag, Co, Си и др.) бензимидазол образует в аммиачном р-ре соли. Бензимидазол устойчив к действию окислителей, но СrO3 в 80%-ной H2SO4 при 80°С окисляет его до имидазол-4,5-дикарбоновой к-ты. Сплавление с S превращает бензимидазол в бензимидазол-2-тион, 1-алкилбензимидазолы - в его 1-алкилзамещенные (формула III, X = S, R = А1К). Б. алкилируется алкилгалогенидами и диалкилсульфатами в присут. щелочей в положение 1. При алкилировании N-алкилбензимидазолов образуются соли 1,3-диалкилбензимидазолия (формула IV). Арилирование бензимидазола в положение 1 с помощью галогенаренов протекает обычно в жестких условиях. Действием ацилхлоридов и ангидридов кислот получают N-ацилпроизводные. Бензимидазол нитруется смесью HNO3 и H2SO4 в положение 5. При сульфировании образуется 5(6)-сульфокислота. Нуклеофильное замещение протекает в положении 2 лишь с N-производными Б. При нагревании с NaNH2 в диметиланилине образуются 2-аминопроизводные Б., при сплавлении с КОН-бензимидазолоны (ф-ла III, X = О). Металлирование (например, фенилнатрием) идет в положение 2.
При взаимодействии o-фенилендиамина с НСООН образуются бензимидазол, с RCOOH в присутствии НС1-2-алкилбензимидазолы, с АrСНО и ацетатом Сu(1)-2-арилбензимидазолы (реакция Вайденхагена). Сам бензимидазол не находит промышленного применения, однако его производные являются лекарственными средствами (например, дибазол), фунгицидами (например, беномил) и др.
1.2. Практическое применениеГастроэнтерология – одна из наиболее динамично развивающихся областей медицины. Прогресс молекулярной патологиии и физиологии, стремительное развитие медицинской генетики, технологии диагностики и лечения, немыслимые без компьютерного обеспечения, о которых ранее можно было только мечтать, позволили выделить новые нозологические формы болезней органов пищеварения, уточнить патогенез гастроэнтерологических страданий, поднять на современный уровень диагностику и пересмотреть многие лечебные алгоритмы. Возможности терапевтического и хирургического лечения ряда заболеваний, приобретенные за последние десятилетия ушедшего века, чрезвычайно раширились, а их результаты впечатляют.
В свете этих достижений перспектива развития гастроэнтерологии на ближайшие 5–15 лет, представляется достаточно ясной.
Производные бензимидазола – ингибиторы протонной помпы париетальных клеток (омепразол, лансопразол, эзомепразол, пантопразол и рабепразол) – самый мощный класс антисекреторных препаратов, революционизировавших терапию гастро-эзофагеальной рефлюксной болезни, язвенной болезни двенадцатиперстной кишки и желудка, синдрома Золлингера–Эллисона. Бензимидазолы необратимо связываются с Н+–К+-АТФазой париетальных клеток (образуя ковалентную связь с сульфгидрильными группами энзима), и для восстановления секреции требуется синтез протонных помп de novo, что и определяет продолжительность антисекреторного эффекта. Бензимидазолы развивают свой антисекреторный эффект, достигая париэтальных клеток через кровоток и трансформируясь из неактивной формы в активную для связи с Н+–К+-АТФазой. Наиболее перспективным препаратом из этой группы является рабепразол, благодаря своей способности быстро трансформироваться в активную форму и насыщать все связи АТФазы.
В качестве средств, повышающих тонус и двигательную активность ЖКТ, перспективно применение агонистов серотониновых 5-НТ4-рецепторов. Препараты этой группы повышают тонус нижнего пищеводного сфинктера, предупреждая заброс содержимого желудка в пищевод, ускоряют опорожнение желудка и 12-перстной кишки, предупреждая стаз и дуодено-гастральный рефлюкс.
Принципиально новый класс лекарственных препаратов предварительно назван антагонистами кислотной помпы. Активно исследуются свойства производного имидазо-пиридина, которое за счет предотвращения переноса ионов К+ протонной помпой париетальных клеток обратимо ингибируют желудочную секрецию. Главное преимущество по сравнению с бензимидазолами – немедленное развитие эффекта, в связи с чем препарат может использоваться у больных при оказании им экстренной помощи и при необходимости скорейшего купирования симптоматики (например, язвенное кровотечении).
Разработанные препараты, непосредственно влияющие на финальный этап кислотной продукции – Н+,К+-АТФазу париетальных клеток, высоко эффективны, и механизм их действия практически не нуждается в совершенствовании. По мнению ряда экспертов, в ближайшие годы вряд ли удастся создать новые антисекреторные препараты, которые мБензимидазолы и пробензимидазолы как антгельминтики широко используются в ветеринарной медицине в связи с их незначительной токсичностью (их терапевтический индекс может быть равен 60, а у левамизола - 4). Производные бензимидазола эффективны в основном против нематод, и в меньшей степени против цестод и трематод. Они действуют как ингибиторы полимеризации тубулина, фиксируя бета-тубулин нематод или цестод. Помимо этого, считается, что механизм их действия связан с теми или иными нарушениями энергетического обмена, в частности, с разобщением цепочки окислительного фосфорилирования и с воздействием на фумаратредуктазу (Новик Т.С., Ястреб В.Б., 2000). Они также умерщвляют гельминтов, вызывая дезорганизацию большого количества скелетоформирующих клеток и клеток эпителия пищевода - у нематод (Ф.Бене, 1999). При неоднократном назначении бензимидазол и пробензимидазол активно действуют на цестод рода Taenia. В обычно применяемой терапевтической дозе они не производят никакого действия на ленточных червей рода Echinococcus и, как правило, не эффективны против Diрylidium caninum. Ларвицидное действие бензимидазола при аскаридозе (Toxocara canis или T. cati) основано на пенетрации препарата в ткани, что не поддается количественной оценке, и поэтому дозу препарата часто приходится завышать, по сравнению с рекомендуемой.
Что касается фенбендазола (новейший бензимидазол - содержится в таких препаратах, как каниквантел плюс, дирофен, панакур, празицид, фебтал), то его антгельминтное действие основано на ингибиции ферментной фумаратредуктазной системы паразитов, повреждении оболочки мышечной ткани и деполяризации нейромышечных ганглиев, что приводит к нарушению энергетического метаболизма, нервно-мышечной иннервации, параличу и в результате – к гибели гельминтов. Фенбендазол плохо всасывается в кишечнике, выводится в основном с фекалиями, в меньшей степени с мочой. Действие фенбендазола против нематод многократно усиливается в сочетании с пирантелом.
Фенбендазол, мебендазол, оксфендазол, оксибендазол, флюбендазол и фебантел (профенбендазол) активно действуют на аскарид и взрослых анкилостом в кишечнике. Оксибендазол обладает широким антигельминтным спектром действия против нематод и цестод. Механизм действия заключается в блокировке фумаратредуктазы и нарушении энергетического метаболизма у гельминта. Часть препарата всасывается, трансформируется в организме и выводится с мочой.
Механизм действия альбендазола основан на нарушении транспорта глюкозы и микротубулярной функции паразитов (трематоды, цестоды, нематоды) угнетении активности фумаратредуктазы и синтеза АТФ, повышении проницаемости клеточных мембран, что приводит к нарушению нервно-мышечной иннервации, параличу и гибели паразитов, в том числе при легочных гельминтозах могли бы конкурировать с уже имеющимися.
1.3. Методика синтеза2-Трихлорметилбензимидазол. К 23 г (0,1 моль) охлажденного раствора моногидрохлорида о-фенилендиамина в 200 мл этанола медленно, по каплям добавляют 17,8 г (0,1 моль) трихлорацетимидата. После завершения экзотермичной реакции смесь оставляют при комнатной температуре на несколько часов. Растворитель отгоняют в вакууме, а твердый остаток кристаллизуют из уксусной кислоты. Выход продукта 9-5%; т. кип. >360°.
2. Литературный обзор. Бензимидазол, его производные, их синтезы и свойства
Данная работа посвящена изучению обладающих ценными свойствами бензимидазолов общей формулы
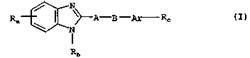
их таутомеров, их стереоизомеров, их смесей, их пролекарственных остатков, их производных, содержащих вместо карбоксигруппы отрицательно заряженную в физиологических условиях группу, их солей, прежде всего их физиологически приемлемых солей с неорганическими или органическими кислотами или основаниями.
Соединения приведенной выше общей формулы I, в которых Rc представляет собой цианогруппу, являются ценными промежуточными продуктами для получения других соединений общей формулы I, а соединения вышеприведенной общей формулы I, в которых Rс представляет собой одну из представленных ниже амидиновых групп, а также их таутомеры, их стереоизомеры, их смеси, их пролекарственные остатки, их производные, содержащие вместо карбоксигруппы отрицательно заряженную в физиологических условиях группу, и их соли, прежде всего их физиологически приемлемые соли с неорганическими или органическими кислотами, и их стереоизомеры обладают ценными фармакологическими свойствами, прежде всего антитромботическим действием.
Объектом настоящего изобретения в соответствии с этим являются новые соединения вышеприведенной общей формулы I, а также их получение, лекарственные средства, содержащие в своем составе фармакологически эффективные соединения, их получение и применение.
В вышеприведенной общей формуле Аr обозначает необязательно замещенную атомом фтора, хлора либо брома, трифторметильной, С1-С3алкильной либо С1-С3алкокси-группой фениленовую или нафтиленовую группу, или обозначает необязательно замещенную в углеродном скелете С1-С3 алкильной группой тиениленовую, тиазолиленовую, пиридиниленовую, пиримидиниленовую, пиразини-леновую или пиридазиниленовую группу,
А обозначает С1-С3алкиленовую группу,
В обозначает атом кислорода либо серы, метиленовую, карбонильную, сульфинильную или сульфонильную группу, необязательно замещенную С1-С3алкильной группой иминогруппу, в которой алкильный фрагмент может быть одно- либо двузамещенной карбокси-группой,
Ra обозначает R1-СО-С3-С5циклоалкильную группу, где
- R1 представляет собоС1-С3алкокси-, амино-, С1-С4алкиламино- либо ди(С1-С4алкил)аминогруппу, в которых соответственно алкильный фрагмент может быть замещен карбоксигруппой,
- 4-7-членную циклоалкиленимино- либо циклоалкенилениминогруппу, которые могут быть замещены одной или двумя С1-С3алкиль-ными группами, при этом один алкильный заместитель одновременно может быть замещен гидрокси-, С1-С3алкокси-, карбокси-, карбокси-С1-С3алкокси-, карбокси-С1-С3алкиламино-, N-(С1-С3алкил)-N-(карбокси-С1-С3алкил)амино-, карбокси-С1-С3алкиламинокарбонильной, N-(С1-С3алкил)-N-(карбокси-С1-С3алкил)амино-карбонильной, карбокси-С1-С3алкиламинокар-бониламино-, 1-(С1-С3алкил)-3-(карбокси-С1-С3 алкил)аминокарбониламино-, 3-(С1-С3алкил)-3-(карбокси-С1-С3алкил)аминокарбониламино-либо 1,3-ди(С1-С3алкил)-3-(карбокси-С1-С3ал-кил)аминокарбониламиногруппой,
- замещенную гидроксигруппой 4-7-членную циклоалкилениминогруппу,
- необязательно замещенную С1-С3 алкильной группой 5-7-членную циклоалкилени-миногруппу, с которой через два смежных атома углерода сконденсировано фенильное кольцо,
- морфолиновую, пиперазиновую, N-(С1-С3 алкил)пиперазиновую, пирролиновую, 3,4- дегидропиперидиновую или пиррол-1-ильную группу, или обозначает R2-СХ-С3-С5циклоалкильную группу, где R2 представляет собой необязательно замещенную С1-С3алкильной группой фенильную, нафтильную либо моноциклическую 5- или 6-членную гетероарильную группу, при этом 6-членная гетероарильная группа содержит один, два или три атома азота, а 5-членная гетероарильная группа содержит необязательно замещенную С1-С3алкильной группой иминогруппу, один атом кислорода либо серы или необязательно замещенную С1-С3алкильной группой иминогруппу и один атом кислорода либо серы или один либо два атома азота и упомянутый выше алкильный заместитель может быть замещен карбокси-, карбокси-С1-С3алкокси-, кар-бокси-С1-С3алкиламино- либо N-(С1-С3алкил) карбокси-С1-С3алкиламиногруппой, и Х представляет собой атом кислорода, С1-С3алкилимино-, С1-С3алкоксиимино-, С1-С3алкилгидразиновую, ди(С1-С3алкил)гидразино-вую, С2-С4алканоилгидразиновую, N-(С1-С3ал-кил)-С2-С4алканоилгидразиновую или С1-С3ал-килиденовую группу, каждая из которых соответственно в алкильном или алканоильном фрагменте либо в алкильном и алканоильном фрагментах может быть замещена карбокси-группой, или обозначает замещенную имидазольной либо имидазолоновой группой С1-С3 алкильную или С3-С5циклоалкильную группу, где имидазольное кольцо может быть замещено фенильной либо карбоксигруппой и одной или двумя С1-С3алкильными группами либо одной, двумя или тремя С1-С3алкильными группами, при этом заместители могут быть идентичными или разными и один из выше названных алкильных заместителей одновременно может быть замещен карбоксигруппой или в положении 2 либо 3 амино-, С2-С4алкано-иламино-, С1-С3алкиламино-, N-(С2-С4алкано-ил)-С1-С3алкиламино- либо ди(С1-С3алкил) аминогруппой, а имидазолоновое кольцо может быть замещено С1-С3алкильной группой, при этом алкильный заместитель может быть замещен карбоксигруппой или в положении 2 либо 3 амино-, С2-С4алканоиламино-, С1-С3алкила-мино-, N-(С2-С4алканоил)-С1-С3алкиламино- либо ди(С1-С3алкил)аминогруппой, и дополнительно с вышеуказанными имидазольным и имидазолоновым кольцами через два смежных атома углерода может быть сконденсировано фенильное либо пиридиновое кольцо, или обозначает имидазолидин-2,4-дион-5-ильную группу, которая может быть замещена одной или двумя С1-С3алкильными группами, при этом одновременно один алкильный заместитель может быть замещен карбоксигруппой, или обозначает С1-С4алкильную группу, замещенную -С1-С3алкил-Y1-С1-С3алкильной, НООС-С1-С3алкил-Y1-С1-С3алкильной, тетразо-лил-С1-С3алкил-Y2-, R3NR4- или R3NR4-С1-С3алкильной группой и необязательно замещенной С1-С3алкильной группой изоксазолидинилкарбонильной группой, пирролинокарбонильной, 3,4-дегидропиперидинокарбонильной, пирролил-1-илкарбонильной, карбокси-, аминокарбониль-ной, С1-С3алкиламинокарбонильной, ди(С1-С3 алкил)аминокарбонильной или 4-7-членной циклоалкилениминокарбонильной группой, при этом в вышеназванных группах циклоалкиле-ниминовый фрагмент замещен одной либо двумя С1-С3алкильными группами и одновременно в каждой из указанных выше С1-С3алкил-аминокарбонильных, ди(С1-С3алкил)амино-карбонильных или циклоалкилениминокарбо-нильных групп один алкильный фрагмент или алкильный заместитель может быть соответственно замещен карбоксигруппой, а остальные атомы водорода С1-С4алкильной группы могут быть полностью либо частично заменены на атомы фтора, где R3 представляет собой атом водорода или необязательно замещенную карбоксигруппой С1-С3алкильную группу, а R4 представляет собой атом водорода, С1-С3алкил-Y1-С1-С3алкил-Y2-, карбокси-С1-С3ал-кил-Y1-С1-С3алкил-Y2-, С1-С3алкил-Y2- или кар-бокси-С1-С3алкил-Y2-группу или R3 и R4 вместе с расположенным между ними атомом азота представляют собой необязательно замещенную карбокси-, С1-С3алкиль-ной либо карбокси-С1-С3алкильной группой 4-7-членную циклоалкилениминогруппу, при этом Y1 представляет собой углерод-углеродную связь, атом кислорода, сульфениль-ную, сульфинильную, сульфонильную, -NH-, -NH-CO-или -NH-CO-NH-группу, а Y2 представляет собой углерод-азотную связь или карбонильную, сульфонильную, ими-но- либо -NH-CO-группу, причем карбонильная группа в составе -NH-CO-группы соединена с атомом азота R3NR4-группы, а каждая из указанных при расшифровке значений остатков Y1 и Y2 иминогрупп дополнительно может быть замещена соответственно С1-С3алкильной либо карбокси-С1-С3алкильной группой, или обозначает замещенную R5NR6-группой С1-С3алкильную или С3-С5циклоал-кильную группу, где R5 представляет собой атом водорода, С1-С3алкильную, С5-С7циклоалкильную, фенилкар-бонильную, фенилсульфонильную или пириди-нильную группу, а R6 представляет собой С1-С3алкильную, карбокси-С1-С3алкильную или карбокси-С1-С3 алкилкарбонильную группу, или обозначает С1-С3алкильную группу, замещенную С2-С4алканоильной либо С5-С7 циклоалканоильной группой, и замещенную атомом хлора, брома либо иода С1-С3алкильную группу, Rb обозначает атом водорода или С1-С3ал-кильную группу и Rc обозначает цианогруппу или необязательно замещенную одной либо двумя С1-С3 алкильными группами амидиновую группу.
Указанные при расшифровке значений вышеназванных остатков карбоксигруппы могут быть, кроме того, заменены на группу, переводимую in vivo в карбоксигруппу, либо на отрицательно заряженную в физиологических условиях группу или указанные при расшифровке значений вышеназванных остатков амино- и иминогруппы могут быть, кроме того, замещены отщепляемой in vivo группой.
Под группой, переводимой in vivo в кар-оксигруппу, имеются в виду, например, гидроксиметильная группа, этерифицированная спиртом карбоксигруппа, в которой спиртовой фрагмент представляет собой предпочтительно С1-С6алканол, фенил-С1-С3алканол, С3-С9циклоалканол, при этом С5-С8циклоалканол дополнительно может быть замещен одной либо двумя С1-С3алкильными группами, С5-С8циклоалканол, в котором метиленовая группа в положении 3 или 4 заменена на атом кислорода либо на необязательно замещенную С1-С3алкильной, фенил-С1-С3алкильной, фенил-С1-С3алкокси-карбонильной или С2-С6алканоильной группой иминогруппу, а циклоалканольный фрагмент дополнительно может быть замещен одной либо двумя С1-С3 алкильными группами, С4-С7 цикло-алкенол, С3-С5алкенол, фенил-С3-С5алкенол, С3-С5алкинол или фенил-С3-С5алкинол, при условии, что отсутствует связь между атомом кислорода и атомом углерода, несущим двойную либо тройную связь, С3-С8циклоалкил-С1-С3 алканол, бициклоалканол с в общей сложности 8-10 атомами углерода, который в бициклоалкильном фрагменте дополнительно может быть замещен одной либо двумя С1-С3алкильными группами, 1,3-дигидро-3-оксо-1-изобензфуранол или же спирт формулы Rd-СО-О-(ReCRf)-ОН, где Rd представляет собой С1-С8алкильную, С5-С7циклоалкильную, фенильную либо фенил-С1-С3алкильную группу, Rе представляет собой атом водорода, С1-С3алкильную, С5-С7циклоалкильную либо фе-нильную группу и Rf представляет собой атом водорода либо С1-С3алкильную группу; под отрицательно заряженной в физиологических условиях группой имеются в виду такие группы, как тетразол-5-ильная, фенилкар-бониламинокарбонильная, трифторметилкарбо-ниламинокарбонильная, С1-С6алкилсульфонил-амино-, фенилсульфониламино-, бензилсульфо-ниламино-, трифторметилсульфониламино-, С1-С6алкилсульфониламинокарбонильная, фенил-сульфониламинокарбонильная, бензилсульфо-ниламинокарбонильная или перфтор-С1-С6 алкилсульфониламинокарбонильная группа, а под отщепляемой in vivo от имино- или аминогруппы группой имеются в виду, например, гидроксигруппа, ацильная группа, такая как одно- либо двузамещенная атомами фтора, хлора, брома или иода, С1-С3алкильными либо С1-С3алкоксигруппами бензоильная группа, при этом заместители могут быть идентичными или разными, пиридиноильная группа или С1-С16алканоильная группа, такая как формильная, ацетильная, пропионильная, бутаноильная, пентаноильная и гексаноильная группа, 3,3,3-трихлорпропионильная либо аллилоксикарбонильная группа, С1-С16алкоксикарбонильная либо С1-С16алкилкарбонилоксигруппа, в которых атомы водорода полностью или частично могут быть заменены на атомы фтора либо хлора, такие как метоксикарбонильная, этоксикарбонильная, пропоксикарбонильная, изопропок-сикарбонильная, бутоксикарбонильная, трет-бутоксикарбонильная, пентоксикарбонильная, гексоксикарбонильная, октилоксикарбонильная, нонилоксикарбонильная, децилоксикарбониль-ная, ундецилоксикарбонильная, додецилокси-карбонильная, гексадецилоксикарбонильная, метилкарбонилокси-, этилкарбонилокси-,2,2,2-трихлорэтилкарбонилокси-, пропилкарбонилок-си-, изопропилкарбонилокси-, бутилкарбони-локси-, трет-бутилкарбонилокси-, пентилкарбонилокси-, гексилкарбонилокси-, октилкарбонилокси-, нонилкарбонилокси-, децилкарбонилокси-, ундецилкарбонилокси-, додецилкарбонилокси- или гексадецилкарбонилоксигруппа, фенил-С1-С6алкоксикарбонильная группа, такая как бензилоксикарбонильная, фенилэтоксикарбонильная или фенилпропоксикарбонильная группа, 3-аминопропионильная группа, в которой аминогруппа является одно- либо двузамещенной С1-С6алкильными или С3-С7циклоал-кильными группами и заместители могут быть идентичными или разными, С1-С3алкилсульфо-нильная, С2-С4алкоксикарбонильная, С1-С3ал-кокси-С2-С4алкокси-С2-С4алкоксикарбонильная, Rd-CO-О-(RdCRf)-О-CO-, С1-С6алкил-СО-NН-(RgCRh)-О-СО- или С1-С6aлкил-CO-О-(RgCRh)-(RgCRh)-O-CO-группa, в которых Rd-Rf имеют значения, указанные выше, a Rg и Rh, которые могут быть идентичными или разными, представляют собой атомы водорода или С1-С3ал-кильные группы.
Кроме того, группы, указанные при расшифровке значений вышеназванных насыщенных алкильных и алкоксифрагментов, содержащих более двух атомов углерода, включают также их разветвленные изомеры, как, например, изопропильная, трет-бутильная, изобу-тильная и т.д. группа.
К предпочтительным соединениям относятся такие соединенияобщей формулы
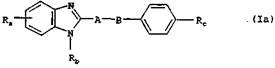
в которой А обозначает С1-С3алкиленовую группу, В обозначает атом кислорода либо серы, метиленовую, карбонильную, сульфинильную или сульфонильную группу, необязательно замещенную С1-С3алкильной группой иминогруппу, в которой алкильный фрагмент может быть одно- либо двузамещенной карбоксигруппой, Rа обозначает R1-СО-С3-С5 циклоалкиль-ную группу, где R1 представляет собой С1-С3алкокси-, амино-, С1-С4алкиламино-либо ди(С1-С4алкил)аминогруппу, в которых соответственно алкильный фрагмент может быть замещен карбоксигруппой, 4-7-членную циклоалкиленилимино- либо циклоалкенилениминогруппу, которые могут быть замещены одной или двумя C1-С3-алкильными группами, при этом один алкильный заместитель одновременно может быть замещен гидрокси-, С1-С3алкокси-, карбокси-, карбокси-С1-С3алкокси-, карбокси-С1-С3алки-ламино-, N-(С1-С3алкил)-N-(карбокси-С1-С3ал-кил)амино-, карбокси-C1-С3алкиламинокарбо-нильной, N-(С1-С3алкил)-N-(карбокси-С1-С3ал-кил)аминокарбонильной, карбокси-С1-С3алкил-аминокарбониламино-, 1-(С1-С3алкил)-3-(карбо-кси-С1-С3алкил)аминокарбониламино-, 3-(С1-С3 алкил)-3-(карбокси-С1-С3алкил)аминокарбонил амино- либо 1,3-ди(С1-С3алкил)-3-(карбокси-С1-С3алкил)аминокарбониламиногруппой, замещенную гидроксигруппой 4-7-членную циклоалкилениминогруппу, необязательно замещенную С1-С3ал-кильной группой 5-7-членную циклоалкилени-миногруппу, с которой через два смежных атома углерода сконденсировано фенильное кольцо, морфолиновую, пиперазиновую, N-(С1-С3 алкил)пиперазиновую, пирролиновую, 3,4- дегидропиперидиновую или пиррол-1-ильную группу,или обозначает R2-СХ-С3-С5циклоал-кильную группу, где R2 представляет собой необязательно замещенную С1-С3алкильной группой фенильную, нафтильную либо моноциклическую 5- или 6-членную гетероарильную группу, при этом 6-членная гетероарильная группа содержит один, два или три атома азота, а 5-членная гетероарильная группа содержит необязательно замещенную С1-С3алкильной группой иминогруппу, один атом кислорода либо серы или необязательно замещенную С1-С3алкильной группой иминогруппу и один атом кислорода либо серы или один либо два атома азота и упомянутый выше алкильный заместитель может быть замещен карбокси-, карбокси-С1-С3 алкок-си-, карбокси-С1-С3алкиламино- либо N-(С1-С3 алкил)карбокси-С1-С3алкиламиногруппой, и Х представляет собой атом кислорода, С1-С3 алки-лимино-, С1-С3алкоксиимино-, С1-С3алкилгидра-зиновую, ди(С1-С3алкил)гидразиновую, С2-С4 алканоилгидразиновую, N-(С1-С3алкил)-С2-С4 алканоилгидразиновую или С1-С3алкилиде-новую группу, каждая из которых соответственно в алкильном или алканоильном фрагменте либо в алкильном и алканоильном фрагментах может быть замещена карбоксигруппой, или обозначает замещенную имидазольной либо имидазолоновой группой С1-С3алкильную или С3-С5циклоалкильную группу, где имидазольное кольцо может быть замещено фенильной либо карбоксигруппой и одной или двумя С1-С3алкильными группами либо одной, двумя или тремя С1-С3алкильными группами, при этом заместители могут быть идентичными или разными и один из вышеназванных алкильных заместителей одновременно может быть замещен карбоксигруппой или в положении 2 либо 3 амино-, С2-С4алкано-иламино-, С1-С3алкиламино-, N-(С2-С4алка-ноил)-С1-С3алкиламино- либо ди(С1-С3ал-кил)аминогруппой, а имидазолоновое кольцо может быть замещено С1-С3алкильной группой, при этом алкильный заместитель может быть замещен карбоксигруппой или в положении 2 либо 3 амино-, С2-С4алканоиламино-, С1-С3ал-киламино-, N-(С2-С4алканоил)-С1-С3алкилами-но- либо ди(С1-С3алкил)аминогруппой, и дополнительно с вышеуказанными имидазольным и имидазолоновым кольцами через два смежных атома углерода может быть сконденсировано фенильное либо пиридиновое кольцо, или обозначает имидазолидин-2,4-диoн-5-ильную группу, которая может быть замещена одной или двумя С1-С3алкильными группами, при этом одновременно один алкильный заместитель может быть замещен карбоксигруппой, или обозначает С1-С4алкильную группу, замещенную -С1-С3алкил-Y1-С1-С3алкильной,НООС- С1-С3алкил-Y1-С1-С3алкильной, тетразолил-С1- С3алкил-Y2-, R3NR4- или R3NR4-С1-С3алкильной группой и необязательно замещенной С1-С3алкиль- ной группой изоксазолидин-1-илкарбонильной группой, пирролинокарбонильной, 3,4-дегидро- пиперидинокарбонильной, пирролил-1-илкарбо- нильной, карбокси-, аминокарбонильной, С1-С3 алкиламинокарбонильной, ди(С1-С3алкил)ами- нокарбонильной или 4-7-членной циклоалкиле- ниминокарбонильной группой, при этом в вышеназванных группах циклоалкилениминовый фрагмент замещен одной либо двумя С1- С3алкильными группами и одновременно в каж дой из указанных выше С1-С3алкиламино- карбонильных, ди(С1-С3алкил)аминокарбонильных или циклоалкилениминокарбонильных групп один алкильный фрагмент или алкильный заместитель может быть соответственно заме щен карбоксигруппой, а остальные атомы водорода С1-С4алкильной группы могут быть полностью либо частично заменены на атомы фтора,где R3 представляет собой атом водорода или необязательно замещенную карбоксигруппой С1-С3алкильную группу, а R4 представляет собой атом водорода, С1-С3алкил-Y1-С1-С3алкилY2-, карбокси-С1-С3алкил-Y1-С1-С3алкил-Y2-, С1-С3алкил-Y2- или карбокси-С1-С3алкил-Y2- группу или R3 и R4 вместе с расположенным между ними атомом азота представляют собой необязательно замещенную карбокси-, С1-С3 алкильной либо карбокси-С1-С3алкильной группой 4-7-членную циклоалкилениминогруппу, при этом Y1 представляет собой углерод-углеродную связь, атом кислорода, сульфениль-ную, сульфинильную, сульфонильную, -NH-, -NH-CO-или -NH-CO-NH-группу, а Y2 представляет собой углерод-азотную связь или карбонильную, сульфонильную, имино- либо -NH-CO-группу, причем карбонильная группа в составе -NH-CO-группы соединена с атомом азота R3NR4-группы, а каждая из указанных при расшифровке значений остатков Y1 и Y2 иминогрупп дополнительно может быть замещена соответственно С1-С3алкильной либо карбокси-С1-С3алкильной группой, или обозначает замещенную R5NR6-группой С1-С3алкильную или С3-С5циклоал-кильную группу, где R5 представляет собой атом водорода, С1-С3алкильную, С5-С7циклоалкильную, фенилкар-бонильную, фенилсульфонильную или пириди-нильную группу, а R6 представляет собой С1-С3алкильную, карбокси-С1-С3алкильную или карбокси-С1-С3алкилкарбонильную группу, или обозначает С1-С3алкильную группу, замещенную С2-С4алканоильной либо С5-С7 циклоалканоильной группой, и замещенную атомом хлора, брома либо иода С1-С3алкильную группу, Rb обозначает атом водорода или С1-С3 алкильную группу и Rc обозначает цианогруппу или амидиновую группу, которая может быть замещена гидроксигруппой, одной либо двумя С1-С3алкильными группами, одной либо двумя С1-С8алкоксикарбонильными группами, при этом указанные выше при расшифровке значений остатков карбокси-, амино- и ими-ногруппы могут быть замещены, кроме того, отщепляемой in vivo группой, их таутомеры, их стереоизомеры и их соли.
Особенно предпочтительными являются такие соединения вышеприведенной общей формулы Iа, в которых А обозначает С1-С3алкиленовую группу, В обозначает атом кислорода, метиленовую, ими-но- или N-(С1-С3алкил)иминогруппу, в которой алкильный фрагмент может быть замещен кар-боксигруппой, Ra обозначает замещенную в положении 1 R1-СО-группой С3-С5циклоалкиль-ную группу, где R1 представляет собой С1-С3алкокси-, амино-, С1-С4алкиламино-либо ди(С1-С4алкил)аминогруппу, в каждой из которых соответственно алкильный фрагмент может быть замещен карбоксигруппой, 4-7-членную циклоалкилениминогруппу, которая может быть замещена гидроксигруппой либо одной или двумя С1-С3алкильными группами, при этом один алкильный заместитель одновременно может быть замещен гидрокси-, С1-С3алкокси-, карбокси-, карбокси-С1-С3алкок-си-, карбокси-С1-С3алкиламино-, N-(С1-С3ал-кил)-N-(карбокси-С1-С3алкил)амино-, карбокси-С1-С3алкиламинокарбонильной, N-(С1-С3алкил)-N-(карбокси-С1-С3алкил)аминокарбонильной, карбокси-С1-С3алкиламинокарбониламино-, 1-(С1-С3алкил)-3-(карбокси-С1-С3алкил)аминокар-бониламино-, 3-(С1-С3алкил)-3-(карбокси-С1-С3алкил)аминокарбониламино- либо 1,3-ди(С1-С3алкил)-3-(карбокси-С1-С3алкил)аминокарбо-ниламиногруппой, необязательно замещенную С1-С3алкильной группой 5-7-членную циклоалкилениминогруппу, с которой через два смежных атома углерода сконденсировано фенильное кольцо, морфолиновую, пиперазиновую, N-(С1-С3алкил)пиперазиновую, пирролиновую, 3,4-дегидропиперидиновую или пиррол-1-ильнуюгруппу, или обозначает замещенную в положении 1 R2-СХ-группой С3-С5циклоалкильную группу, где R2 представляет собой необязательно замещенную С1-С3алкильной группой фенильную, нафтильную либо моноциклическую 5- или 6-членную гетероарильную группу, при этом 6-членная гетероарильная группа содержит один, два или три атома азота, а 5-членная гетероа-рильная группа содержит необязательно замещенную С1-С3алкильной группой иминогруппу, один атом кислорода либо серы или необязательно замещенную С1-С3алкильной группой иминогруппу и один атом кислорода либо серы или один либо два атома азота и упомянутый выше алкильный заместитель может быть замещен карбокси-, карбокси-С1-С3алкокси-, кар-бокси-С1-С3алкиламино- либо N-(С1-С3алкил) карбокси-С1-С3алкиламиногруппой, и Х представляет собой атом кислорода, С1-С3алкилимино-, С1-С3алкоксиимино- или С1-С3алкилиденовую группу, которые соответственно в алкильном либо алкоксифрагменте могут быть замещены карбоксигруппой, или обозначает замещенную в положении 1 имидазольной либо имидазолоновой группой С1-С3алкильную группу, где имидазольное кольцо может быть замещено фенильной либо карбоксигруппой и одной или двумя С1-С3алкильными группами либо одной, двумя или тремя С1-С3алкильными группами, при этом заместители могут быть идентичными или разными и один из вышеназванных алкильных заместителей одновременно может быть замещен карбоксигруппой или в положении 2 либо 3 амино-, С2-С4алка-ноиламино-, С1-С3алкиламино-, N-(С2-С4алка-ноил)-С1-С3алкиламино- либо ди(С1-С3алкил) аминогруппой, а имидазолоновое кольцо может быть замещено С1-С3алкильной группой, при этом алкильный заместитель может быть замещен карбоксигруппой или в положении 2 либо 3 амино-, С2-С4алканоиламино-, С1-С3алкил-амино-, N-(С2-С4алканоил)-С1-С3алкиламино-либо ди(С1-С3алкил)аминогруппой, и дополнительно с вышеуказанными имидазольным и имидазолоновым кольцами через два смежных атома углерода может быть сконденсировано фенильное либо пиридиновое кольцо, или обозначает имидазолидин-2,4-дион-5-ильную группу, которая может быть замещена одной либо двумя С1-С3алкильными группами, при этом одновременно один алкильный заместитель может быть замещен карбоксигруппой, или обозначает С1-С4алкильную группу, замещенную в положении 1 - R3NR4- или R3NR4-С1-С3алкильной группой и пирролинокарбонильной, 2,3-дегидропиперидинокарбонильной, имидазол-1-илкарбонильной, карбокси-, аминокарбонильной, С1-С3алкиламинокарбонильной, ди(С1-С3алкил)аминокарбонильной, изоксазолидин-1-илкарбонильной или 4-7-членной циклоалкиленимино карбонильной группой, при этом в вышеназван ных группах циклоалкилениминовый фрагмент замещен одной либо двумя С1-С3алкильными группами и одновременно в каждой из указанных выше С1-С3алкиламинокарбонильных, ди(С1-С3алкил)аминокарбонильных или цикло-алкилениминокарбонильных групп один алкильный фрагмент или алкильный заместитель может быть соответственно замещен карбоксигруппой, а остальные атомы водорода С1-С4алкильной группы могут быть полностью либо частично заменены на атомы фтора, где R3 представляет собой атом водорода или необязательно замещенную карбоксигруппой С1-С3алкильную группу, а R4 представляет собой атом водорода, С1-С3алкил-Y2- или карбокси-С1-С3алкил-Y2-группу, или R3 и R4 вместе с расположенным между ними атомом азота представляют собой необязательно замещенную в положении 1 карбокси-, С1-С3алкильной либо карбокси-С1-С3алкильной группой 4-7-членную циклоалкилениминогруп-пу, при этом Y2 представляет собой углерод-азотную связь или карбонильную, имино- либо -NH-CO-группу, причем карбонильная группа в составе -NH-СО-группы соединена с атомом азота R3NR4-группы, а указанная при расшифровке значений остатка Y2 иминогруппа дополнительно может быть замещена С1-С3алкильной либо карбокси-С1-С3алкильной группой, или обозначает замещенную в положении 1 R5NR6-группой С1-С3алкильную или С3-С5 циклоалкильную группу, где R5 представляет собой атом водорода, С1-С3алкильную, С5-С7циклоалкильную, фенилкар-бонильную, фенилсульфонильную или пириди-нильную группу, а R6 представляет собой С1-С3алкильную, карбокси-С1-С3алкильную или карбокси-С1-С3 алкилкарбонильную группу, или обозначает С1-С3алкильную группу, замещенную С2-С4алканоильной либо С5-С7 циклоалканоильной группой, и замещенную атомом хлора, брома либо иода С1-С3алкильную группу, Rb обозначает С1-С3алкильную группу и Rc обозначает необязательно замещенную 2,2,2-трихлорэтоксикарбонильной, С1-С8алко-ксикарбонильной, ацетоксиметилоксикарбо-нильной, бензилоксикарбонильной или бензо-ильной группой амидиновую группу, при этом бензоильный фрагмент может быть одно- либо двузамещенным атомами фтора, хлора, брома либо иода, С1-С3алкильными или С1-С3 алкокси-группами, и заместители могут быть идентичными либо разными, их С1-С3алканоловые эфи-ры, их таутомеры, их стереоизомеры и их соли.
Наиболее предпочтительны такие соединения общей формулы I, в которых
А обозначает метиленовую группу,В обозначает атом кислорода или имино-группу,
Ra обозначает замещенную в положении 1 R1-CO-группой циклопропильную группу, где R1 представляет собой необязательно замещенную метильной либо этильной группой пирролидиновую или пиперидиновую группу, в каждой из которых соответственно метильный либо этильный фрагмент может быть замещен карбокси-, карбокси-С1-С3алкокси-, карбокси-С1-С3алкиламино- или N-(С1-С3алкил)карбокси-С1-С3алкиламиногруппой, или обозначает замещенную в положении 1 R2-CX-группой циклопропильную группу, где R2 представляет собой необязательно замещенную С1-С3алкильной группой фенильную, пиридильную или пиразолильную группу, a Х представляет собой атом кислорода, С1-С3алкоксиимино- или С1-С3алкилиденовую группу, замещенные соответственно в алкиль-ном либо алкоксифрагменте карбоксигруппой, или обозначает замещенную в положении 1 имидазольной группой С1-С2алкильную группу, где имидазольное кольцо может быть замещено фенильной или карбоксигруппой и одной- либо двумя С1-С3алкильными группами или одной, двумя либо тремя С1-С3алкильными группами, при этом заместители могут быть идентичными либо разными, а один из вышеназванных ал-кильных заместителей одновременно может быть замещен карбоксигруппой или в положении 2 либо 3 амино-, С2-С4алканоиламино-, С1-С3алкиламино-, N-(С2-С4алканоил)-С1-С3алкила-мино- или ди(С1-С3алкил)аминогруппой, при этом дополнительно с указанными выше имида-зольными кольцами через два смежных атома углерода может быть сконденсировано фениль-ное либо пиридиновое кольцо, или обозначает замещенную в положении 1 бензимидазолон-1-ильной группой С1-С2алкильную группу, при этом имидазолоновое кольцо может быть замещено необязательно замещённой карбоксигруппой метильной либо этильной группой, или обозначает метильную или этильную группу, замещенную в положении 1 R3NR4- или R3NR4-С1-С3алкильной группой и-ди(С1-С3залкил)аминокарбонильной группой, изоксазолидин-1-илкарбонильной группой, необязательно замещенной С1-С3алкильной группой пирролидинокарбонильной либо пиперидинокарбонильной группой, при этом один алкильный фрагмент или алкильный заместитель в указанных выше группах может быть замещен карбоксигруппой, где R3 представляет собой атом водорода или необязательно замещенную карбоксигруппой С1-С3алкильную группу, а R4 представляет собой атом водорода, С1-С3алкил-Y2- или карбокси-С1-С3алкил-Y2-группу илиR3 и R4 вместе с расположенным между ними атомом азота представляют собой необязательно замещенную карбоксигруппой 4-7-членную циклоалкилениминогруппу, при этом Y2 представляет собой углерод-азотную связь, карбонильную группу или необязательно замещенную С1-С3алкильной группой имино-группу, или обозначает замещенную в положении 1 R5NR6-группой С1-С2алкильную группу, где R5 представляет собой пиридинильную, фенилкарбонильную или фенилсульфонильную группу, а R6 представляет собой С1-С3алкильную или карбокси-С1-С3алкильную группу, или обозначает замещенную в положении 3 атомом хлора н-пропильную группу, замещенную в положении 1 циклопентилкарбонильной группой, или обозначает замещенную в положении 1 циклопентиламиногруппой цикло-пропильную группу, замещенную у атома азота карбокси-С1-С3алкилкарбонильной группой, Rb обозначает метильную группу и Rc обозначает необязательно замещенную С1-С8алкоксикарбонильной, ацетоксиметилок-сикарбонильной, 2,2,2-трихлорэтоксикарбо-нильной, бензилоксикарбонильной либо бензо-ильной группой амидиновую группу. Предпочтительны в первую очередь такие соединения общей формулы Iа, в которых А обозначает метиленовую группу, В обозначает иминогруппу, Ra обозначает замещенную в положении 1 R1-СО-группой циклопропильную группу, где R1 представляет собой необязательно замещенную метильной либо этильной группой пирролидиновую или пиперидиновую группу, в которых соответственно метильный либо этиль-ный фрагмент может быть замещен карбокси-, карбокси-С1-С3алкокси-, карбокси-С1-С3алкил-амино- или N-(С1-С3алкил)карбокси-С1-С3алки-ламиногруппой, или обозначает замещенную в положении 1 R2-СХ-группой циклопропильную группу, где R2 представляет собой необязательно замещенную С1-С3алкильной группой фенильную, пиридильную или пиразолильную группу, а Х представляет собой атом кислорода, С1-С3алкоксиимино- или С1-С3алкилиденовую группу, замещенные соответственно в алкиль-ном либо алкоксифрагменте карбоксигруппой, или обозначает замещенную в положении 1 имидазольной группой С1-С2алкильную группу, где имидазольное кольцо может быть замещено 1-3 метильными группами или замещено двумя метильными группами и одной этильной группой, при этом дополнительно один из вышеуказанных метильных или этильных заместителей одновременно может быть замещен карбокси-группой, или обозначает метильную либо этильную группу, замещенную в положении 1 R3NR4- или R3NR4-СН2-группой и ди(С1-С3алкил)аминокарбонильной группой, необязательно замещенной С1-С3алкильной группой пирролидинокарбонильной либо пипе-ридинокарбонильной группой, при этом соответственно один алкильный фрагмент или ал-кильный заместитель в составе вышеназванных групп может быть замещен карбоксигруппой, где R3 представляет собой атом водорода или необязательно замещенную карбоксигруппой С1-С3алкильную группу, а R4 представляет собой С1-С3алкил-Y2- или карбокси-С1-С3алкил-Y2-группу, при этом Y2 представляет собой углерод-азотную связь, карбонильную группу или необязательно замещенную С1-С3алкильной группой имино-группу, Rb обозначает метильную группу и Rc обозначает необязательно замещенную С1-С8алкоксикарбонильной, ацетоксиметилок-сикарбонильной, 2,2,2-трихлорэтоксикарбо-нильной, бензилоксикарбонильной либо бензо-ильной группой амидиновую группу, при этом предпочтительными являются прежде всего те из вышеуказанных соединений общей формулы I, в которых Ra находится в положении 5, их С1-С3алканоловые эфиры, их таутомеры, их стереоизомеры и их соли.
В качестве примеров наиболее предпочтительных соединений можно назвать следующие соединения из группы, включающей (а) 2-(4-амидинофениламинометил)-1-метил-5-[1-(пирролидин-1-илкарбонил)циклопропил]бензимидазол, (б) (E/Z)-2-(4-амидинофениламинометил)1-метил-5-[1-[(пиридин-2-ил)-(карбоксиметил-оксиимино)метилен]циклопропил]бензимидазол, (в) 2-(4-амидинофениламинометил)-1-метил-5-[1-(2-карбоксиэтиламино)-1-(пирролидин1-илкарбонил)этил]бензимидазол, (г) 2-(4-амидинофениламинометил)-1-метил-5-[1-[2-(2-карбоксиэтил)пирролидин-1-илкарбонил]циклопропил]бензимидазол,
(д) 2-(4-амидинофениламинометил)-1-метил-5-[2-(2-карбоксиэтил)-4,5-диметилимидазол-1-илметил]бензимидазол,
(е) 2-(4-амидинофениламинометил)-1-метил-5-[1-(карбоксиметиламино)-1-(пирроли-дин-1-илкарбонил)этил]бензимидазол и
(ж) 2-(4-амидинофениламинометил)-1-метил-5-[1-(N-метилкарбоксиметилкарбонил-аминометил)-1-метил-1-(пирролидин-1-илкар-
бонил)этил]бензимидазол,
а также их С1-С3алканоловые эфиры, их N-(С1-С8алкоксикарбонил)-, N-бензилоксикарбо-нил- и N-бензоиламидины, их таутомеры, их стереоизомеры и их соли.
Согласно изобретению соединения общей формулы I получают по известным способам, например по следующим способам
а) Для получения соединения общей формулы I, в которой Rc представляет собой цианогруппу, циклизуют образующееся при определенных условиях в реакционной смеси соединение общей формулы II
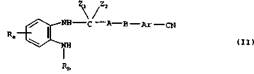 в которой
в которой
Ra, Rb, Ar, А и В имеют значения, указанные выше,
Z1 и Z2 могут быть идентичными либо разными и обозначают необязательно замещенные алкильными группами с 1-6 атомами углерода амино-, гидрокси- либо меркаптогруппы или
Z1 и Z2 вместе обозначают атом кислорода либо серы, необязательно замещенную алкильной группой с 1-3 атомами углерода имино-группу, алкилендиокси- либо алкилендитио-группу соответственно с 2 или 3 атомами углерода.
Циклизацию целесообразно осуществлять в растворителе либо в смеси растворителей, таких как этанол, изопропанол, ледяная уксусная кислота, бензол, хлорбензол, толуол, ксилол, гликоль, монометиловый эфир гликоля, димети-ловый эфир диэтиленгликоля, сульфолан, диме-тилформамид, тетралин или с использованием избытка ацилирующего агента, применяемого для получения соединения общей формулы II, например, в соответствующем нитриле, ангидриде, галогенангидриде кислоты, сложном эфире или амиде, например при температурах в интервале от 0 до 250°С, предпочтительно, однако, при температуре кипения реакционной смеси, необязательно в присутствии агента конденсации, такого как оксихлорид фосфора, тионил-хлорид, сульфурилхлорид, серная кислота, п-толуолсульфокислота, метансульфокислота, соляная кислота, фосфорная кислота, полифосфорная кислота, уксусная кислота, ангидрид уксусной кислоты, N,N-дициклогексилкарбо-диимид, или необязательно в присутствии основания, такого как этилат калия либо трет-бутилат калия. Циклизацию, однако, можно проводить и без растворителя и/или агента конденсации.
Особенно предпочтительно осуществлять реакцию таким образом, чтобы получить соединение общей формулы II в реакционной смеси восстановлением соответствующего о-нитросо-единения, необязательно в присутствии карбо-новой кислоты общей формулы III
HO-CO-A-B-Ar-CN (III),
в которой Аr, А и В имеют указанные выше значения, и ацилированием образующегося при определенных условиях в реакционной смеси аминосоединения.
б) Для получения соединения общей формулы I, в которой Ra обозначает R2-СХ'-С3-С5 циклоалкиленовую группу, где R2 имеет значения, указанные выше, а X' представляет собой одну из вышеуказанных для Х иминогрупп, соединение общей формулы IV
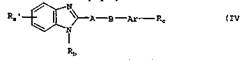
в которой Rb, Rc, Аr, А и В имеют значения, указанные выше, a Ra' представляет собой R2-СО-С3-С5циклоалкиленовую группу, где R2 имеет значения, указанные выше, подвергают взаимодействию с амином общей формулы V Н2Х' (V) в которой X' представляет собой одну из вышеуказанных для Х иминогрупп.
Реакцию целесообразно проводить в растворителе, таком как метанол/толуол, этанол, изопропанол или ксилол, и предпочтительно в присутствии обезвоживающего агента, такого как молекулярное сито, сульфат натрия или хлорид кальция, необязательно в присутствии основания, такого как триэтиламин, при температурах в интервале от 50 до 100°С, предпочтительно при температуре кипения реакционной смеси.
в) Для получения соединения общей формулы I, в которой Ra обозначает R2-СХ"-С3-С5циклоалкиленовую группу, где R2 имеет значения, указанные выше, а X" представляет собой одну из указанных выше для Х алкилиденовых групп, соединение общей формулы IV
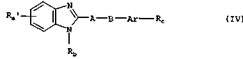
в которой Rb, Rc, Ar, А и В имеют значения, указанные выше, a Ra' представляет собой R2-СО-С3-С5циклоалкиленовую группу, где R2 имеет значения, указанные выше, подвергают взаимодействию с фосфоном общей формулы VI Z3-HX" (VI)
в которой X" представляет собой одну из указанных выше для Х алкилиденовых групп, a Z3 представляет собой трифенилфосфоновую либо ди(С1-С3алкокси)фосфоновую группу, такую как триэтоксифосфоновая группа.
Реакцию предпочтительно проводить в атмосфере защитного газа в растворителе, таком как тетрагидрофуран, диметилформамид, диоксан, диэтиловый эфир или диметилсульфоксид, в присутствии основания, такого как трет-бутилат калия, метилат натрия или гидрид натрия, при температурах в интервале от -25 до 50°С, предпочтительно в интервале от -15°С до комнатной температуры.
г) Для получения соединения общей формулы I, в которой Rс представляет собой амидиновую группу, которая может быть замещена одной либо двумя С1-С3алкильными группами, образующееся при определенных условиях в реакционной смеси соединение общей формулы VII.
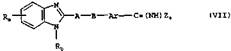
в которой Ra, Rb, Аr, А и В имеют указанные выше значения, а Z4 представляет собой алкокси- либо аралкоксигруппу, такую как метокси-, этокси-, н-пропокси-, изопропокси- или бензилоксигруппа, или представляет собой ал-килтио- либо аралкилтиогруппу, такую как ме-тилтио-, этилтио-, н-пропилтио- или бензилтиогруппа, подвергают взаимодействию с амином общей формулы VIII
H-R7NR8 (VIII),
в которой R7 и R8 могут быть идентичными либо разными и обозначают соответственно атом водорода или С1-С3алкильную группу, либо осуществляют взаимодействие с его солями.
Эту реакцию целесообразно проводить в растворителе, таком как метанол, этанол, н-пропанол, тетрагидрофуран или диоксан, при температурах в интервале от 0 до 150°С, предпочтительно при температурах в интервале от 0 до 80°С, осуществляя при этом взаимодействие с указанным выше амином общей формулы VIII либо с соответствующей кислотно-аддитивной солью, такой как карбонат аммония или ацетат аммония.
Соединение общей формулы VII получают, например, взаимодействием соответствующего цианосоединения с соответствующим спиртом, таким как метанол, этанол, н-пропанол, изопропанол или бензиловый спирт, в присутствии кислоты, такой как соляная кислота, либо взаимодействием соответствующего амида с солью триалкилоксония, такой как тетрафторборат триэтилоксония, в растворителе, таком как метиленхлорид, тетрагидрофуран или диоксан, при температурах в интервале от 0 до 50°С, предпочтительно, однако, при 20°С, либо взаимодействием соответствующего нитрила с сероводородом, предпочтительно в растворителе, таком как пиридин или диметилформамид, и в присутствии основания, такого как триэтила-мин, и последующим алкилированием образовавшегося тиоамида соответствующим алкил- или аралкилгалогенидом.
д) Для получения соединения общей формулы I, в которой Ra представляет собой имида-золидин-2,4-дион-5-ильную группу, которая может быть замещена одной либо двумя С1-С3 алкильными группами, при этом одновременно алкильный заместитель может быть замещен карбокси- либо С1-С3алкоксикарбонильной группой, циклизуют образующееся при определенных условиях в реакционной смеси соединение общей формулы IX
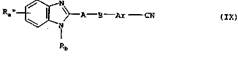
в которой Rb, Ar, А и В имеют значения, указанные выше, a Ra" представляет собой ами-нокарбониламиногруппу, замещенную в положении 3 С1-С3алкоксикарбонил-С1-С3алкильной группой.
Эту реакцию целесообразно проводить в растворителе, таком как метанол, этанол, н-пропанол, изопропанол или бензиловый спирт, в присутствии кислоты, такой как соляная кислота, при температурах в интервале от 0 до 50°С, предпочтительно, однако, при 20°С.
е) Для получения соединения общей формулы I, в которой Rc представляет собой гидроксиамидиновую группу, нитрил общей формулы
Х
в которой Ra, Rb, Аr, А и В имеют указанные выше значения, подвергают взаимодействию с гидроксиламином либо его солями.
Эту реакцию целесообразно проводить в растворителе, таком как метанол, этанол, н-пропанол, вода, метанол/вода, тетрагидрофуран, тетрагидрофуран/вода, диоксан или диоксан/вода, при температурах в интервале от 0 до 150°С, предпочтительно в интервале от 0 до 80°С.
ж) Для получения соединения общей формулы I, в которой Ra содержит карбоксигруппу, a Rc имеет значения, указанные выше, или Raимеет значения, указанные выше, a Rc представляет собой необязательно замещенную гидроксигруппой либо одной или двумя С1-С3 алкильными группами амидиновую группу, соединение общей формулы XI
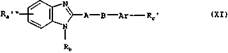
в которой Rb, Ar, А и В имеют значения, указанные выше, а Ra"' и Rc' имеют значения, указанные выше для Ra и Rc соответственно, при условии, что Ra содержит группу, переводимую путем гидролиза, обработки кислотой либо основанием, путем термолиза или гидрогенолиза в карбоксигруппу, a Rc имеет значения, указанные выше, или Rc представляет собой группу, переводимую путем гидролиза, обработки кислотой либо основанием, путем термолиза или гидрогенолиза в необязательно замещенную гидро-ксигруппой либо одной или двумя С1-С3алкильными группами амидиновую группу, a Ra имеет значения, указанные выше, переводят путем гидролиза, обработки кислотой либо основанием, путем термолиза или гидрогенолиза в соединение общей формулы I, в которой Ra содержит карбоксигруппу, a Rc имеет значения, указанные выше, или Ra имеет значения, указанные выше, a Rc представляет собой необязательно замещенную гидроксигруппой либо одной или двумя С1-С3алкильными группами амидиновую группу.
В качестве группы, переводимой в карбоксигруппу, могут рассматриваться среди прочих защищенная защитной группой карбоксильная группа, в том числе ее функциональные производные, например ее незамещенные или замещенные амиды, сложные эфиры, тиоэфиры, триметилсилиловые эфиры, ортоэфиры либо иминоэфиры, которые целесообразно переводить в карбоксильную группу путем гидролиза, ее сложные эфиры с третичными спиртами, например трет-бутиловый эфир, которые целесообразно переводить в карбоксильную группу путем обработки кислотой либо путем термолиза, и ее сложные эфиры с аралканолами, например бензиловый эфир, которые целесообразно переводить в карбоксильную группу путем гидрогенолиза.
Гидролиз целесообразно осуществлять либо в присутствии кислоты, такой как соляная кислота, серная кислота, фосфорная кислота, уксусная кислота, трихлоруксусная кислота, трифторуксусная кислота, или их смесей, либо в присутствии основания, такого как гидроксид лития, гидроксид натрия или гидроксид калия, в соответствующем растворителе, таком как вода, вода/метанол, вода/этанол, вода/изопропанол, метанол, этанол, вода/тетрагидрофуран или во-да/диоксан, при температурах в интервале от -10 до 120°С, например при температурах в интервале от комнатной температуры до температуры кипения реакционной смеси.
Если соединение формулы XI содержит, например, трет-бутильную или трет-бутилоксикарбонильную группу, то эти группы можно отщеплять также путем обработки кислотой, такой как трифторуксусная кислота, муравьиная кислота, п-толуолсульфокислота, серная кислота, соляная кислота, фосфорная кислота или полифосфорная кислота, необязательно в инертном растворителе, таком как ме-тиленхлорид, хлороформ, бензол, толуол, ди-этиловый эфир, тетрагидрофуран или диоксан, предпочтительно при температурах в интервале от -10 до 120°С, например при температурах в интервале от 0 до 60°С, или же путем термообработки, необязательно в инертном растворителе, таком как метиленхлорид, хлороформ, бензол, толуол, тетрагидрофуран или диоксан, и предпочтительно в присутствии каталитического количества кислоты, такой как п-толуолсульфокислота, серная кислота, фосфорная кислота или полифосфорная кислота, предпочтительно при температуре кипения используемого растворителя, например при температурах в интервале от 40 до 120°С.
Если соединение формулы XI содержит, например, бензилокси- или бензилоксикарбо-нильную группу, то эти группы можно также отщеплять путем гидрогенолиза в присутствии катализатора гидрирования, такого как палладий на угле, в соответствующем растворителе, таком как метанол, этанол, этанол/вода, ледяная уксусная кислота, этиловый эфир уксусной кислоты, диоксан или диметилформамид, предпочтительно при температурах в интервале от 0 до 50°С, например при комнатной температуре, и при давлении водорода 1-5 бар.
з) Для получения соединения общей формулы I, в которой Rc представляет собой амидиновую группу, замещенную одной или двумя С1-С8алкоксикарбонильными группами либо отщепляемым in vivo остатком, соединение общей формулы XII
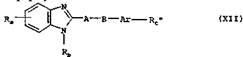
в которой Ra, Rb, Аr, А и В имеют значения, указанные выше, a Rc" обозначает амидиновую группу, подвергают взаимодействию с соединением общей формулы XIII Z5-R9 (XIII) в которой R9 представляет собой С1-С8алкоксикарбонильную группу или ацильную группу одного из указанных выше отщепляемых in vivo остатков, a Z5 обозначает нуклеофобную уходящую группу, такую как атом галогена, например атом хлора, брома либо иода, или обозначает п-нитрофенильную группу.
Эту реакцию целесообразно проводить в растворителе, таком как метанол, этанол, мети-ленхлорид, тетрагидрофуран, толуол, диоксан, диметилсульфоксид или диметилформамид, необязательно в присутствии неорганического либо третичного органического основания, предпочтительно при температурах в интервале от 20°С до температуры кипения используемого растворителя.
Взаимодействие с соединением общей формулы XIII, в которой Z5 представляет собой нуклеофобную уходящую группу, предпочтительно проводить в растворителе, таком как ме-тиленхлорид, ацетонитрил, тетрагидрофуран, толуол, ацетон/вода, диметилформамид или ди-метилсульфоксид, необязательно в присутствии основания, такого как гидрид натрия, карбонат калия, трет-бутилат калия или N-этилдиизопропиламин, при температурах в интервале от 0 до 60°С.
Если согласно изобретению получают соединение общей формулы I, содержащее в своем составе (R3NR4)-С1-С3алкильную группу, в которой, по меньшей мере, один из остатков R3 или R4 представляет собой атом водорода, то его можно переводить затем с помощью соответствующего изоцианата или карбамоилгало-генида в соответствующее карбамидное соединение общей формулы I и/или если получают соединение общей формулы I, содержащее в своем составе NН2-С1-С3алкильную группу, то его можно затем переводить с помощью соответствующего эфира акриловой кислоты в соответствующее 2-(С1-С3алкоксикарбонил)этильное соединение общей формулы I и/или если получают соединение общей формулы I, содержащее в своем составе (R3NR4)-С1-С3алкильную группу, в которой R3 и R4 представляют собой соответственно атом водорода, то его можно затем переводить с помощью соответствующего дигалогеналкана в соответствующее соединение общей формулы I, в которой R3 и R4 вместе с расположенным между ними атомом азота представляют собой соответствующую 4-7-членную циклоалкилениминогруп-пу, и/или если получают соединение общей формулы I, в которой Rс представляет собой амидиновую группу, то его можно затем переводить с помощью производного галогенуксусной кислоты и последующими гидролизом и декарбоксилированием в соответствующее замещенное одной либо двумя метильными группами амидиновое соединение, и/или если получают соединение общей формулы I, в которой Rс представляет собой гидроксиамидиновую группу, то его можно затем переводить путем каталитического гидрирования в соответствующее амидиновое соединение, и/или если получают соединение общей формулы I, в которой Rа содержит карбоксигруппу, то его можно затем переводить этерифицированием в соответствующий сложный эфир.
Указанный выше последующий процесс получения соответствующего карбамидного соединения общей формулы I целесообразно осуществлять с использованием соответствующего изоцианата или карбамоилхлорида, предпочтительно в растворителе, таком как диме-тилформамид, и необязательно в присутствии третичного органического основания, такого как триэтиламин, при температурах в интервале от 0 до 50°С, предпочтительно при комнатной температуре.
Указанный выше последующий процесс получения соответствующего 2-(С1-С3алкокси-карбонил)этильного соединения целесообразно осуществлять с использованием соответствующего эфира акриловой кислоты, предпочтительно в растворителе, таком как метанол, этанол или изопропанол, при температурах в интервале от 50 до 100°С, предпочтительно при температуре кипения реакционной смеси.
Указанный выше последующий процесс получения соответствующего 4-7-членного цик-лоалкилениминосоединения общей формулы I целесообразно осуществлять с использованием соответствующего дигалогеналкана, предпочтительно в растворителе, таком как метанол, этанол или изопропанол, в присутствии основания, такого как карбонат натрия, при температурах в интервале от 50 до 100°С, предпочтительно при температуре кипения реакционной смеси.
Указанное выше последующее алкилирование целесообразно осуществлять в растворителе, таком как метиленхлорид, тетрагидрофу-ран, диоксан, диметилсульфоксид, диметил-формамид или ацетон, необязательно в присутствии ускорителя реакции, такого как иодид натрия или калия, и предпочтительно в присутствии основания, такого как карбонат натрия или карбонат калия, либо в присутствии третичного органического основания, такого как N-этилдиизопропиламин или N-метилморфолин, которые одновременного могут служить и растворителями, либо необязательно в присутствии карбоната серебра или оксида серебра, при температурах в интервале от -30 до 100°С, предпочтительно, однако, при температурах в интервале от -10 до 80°С.
Указанный выше последующий гидролиз целесообразно осуществлять либо в присутствии кислоты, такой как соляная кислота, серная кислота, фосфорная кислота, уксусная кислота, трихлоруксусная кислота, трифторуксусная кислота, или их смесей, либо в присутствии основания, такого как гидроксид лития, гидроксид натрия или гидроксид калия, в соответствующем растворителе, таком как вода, вода/метанол, вода/этанол, вода/изопропанол, метанол, этанол, вода/тетрагидрофуран или вода/диоксан, а последующее декарбоксилирование осуществлять в присутствии кислоты из числа вышеназванных, при температурах в интервале от -10 до 120°С, например при температурах в интервале от комнатной температуры до температуры кипения реакционной смеси.
Последующую этерификацию целесообразно осуществлять с использованием соответствующего спирта, предпочтительно в растворителе либо в смеси растворителей, таких как метиленхлорид, бензол, толуол, хлорбензол, тетрагидрофуран, бензол/тетрагидрофуран или диоксан, предпочтительно, однако, применяя избыток используемого спирта, необязательно в присутствии кислоты, такой как соляная кислота, или же в присутствии обезвоживающего агента, например в присутствии изобутилового эфира хлормуравьиной кислоты, тионилхлорида, триметилхлорсилана, соляной кислоты, серной кислоты, метансульфокислоты, п-толуолсульфокислоты, трихлорида фосфора, пентоксида фосфора, N,N'-дициклогексил-карбодиимида, N,N'-дициклогексилкарбоди-имида/N-гидроксисукцинимида, N,N'-карбонил-диимидазола либо N,N'-тионилдиимидазола, трифенилфосфина/тетрахлорметана или трифенилфосфина/диэтилового эфира азодикарбоно-вой кислоты, необязательно в присутствии основания, такого как карбонат калия, N-этилдиизопропиламин или N,N-диметилами-нопиридин, предпочтительно при температурах в интервале от 0 до 150°С, более предпочтительно при температурах в интервале от 0 до 80°С, или же этерификацию осуществлять с использованием соответствующего галогенида в растворителе, таком как метиленхлорид, тетра-гидрофуран, диоксан, диметилсульфоксид, ди-метилформамид или ацетон, необязательно в присутствии ускорителя реакции, такого как иодид натрия или калия, и предпочтительно в присутствии основания, такого как карбонат натрия или карбонат калия, либо в присутствии третичного органического основания, такого как N-этилдиизопропиламин или N-метил-морфолин, которые одновременно могут служить и растворителями, либо необязательно в присутствии карбоната серебра или оксида серебра при температурах в интервале от -30 до 100°С, предпочтительно, однако, при температурах в интервале от -10 до 80°С.
В описанных выше реакциях в ходе их проведения для необязательно имеющихся ре-акционноспособных групп, таких как гидрокси-, карбокси-, амино-, алкиламино- или имино-группы, можно предусмотреть обычные защитные группы и по завершении реакции снова их отщеплять.
В качестве защитной группы для гидроксигруппы может использоваться, например, триметилсилильная, ацетильная, бензоильная, трет-бутильная, тритильная, бензильная или тетрагидропиранильная группа, в качестве защитной группы для карбоксильной группы - триметилсилильная, метильная, этильная, трет-бутильная, бензильная или тетрагидропиранильная группа, ав качестве защитной группы для амино-, алкиламино- или иминогруппы -ацетильная, трифторацетильная, бензоильная, этоксикарбо-нильная, трет-бутоксикарбонильная, бензилок-сикарбонильная, бензильная, метоксибензиль-ная или 2,4-диметоксибензильная группа, а для аминогруппы, помимо названных, можно использовать и фталильную группу.
В случае использования защитных групп их последующее отщепление можно осуществлять, например, гидролитическим путем в водном растворителе, например в воде, изопропаноле/воде, тетрагидрофуране/воде или диокса-не/воде, в присутствии кислоты, такой как трифторуксусная кислота, соляная кислота или серная кислота, либо в присутствии основания щелочного металла, такого как гидроксид лития, гидроксид натрия или гидроксид калия, или же отщеплением группы простого эфира, например, в присутствии иодтриметилсилана, при температурах в интервале от 0 до 100°С, предпочтительно при температурах в интервале от 10 до 50°С.
В отличие от вышеописанного бензильную, метоксибензильную или бензилоксикарбонильную группу отщепляют, например, путем гидрогенолиза с помощью, например, водорода, в присутствии катализатора, такого как палладий на угле, в растворителе, таком как метанол, этанол, этиловый эфир уксусной кислоты, диметилформамид, диметилформамид/ацетон или ледяная уксусная кислота, необязательно с добавлением кислоты, такой как соляная кислота, при температурах в интервале от 0 до 50°С, предпочтительно, однако, при комнатной температуре, и при давлении водорода в пределах от 1 до 7 бар, предпочтительно, однако, в пределах от 3 до 5 бар.
Отщепление метоксибензильной группы можно осуществлять также в присутствии окислителя, такого как аммонийнитрат церия (IV), в растворителе, таком как метиленхлорид, ацетонитрил или ацетонитрил/вода, при температурах в интервале от 0 до 50°С, предпочтительно, однако, при комнатной температуре.
Отщепление же 2,4-диметоксибензильной группы предпочтительно осуществлять в трифторуксусной кислоте в присутствии анизола.
Отщепление трет-бутильной или трет-бутилоксикарбонильной группы предпочтительно осуществлять путем обработки кислотой, такой как трифторуксусная кислота или соляная кислота, необязательно с использованием растворителя, такого как метиленхлорид, диоксан или простой эфир.
Отщепление фталильной группы предпочтительно осуществлять в присутствии гидразина или первичного амина, такого как метиламин, этиламин или н-бутиламин, в растворителе, таком как метанол, этанол, изопропанол, толуол/вода или диоксан, при температурах в интервале от 20 до 50°С.
Отщепление аллилоксикарбонильной группы осуществляют путем обработки каталитическим количеством тетракис(трифенилфос-фин)палладия (0), предпочтительно в растворителе, таком как тетрагидрофуран, и предпочтительно в присутствии избытка основания, такого как морфолин или 1,3-димедон, при температурах в интервале от 0 до 100°С, предпочтительно при комнатной температуре и в атмосфере инертного газа, либо путем обработки каталитическим количеством хлорида трис (трифе-нилфосфин)родия (I) в растворителе, таком как водный этанол, и необязательно в присутствии основания, такого как 1,4-диазаби-цикло[2,2,2]октан, при температурах в интервале от 20 до 70°С.
Список литературы
1. Терней А. Современная органическая химия: В 2 т. - М.: Мир, 1981. - Т.1 - 670 с; Т.2 - 615 с.
2. В. Ф. Травень. Органическая химия. Том 1. – М.: Академкнига, 2004, - 708 с.
3. Общая органическая химия. Карбоновые кислоты и их производные. Том 4. М., Химия, 1983, 729с.
4. Богословский Б.Н., Казакова З.С. Скелетные катализаторы, их свойства и применение в органической химии. М., Госхимиздат, 1957.
5. Голодников Г.В. Практические работы по органическому синтезу. Л., Изд-во ЛГУ, 1966, 697с.
6. Дорофеенко Г.Н., Жданов Ю.А., Дуленко В.И. и др. Хлорная кислота и ее соединения ворганическом синтезе. Ростов, изд-во Ростовского ун-та, 1965.
7. Голодников Г.В., Низовкина Т.В., Рыскальчук А.Т. Практикум по органическому синтезу. Л., Изд-во ЛГУ, 1967.
8. Крешков А.П., Курбатов И.Н. Лабораторные работы по синтезу и анализу органических соеднений. М., изд-во Артиллерийского ордена Ленина академии Красной армии им. Дзержинского, 1940.
9. Лабораторные работы по органической химии. Изд. 3-е. М., Высшая школа, 1974.
10. Шабаров Ю.С. Органическая химия: В 2-х кн. - М.:Химия, 1994.- 848 с.
11. Петров А.А., Бальян Х.В., Трощенко А.Т. Органическая химия. – М.: Высш. шк., 1973. - 623 с.
12. Препаративная органическая химия. Изд. 2-е, М., Госхимиздат, 1964.
13. Храмкина М.Н. Практикум по органическому синтезу. Изд. 4-ое, Л., Химия. 1977.
0 комментариев