Навигация
Возбуждение, ионизация и отклоняющееся напряжение атома. Схемы энергоуровней
БЕЛОРУССКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ ИНФОРМАТИКИ И РАДИОЭЛЕКТРОНИКИ
Кафедра ЭТТ
РЕФЕРАТ
На тему:
«Возбуждение, ионизация и отклоняющееся напряжение атома. Схемы энергоуровней»
МИНСК, 2008
1. Строение атома
Согласно модели Бора, которая еще мало изменилась к настоящему времени, атом состоит из ядра весьма малого размера (диаметр его равен примерно 10-12 см) и отрицательно заряженной электронной оболочки. В ядре сосредоточено более чем 99,9% всей массы частицы. Положительный заряд ядра атома содержит увеличенный в целое число раз элементарный заряд (e = 1,6*10-19 а*сек); при этом заряд ядра изменяется от одного элементарного заряда (у первого из известных элементов) до 105 элементарных зарядов у последнего 105-го элемента. Так как атомы по отношению к внешнему пространству оказываются нейтральными, то число элементарных зарядов ядра равно числу электронов оболочки атома.
Образование свободных электронов достигается освобождением их из электронной оболочки атома. Электроны окружают ядро атома не хаотично, а согласно определенному закону, именно они закономерно распределены по системе «оболочек», число которых доходит до 7 (таких оболочек у Н - одна; у Ar - 3 [рис.1], у Hg – 6 и у U – 7); эти оболочки при переходе от внутренних к внешним обозначаются буквами от К до Q (K-, L-, М-оболочки и т. д.). В понятие «электронные оболочки» вкладывается также энергетический смысл; обозначения различных электронных оболочек являются одновременно символами для обозначения возможных энергетических состояний электронов в атоме.Эта модель дает лишь весьма грубое представление о действительных взаимосвязях, имеющих место в атоме, так как отдельные энергетические уровни в свою очередь подразделяются на подуровни, достаточно близко расположенные друг от друга.Таким образом, каждый электрон данного атома в каждой оболочке обладает определенной потенциальной энергией Еп. Величина энергии растет с увеличением радиуса оболочки (т. е. по мере удаления от ядра): сначала быстро, затем медленнее и, наконец, приближается к некоторой предельной величине, соответствующей энергии свободного электрона, покинувшего атом.
Если атому сообщить некоторое количество энергии извне, то электроны могут преодолеть силы притяжения ядра и перейти с внутренних оболочек на внешние с более высокой потенциальной энергией, которые остаются не занятыми, если к атому не подводится извне дополнительная энергия. В этом случае атом не находится более в нормальном состоянии; его состояние будет теперь возбужденным. В возбужденном состоянии атом находится лишь очень короткий промежуток времени; спустя 10-8 – 10-9 секунды все перешедшие на внешние оболочки электроны переходят обратно на нормальные для них уровни или даже на ниже расположенные уровни с меньшей потенциальной энергией. Отдаваемая электронами при этом энергия выделяется в виде электромагнитного излучения. Согласно закону сохранения энергии каждый переход электрона сопровождается испусканием фотона. Энергия фотона hv (h - постоянная Планка, v - частота испускаемого света) должна быть равна разности E1 – Е2 энергий электрона до и после перехода с одного уровня на другой:
![]() (1)
(1)
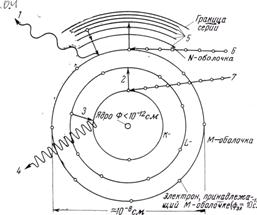
Рис. 1. Энергетические уровни свободного изолированного атома (Ar) и возможные процессы перехода электронов при соударении.
1 - испускание кванта света (с энергией hv); 2 - эмиссия электрона из K-оболочки при соударении с частицами; 3 - переход электрона с L-оболочки на K-оболочку с одновременным испусканием рентгеновского кванта (в результате отдачи энергии); 4 - испускание рентгеновского кванта; 5 - возбужденные уровни электронов на внешней электронной оболочке; 6 - соударение с частицами с энергией в несколько эв; 7 - соударение с частицами с энергией в несколько сот кэв (например, с электронами или квантами рентгеновского излучения).
Таким образом, в свободном атоме возможны только вполне определенные энергетические уровни Е1, Е2, ..., Еn; все остальные энергетические состояния запрещены. Поэтому поглощение излучения или его испускание возможно только при вполне определенных частотах или соответственно при определенных длинах волн. Отсюда ясно происхождение линейчатого спектра излучения или поглощения атома.
Разность энергий электронов, находящихся в двух соседних оболочках атома, уменьшается с увеличением радиуса оболочек. Поэтому в том случае, если переход электрона происходит между двумя удаленными от ядра оболочками (занятыми или свободными), то спектральные линии возникшего излучения лежат в инфракрасной, видимой или ультрафиолетовой областях спектра («оптический спектр») с относительно малой энергией квантов света. Если же переход осуществляется между внутренними, близко расположенными к ядру оболочками, то происходит испускание излучения, лежащего в рентгеновской области спектра, со значительно большей энергией квантов. Поэтому близкие к ядру оболочки К, L и М называют также рентгеновскими уровнями.
Атомы различных элементов отличаются лишь тем, что с увеличением заряда ядра все большее число разрешенных энергетических уровней (оболочек) оказывается занятым электронами. При этом в первую очередь заполняются оболочки, расположенные вблизи ядра атома. Для каждой оболочки существует вполне определенное максимально возможное число заполняющих ее электронов.
Испускание электронов из внутренних оболочек происходит лишь в том случае, если атому передается большая по величине энергия, поскольку электроны внутренних оболочек находятся под действием значительных сил притяжения со стороны атомного ядра. Необходимая для испускания электронов внешней оболочки атомов (называемых также валентными электронами) энергия напротив невелика, так как силы притяжения их к ядру не столь значительны по сравнению с внутренними электронами. Для инертных газов, внешняя оболочка которых полностью занята электронами, требуется большая затрата энергии на испускание электронов, чем у элементов с частично заполненными внешними оболочками.
0 комментариев