Навигация
Расчет материального баланса процесса получения метанола, интенсивности работы катализатора, часовой производительности установки (вариант 1.1)
6. Расчет материального баланса процесса получения метанола, интенсивности работы катализатора, часовой производительности установки (вариант 1.1).
В результате процесса происходят следующие процессы:
1) СО + 2Н2 = СН3ОН + Q
2) СО + 3Н2 = СН4 + Н2О
3) 2СО + 2Н2 = СН4 + СО2
4) 2СО = СО2 + С
5) СО + Н2 = НСНО
6) 2СН3ОН = (СН3)2О + Н2О
7) СН3ОН + Н2 = СН4 + Н2О
Данные для расчета:
1. Рабочий объем катализатора – 24 м3.
2. Расход окиси углерода и метанола на побочные продукты:
СО СН3О
Реакция 2 – 3,8 Реакция 6 – 1,9
Реакция 3 – 4,1 Реакция 7 – 0,5
Реакция 4 – 2,5
Реакция 5 – 0,7
Температура Т = 643 К
Давление Р = 36,5 МПа
Объемная скорость ![]()
Мольное соотношение Н2 : СО = 6,2 : 1
3. База для расчета – 1 час работы установки.
Решение:
1. Рассчитаем объем синтез-газа, подаваемый за 1 час в реактор.
Пересчитаем объем газа из нормальных условий в условия реактора:
![]()
где р, V, Т – соответственно давление, объем при данной температуре,
р0, V0 – давление и объем при нормальных условиях.
Отсюда
![]()
![]()
Тогда учитывая объем катализатора, объем синтез-газа будет равен:
![]() м3/ч
м3/ч
2. Зная мольные отношения, определим массы Н2 и СО2, подаваемые в реактор за 1 час.
Зная, что при нормальных условиях 1 моль любого газа занимает объем 22,4 л (0, 224 м3 ), определим количество молей водорода и оксида углерода:
![]() моль
моль
Тогда количества молей газов составят:
![]() моль/ч
моль/ч
![]() моль/ч
моль/ч
Массовый расход водорода составит
![]() 26,57 · 106 · 2 = 53,14 · 106 г/ч = 53,14 · 103 кг/ч
26,57 · 106 · 2 = 53,14 · 106 г/ч = 53,14 · 103 кг/ч
![]() 4,29 · 106 · 28 = 120 · 106 г/ч = 120 · 103 кг/ч
4,29 · 106 · 28 = 120 · 106 г/ч = 120 · 103 кг/ч
3. Расход окиси углерода на побочные и прямую реакции составит:
На реакцию 2 m (СО) = 120000 · 0,038 = 4560 кг/ч
На реакцию 3 m (СО) = 120000 · 0,041 = 4920 кг/ч
На реакцию 4 m (СО) = 120000 · 0,025 = 3000 кг/ч
На реакцию 5 m (СО) = 120000 · 0,007 = 840 кг/ч
Тогда на прямую реакцию будет израсходовано СО:
m (СО) = 120000 - 4560 – 4920 – 3000 – 840 = 106 680 кг/ч
4. Рассчитаем массу метанола исходя из уравнения реакции (1):
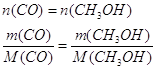
![]() кг/ч
кг/ч
5. Рассчитаем массу метанола, реагирующего по побочным реакциям и метанола, полученного в виде продукта:
На реакцию 6 m(СН3ОН) = 121 920 · 0,019 = 2316,5 кг/ч
На реакцию 7 m(СН3ОН) = 121 920 · 0,005 = 609,6 кг/ч
Тогда в качестве продукта будет получено метанола:
m(СН3ОН) = 121920 – 2316,5 - 609,6 = 118993,9 кг/ч
6.Проведем балансовые расчеты по основной и побочным реакциям:
Реакция 1:
Расход водорода составит:
![]() кг/ч
кг/ч
Реакция 2:
Расход водорода составит:
![]() 977,1 кг/ч
977,1 кг/ч
будет получено метана:
![]() кг/ч
кг/ч
будет получено воды:
![]()
Реакция 3:
Расход водорода составит:
![]() кг/ч
кг/ч
Будет получено метана:
![]() кг/ч
кг/ч
Будет получено диоксида углерода:
![]() кг/ч
кг/ч
Реакция 4:
Будет получено диоксида углерода:
![]() кг/ч
кг/ч
Будет получено углерода:
![]() кг/ч
кг/ч
Реакция 5:
Израсходовано водорода:
![]() кг/ч
кг/ч
Будет получено формальдегида:
![]() кг/ч
кг/ч
Реакция 6:
Будет получено диметилового эфира:
![]() кг/ч
кг/ч
Будет получено воды:
![]() кг/ч
кг/ч
Реакция 7:
Будет израсходовано водорода:
![]() кг/ч
кг/ч
Будет получено метана:
![]() кг/
кг/
Будет получено воды:
![]() кг/ч
кг/ч
Масса непрореагировавшеговодорода составит:
m(Н2) = 53 140 – 15 240 – 977,1 – 351,4 – 60 – 38,1 = 36 473,4 кг/ч
7. Результаты расчетов сведем в таблицу материального баланса:
| Компонент | Загрузка, кг/ч | Не вступило в реакцию, кг/ч | Продукты реакции, кг/ч |
| СО Н2 СН3ОН СН4 СО2 Н2О НСНО С (СН3)2О | 120 000 53 140 | 36473,4 | 118 993,9 4316,2 6222,8 3925,8 900 642,9 1665 |
| Итого: | 173140 | 36473,4 | 136666,6 |
Составим баланс по метанолу:
| Приход | кг/ч | т/сут | Расход | кг/ч | т/сут | |
| Синтез-газ, в т. ч. Н2 СО | 53 140 120 000 | 1275,36 2880 | СН3ОН (СН3 )2О Н2О СН4 СО2 НСНО С Н2 | 118 993,9 1 665 3 925,8 4 316,2 6 222,8 900 642,9 36473,4 | 2855,85 39,96 94,22 103,59 149,35 21,6 15,43 875,36 | |
| ИТОГО | 173 140 | 4155,36 | ИТОГО | 173 140 | 4155,36 | |
2) Селективность – доля (или процент) превращенного сырья, израсходованная на образование целевого продукта:
![]()
Так как в реактор поступает 120 000 кг/ч оксида углерода, а на образование метанола израсходуется 106 680 кг/ч СО, то селективность процесса составит:
![]()
Так как расход водорода на основную реакцию составит 15 240 кг/ч, то селективность по водороду составит:
![]()
3) Расходный коэффициент - расход сырья на получение одной тонны целевого продукта. Расходный коэффициент с учетом селективности рассчитывается по уравнению:
![]()
Таким образом, расходный коэффициент оксида углерода на получение 1 тонны метанола составит:
![]() т/т
т/т
Суммарные потери водорода в % масс. на всех стадиях будет равна:
![]()
Расходный коэффициент по водороду с учетом потерь составит:
![]() т/т
т/т
4) Конверсия исходного сырья – количество превращенного сырья, отнесенное к загрузке реактора, выраженное в процентах или долях единицы. Конверсия характеризует степень превращения сырья в целевые и побочные продукты и, в конечном счете, количество сырья, подлежащего рециркуляции. Конверсию определяем по формуле:
![]()
где ![]() - количество компонента А в загрузке реактора, кг/ч
- количество компонента А в загрузке реактора, кг/ч
![]() - количество компонента А в продуктах реакции, кг/ч.
- количество компонента А в продуктах реакции, кг/ч.
Конверсия по оксиду углерода СО составит:
![]()
Конверсия по водороду составит:
![]()
Похожие работы
... металлов ведет к образованию высших спиртов,(4).Также протекает реакция Будуара (6), но только до тех пор, пока не достигнута определенная температура. Влияние вида катализатора на параметры, скорость и глубину процесса Синтез метанола на цинк-хромовом катализаторе В 1923 г. фирмой BASF было предложено проводить синтез метанола на цинк-хромовом катализаторе. На этом катализаторе процесс ...
... опасность перегрева катализатора, кроме того, процесс восстановления можно вести без циркуляционных компрессоров. Пробег промышленного цинк-хромового катализатора в значительной степени определяется условиями восстановления катализатора и процесса синтеза метанола на нем. В начальной стадии развития производств метанола, когда в качестве сырья использовали водяной газ со значительным ...
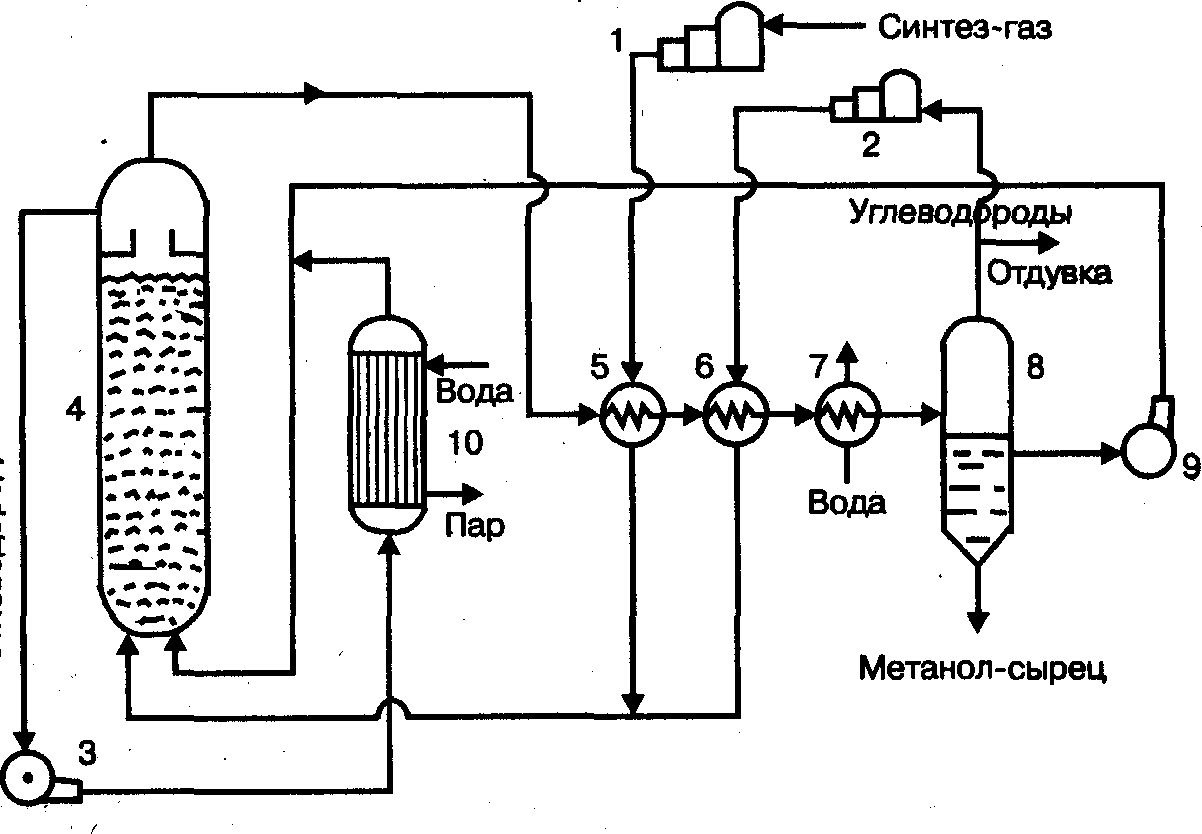
... с циркуляционным газом, который поджимается до рабочего давления в компрессоре 2. Газовая смесь проходит через адсорбер. Высшие спирты Рис. 1. Технологическая схема производства метанола при низком давлении: 1 — турбокомпрессор, 2 — циркуляционный компрессор, 3, 7 —холодильники, 4 — сепаратор, 5 — адсорбер, 6 — реактор адиабатического действия, б — ...
... эту высокую стоимость. К тому же метанол сильно ядовит. Что касается дизельных двигателей, то в них можно использовать продукт разложения метанола – ДМЭ. 4. Получение диметилового эфира дегидратацией метанола Дегидратация метанола с получением диметилового эфира-исторически первый путь проведения данного синтеза. Этому процессу ещё с 1960-х годов было посвящено множество работ советских и ...
0 комментариев