Навигация
Конденсации, при которых в готовый углеродный скелет вводится атом азота при помощи аммиака или аминов
2.1.2. Конденсации, при которых в готовый углеродный скелет вводится атом азота при помощи аммиака или аминов.
Наиболее важной в этой группе реакций является взаимодействие 1,4-дикарбонильных соединений с аммиаком по Паалю-Кнорру [19,23]. Механизм реакции, очевидно, включает нуклеофильное присоединение аммиака к двум карбонильным атомам углерода и последующее отщепление двух молекул воды [24].
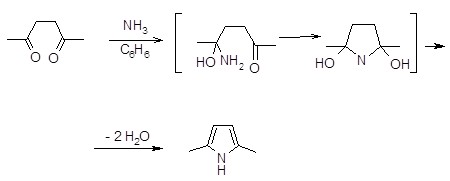
Отмечено также, что реакция может протекать с ацетатом аммония c хорошим выходом (~ 70%), причем, чем более электроноакцепторные заместители в 1,4-дикетоне, тем в более жестких условиях протекает реакция [25].
К этой же группе реакций можно отнести получение пирролов по Ганчу из a‑галогенкетонов, b-кетоэфиров и аммиака [26].
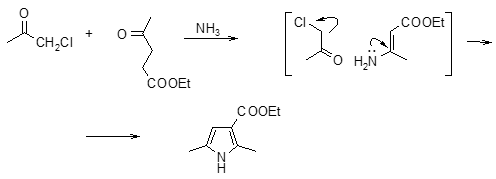
Согласно предложенному механизму, сначала происходит образование С-С связи и возникает g-дикетон, который далее реагирует с амином. К реакциям этой группы относится также взаимодействие аммиака и аминов с полиокси- и полигалоидными соединениями [27].
1H-пирролы также образуются в результате термической 1,5-сигматропной перегруппировки 3Н-пирролов, которые образуются по реакции Пааля-Кнорра [28].
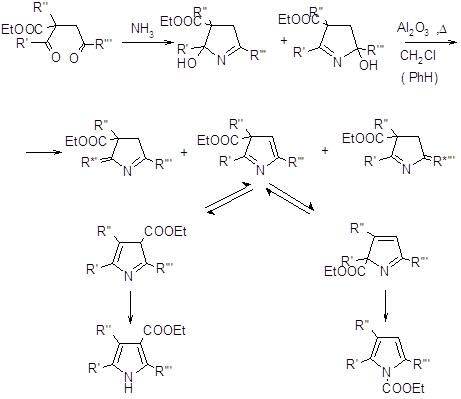
Однако представленный выше метод не отличается хорошей селективностью, в результате реакции образуются изомеры, которые дают множество побочных продуктов при дальнейшей обработке. Низкий выход целевого продукта (~ 20%), а также общее время протекания всех стадий (от 90 до 160 часов) делают этот метод малоприемлемым для широкого применения.
Метод получения 2,5-диметилпиррола (17) из 2,5-гександиона (15) и гексаметилдисилазана (ГМДС) в присутствии трифторметансульфокислоты является отличным по выходу-100%, но дорогим из-за использования трифторметансульфокислоты. Реакция протекает через промежуточное соединение (16). Попытки получить 2,5-диметилпиррол (17) из 2,5‑диметилфурана (18) через это соединение закончились неудачно [29].
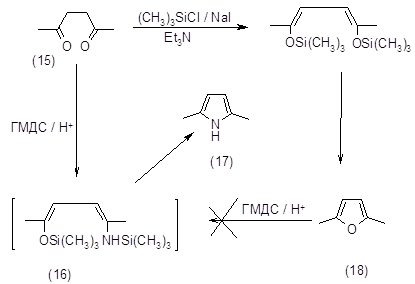
2.1.3. Реакции присоединения аминов по кратным связям.
При реакции эфиров ацетиленкарбоновой кислоты с различными нуклеофилами образуются производные пиррола [30]. Первая стадия заключается в присоединении по Михаэлю, образующееся при этом соединение циклизуется затем по ниже приведенному механизму.
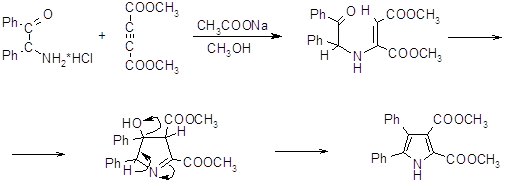
К этой же группе реакций можно отнести образование производных пиррола из N‑замещенных эфиров b-аминокротоновой кислоты (19) и 1-нитропропена (20), которые в реакции типа Михаэля дают аддукт, превращающийся в пирролин, окисляющийся затем в пиррол (21) [31,32].
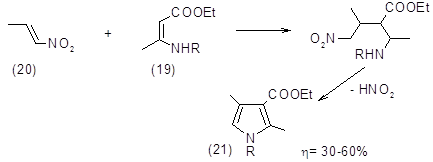
Производные пиррола из эфиров N-тозилглицина и a,b-ненасыщенных кетонов являются промежуточными в синтезе порфиринов [33].

Присоединение по Михаэлю эфира N-тозилглицина (23) к кетону (22) в присутствии третбутилата калия с последующей внутримолекулярной альдольной конденсацией приводит к образованию гидроксипирролидина (24), при дегидрогалогенировании которого образуется Δ3-пирролин (25); отщепление от него п-толуолсульфиновой кислоты под действием этилата натрия приводит к пирролу (26) с удовлетворительным выходом ~ 30-40% [16].
Ещё одним способом получения пирролов является получение пирролов по Хьюгенсу с помощью 1,3-диполярного присоединения диэфиров ацетилендикарбоновых кислот к азолактонам, образующимся в результате циклизации N-замещенных фенилглицинов в присутствии уксусного ангидрида [16]. В результате таутомерии азолактон находится в равновесии с ароматическим азометинилидом, к которому присоединяется диэфир ацетилендикарбоновой кислоты с образованием бициклического интермедиата, при отщеплении от которого CO2 образуется тетразамещенный пиррол с выходом 70-80% [34].
.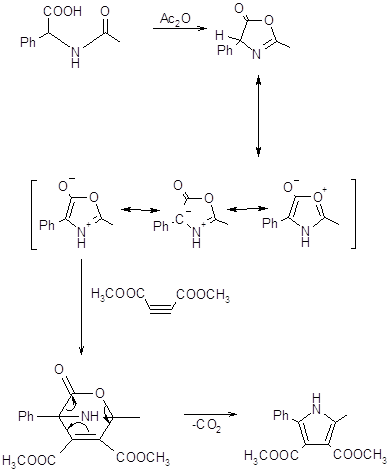
Синтез замещенных пирролов может быть также осуществлен с хорошим выходом реакцией γ-кетоалкинов с бензиламином или аммиаком. Механизм реакции, вероятно, включает образование имина, который подвергается 5-экзодициклизации с последующей изомеризацией давая пиррол [35].

В последние годы было обнаружено, что при взаимодействии 1,4-дикарбонильных соединений с солями аммония по Паалю-Кнорру, могут образовываться как производные пиррола, так и производные фурана [25, 36].
.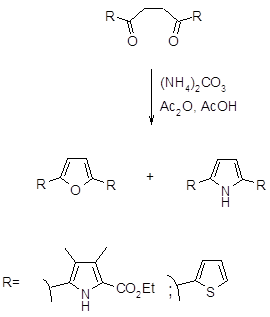
0 комментариев