Навигация
Синтез роданоспиртов и роданоэфиров
2.3. Синтез роданоспиртов и роданоэфиров
К настоящему времени в литературе не описано спиртов, содержащих родан- и гидроксильную группы при одном и том же углеродном атоме, хотя эфиры такого типа спиртов известны и легко получаются при кипячении эфиров соответствующих спиртов с роданистым калием в абсолютном спирте. В частности, этим способом получено большое число роданметиловых эфиров различных арилкарбаминовых кислот.
Попытки получения β-роданэтанола взаимодействием этиленхлоргидрина с солями роданистоводородной кислоты в обычных условиях замены галоида на родан окончилась неудачно. Конечным продуктом реакции этиленхлоргидрина с роданистым калием или аммонием являются гетероциклические соединения, образовавшиеся, по-видимому, в результате превращения нестойкого роданэтанола:
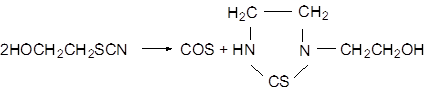
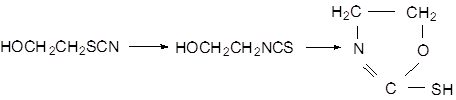
Действием роданистого калия в водном спирте и роданистого натрия в безводном ацетоне на галоидзамещённые спирты синтезирован ряд роданспиртов. Установлено, что устойчивость роданспиртов возрастает по мере удаления родангруппы от гидроксила.
С целью изучения инсектицидных свойств получен ряд эфиров, например:
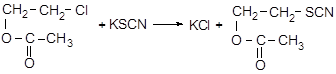
2.4. Свойства тиоцианатов
Сравнительно высокая реакционная способность органических тиоцианатов позволяет использовать их для синтеза различных других серосодержащих соединений. Так, при изомеризации тиоцианатов получаются горчичные масла. Эта изомеризация протекает в ряде случаев настолько легко,что уже при синтезе тиоцианатов образуются значительные количество горчичных масел.
При восстановлении или при гидролизе из роданидов получаются меркаптаны и соответственно дисульфиды:
RSCN + H2 → RSH + HCN
2RSCN + 2NaOH → RSSR + NaCN + NaOCN + H2O
Дисульфиды практически с количественным выходом получаются и при нагревании роданидов с третичными аминами.
При окислении роданидов азотной кислотой, перманганатом калия или электролитические образуются с хорошим выходом соответствующие сульфокислоты. Если окисление проводить хлором в присутствии воды, то конечным продуктом реакции является хлорангидрид сульфокислоты и в качестве побочного продукта получается хлористый циан – ценное сырьё для фунгицидов, гербицидов и пластических масс. При недостатке хлора получается сульфинилцианид, в результате гидролиза которого образуется сульфиновая кислота:
RSCN + Cl2 + H2O → RSOCN + 2HCl
Алкилроданиды в присутсвии воды с галогеналкилами могут давать эфиры алкилтиокарбаминовой кислоты:
RSCN + R´Br + H2O → RSCONHR´ + HBr
Аналогичная реакция протекает между алкилроданидами и спиртами в присутствии галоидводородов.
При взаимодействии алкилроданидов с диалкил- и триалкилфосфитами с хорошим выходами получаются эфиры тиофосфорной кислоты:
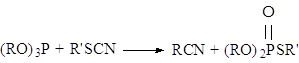
Большой интерес представляют реакции роданадов, сопровождающиеся образованием гетероциклическихсоединений. Наиболее типичным случаем такой реакции является образование бензаминотиазолов из ортоамнороданидов:
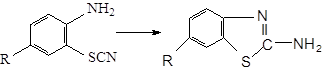
Роданфенолы при изомеризации также способны давать циклические соединения, которые при действии воды отщепляют аммиак и образуют циклические эфиры тиоугольной кислоты:
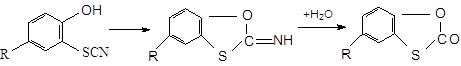
Список реакций органических тиоцианатов можно было бы продолжать, но и приведённых примеров достаточно для характеристики этой группы соединений.
Наиболее доступным методом получения тиоцианатов жирного ряда является реакция солей роданистоводородной кислоты с различными галоидпроизводными. Таким же способом могут быть синтезированы и некоторые ароматические роданиды. Вместо галоидалкила возмлжно применений эфиров серной кислоты и ароматических сульфокислот.
Тиоцианаты могут быть получены также из диазосоединений, сульфидов, хлорангидридов сульфеиновых кислот и некоторых других веществ. Однако эти последние методы роданирования имеют лишь частное значение.
3. Экспериментальная часть
Получение тиоцианомалонового эфира из броммалонового эфира.
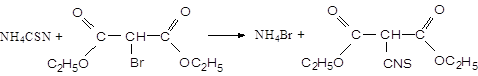
Свойства исходных веществ, применяемых при синтезе:
| Название | Формула | Молекулярная масса | Т.кип., 0С | Плотность |
| Роданистый аммоний | NH4SCN | 76,12 | 170 | 1,305 |
| Этиловый спирт | C2H5OH | 46,10 | 78,50 | 0,7893 |
| Броммалоновый эфир | C7H11O4Br | 239 | 235 | 1,48 |
| Вода | H2O | 18 | 100 | 1,00 |
Тиоцианомалоновый эфир C7H11O4CSN; молекулярная масса 217,24; регистрационный номер CAS 55602-07-8; т. кип. 169-170ОС при 22-23 мм рт. ст. и 129-130ОС при 4 мм рт. ст.
3.2. Лабораторная посуда и оборудованиеТрёхгорлая колба
Механическая мешалка
Капельная воронка
Обратный холодильник
Электроплита
3.3. Методика синтеза
Работа проводится в вытяжном шкафу!
В трёхгорлую колбу, снабжённую механической мешалкой, обратным холодильником и капельной воронкой, помещают 12 г (0,1576 моль) роданистого аммония и 27 мл (0,4623 моль) этилового спирта и, при перемешивании, прибавляют по каплям 14 мл (0,0837 моль) броммалонового эфира. Равномерное кипение смеси поддерживают в течении 1,5 часов, после чего к реакционной смеси приливают 24 мл (1,3333) воды и извлекают продукт экстракцией хлороформом. Полученный раствор сушат безводным хлористым кальцием и хлороформ отгоняют на роторном испарителе. Выход тиоциномалонового эфира составляет 11,7 мл (92% от теории). (т. кип. 169-170ОС при 22-23 мм рт. ст. и 129-130ОС при 4 мм рт. ст.)
4. Обсуждение полученных результатов
Для проведения предложенного синтезирования тиоцианомалонового эфира из броммалонового эфира, был найден один метод получения данного продукта.
Данный синтез представляет собой комплексную экспериментальную работу, включающую различные виды операций по проведению реакций (нагревание, охлаждение, перемешивание и др.) и выделению вещества из реакционной смеси.
В ходе эксперимента были отличия получения от литературной методики (экстракция хлороформом, отгонка хлороформа на роторном испарителе, нет перегонки в вакууме).
Подготовка к синтезу не была затруднительна, так как в лаборатории имелись все необходимые реактивы и приборы.
5. Выводы
Изучив синтез получения органического соединения, как тиоцианомалоновый эфир, и выполнив эксперимент, получен максимальный теоретический выход (92%) целевого продукта. Результаты опыта достаточно приближены к идеальным (93% теор. выхода). С помощью ИК-спектроскопии подтверждно строение полученного соединения. В спектре присутствуют полосы поглощения групп SCºN (2986 см-1), С=О (1447 см-1), С-О (1300-1200 см-1) и другие.
6. Библиография
1. Родионов В. М. Реакции и методы исследования органических соединений Т. 8. М: «Госхимиздат» 1959 стр. 9-21,53
2. Руководство к лабораторным занятиям по органической химии. / Под ред. Тюкавниковой Н. А. Изд. «Дрофа» М: 2003 стр. 101-108
3. Journal; Wheeler; ACJOAZ; Am. Chem. J.; 26; 1901; 353;
4. Journal; Kambe; Hayashi; CHINAG; Chem.Ind.(London); 1979; 479.
ПРИЛОЖЕНИЯ
0 комментариев