Навигация
С ростом температуры степень конверсии этилена возрастает
1. С ростом температуры степень конверсии этилена возрастает.
2. Количество реагирующего кислорода сначала быстро растет с повышением температуры – при 360°С в реакцию вступает более 80% исходного кислорода. Выше этой температуры кривая расхода кислорода
резко изменяет свой наклон и асимптотически приближается к 100% ![]() .
.
В данном процессе возможно протекание нескольких побочных реакций. В частности возможно при температурах 320 - 335ºС образование формальдегида:
![]()
Другой побочной реакцией, которая может идти в этих условиях, является образование бирадикала диметиленоксида и дальнейшее его взаимодействие с этиленом с образованием пропилена и формальдегида:
![]()
Такой процесс наблюдался при взаимодействии окиси этилена с этиленом при температурах выше 400°С. При температурах ниже 350°С образование пропилена не происходило ![]() .
.
Исследования показали влияние на процессы окисления этилена добавления небольших количеств озона, который ускорял процессы окисления. Это можно считать доказательством цепного механизма окисления этилена в окись этилена ![]() .
.
В наше время существуют полупромышленные установки для получения окиси этилена методом гомогенного окисления.
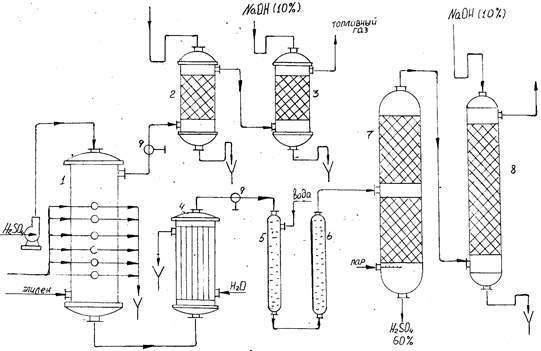
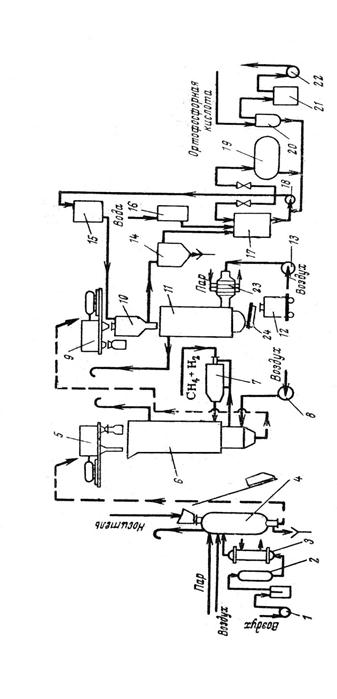
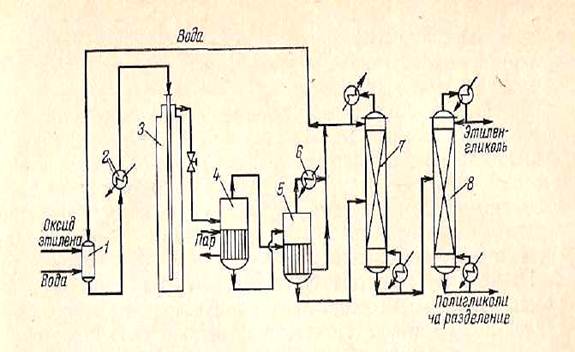
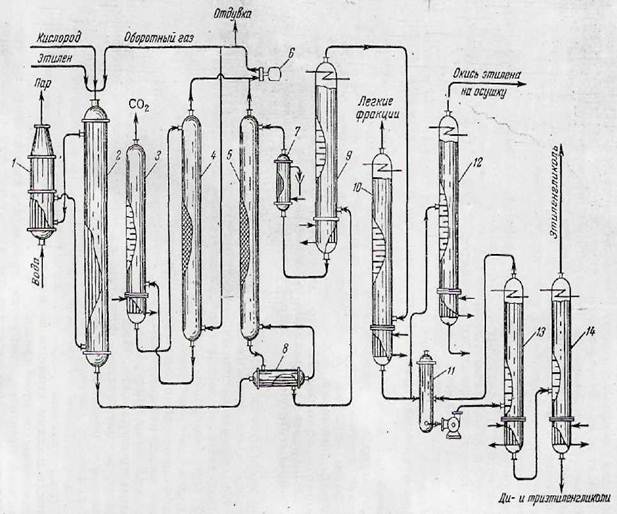
Схема процесса приведена на рис. 2.4. Реакционная смесь после реактора 2 поступает в холодильник 7 и далее в скруббер 9, где большая часть образующихся продуктов поглощается водой. Газовая смесь после скруббера вновь возвращается в реактор; предварительно к ней добавляют этан и кислород. Основными продуктами реакции являются окись этилена, уксусный и муравьиный альдегид, перекись водорода, окись и двуокись углерода. Оптимальный выход окиси этилена (36%) соответствует степени конверсии кислорода менее 35%.
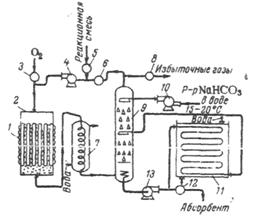
Рис. 2.4. Схема установки для гомогенного окисления смеси этилена и этана.
1) змеевик для обогрева и охлаждения реактора, 2) реактор, 3) вентиль для подачи кислорода, 4) циркуляционный насос, 5) вентиль для подачи реакционной смеси, 6) вентиль для подачи рециркуляционного газа, 7) холодильник. 8) вентиль для отвода избыточных газов, 9) скруббер, 10) насос орошения скруббера, 11) холодильник для адсорбента, 12) вентиль для подачи адсорбента на ректификацию, 13) насос для отвода адсорбента.
Съем окиси этилена с 1 л реакционного объема составляет 60 г/ч. Если стенки реактора покрыть раствором борной кислоты, то показатели процесса улучшаются. При дешевом сырье этот процесс представляется экономически выгодным. Наиболее дорогостоящей стадией, определяющей экономику процесса, является выделение продуктов реакции.
Глава 3. Применение оксида этилена.
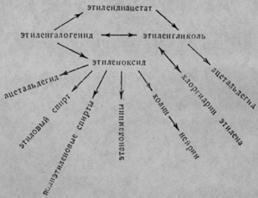
Оксид этилена ![]() используется для получения многих крупнотоннажных химических продуктов и промежуточных соединений. На рисунке 3.1 приведены в общем виде направления получения основных химических продуктов на основе окиси этилена.
используется для получения многих крупнотоннажных химических продуктов и промежуточных соединений. На рисунке 3.1 приведены в общем виде направления получения основных химических продуктов на основе окиси этилена.
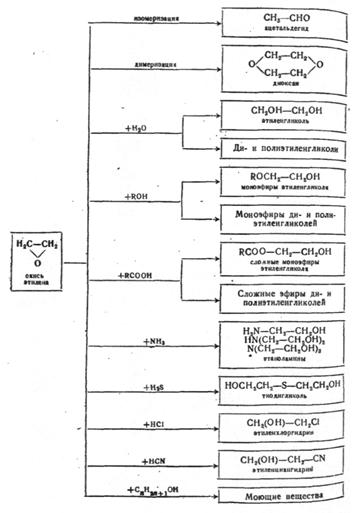
Рис. 3.1. Синтезы на основе окиси этилена.
Далее мы рассмотрим получение основных продуктов, получаемых из окиси этилена.
При нагревании до 500°С без катализаторов или до 150 – 300°С в присутствии некоторых катализаторов (активная окись алюминия, фосфорная и соляная кислоты, фосфаты) окись этилена необратимо изомеризуется в ацетальдегид:

Причем при каталитической изомеризации в качестве побочного продукта образуются диоксан и этиленацеталь ацетальдегида.
Гидрированием окиси этилена при повышенном давлении и температуре 80ºС в присутствии никелевого катализатора можно получить этиловый спирт (этанол).

Данная реакция в промышленности почти не используется, поскольку для получения этанола есть более простые и дешевые способы получения. При повышении температуры гидрирования получаем моноэтиловый эфир этиленгликоля.
Путем гидратации окиси этилена можно получить важный химический продукт – этиленгликоль.

Гидратацию можно проводить при 50 – 100°С в присутствии катализаторов (следы серной, фосфорной и других кислот) или без катализатора при 200°С и повышенном давлении. Кроме этиленгликоля, при этом образуются диэтиленгликоль, триэтиленгликоль, а также высшие полиэтиленгликоли:
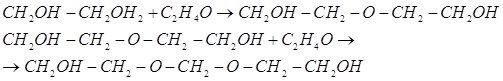
Будучи весьма гигроскопичным, этиленгликоль в то же время хорошо растворяет смолы, красители и некоторые вещества растительного происхождения. Благодаря сочетанию этих свойств этиленгликоль применяется при крашении тканей, в ситцепечатании, для приготовления штемпельных красок и косметических препаратов, для увлажнения табака и т. д. Этиленгликоль является также важным полупродуктом в производстве синтетических смол, растворителей, взрывчатых веществ и пр.
Важным свойством этиленгликоля является его способность сильно понижать температуру замерзания воды. Водный раствор, содержащий 40 об. % этиленгликоля, замерзает при -25°С, а 60%-ный водный раствор при -40°С. Поэтому этиленгликоль с успехом применяется для приготовления антифризов.
Диэтиленгликоль НОСН2СН2—О—СН2СН2ОН (т. кип. 245,5°С) применяется как растворитель и как уплотняющая жидкость для тормозных гидравлических приспособлений; в текстильной промышленности его используют при отделке и крашении тканей. Триэтиленгликоль и тетраэтиленгликоль являются растворителями и пластификаторами.
Аналогично реакции гидратации протекают реакции окиси этилена со спиртами. При этом образуются моноэфиры этиленгликоля, диэтиленгликоля.

Моноэфиры этиленгликоля, известные под названием целлозольвов и моноэфиры диэтиленгликоля применяются в качестве растворителей лаков и красок.
Окись этилена способна полимеризироваться под влиянием третичных аминов, хлорного олова и некоторых других катализаторов с образованием твердой белой массы, представляющей собой смесь полимергомологов состава ![]() . При полимеризации выделяется очень большое количество тепла, и процесс может протекать со взрывом. Высокомолекулярный полиоксиэтилен (мол. вес
. При полимеризации выделяется очень большое количество тепла, и процесс может протекать со взрывом. Высокомолекулярный полиоксиэтилен (мол. вес ![]() ) растворим в воде, и поэтому его применяют в качестве эмульгатора и загустителя.
) растворим в воде, и поэтому его применяют в качестве эмульгатора и загустителя.
В растворе этанола при 0ºС окись этилена реагирует с натрийацетоуксусным эфиром. Образующийся при этом ацетобутиролактон в присутствии разбавленной серной кислоты дает ![]() -ацетопропиловый спирт
-ацетопропиловый спирт ![]() .
.

Ацетобутиролактон используют для получения витамина В1, а ![]() -ацетопропиловый спирт используют для получения противомалярийных препаратов и витамина С.
-ацетопропиловый спирт используют для получения противомалярийных препаратов и витамина С.
Окись этилена способна присоединять углеводороды. Так в присутствии безводного хлорида алюминия окись этилена с бензолом образует ![]() - фенилэтиловый спирт с выходом около 60 – 65%
- фенилэтиловый спирт с выходом около 60 – 65% ![]() .
.
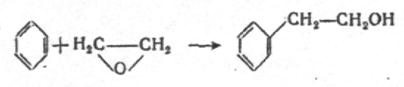
Данное вещество обладает приятным запахом и поэтому широко применяется в парфюмерии.
ЗаключениеОкись этилена, являясь одним из самых реакционноспособных органических веществ, широко используется в химической промышленности для получения этиленгликоля, полиэтиленгликоля, этанола, формальдегида, и многих других многотоннажных химических продуктов.
Для получения окиси этилена современная химия использует три основных метода его получения: получение из этилена каталитическим окислением последнего, некаталитическое окисление этилена и получение из этиленхлоргидрина. Сопоставляя показатели этих процессов можно сделать вывод, что хлоргидринный метод является наиболее экономичным. Но для своего проведения он требует использования хлора, что требует специальной конструкции реакторов, использования хлоростойких материалов и футеровки реакторов, а также следования некоторым правилам техники безопасности при работе с хлором. Каталитические методы получения окиси этилена не требуют этого, но они требуют большего расхода электроэнергии и высокой чистоты химического сырья для процесса. Поскольку загрязненное серой и другими веществами сырье способно вывести из строя катализаторы. Метод некаталитического окисления этилена в окись этилена является наиболее перспективным, но он пока не вышел за границы полупромышленного применения.
Список использованной литературы
1. Бесков В.С., Сафронов В.С. Общая химическая технология и основы промышленной экологии. – М.: Химия, 1999. – 412 с.
2. Зимаков П. В., Дымент О. Н., Богословская Н. А. и др. Окись этилена – М.: Химия, 1967. – 319 с.
3. Клименко А.П. Получение этилена из нефти и газа. – М.: ГНТИНиГТЛ, 1962. – 412 с.
4. Лебедев Н.Н. Химия и технология основного органического и нефтехимического синтеза. – М.: ОНТВ РФ, 1936. – 318 с.
5. Общая органическая химия. Т.1: Стереохимия, углеводороды, галогенсодержащие соединения. Под ред. Д. Бартона и У. Д. Оллиса. – М.: Химия, 1981. – 735 с.
6. Одабашян Г.В., Швец В.Ф. Лабораторный практикум по химии и технологии органического и нефтехимического синтеза. – М.: Химия, 1992.
7. Паушкин Я.М., Адельсон С.С. Технология нефтехимического синтеза. – М.: Химия, 1976. 648 с.
8. Синтезы органических соединений. Методические указания к лабораторному практикуму. Под ред. Б. Д. Березина. – Иваново, Изд. Ив. ХТУ, 1976. – 110 с.
9. Смит В., Бочков А., Кейпл Р. Органический синтез: Наука и искусство. – М.: Мир, 2001. – 345 с.
10. Современные методы органического синтеза. Под ред. проф. Б. В. Иоффе. – Л.: Изд. ЛГУ, 1980. – 232 с.
11. Углеводороды. – М.: РХТУ им. Менделеева, 2000. – 287 с.
12. Хавкинс Э. Дж. Органические перекиси, их получение и реакции. – М. – Л.: Химия, 1964. – 387 с.
13. Юкельсон И.И. Технология основного органического синтеза. – М.: Химия, 1968. – 847 с.
Похожие работы
... гомологов этилена Ближайшие гомологи этилена - пропилен и бутилены - более активны в химическом отношении, чем сам этилен. Их реакции разнообразны и протекают с большей лёгкостью, и такие углеводороды начинают всё в большей степени использоваться в промышленном органическом синтезе. Алкирирование пропиленом бензола даст изопропилбензол (кумол), окислением которого получают фенол и ацетон. При ...
... процесса, более высокий выход спирта. Недостатками прямой гидратации является частая замена катализатора и использование более дорогих концентрированных этиленовых фракций. Процесс синтеза этилового спирта прямой гидратацией этилена технически более прогрессивен, чем сернокислотной гидратацией, поэтому он получил значительно большее распространение в промышленности. Характерной особенностью ...
... и осуществлялись им с исключительной строгостью Экспериментальных данных Вюрца впоследствии никто не опровергал, они были безукоризненны. С первыми теоретическими работами Вюрц выступил в 40-е годы XIX в.— время становления теоретических основ химии, когда подрывались принципы дуалистической системы и теории сложных радикалов, когда трудами французских химиков Дюма, Лорана и Жерара закладывались ...
... ; Н ׀׀ ׀׀ ׀ СН2OH С - С СООН ׀ ׀ ֽ ֽ 4. Отщепление воды от этиленгликоля может иметь внутримолекулярный и межмолекулярный характер. Направление отщепления воды зависит от условий реакции. Пример внутримолекулярного ...

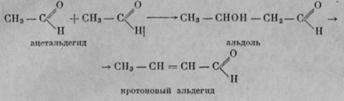
0 комментариев