Функциональная группа спиртов содержит электроотрицательный атом кислорода с двумя неподеленными парами электронов. В молекуле спиртов можно выделить следующие реакционные центры:
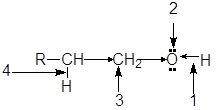
1. ОН-кислотный центр, обусловливающий возможность отщепленя протона вследствие высокой полярности связи О-Н;
2. нуклеофильный и n-основный центр - атом кислорода, имеющий неподеленные пары электронов;
3. электрофилный центр - a-атом углерода, на котором дефицит электронов вызван -I-эффектом соседней гидроксильной группы;
4. b-С-кислотный центр, в котором поляризация связи С-Н также обусловлена электроноакцепторным влиянием гидроксильной группы.
1. Получение алкилгалогенидов действием на спирты
тионилхлорида
Одним из лучших лабораторных способов превращения спиртов в алкилхлориды является их взаимодействие с тионилхлоридом. Тионилхлорид превращает первичные и вторичные спирты в алкилхлориды с выходом 70-90%. Образующиеся наряду с продуктом замещения хлороводород и диоксид серы газы, что облегчает выделение целевого продукта. Следует различать две разновидности этой реакции: в присутствии или в отсутствии основания (пиридина С5Н5N или триэтиламина Et3N и других третиичных аминов). Амин играет двоякую роль. Прежде всего, он способствует образованию алкоксид-аниона. Кроме того, он связывает выделяющийся хлороводород:
Реакция (S)-2-бутанола с тионилхлоридом в присутствии пиридина проходит с обращением конфигурации:
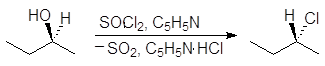
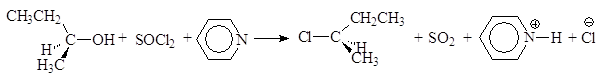 (56)
(56)
(S)-2-бутанол (R)-2-хлорбутан пиридинийхлорид
Механизм:
На первой стадии реакции с сохранением конфигурации образуется хлорсульфит:
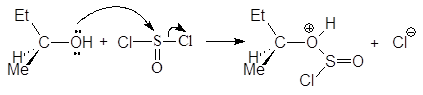 (М 11)
(М 11)
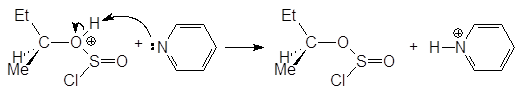
втор-бутилхлорсульфит
На второй стадии хлорсульфитная группа замещается на хлор по механизму SN2 с обращением конфигурации. В присутствии основания выделяющийся на первой стадии хлороводород превращается в соль:
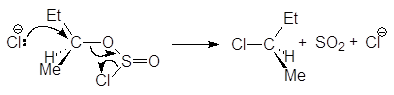
Замещение гидроксильной группы первичных и вторичных спиртов на хлор под действием тионилхлорида в присутствии пиридина сопровождается перегруппировками, например:
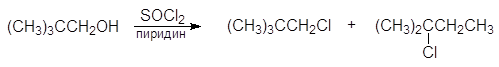 (57)
(57)
Реакция (S)-2-бутанола с тионилхлоридом в отсутствии пиридина проходит с рацемизацией:
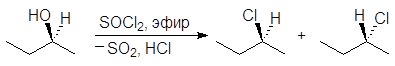 (58)
(58)
Дело в том, что в отсутствии основания хлорсульфит превращается сначала в ионную пару. Ионная пара далее превращается в алкилгалогенид и диоксид серы. При этом образуются продукты, как с сохранением, так и с обращением конфигурации.
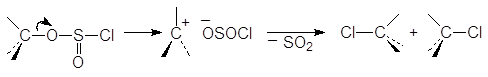 (М 12)
(М 12)
ионная пара
Третичные спирты в этих условиях превращаются в алкены.
2. Образование алкилсульфонатов
Еще один путь превращения гидроксильной группы спиртов в хорошую уходящую группу - превращение их в мезилаты и тозилаты. Например, спирты реагируют с метансульфонилхлоридом (мезилхлоридом Ms¾Cl) или с п-толуолсульфонилхлоридомом (тозилхлоридом Тs¾Cl) превращаясь соответственно в алкилмезилаты или алкилтозилаты:
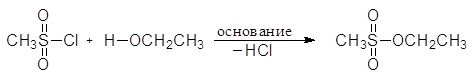 (59)
(59)
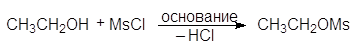
мезилхлорид этилмезилат
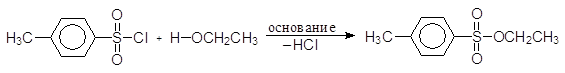 (60)
(60)
п-толуолсульфонилхлорид этил-п-толуолсульфонат
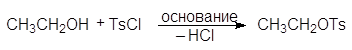
тозилхлорид этилтозилат
Превращение спиртов в алкилсульфонаты позволяет осуществлять с ними реакции нуклеофильного замещения. Стадия превращения спирта в алкилсульфонат идет с сохранением конфигурации, а вот стадия взаимодействия алкилсульфоната с нуклеофилом проходит с обращением конфигурации:
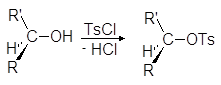
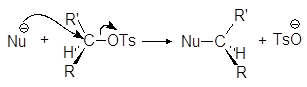 (М 13)
(М 13)
Алкилсульфонаты вступают во все реакции, характерные для галогенуглеводородов. Из них, например, могут быть получены различные галогензамещенные углеводороды. Для этого спирты сначала превращают в алкилсульфонаты, например в тозилаты, которые легко могут быть выделены и очищены. Далее сульфонатную группу замещают на другую функциональную группу. Подобного рода превращения иллюстрируются упражнениями 17-21.
Упр.17. Какова конфигурация 2-бутанола, образующегося в результате превращения (R)-2-бутанола в тозилат и с последующей реакцией тозилата со щелочью по механизму SN2?
Ответ:
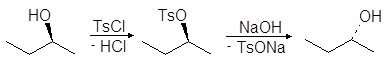
Упр.18. Каким образом через тозилат может быть осуществлено следующее превращение?
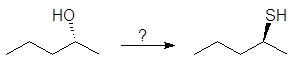
3. Дегидратация
Дегидратация спиртов подробно осуждалась в главе 8 Алкены (см. реакции 5-10, м 1-5 и упр 8.1 и 8.2). При нагревании спиртов с концентрированной серной кислотой они отщепляют воду. В случае вторичных и третичных спиртов отщепление воды протекает согласно эмпирическому правилу Зайцева: протон отщепляется предпочтительно от наименее гидрогенизированного b-атома углерода. Иными словами, двойная связь образуется у наиболее замещенного атома углерода:
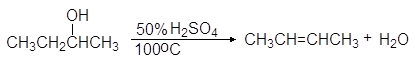 (61)
(61)
Легкость элиминирования возрастает при переходе от первичных спиртов к третичным, что нашло отражение в условиях проведения реакций. Так первичные спирты дегидратируются в довольно жестких условиях - 170 - 200оС с использованием концентрированной серной кислоты:
![]() (62)
(62)
Дегидратация вторичных спиртов происходит при температур 100 - 150оС с менее концентрированными кислотами:
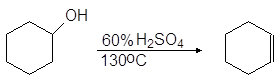 (63)
(63)
Еще легче отщепляют воду третичные спирты - 80 - 100оС в присутствии более мягких дегидратирующих агентов (разбавленная серная кислота, щавелевая или п-толуолсульфоновая кислота):
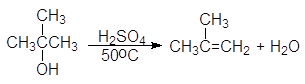 (64)
(64)
Дегидратация вторичных и третичных спиртов протекает по механизму Е1.
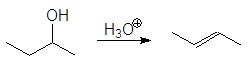 (65)
(65)
Механизм:
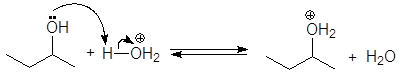 (М 14)
(М 14)
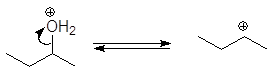
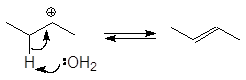
Реакция
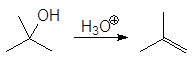 (66)
(66)
проходит по механизму:
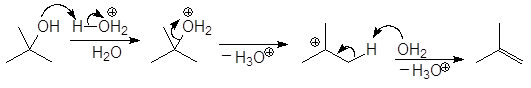 (М 15)
(М 15)
Первичные спирты дегидратируются по механизму E2,
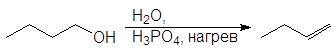 (67)
(67)
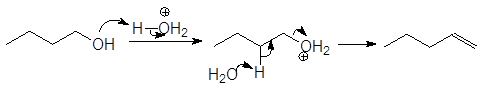
(М16)
Дегидратация первичных и вторичных спиртов часто сопровождается перегруппировками, например:
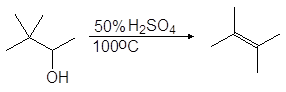 (68)
(68)
Упр.22. Опишите механизм реакции (68).
Упр.23. Опишите механизмы реакций:
(а) 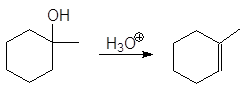 (б)
(б)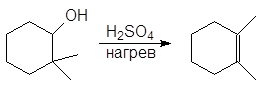
(в) 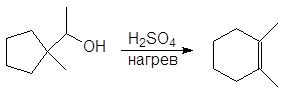
Ответ:
(а)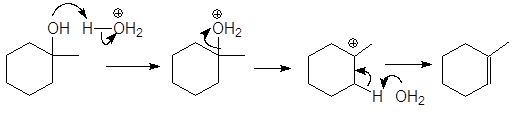
Упр. 24. Напишите реакции:
(а)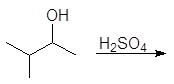 (б)
(б) 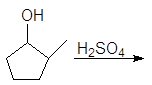
(в)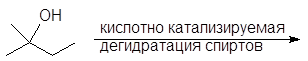
(г)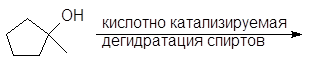
и опишите их механизмы.
Упр. 25. Завершите реакции:
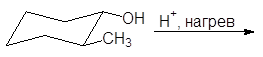 | |||
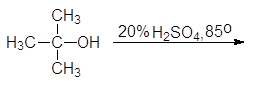 | |||
(а) (б)
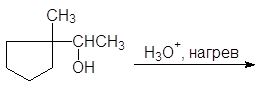 | |||
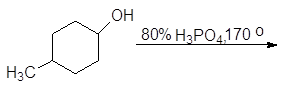 | |||
(в) (г)
Похожие работы
... недостатками метода гомогенного кислотного катализа. В последнее время разработан метод получения некоторых эфиров уксусной кислоты этерификацией уксусной кислоты соответствующими спиртами в присутствии ионообменной смолы КУ-2. Использование ионитов как катализаторов реакции этерификации позволяет применить эквивалентные количества реагирующих веществ, что значительно облегчает очистку готового ...
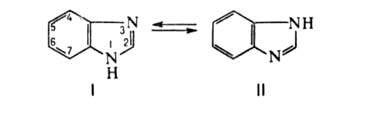
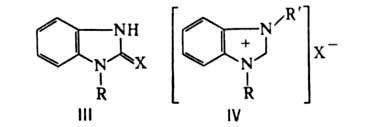
... комнатной температуре на несколько часов. Растворитель отгоняют в вакууме, а твердый остаток кристаллизуют из уксусной кислоты. Выход продукта 9-5%; т. кип. >360°. 2. Литературный обзор. Бензимидазол, его производные, их синтезы и свойства Данная работа посвящена изучению обладающих ценными свойствами бензимидазолов общей формулы их таутомеров, их стереоизомеров, их смесей ...
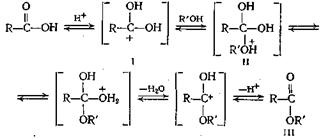
... была столь высока, что единственными продуктами были сильно окрашенные полииминиевые соли. 2.2.6 Комплексы a,b - непредельных амидов с ангидридом трифторметансульфоновой кислоты в реакции Вильсмейера-Хаака-Арнольда Синтез тетрагидрохинолин- 4- онов Недавно Баленковой и сотр. [25] был предложен новый электрофильный реагент, представляющий собой комплекс N,N- ...
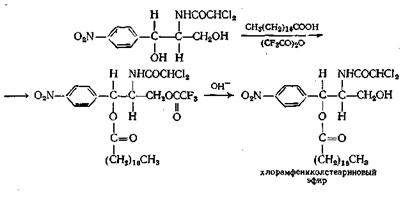
... качестве этерифицирующего реагента использовать непосредственно кислоты, однако при применении хлорангидридов этих кислот этерификация осуществляется достаточно легко. Наконец, в результате сложных химических превращений получен ряд сложных эфиров хитозана. Хотя механизм этих реакций недостаточно выяснен, известно, что цианаты хитозана, например, можно получить нагреванием хитозана, пропитанной ...
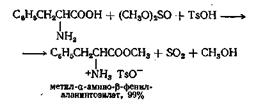
0 комментариев