Министерство образования Российской Федерации
Ижевский государственный технический университет Рефератна тему:
Обескремнивание воды
Выполнил: Князев К.П.
студент гр. 1-50-8
Проверил: преподаватель
Татура А.Е.
Ижевск, 2009 г.
При длительном нагреве воды на поверхности различных материалов образуется накипь, являющаяся результатом химических реакций с участием растворимых примесей, которые переходят в нерастворимое состояние. В состав накипи входят карбонаты кальция и магния, а также сульфаты и хлориды этих же катионов. Кроме того, в накипи присутствуют продукты коррозии железа и меди, а также силикаты кальция и магния
Состав накипи влияет на ее прочность и степень сложности ее удаления. Наиболее легко удаляются карбонат кальция и гидроокись магния, несколько сложнее – продукты коррозии и наносные шламы, содержащие оксиды железа. Один из самых трудноудаляемых видов отложений – накипь, в состав которой входят силикаты – соединения кремния. Они являются постоянным компонентом примесей в природных водах. Обычно в поверхностных и артезианских водах общее содержание примесей кремния меняется от 1 до 30 мг/л.
Основной источник поступления соединений кремния в природную воду – растворимые продукты различных минералов, особенно алюмосиликатов. При воздействии на них воды с примесью двуокиси углерода происходит вымывание кремниевой кислоты.
Кроме кислого гидролиза натуральных силикатов, источником поступления в природные воды соединений кремния является разложение биомассы наземных и водных растительных организмов. Помимо этого, повышение содержания данного вида примесей происходит в результате загрязнения окружающей среды отходами предприятий, производящих керамические, цементные и стекольные изделия, силикатные краски, вяжущие материалы и кремнийорганические каучуки.
Примеси соединений кремния, встречающиеся в воде, находятся в растворенном или коллоидном состоянии, а их основные компоненты – производные орто- (H4SiO4) и метакремниевой (H2SiO3) кислот. По степени диссоциации в воде такие соединения относятся к категории очень слабых кислот. Наиболее сильная из них – ортокремниевая кислота, которая диссоциирует по схеме:
H4SiO4 = (H3SiO4)![]() + Н
+ Н ![]()
Несмотря на низкую степень диссоциации, кремниевая кислота образует соли с кальцием, магнием, железом и алюминием – силикаты. Стоит отметить, что двух- и трехзамещенные силикаты кальция после затвердевания превращаются в очень прочный материал – присутствие подобных компонентов в накипи приводит к увеличению ее прочности и трудности удаления.
Кремниевая кислота в коллоидном состоянии способна к самопроизвольному образованию полимерных соединений:
O О Н
// /
HO- (-Si - O - )n- OH или HO- (-Si - O - )n- OH ,
О Н
где n – степень полимеризации.
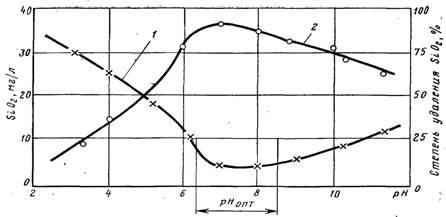
Степень полимеризации таких соединений определяется содержанием соединений кремния в воде, степенью минерализации воды, а также величиной рН. Так, в нейтральной среде кремниевая кислота находится преимущественно в мономерном состоянии, а доля поликремниевой кислоты составляет всего 0,1 % от всего содержания кремниевых соединений. В то же время в щелочной среде при рН = 10 доля полимерных соединений возрастает до 58,5 %.
Вид коллоидного состояния соединений кремния определяется их соотношением с водой. Так, если на одну молекулу двуокиси кремния в коллоидном состоянии приходится около 300 молекул воды, то образуется гель. В случае если содержание воды понижается до 30–40 молекул – появляется твердый продукт, образующий при нагреве хрупкое рыхлое вещество (ксерогель). Данное вещество, имеющее большую удельную поверхность, которая может достигать 800 м2/г, обладает сильной адсорбцией к различным веществам. Эти гели поглощают различные частицы, не вступая с ними в химическое взаимодействие, и образуют прочные системы за счет своего связующего действия.
Находясь в воде в коллоидном состоянии, соединения кремния могут оседать на твердых поверхностях. На нагретых поверхностях процесс оседания и гелеобразования идет быстрее. С течением времени гель уплотняется и захватывает из водной фазы механические примеси и некоторые растворенные вещества. При этом соединения кремния играют роль цементирующего компонента. Накипь, образованная в присутствии соединений кремния, обладает повышенной прочностью, что затрудняет ее удаление.
Кроме того, соединения кремния в воде могут принимать участие в химическом взаимодействии. Так, кремниевая кислота может взаимодействовать с катионами железа, находящимися в степени окисления +3, и быть совершенно инертной по отношению к ионам железа со степенью окисления +2. В результате такого химического взаимодействия появляются устойчивые коллоидные образования, которые не удаляются ни фильтрованием, ни отстаиванием. Склонность кремневой кислоты к такому химическому взаимодействию значительным образом затрудняет очистку воды от примесей железа. Это связано с тем, что распространенные методы удаления примесей железа при водоподготовке заключаются в окислении примесей железа по реакции:
Fe![]() ----------à Fe
----------à Fe![]()
Обычно, в отсутствие примесей кремния, соединения железа переходят в осадок и легко удаляются, а при их наличии такая стадия очистки значительно теряет свою эффективность.
Примеси соединений кремния негативно влияют на фильтрующие среды, являющиеся катализатором окисления соединений железа. Одни из наиболее распространенных видов катализаторов для окисления примесей железа – «зеленые» или «черные» пески, действующим началом в которых является двуокись марганца, нанесенная на сыпучий фильтрационный материал.
Однако присутствие кремниевой кислоты в определенных концентрациях блокирует активные центры такого катализатора, а вследствие этого – снижает выход продуктов окисления. Взаимодействие аниона кремниевой кислоты с пленкой катализатора (двуокись марганца) приводит к образованию коллоидного вещества, легко смываемого с носителя потоком воды. В итоге происходит разрушение катализатора.
Обычно удаление примесей соединения кремния не выделяют при водоподготовке в отдельную стадию, а проводят совместно с удалением других примесей, например, с процессом умягчения и последующим осаждением образованного осадка. Поэтому и реактивы, используемые для этой цели, подобны.
Достаточно часто для удаления соединений кремния из воды используют такой доступный и дешевый продукт, как гашеная известь. Этот реагент, представляющий собой сильное основание – Са(ОН)2, взаимодействует с кремниевой кислотой, в результате чего происходит образование нерастворимого силиката кальция. Практика показывает, что введение в воду гашеной извести позволяет снизить содержание примесей кремния в пересчете на анион SiO32- до 0,3–0,5 мг/л.
Другим распространенным способом, позволяющим снизить содержание примесей кремния, является обработка воды магнезитом, обожженным при 1000 0С. В процессе такого прокаливания магнезит превращается в оксид магния (каустическая магнезия):
![]() MgСО3 t=
1000
MgСО3 t=
1000![]() C à MgO + СО2.
C à MgO + СО2.
Обработка воды оксидом магния приводит к его превращению в гидроокись (MgO + Н2O ---à Mg(OH)2),которая затем взаимодействует с H2SiO3, переводя ее в осадок. Введение каустической магнезии в обрабатываемую воду с температурой до 40![]() С в количестве 10–15 мг на 1 мг H2SiO3, позволяет снизить содержание примесей кремния до 1–1,5 мг/л. При повышенной температуре процесс удаления примесей кремния протекает более интенсивно. Так, при температуре 98 °С остаточное содержание этого вида примесей уже составляет всего лишь 0,25 мг/л.
С в количестве 10–15 мг на 1 мг H2SiO3, позволяет снизить содержание примесей кремния до 1–1,5 мг/л. При повышенной температуре процесс удаления примесей кремния протекает более интенсивно. Так, при температуре 98 °С остаточное содержание этого вида примесей уже составляет всего лишь 0,25 мг/л.
Аналогичные химические процессы протекают и при обработке воды обожженным доломитом – CaMg(CO3)2. После прокаливания этот минерал превращается в смесь оксидов кальция и магния, которые, взаимодействуя с водой, превращаются в соответствующие гидроокиси, реагирующие с кислотным остатком кремниевой кислоты. При использовании данного реагента в холодной воде удается добиться остаточного содержания примесей соединений кремния около 2 мг/л, а при обработке воды с температурой чуть ниже 100 °C концентрация этих примесей составляет примерно 0,2 мг/л.
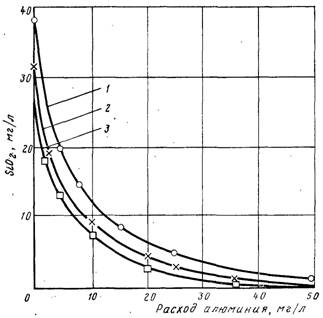
В ряде случаев удаление соединений кремния проводится на стадии осветления и обесцвечивания. Такие процедуры на очистных сооружениях осуществляются при коагуляции взвешенных и коллоидных соединений. Довольно часто для этих целей используют соединения алюминия или соли железа (3). Образующаяся хлопьевидная масса гидрооксида алюминия или гидроокиси железа захватывает частицы примесей, находящиеся в коллоидном состоянии или растворенном виде. Так, при очистке воды от соединений кремния с помощью коагуляции эффективный расход солей железа (3) составляет около 2 мг на миллиграмм удаляемой кремниевой кислоты. При использовании соединений алюминия наиболее распространенными реагентами являются алюминат натрия и сульфат алюминия. Причем наиболее эффективный осадитель – алюминат натрия, который вводится в очищаемую воду в концентрации 10–15 мг/л.
Помимо вышеперечисленных коагулянтов применяются и другие, например, «Гидро-Икс». В основном он содержит крахмал и полиальгинат натрия. Крахмал в этой композиции играет роль коагулянта, вызывая осаждение широкого круга примесей. Другой компонент этого препарата – полиальгинат натрия, представляющий собой натриевую соль альгиновых кислот.
Собственно альгиновые кислоты плохо растворяются в воде, но их натриевые соли легко растворяются и образуют вязкие растворы, которые являются флокулянтами. Действие коагулянта сводится к частичному укрупнению частиц, а флокулянт ускоряет процессы образования хлопьев и осаждения.
Удаление соединений кремния может осуществляться и посредством ионного обмена. Необходимо отметить, что при этом способе происходит наиболее полное удаление данного вида примесей. Так, ионный обмен позволяет достичь остаточного содержания примесей в пределах 0,02–0,05 мг/л.
Как показали практические наблюдения, наиболее эффективный способ удаления примесей связан с применением ионитов смешанного действия, которые представляют собой смесь катионита в Н-форме и ОН-анионита.
Многие марки ионообменных смол не могут применяться при температуре очищаемой воды свыше 30 °С. Это требование связано с техническими возможностями многих ионообменных материалов. Впрочем, данная задача может быть решена посредством охлаждения воды, из которой необходимо удалить соединения кремния. Конечно, такое ограничение не может быть преградой для использования ионного обмена при удалении примесей кремния. Однако по причине сложности процесса данное техническое решение применяют редко.
Удаление из воды соединения кремния может осуществляться также с помощью мембранного метода, имеющего, однако, существенный недостаток. Как показали исследования по обессоливанию воды с высокой минерализацией, на поверхности мембраны происходит полимеризация соединений кремния, переход их в коллоидное состояние. Это приводит к забиванию пор мембраны и, в конечном счете, снижает скорость фильтрации.
Похожие работы
... кислота или фторид натрия переводят кремниевую кислоту в сильную кремнефтористоводородную, которая достаточно полно поглощается слабоосновными анионитами: Электрохимическое декремнизирование воды Обескремнивание воды при электролизе растворимым алюминиевым анодом основано на способности образующегося в процессе электролиза гидроксида алюминия сорбировать соединения кремния. Как показали ...
... 12831,065 12831,065 D1 т/год 89817457,5 89817457 Do т/ч 1069255,4 1069255,4 Добавочная вода 13642,805 13365,693 Ca2+*f''*SO42-*f" 6,88E-05 3,03E-05 ПРCaSO4 2,50E-05 ...
... свою очередь, С определяют, используя зависимость где Ми - содержание взвешенных веществ в исходной воде, мг/л; m - содержание СаО в товарной извести, %. Известково-содовый метод умягчения воды описывается следующими основными реакциями: По этому методу остаточная жесткость может быть доведена до 0,5.1, а щелочность с 7 до 0,8.1,2 мг-экв/л. Дозы извести Ди и соды Дс (в пересчете на ...
... с 8,3 до 0,03 мг/л, что ниже ПДК, степень очистки 99,6 % поэтому возможно использовать реагентную очистку в этом случае. Глава 4. Экономическая часть В данной работе проводилась очистка сточной воды машиностроительного предприятия , в процессе которой было использовано оборудование, химическая посуда, химические реактивы. В данной главе просчитаны общие затраты за год на очистку сточных вод ...
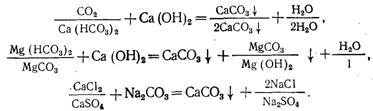

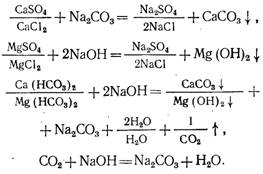
0 комментариев