Навигация
Герпес.Этиология и патогенез
ГЕРПЕС. ЭТИОЛОГИЯ И ПАТОГЕНЕЗ.
Общая характеристика герпетическоЙ инфекции
Вирусы (от лат. virus — яд) — мельчайшие доклеточные живые образования, основным условием осуществления жизненного цикла которых является паразитирование в клетке, предоставляющей свои структуры, ферменты, материалы и энергию для репродукции вируса.
Вирусные заболевания могут иметь различное клиническое течение, в связи с чем инфекцию классифицируют как очаговую и генерализованную, каждая из которых может быть острой или персистентной (схема 1). Острая инфекция может протекать без клинических симптомов (инаппарантная инфекция) или иметь характерные клинические симптомы (манифестная инфекция). К персистентной инфекции относят истинно латентную (вирус остается в организме хозяина в скрытой форме), латентную с периодическими абортивными рецидивами, хроническую (с постоянным воспроизводством и выделением вируса) и медленную (с многодневным циклом удвоения вируса и инкубационным периодом, продолжающимся годами).
Семейство Herpesviridae (от греч. hérpеs — лишай) объединяет 80 вирусов, 8 из которых связаны с патологией человека. Герпесвирусы этого семейства вызывают различные заболевания, в том числе с проявлениями в полости рта (табл. 1).
Все описанные герпесвирусы имеют сходные структурные характеристики. С точки зрения патологии человека, герпесвирусы объединены способностью персистентной инфекции, характер которой и определяет широкой спектр проблем эпидемиологического контроля, клинической и лабораторной диагностики, этиотропной и патогенетической терапии.
| Очаговая инфекция |
| Генерализованная инфекция |
| |||||||||||||||||||
| острая | персистентная | острая | персистентная | |||||||||||||||||||
| манифестная | истинно латентная | манифестная | истинно латентная | |||||||||||||||||||
| инаппарантная | латентная с рецидивами | инаппарантная | хроническая | |||||||||||||||||||
| хроническая | медленная | |||||||||||||||||||||
Схема 1. Классификация вирусной инфекции
Особенности каждой нозологической формы герпетической инфекции определяются влиянием многих факторов, таких как: тип вируса, локализация входных ворот инфекции, способ распространения вируса в тканях организма, компетентность иммунной системы, первичный или вторичный характер инфекции и т. д.
Таблица 1 Герпесвирусы и патология человека
| Герпесвирусы | Заболевания, ассоциируемые с первичной инфекцией | Заболевания, возникающие при активации латентной инфекции | ||
| Подсемейство | Тип | |||
| α | – тропность к эктодермальным тканям; – короткий репродуктивный цикл; – быстрое распространение; – литический цикл размножения; – латенция преимущественно в нервных ганглиях | вирус простого герпеса 1 типа (син.: ВПГ-1, herpes simplex virus 1, HSV-1) | – врожденный и неонатальный герпес; – острый герпетический стомататит; – герпес кожи лица и верхних конечностей; – офтальмогерпес; – менингоэнцефалит | – герпетический стоматит; – многоформная эксссудативная эритема; – офтальмогерпес; – менингоэнцефалит |
| вирус простого герпеса 2-типа (син.: ВПГ-2, herpes simplex virus 2, HSV-2) | – врожденный и неонатальный герпес; – генитальный герпес; – герпес кожи нижних конечностей; – менингоэнцефалит | – герпес гениталий; – герпес кожи бедер, ягодиц, нижних конечностей; – миелит, энцефалит | ||
| вирус ветряной | – ветряная оспа; – пре- и перинатальная инфекция | – опоясывающий | ||
| Герпесвирусы | Заболевания, ассоциируемые с первичной инфекцией | Заболевания, возникающие при активации латентной инфекции | ||
| Подсемейство и его свойства | Тип | |||
| – тропность к лимфоидным и железистым тканям; – длительный репродуктивный цикл; – увеличение зараженных клеток; – длительная персистенция; – латенция | цитомегаловирус (син.: вирус герпеса человека 5-го типа, HHV-5, cytomegalovirus, CMV) | – тератогенные эффекты; – врожденная инфекция; – иммунодефицит; – патология органов дыхания; – язвенно-некротичес-кий гингивостоматит; – диссеминированная инфекция | – ретинит; – колит; – стоматит; – энцефалит | |
| γ | – лимфотропность (специфичность к Т- или В-лимфо-цитам); – пролиферация тканей и онкогенез; – латенция | вирус герпеса человека 6-го типа (син.:HHV-6) | – кофактор ВИЧ; – синдромом хронической усталости; – оральная карцинома; – цервикальная карцинома | – системная патология при пересадке органов и тканей; – гистиоцитоз из клеток Лангерганса |
| вирус герпеса человека 7-го типа (син.: HHV-7) | -синдром хронической усталости; -экзантема новорожденных | системная патология при пересадке органов и тканей | ||
| вирус Эпштейн–Барра (син.: вирус герпеса человека 4-го типа, HHV-4, Epstein–Barr virus, EBV)- | – инфекционный мононуклеоз; – В-лимфопролифера-тивные заболевания; – карцинома; – лимфоэпителиома слюнной железы | – назофарингеальная карцинома; – лимфома Беркитта; – идиопатическая лимфоцитарная пневмония; – лейкоплакия | ||
| вирус герпеса человека 8-го типа (син. HHV-8) | неизвестно | – Сакома Капоши, – первично распространяющаяся лимфома | ||
ПАТОГЕНЕЗ ОСТРОЙ ГЕРПЕТИЧЕСКОЙ ИНФЕКЦИИ
Патологические эффекты при вирусных заболеваниях являются совокупным результатом прямого воздействия вирусов на организм хозяина и повреждения тканей при иммунном ответе.
Ниже схематически представлены основные «клеточные» и «хозяйские» стадии взаимодействия герпесвирусов и человека. Этот перечень подробно раскрывает содержание классических стадий развития инфекционного заболевания: заражения, инкубационного периода, продромального периода, стадий разгара и разрешения клинических симптомов.
| «Хозяйские» стадии вирусного патогенеза 1) проникновение вируса в организм; 2) первичное воспроизведение вируса в клетках в области входных ворот; повреждение клеток; 3) распространение вируса внутри хозяина; 4) распределение вируса в тканях в соответствии с клеточным и тканевым тропизмом; 5) воспроизведение в восприимчивых клетках; повреждение клеток; 6) иммунный ответ и другие защитные реакции хозяина; 7) персистенция, латенция инфекции | «Клеточные» стадии вирусного 1) адсорбция на поверхности клетки; 2) слияние оболочек вируса и клетки; 3) проникновение «голого» вириона в клетку; 4) проникновение нуклеоида вируса в клеточное ядро; 5) использование вирусного генома и ферментов клеточного ядра для синтеза вирусных белков, необходимых для воспроизводства вируса; 6) репликация вирусного генома; 7) синтез капсомеров; 8) упаковка генома в капсид; 9) выведение нуклеокапсида из ядра; 10)дозревание вириона (создание внутренней и внешней оболочек); 11) выведение вириона из клетки |
Клеточные стадии патогенеза Репликативный цикл вирусов простого герпеса
Вирусы семейства Herpesviridae, в том числе ВПГ-1 и ВПГ-2, представляют собой сферические образования диаметром 100–300 нм со сложной структурой, в которой различают как минимум 4 компонента:
а) нуклеоид — центральная часть вириона, представленная двумя нитями ДНК, намотанными на цилиндрический белковый стержень;
б) капсид (от лат. capsa — вместилище, футляр) — белковая капсула, в которую заключен нуклеоид; капсид имеет вид правильного двадцатигранника, собранного из сотен одинаковых белковых призматических полых капсомеров;
в) внутренняя оболочка (в англ. языке tegumen — покров) — суперкапсидная структура, представляющая собой трехслойную мембрану с неправильными очертаниями;
г) внешняя оболочка (в англ. языке envelope — чехол, обложка, конверт) — липо- и гликопротеидная структура неправильной формы с обращенными вовне выступами, покрывающая один или несколько нуклеокапсидов герпеса с их индивидуальными внутренними оболочками.
Заражение начинается с того, что вирус простого герпеса (ВПГ) прикрепляется гликопротеидами внешней оболочки (gB, gC и gD) к специфическим рецепторам мембраны клетки, чувствительной к ВПГ.
Как только устанавливается стабильное прикрепление, другие гликопротеиды внешней оболочки вируса (gH и gL) организуют слияние внешней оболочки вируса и клеточной мембраны.
Проникновение вирусного капсида, окруженного внутренней оболочкой, в клетку происходит путем почкования, без повреждения целостности клеточной мембраны. Продвижению вирусной частицы внутрь клетки способствует вирус-индуцированная микрофиламентная активность цитоскелета. Затем клеточные ферменты растворяют внутреннюю оболочку вируса, и «голый» капсид направляется к ядру клетки. Здесь ДНК вируса под контролем вирусных факторов выходит из капсида и через ядерную пору проникает в ядро клетки.
В ядре клетки происходит транскрипция вирусной ДНК.
ДНК ВПГ — крупная двухцепочечная молекула, в которой различают два ковалентно связанных компонента — длинный и короткий. Встречаются четыре варианта взаиморасположения компонентов, а также различные сочетания повторов и разрывов в нуклеотидных последовательностях, что обеспечивает многочисленность штаммов ВПГ (их известно более 120).
ДНК ВПГ содержит 84 различных гена, кодирующих белки для выполнения трех основных функций:
· ферменты для репликации вирусного генома: данные белки практически полностью обеспечивают процесс репликации, так что вирус на этом этапе нуждается лишь в нескольких клеточных белках. Следствием такой самодостаточности является высокая инфекционность герпевирусов;
· белки для упаковки воспроизведенного вирусного генома в капсид (клеточные белки к этому процессу не привлекаются вовсе) и гликопротеиды для синтеза оболочек вируса;
· белки для изменения структуры и/или функции зараженных клеток в интересах вируса (для этой цели служат не менее 47 генов из 84).
Транскрипция ДНК ВПГ происходит в клеточном ядре с участием клеточной ДНК-зависимой РНК-полимеразы (поэтому репликация ВПГ возможна лишь в клетках, способных к размножению, и маловероятна в нервных клетках).
Трансляция, синтез и процессинг белков вируса простого герпеса происходит в основном в цитоплазме клетки с участием как клеточных, вирусиндуцированных и вирусных ферментов, синтезированных на ранних этапах репродукции.
Синтез белков осуществляется в той же последовательности, что и их транскрипция.
Для сборки вириона синтезированная в цитоплазме ДНК ВПГ возвращается в ядро и претерпевает некоторые изменения конфигурации, необходимые для предстоящей упаковки в капсид. Здесь же накапливаются капсомеры (белки для их создания синтезируются в цитоплазме, а затем избирательно транспортируются в ядро), из капсомеров собираются пустые капсиды, внутри которых размещается ДНК ВПГ.
Сформированный нуклеокапсид прикрепляется к ламеллам внутренней мембраны ядра и «почкуется» в цитоплазму.
Судьба зараженной клеткиРепродукция ВПГ наносит прямой вред пораженной вирусом клетке:
· вирус качественно изменяет мембраны зараженных клеток, чем провоцирует их слияние и образование гигантских многоядерных клеток-симпла-стов еще до того, как начинает размножаться;
· вирусиндуцированные изменения клеточной мембраны приводят к нарушению транспорта электролитов и утечке макромолекул клетки через плазматическую мембрану;
· вирус избирательно воздействует на синтетический аппарат клетки:
– выключает синтез белков клетки («вирусная блокада белков») и метаболизм других ее макромолекул (вирус производит белок ICP47, который инактивирует и разрушает клеточную и-РНК и, таким образом, прекращает транскрипцию клеточной ДНК);
– искажает митотический режим клетки (замедляется темп деления клеток, растет доля патологических митозов).
Клетки, в которых ВПГ активно реплицируется (в одной клетке может быть синтезировано до 200 вирионов!), не выживают, поэтому ВПГ считают литической инфекцией.
Помимо прямого негативного воздействия на клетку, ВПГ провоцирует иммунное разрушение клетки: встраивая гликопротеиды своей внешней оболочки в клеточную мембрану, ВПГ передает ей свои антигенные свойства и превращает клетку в мишень для иммунных сил.
Хозяйские стадии патогенеза Механизмы распространения вируса в организмеВнедрение ВПГ в организм чаще всего происходит через поврежденную кожу или неповрежденный эпителий. Клетки кожи эпителия роговицы, эпителия слизистых оболочек гениталий и полости рта имеют рецепторы к ВПГ, поэтому являются высокочувствительными к герпетической инфекции, что позволяет им играть роль входных ворот.
Контакт ВПГ в области входных ворот происходит не только с эпителиоцитами, но и с расположенными здесь нервными окончаниями (они тоже имеют рецепторы для ВПГ), а также клетками миелоидного и лимфоидного ряда.
Распространение ВПГ по организму происходит несколькими способами — как по поверхности, так и вглубь тканей организма:
· со слюной, пищей при глотании;
· при переносе инфицированной слюны на кожу пальца, лица, головы (аутозаражение);
· при делении инфицированной клетки;
· по межклеточным мостикам;
· через межклеточное пространство;
· с током лимфы и крови;
· в связи с клетками крови (эритроцитами, лифоцитами, макрофагами, тромбоцитами);
· в нервных тканях — по периневральному пространству или по цепочке делящихся шванновских клеток, или с током аксоплазмы.
Первичное распространение ВПГ от входных ворот по организму проявляется в т. н. первичной вирусемии — ВПГ в течение нескольких дней накапливается в кровеносном русле (при этом плотность вирионов достигает 103 в 1 мл крови) и приносится в ткани-мишени, в частности, в слизистую оболочку полости рта.
Активная репликация ВПГ в эпителиоцитах и иммунный ответ на инфекцию приводит к разрушению клеток, нарушению целостности тканей и таким образом формирует местные проявления герпетического стоматита.
Высвободившиеся из клеток вирусы-потомки (и продукты распада тканей) попадают в ток крови — наступает период вторичной вирусемии, когда плотность ВПГ достигает 106 частиц в 1 мл крови. С периодом вторичной вирусемии связаны явления интоксикации, поражение тканей экто-, мезо- и энтодермального происхождения во внутренних органах: в печени, селезенке, легких, желудочно-кишечном тракте и т. д. С вирусным поражением стволовых клеток, участвующих в процессах синтеза коллагена, связывают нарушения в синтезе соединительной ткани стенок мелких капилляров и, соответственно, геморрагические явления в области герпетического поражения.
Для прекращения острых проявлений заболевания необходимо установить контроль над репродукцией ВПГ при помощи иммунных сил и/или лекарственных препаратов.
Иммунная защита от герпетической инфекцииЗащита организма от острой вирусной инфекции обеспечивается последовательным включением нескольких взаимодействующих систем:
· врожденной (неиммунной) резистентности;
· неспецифического гуморального и клеточного иммунитета;
· адаптивного (специфического) гуморального и клеточного противогерпетического иммунитета.
Организация иммунной защиты соответствует особенностям паразитирования вирусов в организме: иммунитет направлен как против свободных вирионов, находящихся вне клеток, так и против собственных клеток, продуктивно зараженных ВПГ (схема 2.).
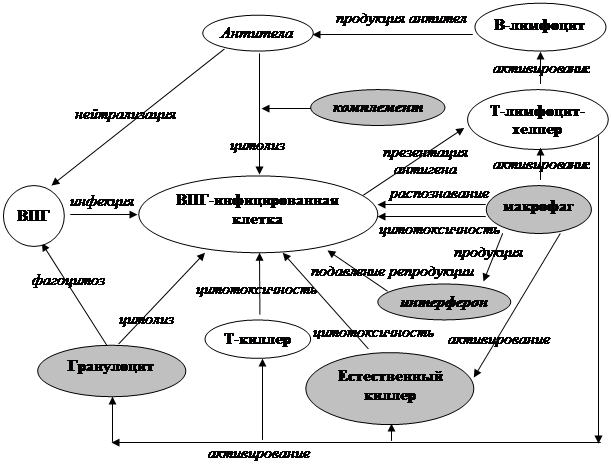
Схема 2. Основные этапы и факторы иммунного ответа на первичную инфекцию ВПГ
Врожденная (неиммунная) резистентность
Многие ткани организма невосприимчивы к ВПГ потому, что клеточные мембраны составляющих их клеток не имеют рецепторов для адгезии вириона.
Для кожи важным фактором безопасности является сохранность целостности, так как неповрежденный роговой слой является механическим барьером, устойчивым к инвазии ВПГ. Поверхность кожи и СОПР покрыта секретом желез, обладающими защитными свойствами.
На стадиях развернутой инфекции для борьбы с вирусом мобилизуются силы врожденной резистентности, проявляющейся на уровне всего организма: создаются условия, неблагоприятные для репродукции вируса (гипертермия, гипоксия, ацидоз) и способствующие скорейшему выведению вируса из организма (слюнотечение, кашель, полиурия).
Неспецифическая противовирусная иммунная защита
При внедрении вируса в ткани в действие вступают факторы неспецифического иммунитета — гуморального (интерфероны и другие цитокины, лизоцим, естественные антитела, белки системы комплемента) и клеточного (естественные киллеры, макрофаги, полиморфно-ядерные лейкоциты).
· Неспецифический гуморальный иммунитет.
Интерфероны — гликопротеиды, синтезируемые иммунными клетками под влиянием чужеродных индукторов. Различают около 20 разновидностей интерферонов, распределенных в три основных класса:
– интерферон-α — вырабатывается лейкоцитами, активен против вирусной инфекции;
– интерферон-β — вырабатывается фибробластами, активен против вирусной инфекции;
– интерферон-γ — вырабатывается Т-лимфоцитами (хелперами), естественными киллерами и макрофагами. Предназначен для обезвреживания любых антигенов и митогенов; обладает выраженными антипролиферативными, а также иммуномодулирующими эффектами (стимулируют активность макрофагов, естественных киллеров, Т-киллеров и В-лимфоцитов).
Интерфероны образуются в местах и во время репродукции вируса, поэтому вступают в борьбу с инфекцией на самых ранних стадиях заболевания. Интерфероны не взаимодействуют с вирусом и не мешают его адсорбции на клетке, но активно подавляют репродукцию вируса, проникшего в клетку. Для этого интерфероны инициируют ферментативные реакции, одна из которых приводит к блокаде синтеза вирусных белков на стадиях их транскрипции и трансляции, а другая — к активации внутриклеточного разрушения вирусных нуклеиновых кислот, в том числе и РНК. Таким образом, интерфероны подавляют сборку белков, входящих в состав генома, капсида и оболочки вирусов.
Естественным интерферонам сопутствуют другие многочисленные цитокины (интерлейкины, колониестимулирующие факторы, факторы некроза опухолей и т. д.), расширяющие спектр их действия за пределы, доступные рекомбинантным, синтетическим интерферонам — продуктам генной инженерии. Интерфероны являются важнейшим фактором неспецифической резистентности, противовирусная эффективность которого сравнима с совокупной эффективностью всех других факторов иммунитета.
Лизоцим — фермент, который вырабатывается нейтрофилами и запасается в их специфических гранулах. Защитные эффекты лизоцима особенно значительны на слизистых оболочках, так как он обладает прямым бактерицидным и (в меньшей степени) вируцидным действием. Кроме того, лизоцим стимулирует лизис клеток макрофагами и нейтрофилами, активизирует синтез антител. Лизоцим высвобождается из нейтрофилов почти мгновенно — уже через 60 с после активации иммунной системы.
Естественные антитела — иммуноглобулины М, обладающие поливалентной специфичностью; слущиваются с поверхности зрелых покоящихся В-лимфоцитов.
Белки системы комплемента способны нейтрализовать некоторые вирусы, но их главной функцией является посредничество: а) в неспецифическом фагоцитозе; б) в специфических цитотоксических процедурах, обусловленных функцией противовирусных антител; в) в развитии экссудативной фазы воспаления.
· Неспецифический клеточный иммунитет.
Естественные киллеры (ЕК) — тип лимфоцитов, не имеющих специфических рецепторов к конкретным вирусам, но способных опознавать «неправильные» клетки (инфицированные, ксеногенные, опухолевые) без предварительной сенсибилизации и убивать их.
Активные ЕК-клетки появляются через 2-е суток после заражения вирусом, т. е. прежде, чем появляются специфические Т-киллеры. Помимо того, что ЕК-клетки проявляют прямую (неспецифичную) цитотокисчность, они участвуют в реакциях цитотолиза, опосредованного антителами. Активность ЕК регулируется интерферонами-γ и интерлейкинами.
Цитотоксичность ЕК реализуется следующим образом:
1) медиаторы, произведенные ЕК, повышают проницаемость мембраны клетки-мишени через изменение активности клеточных ферментов и путем прожигания пор в мембране метаболитами кислорода;
2) цитотоксичные вещества, синтезированные ЕК, вводятся в цитоплазму клетки-мишени и дезорганизуют ее.
Макрофаги выполняют две основные функции: эффекторную (фагоцитоз свободных вирусов и зараженных ими клеток) и регуляторную (презентация вирусных антигенов Т-лимфоцитам, активация Т- и В-лимфоцитов).
Процесс презентации антигенов клеткам, обеспечивающим специфический иммунитет, проходит в несколько стадий:
· макрофаги осуществляют эндоцитоз (фаго- или пиноцитоз) вирусов;
· производят ферментативную переработку вирусных антигенов до уровня пептидов;
· выводят вирусные пептиды на свою поверхность;
· представляют их распознавания Т-лимфоцитам (весь процесс занимает около получаса).
Таким образом, с началом репродукции вируса происходит быстрая инфильтрация зоны зараженного эпителия факторами естественного иммунитета для ограничения инфекции путем подавления репликации вируса в клетках и/или разрушения инфицированных клеток.
Адаптивный (специфический) противовирусный иммунитет
Репродукция вируса в эпителии вызывает развитие антиген-специфи-ческого иммунного ответа, связанного с деятельностью лимфоцитов. Различают клеточный и гуморальный приобретенный противовирусный иммунитет.
· Т-клеточный иммунитет.
Лимфоциты CD4+(син. регуляторы, хелперы)выполняют организационные функции: распознают антигены вирусов, представленныемакрофагами, и передают информацию клеткам-эффекторам. Кроме того, Т-хелперы первого типа синтезируют интерлейкин-2, необходимый для пролиферации Т-клеток, и интерферон-γ, стимулирующий цитотоксичные Т-лимфоциты. Т-хелперы второго типа (син. супрессоры) регулируют интенсивность инфильтрации пораженных тканей клетками Т-системы.
Цитотоксические Т-лимфоциты CD8+(син. эффекторы или Т-киллеры) созревают в течение 1–3 суток от начала первичного заражения, их максимальное количество регистрируется спустя неделю. Т-киллеры мигрируют в орган-мишень вирусной инфекции, выявляют специфические антигены на поверхности клеток, в которых реплицируются вирусы, и уничтожают эти клетки.
Механизм Т-киллинга клеток, инфицированных вирусом, включает в себя следующие стадии:
1) специфический контакт с мембраной клетки-жертвы;
2) активация ферментативных систем на участке контакта;
3) повышение проницаемости клеточной мембраны;
4) осмотическое набухание клетки;
5) разрыв мембраны и выход содержимого во внеклеточную среду.
Т-киллеры являются более успешными эффекторами, чем макрофаги и полиморфно-ядерные лейкоциты. Полагают, что Т-киллеры вместе с интерферонами оставляют основные силы иммунитета, которые обеспечивают нейтрализацию вируса и, соответственно, клиническое выздоровление больного при острой первичной вирусной инфекции. Численность Т-киллеров постепенно снижается в течение нескольких недель после клинического выздоровления, но Т-клон памяти сохраняется пожизненно.
· Гуморальный специфический иммунный ответ.
Гуморальная специфическая защита организуется системой В-лимфоци-тов при участии регуляторных механизмов Т-клеточного иммунитета: Т-хел-перы, активированные макрофагами, синтезируют и секретируют факторы для активации, пролиферации и дифференциации В-лимфоцитов, которые, в свою очередь, продуцируют антитела.
Антителами называют иммуноглобулины (гликопротеины) с известной антигенной специфичностью. В зависимости от строения различают пять классов имуноглобулинов: G, A, M, D, E.
Антитела — главное иммунное средство воздействия на вирионы, находящиеся вне клетки. На оболочку вируса они воздействуют следующим образом:
· соединяются с антигенами оболочки вируса, блокируя их активные участки;
· провоцируют агглютинацию и агломерацию вирионов;
· в сотрудничестве с комплементом повреждают оболочку вириона.
Все перечисленные эффекты снижают вероятность заражения клеток хозяина ВПГ.
Комплекс «антитело + комплемент» участвует в процессе цитолиза, являясь связующим звеном между зараженной клеткой и Fс-рецепторами клеток-эффекторов. Вирусы, высвобожденные из клетки в результате цитолиза, нейтрализуются антителами.
Антитела играют иммуномодулирующую роль, стимулируя выработку интерферона лимфоцитами.
На выработку антител требуется значительное время, поэтому часто клиническое разрешение острой инфекции наступает до того, как в крови обнаруживается высокий титр антител. IgM появляются в крови в течение первых 1–3 недель после заражения, затем появляются IgG (составляют до 80 % количества антител!), IgА выявляются через 2–3 недели. Значение антител четко проявляется при повторной инфекции или рецидиве: они не могут полностью контролировать инфекцию, но, как предполагают, ограничивают ее частоту и интенсивность.
Титр антител после клинического выздоровления постепенно снижается, но, при сохранении достаточного уровня В-клеток памяти, приобретенный гуморальный иммунитет может быть пожизненным. Антитела IgА и IgG поровну распределены между плазмой и межсосудистыми тканями и всегда обнаруживаются здесь, в том числе и вне рецидива. IgА накапливается в секретах многих желез, в том числе слюнных и слизистых. Полагают, что Т-хелперы, IgA и интерферон-γ обеспечивают т. н. мукозальный иммунитет, препятствующий реинфицированию СОПР.
Особенности иммунной защиты детей от вирусных инфекций
Неиммунные факторы защиты ребенка не оказывают должного противодействия вирусной инфекции: незрелые ткани эпидермиса легко травмируются, и, так же как и тонкая, рыхлая, слабо дифференцированная слизистая оболочка полости рта, легко воспринимают ВПГ и допускают его дальнейшее распространение.
Иммунная система формируется постепенно, достигая «взрослого» состояния примерно к 6–7 годам.
Неспецифическая защита. У новорожденных отмечается выраженный дефицит интерферона-γ и его слабая антивирусная активность; продукция интерферонов и большинства других интерлейкинов достигает взрослого уровня только к 10-летнему возрасту. Естественных киллеров относительно мало, их цитоксическая активность невелика. Фагоцитоз у детей первых лет жизни протекает вяло, что обусловлено невысоким содержанием в крови хемотаксических факторов.
Специфическая защита. Абсолютное число лимфоцитов резко повышается на пятый день после рождения и остается таким до 5-летнего возраста, однако функциональная активность Т-хелперов достигает взрослой нормы только к 3-летнему возрасту. Количество В-лимфоцитов у детей в 4–5 раз больше, чем у взрослых, но эти лимфоциты не имеют достаточной чувствительности к лимфокинам и не проявляют должной активности. В течение первого года жизни доминирует супрессорная направленность Т-клеточного иммунитета ребенка, и только на втором году начинает преобладать хелперная функция по отношению к В-лимфоцитам, вырабатывающим иммуноглобулины. В грудном молоке есть зрелые материнские нейтрофилы, Т- и В-лимфоциты.
IgМ вырабатываются у ребенка достаточно интенсивно, достигая взрослых нормативов к концу первого года жизни. Этот иммуноглобулин и обеспечивает специфический иммунный ответ ребенка в течение первого года жизни на большинство антигенов, не оставляя после заболевания иммунологической памяти.
IgG к тем инфекциям, которые перенесла мать, передаются ребенку трансплацентарно и сохраняют свою активность в течение первых 3–6 месяцев жизни. К полугоду количество материнских антител резко снижается, а выработка собственных тел нарастает крайне медленно, достигая взрослого уровня только к 4–6 годам.
IgА начинает вырабатываться с 2-месячного возраста, уровень взрослых достигается к 4–6 годам.
При грудном вскармливании в организм ребенка в течение суток с молозивом поступает 8–10 г Ig G и IgА, с молоком — 1–2 г.
sIgА в секретах новорожденных отсутствует, начинает вырабатываться с 3 месяцев, достигая уровня взрослых только к 10–11 годам. Секреторный IgА поступает с материнским молоком, не всасывается, но, покрывая СОПР, защищает ее.
Таким образом, неиммунные барьеры и собственный мукозальный иммунитет детей младше 2-летнего возраста не являются эффективной защитой от внедрения первичной герпетической инфекции. Специфический иммунитет ребенка, ранее инфицированного герпесвирусом, также отличается по эффективности от иммунитета взрослых, что обуславливает особенности клинического течения как острой, так и хронической герпетической инфекции у детей.
Воспаление в патогенезе герпетического стоматитаВирусная инфекция клеток СОПР и иммунная реакция, для запуска которой достаточно нескольких репродуктивных циклов вируса, обуславливают развитие воспаления — сосудисто-тканевой реакции, определяющего метаморфозы симптомов и элементов поражения СОПР на различных стадиях развития герпетического стоматита.
Альтеративное воспаление проявляется в гибели инфицированных клеток, масштабы которой постепенно увеличиваются и выводят на первый план признаки нарастающей экссудации.
Экссудативное воспаление проявляется в диффузной гиперемии и отечности СОПР и десны, накоплении серозного, а затем и фибринозного экссудата в толще тканей и образованием папул. В полости рта экссудат пропотевает через неороговевающую СОПР и образует на ее поверхности очажки белесого налета, а в более плотной ткани красной каймы губ экссудат формирует везикулы.
Продолжающаяся альтерация приводит к макроскопическому нарушению целостности слизистой оболочки полости рта и формированию вторичных элементов поражения к различной площади и глубины (от эрозий до язв); на красной кайме губ очаги некроза прикрыты корочками серозного или геморрагического происхождения.
Стадия пролиферации начинается при условии прекращения репродукции ВПГ как в зоне поражения СОПР, так и в организме в целом. В этой стадии экссудация ограничивается зоной некроза (вокруг эрозии формируется «венчик гиперемии»), поверхность эрозии покрывается фибрином — зона поражения приобретает вид афты. Эпителий по окружности и на дне афты регенерирует, постепенно сокращается площадь и глубина афты — целостность тканей восстанавливается, непродолжительное время сохраняя более яркую окраску (пятно). Заживление очагов глубокого некроза, распространившегося за пределы базальной мембраны СОПР, сопровождается образованием рубца.
Эволюция элементов герпетического поражения красной каймы губ
|
|
|
Эволюция элементов герпетического поражения СОПР
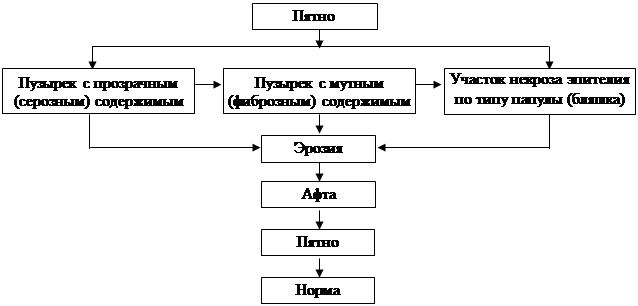 |
Исходы острой герпетической инфекции
Степень клинической тяжести острой инфекции зависит, с одной стороны, от агрессивности инфекции, а с другой стороны, — от активности противовирусной защиты, иммунной и/или фармакологической. В иммунокомпетентном организме герпетическая инфекция ведет себя как «самоограниченная»: клиническое выздоровление наступает без лечения на 10–14-й день и процесс переходит в персистентную форму. В случае врожденных или приобретенных дефектов иммунной системы, а также в связи с особенностями типа (штамма) вируса и локализации процесса, репродукция ВПГ продолжается, распространяясь на другие органы и системы (печень, легкие, почки, ЦНС), вплоть до развития генерализованной формы герпетической инфекции.
Патогенез персистентной инфекции вирусом простого герпесаВ большинстве случаев у лиц, перенесших острую стадию первичной ВПГ-инфекции, наступает клиническое выздоровление, однако, организм никогда не освобождается от ВПГ: к 10–14-му дню после первичного заражения вирус герпеса в латентной форме обнаруживается в эпителиоцитах в области входных ворот, в клетках крови и лимфы, а также в нейронах и клетках-сателлитах региональных ганглиев, где сохраняется пожизненно.
Таким образом, после острого периода герпетической инфекции наступает период персистентной пожизненной инфекции, которая чаще всего протекает как латентная либо как истинно латентная (неинфекционная), либо с периодическими, более или менее частыми рецидивами.
Факторы, обуславливающие установление латентной герпетической инфекции
Механизмы латенции не вполне ясны. Известно, что латенцию вируса простого герпеса обеспечивают следующие принципиальные обстоятельства:
· вирус способен ускользать от иммунитета и поэтому пожизненно сохраняется в организме (противогерпетический иммунитет не является стерильным);
· клетка-хозяин и иммунитет в известных пределах сдерживают активность вируса, т. е. ограничивают частоту и тяжесть клинических рецидивов
инфекции;
· ВПГ оснащен специальными механизмами для латенции и реактивации, отличными от механизмов обычной репликации, не контролируемыми ни иммунитетом, ни современной химиотерапией.
Механизмы ускользания вируса от иммунного разрушения1. Противодействие вируса простого герпеса защитным силам клетки-хозяина:
· вирус блокирует клеточные механизмы элиминации белков (нормальная клетка обеспечивает «санитарную» деградацию собственных белков; продукты деградации, а также вирусные белки переносятся на эндоплазматический ретикулум при помощи транспортных белков для дальнейшего выведения за пределы клетки; ВПГ же производит специальный белок ICP 47, который связывается с транспортными клеточными белками и блокирует их активность);
· вирус предотвращает «аварийную» полную блокаду клеточного аппарата синтеза белков (клеточный фактор инициации трансляции белков eiF-2α при инфицировании клеточного ядра должен блокировать синтез всех белков для того, чтобы остановить репродукцию вируса; ВПГ производит два специальных фактора — вирусную комплементарную РНК и белок γ134·5, способные опосредованно, через торможение или активирование клеточных ферментов, препятствовать включению (фосфорилированию) «аварийного» фактора);
· вирус блокирует программируемую смерть зараженной клетки (апоптоз) (по крайней мере три вирусных белка — US3, gJ и gD — препятствуют клеточной смерти, запрограммированной на случай повреждения клеточных механизмов вирусами и/или иммунными силами).
2. Ускользание от распознавания ВПГ-антигенов иммунными факторами:
· ВПГ персистирует в виде нуклеиновых кислот, не имеющих антигенных свойств. Уровень ДНК вируса контролируется только ДНК-азой крови;
· геном ВПГ встраивается в геном клетки-хозяина;
· при лизисе «материнской» клетки ВПГ переходит в соседнюю клетку по межклеточным мостикам, ускользая от нейтрализации антителами во внеклеточном пространстве;
· антигены ВПГ сходны с антигеном цитокератина, с рецепторами ацетилхолина и т. д., что обеспечивает заметную естественную толерантность иммунных сил к ВПГ;
· в условиях дефицита комплемента вирус, атакованный антителами и образовавший с ними комплекс, сохраняет свою активность при том, что блокированные антителами антигенные рецепторы ВПГ больше не распознаются иммунными факторами.
3. Использование иммунных сил организма в интересах ВПГ:
· ВПГ внедряется в иммунные клетки молодых организмов — макрофаги, Т- и В-лимфоциты, которые становятся не только резервуарами инфекции, но и ее разносчиками;
· антитела, связываясь с антигенами вируса, в некоторых обстоятельствах не только защищают вирусы от распознавания иммунными силами (см. выше), но даже могут провоцировать феномен усиления репродукции вируса;
· вокруг эпителиоцитов, инфицированных комплексом «ВПГ + АТ + комплемент», под действием анафилактоксина нарастает инфильтрация тканей лейкоцитами — создается «муфта» из лейкоцитов, ограничивающая инфицированную зону от иммунных атак.
4. Искажение иммунного ответа (аутоиммунные и аллергические
процессы):
· сходство антигенов ВПГ с антигенами ряда белков организма рецепторами провоцирует перекрестные иммунные реакции;
· появление иммунных комплексов из АГ+АТ провоцирует иммунокомплексные поражения, сопровождающиеся массовым распадом собственных клеток, т. е. аутоиммунные болезни.
5. Подавление иммунного ответа:
· ВПГ, инфицируя иммунные клетки, снижает их прямую функциональную активность;
· ВПГ снижает активность системы Т-хелперов;
· ВПГ подавляет продукцию и активность интерферонов;
· ВПГ ингибирует активацию системы комплемента, что снижает эффективность антител (см. выше).
Похожие работы
... были однояйцевыми; 3) возможна имитация аутизма у детей, перенесших органическое поражение головного мозга (асфиксию, энцефалит); 4) симптоматология аутизма единообразна и характерна, проявляется с момента рождения. Современные взгляды на этиологию и патогенез детского аутизма Теории психогенеза Эти концепции возникли одновременно с описанием раннего детского аутизма Каннером, который, как ...
... отклонение от нормы сосудистых реакций на холод, тепло, болевые раздражители. Полагают, что при нейроциркуляторной гипотензии (так же как при гипертонической болезни) имеет место нарушение центральных механизмов регуляции сосудистого тонуса. Основные патологические изменения при гипотензии возникают в тех же сосудистых областях, что и при гипертензии — в артериолах. Нарушение механизмов регуляции ...
... красной каймы губ на акантолитические клетки – отрицательный; 27.08.2010: Лейкоциты - 12,0*109 л-1, СОЭ - 30 мм/ч), больному можно поставить диагноз: "Многоформная экссудативная эритема с поражением слизистой полости рта, ассоциированная с вирусом простого герпеса". Дифференциальная диагностика Симптом Многоформная экссудативная эритема Акантолитическая пузырчатка Буллезный пемфигоид ...
... ревматизма обусловила значительное снижение заболеваемости — до 0Д8 на 1000 детского населения. В разработку проблемы детского ревматизма внесли большой вклад отечественные педиатры В. И. Молчанов, А. А. Кисель, М. А, Скворцов, А. Б. Воловик, В. П. Бисярина, А. В. Долгополова и др. Эпидемиология, Установлена связь между началом заболевания и перенесенной стрептококковой инфекцией, в основном в ...
0 комментариев