Навигация
Дослідження фагоцитарної функції з визначенням фагоцитарного числа (ФЧ) та фагоцитарного індексу (ФІ) за загальноприйнятою методикою [Караулов А.В.];
1. дослідження фагоцитарної функції з визначенням фагоцитарного числа (ФЧ) та фагоцитарного індексу (ФІ) за загальноприйнятою методикою [Караулов А.В.];
2. дослідження Т–системи: визначення відносної (%) кількості Т–лімфоцитів [Е.Ф. Чернушенко, Л.С. Когосова, 1978];
3. дослідження В–системи: визначення відносної (%) кількості В–лімфоцитів в периферичній крові; визначення рівня імуноглобулінів основних класів (A,M,G) у сироватці крові методом радіальної імунодифузії [Manchini, 1965]; визначення концентрації циркулюючих імунних комплексів (ЦІК) [Ю.А.Гриневичем, А.М. Алферовим].
ІІ рівень – імуногенетичне дослідження – типування алелей HLA DQ, проводили в цитогенетичній лабораторії Львівського інституту спадкової патології МОЗ України.
З метою встановлення основного діагнозу і виключення поєднаної патології проводили інструментальні методи дослідження. За даними ендоскопічного обстеження відповідно до класифікації виділяли 3 ступеня запалення гастродуоденальної ділянки. [П.Я.Григорьєва і Є.П.Яковенко, 1990]. Дані кислотоутворення оцінювались за критеріями Лінара Є.Ю. та ін. [Ю.М.Ковальова].
Для визначення Нр використовували інвазивні та неінвазивні методи діагностики. Для ендоскопічної варифікації діагнозу використовували критерії Нр–асоційованої ГДП [Л.И Аруин. и др., 1993]. Визначали рівня сечовини шлункового вмісту (в трьох послідовно взятих порціях) за загальноприйнятою методикою. Неінвазивна діагностика в нашому дослідженні включала в себе імуноферментний аналіз [Н.Б. Губергриц и др., 2004], який проводили за загальноприйнятою методикою з використанням набору реактивів фірми “Vectory Best” ( Росія).
Групою контролю для дітей хворих на гастродуоденальну патологію послужило 99 відносно здорових дітей.
Роботу розглянуто комісією з біомедичної етики Буковинського державного медичного університету (витяг з протоколу № 19 від 21.06.07). Порушень морально–етичних норм при проведенні дослідження виявлено не було.
Аналіз одержаних результатів. Серед загальної кількості хворих на гастродуоденальну патологію дітей, які знаходились під спостереженням, переважали дівчатка. У більшості дітей (58,7%), був обтяжений спадковий анамнез щодо захворювань гастродуоденальної ділянки. Передача гастродуоденальної патології здійснювалась частіше по батьківській лінії (59,4%), що співпадає з результатами досліджень інших науковців [А.И.Волков,1999], рідше – по материнській (27,1%) та за обома (13,5%) лініями. Виявлено відмінності в генеалогічному анамнезі залежно від нозології. При гастродуоденіті (312 дітей) встановлена спадкова схильність серед родичів І ступеня споріднення у 31,0%, успадкування спостерігалося як по материнській, так і по батьківській лінії майже з однаковою частотою (48,2% та 51,2% відповідно), але частіше спостерігалися в сім’ї хворі сибси (38,6%). При ерозивному гастродуоденіті виявлено збільшення частоти спадкової схильності серед родичів першого ступеня споріднення порівняно з хворими на гастродуоденіт (68,9%). У цій групі встановлено успадкування переважно по батьківській лінії, при якому майже в 35,9% випадків у батька в анамнезі була виразкова хвороба ДПК. Серед дітей в яких було діагностовано виразкову хворобу ДПК у 93,2% випадків встановлена спадкова схильність серед родичів І ступеня споріднення. В той самий час серед майже здорових дітей (група порівняння) не встановлено жодного випадку ВХ серед родичів І ступеня споріднення. Коефіцієнт успадкування схильності до розвитку гастродуоденіту становить 66,3%, до розвитку виразкової хвороби ДПК – 74,6%. Все вищезазначене вказує на високу питому вагу спадковості в розвитку гастродуоденальної патології.
За результатами проведених досліджень в дітей з обтяженою спадковістю середній вік виникнення ГДП припадає на вік 10,8±1,5 років на відміну від дітей з необтяженою спадковістю – 14,6±1,3 років.
Виникнення гастродуоденальної патології за нашими даними відрізнялося залежно від статі та нозології. Частота виникнення гастродуоденіту, як у хлопчиків, так і дівчаток, характеризувалась поступовим зростанням, починаючи з віку 3–5 років, пік припадав на 10,6±1,1 років, після чого з повільним зниженням мінімального значення сягала у віці 15–17 років. Динаміка частоти виникнення ерозивного гастродуоденіту у хлопчиків характеризувалась поступовим зростанням від 5 років (виявили випадки ерозивного ураження у хлопчиків 5 і 6 років) з піком в 10,3±3,8 років та повільним зниженням до 17 років. У дівчаток спостерігали різке зростання частоти починаючи з 11 років та піком в 13,8±3,4 років, слід зазначити, що частота виникнення значно перевищувала таку у хлопчиків. Піки частоти виникнення виразкової хвороби ДПК у хлопчиків та дівчаток майже не відрізнялися (13,5±3,6 та 13,9±3,4 років відповідно), але аналізуючи динаміку її зростання виявили поступове у хлопчиків та різке у дівчаток починаючи з 7 років.
Формуванню гастродуоденальної патології у обстежених дітей сприяють такі чинники: наявність токсикозу у матері під час вагітності (31,4%), прояви анте- та інтранатальної гіпоксії (35,1%), раннє штучне та змішане вигодовування (70,3%), часті респіраторні (93,2%) та перенесені кишкові інфекції (44,9%), хронічні вогнища інфекції (64,4%), пасивне тютюнокуріння (59,1%). Початок гастродуоденальної патології пацієнти та їх батьки пов’язували з порушенням режиму харчування (37,9%), стресовим перевантаженням (17,6%), перенесеними інфекційними хворобами (2,2%), але більшість (42,4%) вказувала на безпричинний початок.
Результати наших досліджень підтверджують дані низки авторів [А.А. Михайленко и др., 2005, П.В.Новиков, 2004], що гастродуоденальна патологія – це мультифакторні захворювання, які здебільшого виникають на тлі обтяженої спадковості, трапляються в членів однієї сім’ї і передається з покоління в покоління, і не збігається з думкою інших дослідників [М.А. Бутов, 2003], які вважають ГДП лише набутими поліетіологічними захворюваннями, виникнення яких в межах однієї родини пов’язують з загальними умовами проживання, особливостями харчування та впливом однакових шкідливих чинників.
За даними нашого дослідження, клінічні прояви захворювань гастродуоденальної ділянки під час загострення, дещо відрізнялися залежно від нозології та розміру дефектів слизової оболонки. Хворі на гастродуоденіт частіше відмічали нетривалий, ниючий біль в епігастральній ділянці, який частіше виникав після прийому їжі. Скарги на тривалий нападоподібний біль різного характеру та інтенсивності, який виникав частіше після вживання гострої їжі, нервово–психічного та фізичного навантаження, відмічали хворі на ерозивний гастродуоденіт та виразкову хворобу ДПК. Безболісна форма гастродуоденальної патології виявлена нами у 2,5% випадків, яка не залежала від нозології.
Морфологічні зміни слизової оболонки шлунка та ДПК переважно (83,0%) характеризувалися малими розмірами (до 0,5 см), супроводжувалися розповсюдженим запальним процесом. Великі розміри дефекту слизової оболонки (>0,5см) частіше (35,6%) діагностувались у хворих через 4 роки після початку захворювання. Нами виявлені випадки наявності дефектів слизової оболонки великих розмірів у дітей на першому році захворювання, ці діти мали обтяжену спадковість щодо захворювань гастродуоденальної ділянки.
У дітей, хворих на гелікобактер–асоційовану гастродуоденальну патологію, виявлялися значні зсуви показників клітинної та гуморальної ланок імунітету, неспецифічної резистентності, що підтверджується дослідженнями інших науковців [А.А.Корсунский, П.Л.Щербаков, В.А. Саков, 2002] (табл. 1).
Таблиця 1
Імунологічні показники хворих на гастродуоденальну патологію та практично здорових дітей
| Лабораторні показники | І група (n= 30) | ІІ група (n=30) |
| Т–лімфоцити (%) | 45,50±1,23* | 55,60±0,50 |
| В–лімфоцити (%) | 23,80±1,53 | 23,7±0,1 |
| Т–хелпери (%) | 30,7±1,2 | 34,50±0,70 |
| Т–супресори (%) | 14,50±0,52 | 18,80±0,66 |
| Імунорегуляторний індекс | 2,1 | 1,8 |
| Ig A (г/л) | 0,9±0,1* | 1,7±0,3 |
| Ig G (г/л) | 12,88±0,79 | 11,3±1,2 |
| Ig M (г/л) | 1,7±0,2 | 1,6±0,3 |
| Фагоцитарний індекс | 17,7±0,9* | 26,4±0,9 |
| Фагоцитарне число | 2,5±0,2* | 2,95±0,1 |
| ЦІК (ум. од.) | 102,50±3,77 | 88,41±2,54 |
Примітка. * Вірогідність різниці р < 0,05
При проведенні дослідження ми виявили зв’язок між змінами імунної системи та характеру ураження гастродуоденальної ділянки. У хворих на гастродуоденіт не спостерігали суттєвих відмінностей при дослідженні показників кількості В–лімфоцитів відносно групи порівняння, вони максимально були наближені до нормативних показників. Кількість Т–лімфоцитів в крові хворих були знижені. Оцінюючи показники вмісту сироваткових імуноглобулінів, виявили, що під час загострення гастродуоденіту має місце незначне зниження вмісту Ig A (1,1±0,2 г/л порівняно з 1,7±0,3 г/л в групі порівняння). Ми виявили тенденцію до підвищення вмісту ІgG в сироватці крові у хворих на гастродуоденіт відносно групи порівняння (12,8±0,8г/л та 9,6±1,2г/л відповідно), в той час як концентрація IgМ майже ідентичний з такою групи порівняння. При досліджені фагоцитарної здатності виявили зниження показників фагоцитарного числа та фагоцитарного індексу в пацієнтів, хворих на гастродуоденіт.
Аналізуючи стан імунної системи при ерозивному ураженні гастродуоденальної ділянки спостерігали зниження основних показників відносно групи порівняння, а також відносно хворих на гастродуоденіт дітей. Так при дослідженні кількості Т–лімфоцитів виявили зниження показника на 9,8% відносно групи порівняння та на 4,1% відносно хворих на гастродуоденіт. Вміст Ig A, в сироватці крові хворих на гастродуоденіт склав 1,1±0,2 г/л, на ерозивний гастродуоденіт – 0,95±0,4 г/л порівняно з 1,7±0,3 г/л в групі порівняння. При дослідженні вмісту ІgG не виявлено відмінності його показника відносно групи порівняння, але тенденція до його підвищення при гастродуоденіті не мала місця при ерозивному ураженні. Фагоцитарне число та фагоцитарний індекс, аналогічно до решти показників, мали тенденцію до зниження відносно хворих на гастродуоденіт (2,8±0,3 та 2,6±0,1, 19,7±0,8 та 18,1±0,2 відповідно) та групи порівняння (2,8±0,3 та 2,95±0,1, 18,1±0,2 та 26,4±0,9 відповідно). При дослідженні виявили динаміку підвищення ЦІК відносно групи порівняння на 9,2% та хворих з гастродуоденітом – на 9,0%.
Значні зміни, як гуморальної так і клітинної ланок імунної системи, спостерігалися при аналізі отриманих показників у хворих на виразкову хворобу ДПК: зниження показників Т–лімфоцитів, як по відношенню до аналогічного показника практично здорових (44,5±1,4% та 55,5±0,5%, відповідно) так і до хворих на поверхневий та ерозивний гастродуоденіти (50,6±0,4%, 46,9±0,3% та 44,5±1,4%, відповідно). Аналізуючи вміст імуноглобулінів виявили значне зниження вмісту IgA до 0,8±0,1г/л порівняно з групою порівняння – 1,7±0,1г/л, хворими на гастродуоденіт – 1,1±0,2г/л, хворими на ерозивний гастродуоденіт – 0,95±0,4г/л. З боку фагоцитарної ланки спостерігалися аналогічні зміни: зниження показників фагоцитарного числа та фагоцитарного індексу відносно групи порівняння та решти нозологій гастродуоденальної ділянки. Динаміка зростання виявлена і при дослідженні показника ЦІК відносно групи порівняння на 15,9%, хворих на гастродуоденіт – на 14,8%, хворих на ерозивний гастродуоденіт – на 5,6%.
Таким чином, у дітей, хворих на гелікобактер–асоційовану гастродуоденальну патологію, під час загострення захворювання визначались зміни основних імунологічних показників: відносна недостатності клітинної ланки (зменшення відносної кількості Т–лімфоцитів І ступеня), порушення гуморальної ланки імунітету (зменшення кількості сироваткового Ig A – ІІ ступеня), недостатності фагоцитарної функції (зниження показників фагоцитарного числа та фагоцитарного індексу – І ступеня). Отримані результати дозволили вивести формулу розладів імунної системи (ФРІС): Т–лімф.І– Ig AІІ– ФЧІІ– ФІІ–, притаманну загостренню гелікобактер-асоційованої гастродуоденальної патології, яка відображає всі виявлені нами зміни при дослідженні.
Проведені дослідження дозволили встановити, що підвищення відносного ризику розвитку гастродуоденальної патології в дітей (в 4,2–8,9 раза) асоціюється з наявністю генів HLA ІІ класу алелів DQ A1 0103 та 0201. Враховуючи, що поєднання окремих алелів трапляється з різною частотою, ми дослідили асоціацію гаплотипів HLA DQ A1з урахуванням нерівноважного зчеплення. За отриманими даними, підвищення відносного ризику розвитку захворювань гастродуоденальної ділянки спостерігається у дітей з гаплотиповим поєднанням 0103 0103, 0201 0103 та 0201 0101.
В дітей з різними нозологіями виявлені особливості розподілу алелей генів комплексу гістосумісності. Виявлено, що гаплотипове поєднання 0103 0103 асоціюється з ерозивними та виразковими ураженнями гастродуоденальної ділянки і не виявляється в групі порівняння. Слід зазначити, що найважчий перебіг гастродуоденіту асоціювався з наявністю у хворих гаплотипів 0501 0102, ерозивного гастродуоденіту та виразковою хворобою ДПК – 0103 0103.
При дослідженні нами виявлено сильний прямий кореляційний зв’язок між частотою антигенів HLA DQ A1 0103, 0201 та зниженими показниками фагоцитарної активності (r0103.0201/ФА = –0,933), що вказує на те, що при збільшенні частоти антигенів DQ А1 0103, 0201 будуть знижуватись показники фагоцитарної активності, а саме ФЧ та ФІ. Це, на нашу думку, знижує протективні механізми, що сприяє виникненню гастродуоденальної патології.
Наші дослідження виявили виражений асоціативний зв'язок між системою HLA та ризиком виникнення гастродуоденальної патології. Отримані під час проведення дослідження дані можуть використовуватися для виділення дітей, схильних до розвитку гастродуоденальної патології, та як маркера окремої нозоформи.
Задля узагальнення отриманих даних, нами розроблена прогностична оцінка впливу внутрішніх та зовнішніх факторів на розвиток гастродуо-денальної патології в дітей. З метою оцінки вірогідності впливу різних чинників на розвиток, тяжкість перебігу, частоту рецидивів гастродуоденальної патології у дітей, провели регресійний аналіз результатів обстеження дітей основної групи методом множинної кореляції. Цей метод дав можливість виразити зв'язок зміни величини ризиків розвитку, тяжкості перебігу та рецидивування гастродуоденальної патології залежно від різних чинників, які на них впливають.
Отримана кореляційна модель вказує на те, що за наявності в дитини обтяженого генеалогічного анамнезу щодо гастродуоденальної патології по батьківській лінії, факту порушення харчування та тютюнокуріння на тлі наявності гаплотипів HLA локусів DQ A1 0103 0103, 0201 0103 або 0201 0301, ризик розвитку гастродуоденальної патології в дитини значно підвищується.
За даними багатофакторного аналізу імовірність розвитку ГДП в дитини було представлено у вигляді математичної моделі: ризик розвитку захворювання = 0,48Ф1+0,54Ф2+0,36Ф3
Використовуючи популяційний метод визначили показники ризику розвитку ГДП в дітей. Встановлено, що на розвиток гастродуоденальної патології впливають обтяжена спадковість, наявність імуногенетичних факторів та імунна недостатність.
Використання результатів регресійного та багатофакторного аналізів обґрунтовує точніше формувати групи ризику в кожному конкретному випадку з істотними чинниками формування хвороби, що в свою чергу розширює можливості досимптомної діагностики, підвищує ефективність первинної профілактики при проведенні медико–генетичного консультування.
Нами проведений регресійний та багатофакторний аналізи імовірних чинників які впливають на ступінь тяжкості перебігу гастродуоденальної патології та на розвиток рецидиву захворювання. Виходячи з результатів багатофакторного аналізу, з метою прогнозування тяжкості перебігу гастродуоденальної патології в обстежених дітей, тяжкість клінічного перебігу та ризик розвитку рецидиву гастродуоденальної патології представили у вигляді математичних моделей:
ризик тяжкого перебігу гастродуоденальної патології = 0,39Ф1+0,47Ф2+0,35Ф3
ризик рецидиву гастродуоденальної патології = 0,59Ф1+0,57Ф2+0,46Ф3
Встановлено, що на тяжкість перебігу впливають статева приналежність, обтяжена спадковість, тривалість захворювання, ступінь імунних порушень та наявність імуногенетичних маркерів. Основні чинники ризику виникнення рецидиву гастродуоденальної патології в обстежених дітей: обтяжена спадковість, тривалість захворювання, розмір дефекту, результати попередніх курсів лікування з визначенням індексу імунної стимуляції, наявність імуногенетичних маркерів. Сукупне використання регресійного та багатофакторного аналізу дозволило всебічно проаналізувати велику кількість чинників, які впливають на розвиток, тяжкість перебігу та виникнення рецидивів гастродуоденальної патології в дітей. Все вищезазначене дозволить використовувати отримані математичні моделі з інтерпретацією її параметрів на практиці.
Дітям, хворим на гелікобактер–асоційованиу гастродуоденальну патологію, в гострому періоді захворювання проводили лікування, спрямоване на ерадикацію Нр, усунення запального процесу та загоєння дефектів гастродуоденальної ділянки. Разом з тим, в одній групі нами запропоновано комплексне використання Протефлазиду з загальноприйнятою терапією. Беручи до уваги результати нашої роботи, хворим на гелікобактер–асоційовану гастродуоденальну патологію дітям притаманні характерні зміни імунної системи, ступінь зниження показників якої потребує призначення імунокорегувальної терапії.
Проводячи порівняльну оцінку ефективності застосування розробленої нами схеми лікування в дітей хворих на гелікобактер–асоційовану ГДП та загальноприйнятого лікування, виявили певні відмінності. Залежно від схеми лікування діти основної групи поділені на дві групи: І – діти (n=30), яким проводилася антигелікобактерна терапія в поєднанні з Протефлазидом (патент № 15578 А61Р 1/00, Бюл. №7, 17.07.2006), ІІ – діти (n=26), яким призначали загальноприйняту антигелікобактерну терапію.
Порівняльний аналіз динаміки клінічних проявів виявив, що динаміка больового синдрому в першій групі мало відрізняється в порівнювальних підгрупах з невеликим переважанням до зниження інтенсивності в перші два дні в основній групі – 64,29% пацієнтів, 35,71% – контрольної групи. У понад половини дітей, які не отримували Протефлазид больовий синдром зберігався до 3–4 днів (60,0%). Спостерігається подібна динаміка диспепсичного синдрому. В основній групі 75,0% пацієнтів відмічали відсутність нудоти, печії в перші два дні терапії, у 80,0% дітей контрольної групи, навпаки, диспепсія зберігалась до 3–4 доби терапії. Подібна тенденція відмічається при спостереженні за динамікою локальної пальпаторної болючості.
Об’єктивним підтвердженням ефективності Протефлазиду є позитивна динаміка ендоскопічної картини слизової оболонки шлунка і ДПК. Після лікування запропонованою нами схемою в жодної дитини не виявлений пангастрит чи ерозії. При виразковій хворобі ДПК швидкість відновних процесів у дітей І підгрупи вища від такої в дітей з традиційною терапією. Це пояснює скорочення тривалості клінічних проявів в даній групі.
Призначення Протефлазиду в лікувальній дозі сприяло прискоренню позитивної динаміки імунологічних показників. Задля проведення оцінки ефективності Протефлазиду, як імунокерегувального засобу, розрахували індекси стимуляції основних показників імунограмм, але враховуючи, що Протефлазид комплексно використовувався в поєднанні із традиційним лікуванням, яке можливо зумовлює динаміку деяких показників, ми вираховували індекс стимуляції і серед пацієнтів з традиційною терапією. Аналізуючи отримані результати ми виявили, що індекс стимуляції імунологічних показників значно вище у пацієнтів після проведеного комплексного лікування з використанням Протефлазиду порівняно з аналогічним після лікування за загальноприйнятою схемою.
Стосовно ерадикації Нр то в основній групі вона становила 93,3%, в групі порівняння – 72,1% (табл. 2).
Таблиця 2
Порівняльна характеристика застосування Протефлазиду в комплексній терапії
| Клінічні прояви | І–а група | ІІ–а група |
| Ерадикація Нр | 29 (96,7%) | 19 (72,1%) |
| Ендоскопічна ремісія | 29 (96,7%) | 19 (72,1%) |
| Нормалізація інтрагастральної кислотності | 20 (66,7%) | 15 (57,7%) |
| Ліжко–дні | 13–14 | 19–21 |
| Скорочення ліжко–днів | 33,7% | 16,6% |
| Кількість ерадикаційних курсів | 1,2+0,4 | 2,4+0,5 |
Ефективність лікування оцінювали за допомогою епідеміологічних показників: зниження відносного ризику, зниження абсолютного ризику та визначення кількості хворих, яких потрібно пролікувати для попередження несприятливих наслідків лікування – Number Needed to Treat (NNT), в нашому випадку рецидиву захворювання. Відносний ризик розвитку рецидивів гелікобактер–асоційованої гастродуоденальної патології в дітей знизився в 0,8 раза (чІ =3,96, р<0,05) порівняно з традиційною схемою.
Підсумовуючи вищезазначені результати власних клінічних спостережень та спеціальних досліджень, можливо зробити висновок, що в хворих на гастродуоденальну патологію дітей були уточнені чинники схильності до розвитку захворювання, вивчені особливості клінічних проявів та змін клінініко–лабораторних показників під час загострення. У хворих дітей, які знаходилися на спостереженні, були досліджені особливості розподілу алелів генів головного комплексу гістосумісності та їх гаплотипових комбінацій, що дає можливість більш детально орієнтуватись по відношенню до ризику розвитку та прогнозування перебігу гастродуоденальної патології. Досліджений характер змін показників імунологічної реактивності організму у пацієнтів з різними захворюваннями гастродуоденальної ділянки, що дозволяє дати більш об’єктивну оцінку ефективності терапії
Виявлені та проаналізовані за допомогою регресійного та багатофакторного аналізів чинники ризику розвитку, тяжкості перебігу та рецидивування гастродуоденальної патології можуть бути застосовані на практиці з подальшим формуванням груп ризику, що значно полегшить досимптомну діагностику та розширить можливості проведення профілактичних заходів. Все вищезазначене дозволить зменшити частоту та швидкість поширення гастродуоденальної патології серед дитячого населення.
Результати дослідження вказали, що використання імуномодулятора в дітей з гастродуоденітом, ерозивним гастродуоденітом та виразковою хворобою ДПК сприяло нормалізації більшості параметрів імунологічної реактивності, ерадикації Нр і виявило протирецидивну дію. При використанні Протефлазиду в комплексі з традиційною терапією констатували швидшу позитивну динаміку клінічних проявів з настанням клінічної ремісії, що сприяло скороченню ліжко–днів на 33,7%.
Узагальнюючи отримані результати нами розроблений профілактично–діагностичний алгоритм гастродуоденальної патології у дітей (рис. 1).


![]()

![]()
![]()

![]()

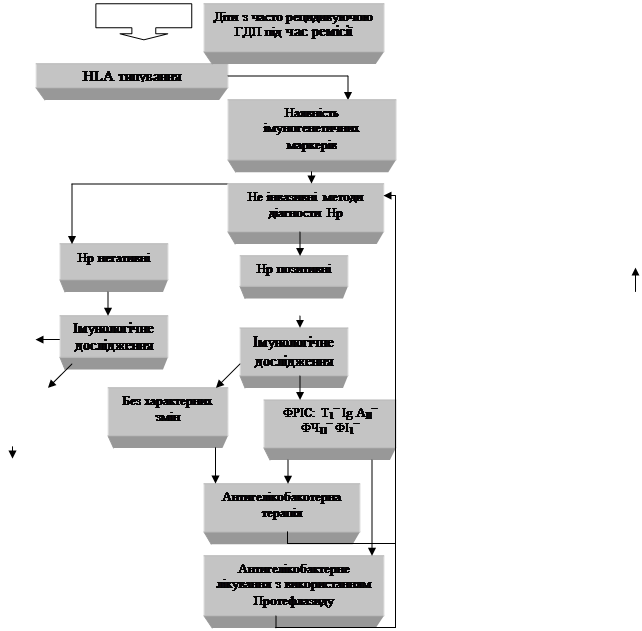

Рис. 1. Діагностичний алгоритм гастродуоденальної патології у дітей.
ВИСНОВКИ
У дисертації наведені теоретичне узагальнення і нове вирішення актуального завдання стосовно клініко-генетичних особливостей перебігу гастродуоденальної патології в дітей. На основі визначення ролі HLA-системи у виникненні і характері перебігу гастродуоденальних захворювань розроблені нових критерії формування груп ризику розвитку патології гастродуоденальної ділянки в дітей.
1. Частка генетичної компоненти у виникненні гастродуоденальної патології є вагомою, про що свідчить високий коефіцієнт успадкування схильності до розвитку в дітей гастродуоденіту (КУС = 66,3% ) та виразкової хвороби (КУС = 74,6%). У дітей зі спадковою обтяженістю гастродуоденальна патологія клінічно виявляється в більш ранньому віці (10,8+1,5 років), ніж у хворих без обтяженої спадковості (14,6±1,3 років), і характеризується тяжчим перебігом.
2. У дітей, хворих на хронічний гастрит, гастродуоденіт та виразкову хворобу, в період загострення реєструються майже однакові зсуви параметрів імунологічної реактивності: зниження відносної кількості Т–лімфоцитів у крові, дисімуноглобулінемія ІV ступеня та зниження показників фагоцитарної функції (ФІ 2,5+0,2; ФІ 17,7+0,9).
3. Імуногенетичними маркерами у дитячого населення Північної Буковини схильності до розвитку гастродуоденальної патології виділено гени HLA–комплексу ІІ класу DQ A1 0103, 0201 та гаплотипове поєднання генів 0103 0103, 0201 0103, 0201 0301. При успадкуванні двох і більше генів та їх комбінації, що асоціюються з гастродуоденальними захворюваннями, віднос-ний ризик виникнення захворювань зростає в 4,2–8,9 раза.
4. За наявності детермінант-протекторів або їх комбінацій (0101, 0501) в генному складі тканин головного комплексу гістосумісності дитини ризик виникнення гастродуоденальної патології є мінімальний.
5. Несприятливими прогностичними чинниками виникнення гастродуоде-нальної патології слід вважати позитивний генеалогічний анамнез – OR = 5.24 [2.11-5.98], (р<0,0001), всі типи сімейної спадковості та наявність у дитини імуногенетичних маркерів – OR =6,11 [4,57–11,23] (р<0,01).
6. Диференційоване лікування гелікобактер–асоційованої гастродуоденаль-ної патології з включенням до лікувального комплексу протефлазиду призводить до скорочення тривалості лікування (на 26,4%) і загоєння виразкового дефекту (на 29,5%) та зменшення вдвічі кількості ерадикаційних курсів порівняно з традиційною терапією. Клінічна ефективність запропонованого комплексного лікування гелікобактер–асоційованої гастродуоденальних захворювань в дітей становить 96,7%.
РЕКОМЕНДАЦІЇ ЩОДО НАУКОВОГО ТА ПРАКТИЧНОГО ВИКОРИСТАННЯ ОДЕРЖАНИХ РЕЗУЛЬТАТІВ
1. На доклінічному етапі доцільно формувати “групи ризику” розвитку гастродуоденальних захворювань у дітей на основі їхнього позитивного генеалогічного анамнезу.
2. У практику роботи медико-генетичих консультацій доцільно впровадити імуногенетичне обстеження сімей із гастродуоденальною патологією для встановлення ступеня ризику розвитку хронічного гастриту, гастродуоденіту та виразкової хвороби.
3. Дітям “групи високого ризику” потрібно проводити періодичні профілактичні огляди з метою виключення керованих чинників ризику розвитку гастродуоденальної патології (розробка індивідуального раціону та режиму харчування, заходів, спрямованих на зменшення нервово–психічного та фізичного навантаження, санація хронічних вогнищ інфекції).
4. З метою об’єктивної оцінки тяжкості гастродуоденальних захворювань у дітей під час загострення та корекції лікування варто використовувати сукупність параметрів імунологічної реактивності у вигляді ФРІС: Тлім.І– Ig AІІ– ФЧІІ– ФІІ–.
5. При гелікобактер–асоційованих гастритах, гастродуоденітах та виразковій хворобі дванадцятипалої кишки рекомендовано додавати до комплексної терапії протефлазид: дітям 6–12 років – по 5 крапель тричі за добу, старшим 14 років – по 10 крапель тричі за добу при збереженій кислотоутворювальній функції шлунка за 40 хв. до їди, при підвищеній – через 60 хв. після їди впродовж 3 тижнів. Лікування протефлазидом слід розпочинати під час загострення гастродуоденальної патології і проводити повторні курси з інтервалом 6 місяців під час диспансерно–поліклінічного спостереження.
СПИСОК НАУКОВИХ ПРАЦЬ, ОПУБЛІКОВАНИХ ЗА ТЕМОЮ ДИСЕРТАЦІЇ
1. Боднар Г.Б. Прогнозування виникнення, розвитку та прогресування гастродуоденальної патології дитячого віку // Хірургія дитячого віку. – 2006. – Т. ІІІ. № 4 (14). – С. 35–42. Особистий внесок дисертанта: проведено інформаційний пошук, аналіз джерел літератури, написання роботи.
2. Бондар Г.Б., Сорокман Т.В. Асоціації генів HLA–системи з розвитком гастродуоденальної патології в дітей Буковини // Буковинський медичний вісник – 2007. - № 2. – С. 81–83. Особистий внесок дисертанта: проведення імуногенетичного дослідження дітей, хворих на гастродуоденальну патологію, та практично здорових дітей, аналіз отриманих результатів з їх статистичною обробкою, написання роботи.
3. Боднар Г.Б. Особливості симптомокомплексу гастродуоденальної патології в дітей на сучасному етапі // Клінічна та експериментальна патологія. – 2007. – Т. VІ, № 1. – С. 15–17. Особистий внесок дисертанта: клінічне обстеження дітей із гастродуоденальною патологією, встановлення відмінностей клінічних проявів залежно від тяжкості та тривалості захворювання.
4. Боднар Г.Б., Сорокман Т.В. Ефективність використання протефлазиду при гелікобактер–асоційованій гастродуоденальній патології у дітей. // Галицький лікарський вісник. – 2007. – № 2. – С. 71–72. Особистий внесок дисертанта: лікування хворих дітей, розробка та впровадження власного способу удосконалення лікування, аналіз отриманих результатів з їх статистичною обробкою, написання роботи.
5. Деклараційний патент на корисну модель № 15578, Україна, МПК (2006) А61Р 1/00 „Спосіб лікування гелікобактерної інфекції у дітей” // Боднар Г.Б., Сокольник С.В., Сорокман Т.В.; . Бюл. № 7 від 17.07.2006 р. Особистий внесок дисертанта: розробка схеми антигелікобакерного лікування, оцінка клінічної ефективності запропонованого способу лікування, оформлення тексту винаходу.
6. Боднар Г.Б. Шлукново–стравохідний рефлюкс у дітей // Проблемні питання лікування дітей: Матеріали науково-практичної конференції – Київ, 2006. – С. 31.
7. Боднар Г.Б., Сорокман Т.В., Сокольник С.В. Застосування Протефлазиду у дітей, хворих на гелікобактерасоційовані гастродуоденіти // Сучасні наукові дослідження: Матеріали науково-практичної конференції з міжнародною участю – Дніпропетровськ, 2006. - С. 23.
8. Боднар Г.Б. Використання Протефлазиду при гелікобактер–асоційованій гастродуоденальній патології у дітей // Сучасні лікувально–діагностичні технології в хірургії дитячого віку: Матеріали І всеукраїнського конгресу дитячих хірургів з міжнародною участю. – Вінниця, 2007. – С.331.
9. Боднар Г.Б. Гастродуоденальна патологія дитячого населення // Матеріали Всеукраїнської науково–практичної конференції “Функціональні захворювання шлунково–кишкового тракту в дітей – актуальні проблеми дитячої гастроентерології”. – Чернівці, 2006. – С.3.
10. Боднар Г.Б., Сокольник С.О., Боднар Б.М. Функціональні порушення шлунково–кишкового тракту в дітей з гастродуоденітом в практиці дитячого хірурга // Матеріали Всеукраїнської науково–практичної конференції “Функціональні захворювання шлунково–кишкового тракту в дітей – актуальні проблеми дитячої гастроентерології”. – Чернівці, 2006. – С.4.
АНОТАЦІЯ
Боднар Г.Б. Імуногенетична характеристика та критерії формування груп ризику розвитку гастродуоденальної патології у дітей.
Дисертація на здобуття наукового ступеня кандидата медичних наук за спеціальністю 14.01.10 – педіатрія. – Тернопільський державний медичний університет імені І.Я. Горбачевського МОЗ України, Тернопіль, 2008.
Дисертація присвячена вивченню факторів ризику (генеалогічних, аліментарних, імунологічних, імуногенетичних) та визначенню маркерів гастродуоденальної патології у дітей.
Встановлено, що у дітей з обтяженою спадковістю, відносно гастродуоденальної патології у родині, наявні гени HLA–комплексу ІІ класу DQ A1 0103, 0201 та гаплотипове поєднання генів 0103 0103, 0201 0103, 0201 0301. При успадкуванні двох і більше генів та їх комбінації, що асоціюються з гастро-дуоденальними захворюваннями, відносний ризик виникнення захворювань зростає в 4,2-8,9 рази.
В результаті проведеного дослідження встановлено, що на формування гастродуоденальної патології у дітей значний вплив мають аліментарні, імуногенетичні, імунологічні чинники. Науково обґрунтована та вивчена клінічна ефективність доповнення класичної терапії гелікобактер–асоційованих захворювань протифлазидами у дітей.
Ключові слова: діти, чинники ризику, гастродуоденальна патологія, профілактика.
АНHОТАЦИЯ
Боднарь А.Б. Иммуногенетическая характеристика и критерии формирования групп риска развития гастродуоденальной патологии у детей. – Рукопись.
Диссертация на соискание ученой степени кандидата медицинских наук по специальности 14.01.10 – педиатрия. – Тернопольский государственный медицинский университет им. И.Я. Горбачевского МОЗ Украины, Тернополь, 2008.
Диссертационная робота посвящена изучению генетических, иммуногенетичес-ких, иммунологических факторов риска развития гастродуоденальной патологии.
Обследованию подвергались дети больные гастродуоденитом, эрозивным гастродуоденитом и язвенной болезнью двенадцатиперстной кишки 6-18 лет. Установлено что коэффициент наследования при гастродуодените составляет 66,3% при язвенной болезни двенадцатиперстной кишки – 74,6%.
При иммуногенетическом исследовании установлены маркеры предрасположенности к развитию патологии гастродуоденальной области, так повышенный риск развития гастродуоденальной патологии у детей ассоциируется с наличием аллелей HLA DQ A1 0103, 0201 и их гаплотипного сочетания 0103 0103, 0201 0103, 0201 0301. При наличии аллелей детерминант-протекторов или их комбинации (0101,0501) в геномном составе главного комплекса гистосовместимости риск развития гастродуоденальной патологии является минимальным.
В результате исследования было установленно, что для больных хеликобактер-асоциированной гастродуоденальной патологией, во время обострения характерны изменения со стороны иммунной системы, а именно: уменьшение относительного количества Т-лимфоцитов, дисимуноглобулинемия ІV типа, снижение показателей фагоцитарной функции. На основе полученных данных создана формула расстройств иммунной системы, характерная для хронических воспалительных заболеваний гастродуоденальной области. Исходя из вышесказанного – сдвиги иммунной системы являются показанием к назначению иммуномодулирующей терапии.
В результате проведенных исследований разработаны математические модели риска развития, тяжести течения и риска развития рецидива гастродуоденальной патологии на основе проведенного многофакторного анализа всех возможных факторов которые могу влиять на развитие и течение хронических воспалительных заболеваний гастродуоденальной области.
В работе научно обоснована целесообразность и изучена клиническая эффективность дополнения антихеликобактерной терапии хеликобактер-ассоциированной гастродуоденальной патологии у детей в качестве иммунномодулирующего средства – Протефлазид (что значительно ускорило позитивную динамику диспепсического и купирование болевого синдрома). А также способствовало ускорению репаративных процессов слизистой гастродуоденальной области. Комбинированное использование Протефлазида уменьшило срок пребывания больного на стационарном лечении и вдвое сократило количество эрадикационных курсов. Клиническая эффективность использования Протефлазида составила 96,7%.
При хеликобактер-ассоциированной гастродуоденальной патологии рекомендовано добавлять к комплексному лечению протефлазид: детям 6-12 лет – по 5 капель трижды в день, старше 14 лет – по 10 капель трижды в день при не нарушенной кислотообразующей функции желудка за 40 мин до еды, при повышенной – через 60 мин после приема пищи. Лечение протефлазидом следует начинать во время обострения гастродуоденальной патологии и проводить повторные курсы с интервалом 6 месяцев во время диспансерно-поликлинического наблюдения.
Ключевые слова: дети, факторы риска, гастродуоденальная патология, профилактика.
ANNOTATION
Bodnar A.B. Immunogenetic the characteristic and criterion of formation of groups of risk of development gastroduodenal of pathology at children. – Manuscript.
The dissertation on competition of a scientific degree of the candidate of medical sciences on a speciality 14.01.10 – pediatrics – Ternopil Ivan Horbachevsky medical state university, Ternopil, 2008.
Dissertation of the robot is devoted to study genetic, immunogenetic, immunolodgy of risk factors of development gastroduodenal of pathology. Is established that factor of inheritance at gastroduodenal makes 66,3 % at ulcer of illness duodenum – 74,6%. At immunogenetic research the markers of predisposition to development of a pathology gastroduodenal of area are established, so the raised risk of development gastroduodenal of pathology at children associates with presence alleles HLA DQ A1 0103, 0201 and them of a combination 0103 0103, 0201 0103, 0201 0301. At presence alleles a determinant – protective or their combinations (0101, 0501) in genome structure of the main complex histocompatibility the risk of development gastroduodenal of pathology is minimal.
In work the expediency is scientifically proved and the clinical efficiency of addition antyhelicobacter of therapy helicobacter-associated gastroduodenal by a pathology at children in quality immunomodulator of a means – Proteflazid. The clinical efficiency of use Proteflazid has made 96,7%.
Key words: children, gastroduodenal a pathology, risk factors, preventive maintenance.
ПЕРЕЛІК УМОВНИХ ПОЗНАЧЕНЬ
Нр – Helicobacter pylori
ГДП – гастродуоденальна патологія
КУС – коефіцієнт успадкування схильності
ФЧ – фагоцитарне число
ФІ – фагоцитарний індекс
ЦІК – циркулюючі імунні комплекси
0 комментариев