Навигация
Положення у ліжку з піднятим головним кінцем на 15-20 °
1. Положення у ліжку з піднятим головним кінцем на 15-20 °.
2. ШВЛ у режимі нормовентиляції (ДО = 6-7 мл/кг, ЧД = 16-18 за хв., FiO2 = 30 %) частотним респіратором протягом всього періоду коматозного стану.
3. Загальний об’єм інфузійної терапії призначався з розрахунку 40 мл/кг на добу з корекцією патологічних втрат за методом балансів. Основним препаратом для інфузії був ізотонічний розчин натрію хлориду. Для підтримання колоїдно-осмотичного тиску використовувались препарати на основі гідроксиетильованого крохмалю (Рефортан) та модифікованої желатини (Гелофузін) в об’ємі 20% від загальної кількості рідини, що вводилась. Розчин альбуміну призначали лише при наявності гіпопротеінемії менш ніж 50 г/л. Еритроциарна маса призначалась при рівні гемоглобіну менш ніж 80 г/л.
4. З метою корекції показників гемодинаміки за необхідністю використовувались симпатомиметики (адреналін 0,05-0,1 мкг/кг/хв. або дофамін 7-10 мкг/кг/хв.). Середній артеріальний тиск утримувався на рівні не менше 90 мм рт. ст.
5. Аналгоседація проводилась у пацієнтів протягом перших 2-3 діб.
6. З антиоксидантних препаратів усім пацієнтам вводилась аскорбінова кислота в дозі 500 мг/добу.
7. Антибактеріальні препарати використовували з урахуванням ступеню проникності їх крізь ГЕБ (цефалоспорини 3 та 4 покоління). При приєднанні вентилятор-асоційованої пневмонії призначався другий антибактеріальний препарат (фторхінолони або аміноглікозиди).
8. Усім пацієнтам призначалося раннє (з 2 доби) зондове харчування готовими сумішами відповідно міжнародним рекомендаціям за системою ESPEN.
9. Лікувальні заходи, спрямовані на профілактику утворення стресових виразок, проводили за допомогою Н2-блокаторів (квамател 40мг/добу).
10. Ноотропні стимулюючі засоби (пірацетам 10 г/добу) призначали при підвищенні рівня свідомості до 10 балів ШКГ та вище.
Забір крові для визначення концентрації GFAP та NSE у пацієнтів з ТЧМТ проводили протягом перших 2 годин після надходження та в подальшому на 2-3, 6-7, 10-11 та 13-15 добу. Кров центрифугували 10 хв. при 2000 g, сироватку заморожували при температурі -20 °С та тримали при цих умовах до проведення дослідження.
Під керівництвом д.мед.н. О.І. Гуріної нами були отримані високоочищені препарати нейроспецифічних білків GFAP та NSE та на їх основі розроблені діагностичні тест-системи на основі моноклональних антитіл для «сендвіч-варіанту» імуноферментного аналізу, які дозволяли надійно та відтворювано визначати концентрації GFAP та NSE у сироватці крові у інтервалі концентрацій від 1 до 128 нг/мл з межею чутливості 1 нг/мл.
Статистичний аналіз проводили за допомогою ліцензійних програмних пакетів MS Office XP. Розраховувались М (середня), s (стандартне відхилення) та m (стандартна похибка стандартного відхилення). Для оцінки достовірності відмінностей використовували t – критерій Стьюдента. Для багаторазових порівнянь використовувалась поправка Бонфероні. Для виявлення зв’язку між величинами використовувався кореляційний аналіз з розрахунком коефіцієнту кореляції Пірсона.
Результати власних досліджень. Аналіз етіології ізольованої тяжкої ЧМТ показав, що найбільшу кількість хворих складали пацієнти, що отримали травму внаслідок падіння з висоти зросту (84,8%). Друге місце займав дорожньо-транспортний травматизм (11%). Більшість пацієнтів – це чоловіки у віці понад 35 років, що страждали на хронічний алкоголізм. Найчастішим проявом ізольованої ТЧМТ була субдуральна гематома (63,9% постраждалих); рідшим інтракраніальним проявом тяжкої ЧМТ була епідуральна гематома (25,6% пацієнтів). Вогнища забою, що потребували хірургічної корекції, спостерігалися у 45% постраждалих.
При імунохімічному дослідженні сироватки крові здорових донорів було визначено, що концентрація GFAP складала 3,0 ± 0,12 нг/мл (не перевищувала 4,1 нг/мл), а концентрація NSE складала 7,7 ± 0,39 нг/мл (не перевищувала 12,4 нг/мл).
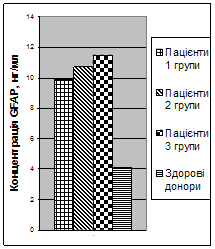
При дослідженні концентрації GFAP у сироватці крові пацієнтів з ТЧМТ (рис. 3) було виявлено, що у пацієнтів 1, 2 та 3 груп вона достовірно не відрізнялась, складаючи 9,9 ± 0,5 нг/мл, 10,7 ± 0,9 нг/мл та 11,5 ± 0,9 нг/мл відповідно, та достовірно (p < 0,01) перевищувала донорський рівень.
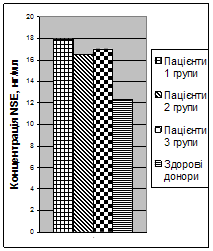
При дослідженні концентрації NSE (рис. 2) при надходженні також не було виявлено різниці між групами (концентрація складала 18,3 ± 3,5 нг/мл, 16,5 ± 2,5 нг/мл та 17,0 ± 1,8 нг/мл відповідно у пацієнтів 1, 2 та 3 груп), та концентрація достовірно (p < 0,01) перевищувала донорський рівень. Виявлений середньої сили кореляційний зв’язок (r = - 0,57) між концентрацією NSE та рівнем свідомості при надходженні у пацієнтів з ТЧМТ.
|
Рис. 2 Концентрація NSE у сироватці крові у перші 6 годин після тяжкої ЧМТ |
Рис. 3 Концентрація GFAP у сироватці крові у перші 6 годин після тяжкої ЧМТ |
Таким чином, протягом перших 6 годин тяжкої ЧМТ відзначався прорив ГЕБ з «виходом» у кров нейроспецифічних білків GFAP та NSE, що є результатом значного первинного ушкодження нейронів та астроцитів. Нейронспецифічна енолаза може служити додатковим діагностичним критерієм тяжкості нейротравми.
При кількісному динамічному моніторингу концентрації GFAP у пацієнтів, що отримували стандартну терапію (1 група), були виявлені наступні зміни (рис. 5). У динаміці травматичної хвороби головного мозку концентрація GFAP продовжувала зростати та досягала максимальних значень (23,0 ± 8,8 нг/мл, що в 5,6 раз перевищує донорський рівень) на 10-11 добу. Необхідно відзначити, що концентрація даного білка не досягала нормальних значень до кінця дослідження (13-15 доба). Цей факт можна пояснити з позицій розвитку реактивного астрогліозу, функцією якого є репарація та ізоляція зони ушкодження.
При кількісному динамічному моніторингу концентрації NSE у пацієнтів, що отримували стандартну терапію (1 група), були виявлені наступні зміни (рис. 4). На 2-3 добу відзначався значний підйом концентрації даного білка до 30,8 ± 5,1 нг/мл, що у 2,5 рази більше донорського рівня. У подальшому на 6-7 добу відзначалося достовірне (р = 0,005) зниження концентрації NSE до рівня 18,8 ± 2,1 нг/мл. Нормалізація концентрації NSE відзначалася на 13-15 добу посттравматичного періоду. Дана динаміка концентрації нейронспецифічної енолази відповідає концепції вторинних ішемічних ушкоджень головного мозку.
При кількісному динамічному моніторингу концентрації GFAP у пацієнтів, що отримували додатково до стандартної терапії L-лізину есцинат (2 група) були виявлені наступні зміни (рис. 5). На 2-3 та 6-7 добу концентрація даного білка складала 7,8 нг/мл та 11,4 нг/мл відповідно та була достовірно вище донорського рівня (p < 0,05) та достовірно нижче, ніж у пацієнтів 1 групи (p < 0,05). Це свідчить про здатність протинабрякового препарату L-лізіину есцинату зменшувати вторинну загибель астроцитів у період максимально вираженого набряку головного мозку та стабілізувати ГЕБ. У подальшому концентрація GFAP не відрізнялася від пацієнтів 1 групи та була достовірно вище донорського рівня (p < 0,05).
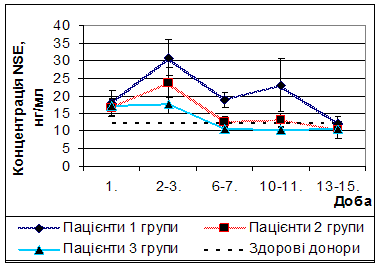
Рис. 4 Динаміка концентрації нейронспецифічної енолази у пацієнтів досліджуваних груп.
При кількісному динамічному моніторингу концентрації NSE у пацієнтів, що отримували додатково до стандартної терапії L-лізину есцинат (2 група) були виявлені наступні зміни (рис. 4). На 2-3 добу відзначався пік концентрації NSE (23,7 ± 4,1 нг/мл), проте на 23% менший, аніж у пацієнтів 1 групи.
Нормалізація концентрації NSE у сироватці крові пацієнтів 2 групи наступала на 6-7 добу, у той час, як у пацієнтів, що отримували стандартну терапію, вона досягала норми лише на 13-15 добу після травми. Це свідчить про здатність L-лізину есцинату у комплексі інтенсивної терапії тяжкої ЧМТ вже на 6-7 добу стабілізувати ГЕБ та зменшувати вторинні ушкодження нейронів.
При кількісному динамічному моніторингу концентрації GFAP у пацієнтів, що отримували додатково до стандартної терапії L-лізину есцинат та мексидол (3 група) були виявлені наступні зміни (рис. 5). На 2-3добу концентрація GFAP була на 65,6% менше, аніж у пацієнтів 1 групи. У подальшому, на протязі всього періоду спостереження (з 2 до 15 доби), концентрація GFAP у пацієнтів 3 групи була нижче, ніж у пацієнтів 1 групи, та – на 13-15 добу – ніж у пацієнтів 2 групи, проте була вищою за донорський рівень. Це свідчить про здатність у комбінації L-лізину есцинату та мексидолу стабілізувати ГЕБ та зменшувати відстрочену загибель астроцитів.
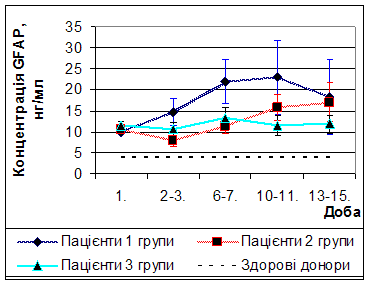
Рис. 5 Динаміка концентрації гліофібрилярного кислого протеїну у пацієнтів досліджуваних груп
При кількісному динамічному моніторингу концентрації NSE у пацієнтів, що отримували додатково до стандартної терапії L-лізину есцинат та мексидол (3 група), були виявлені наступні зміни (рис. 4). На 2-3 добу концентрація NSE у сироватці крові була достовірно (р < 0,05) вищою за донорський рівень та достовірно (р < 0,05) нижчою, аніж у пацієнтів 1 групи. На 6-7 добу концентрація NSE була у межах норми та була достовірно (р < 0,05) нижчою, аніж у пацієнтів 1 групи. В подальшому концентрація NSE не підвищувалася. Відсутність підйому концентрації нейронспецифічної енолази на 2-3 добу у пацієнтів 3 групи, а також її швидка нормалізація свідчить про значний нейропротекторний ефект у комбінації L-лізину есцинату та мексидолу у комплексі інтенсивної терапії тяжкої ЧМТ.
Для клінічного аналізу ефективності запропонованих методів інтенсивної терапії тяжкої ЧМТ використовувались наступні параметри: динаміка рівня свідомості та тривалість ШВЛ у пацієнтів, що вижили, та летальність.
Рівень порушення свідомості оцінювався в балах шкали ком Глазго в динаміці травматичної хвороби головного мозку.
При надходженні рівень порушення свідомості у пацієнтів 1, 2 та 3 груп складав 7,0 ± 0,18 бала, 7,0 ± 0,16 бала и 6,8 ± 0,20 бала відповідно (табл. 1). На 2-3 добу рівень свідомості збільшився у пацієнтів 1 групи на 0,7 бала, у пацієнтів 2 групи на 1,1 бала та у пацієнтів 3 групи – на 1,3 бала. Дана динаміка корелювала з концентрацією нейронспецифічної енолази (- 0,43 > r > - 0,56). На 6-7 добу середній рівень свідомості у пацієнтів 1 групи підвищувався на 2 бали, в 2 групі – на 2,2 бали та в 3 групі - на 2,7 бали. Загалом під час спостереження у пацієнтів 1 групи свідомість відновилась на 4,6 бали, у пацієнтів 2 групи – на 4,8 бали, а у пацієнтів 3 групи – на 5,4 бали. Більш швидкий темп відновлення свідомості у пацієнтів 2 та 3 груп, порівняно з 1 групою, що корелює зі ступенем загибелі нейронів, вказує на ефективність оптимізованих методів інтенсивної терапії в профілактиці вторинних ішемічних пошкоджень.
Таблиця 1
Динаміка рівню свідомості (бали ШКГ) у пацієнтів досліджуваних груп, що вижили, M ± m
| 1 доба | 2-3 доба | 6-7 доба | 10-11 доба | 13-15 доба | |
| 1 група (n=31) | 7,0 ± 0,18 | 7,7 ± 0,25 | 9,0 ± 0,32 | 10,6 ± 0,38 | 11,6 ± 0,34 |
| 2 група (n=25) | 7,0 ± 0,16 | 8,1 ± 0,26 | 9,2 ± 0,36 | 10,9 ± 0,34 | 11,8 ± 0,40 |
| 3 група (n=29) | 6,8 ± 0,20 | 8,0 ± 0,35 | 9,5 ± 0,43 | 11,1 ± 0,50 | 12,2 ± 0,39 |
Штучна вентиляція легенів у пацієнтів досліджуваних груп проводилась з моменту надходження до моменту відновлення свідомості вище 8 балів ШКГ частотним респіратором PLV-100 в режимі нормовентиляції (ДО = 6 - 7 мл/кг, ЧД = 16-18 в 1 хв, FiO2 = 30%). При проведенні кореляційного аналізу нами було виявлено, що тривалість ШВЛ залежить від первинного рівня порушення свідомості (r = - 0,72) та від віку пацієнта (r = 0,53), а від тривалості ШВЛ залежить частота розвинення вентилятор-асоційованої пневмонії (r = - 0,47).
Враховуючи, що рівень порушення свідомості при надходженні та вік пацієнтів усіх груп співставимі, тривалість ШВЛ визначалась характером та ефективністю інтенсивної терапії, що проводилась.
Таблиця 2
Тривалість ШВЛ у пацієнтів досліджуваних груп, що вижили, M ± m
| Кількість трахеостом | Кількість вентилятор-асоційованих пневмоній | Тривалість ШВЛ, діб, M ± m | |||
| Кількість пацієнтів | % | Кількість пацієнтів | % | ||
| 1 група (n=31) | 11 | 35,5 | 11 | 35,5 | 8,9±0,21 |
| 2 група (n=25) | 9 | 36,0 | 8 | 32,0 | 7,4±0,28 |
| 3 група (n=29) | 10 | 34,4 | 8 | 27,6 | 6,3±0,17 |
При порівнянні термінів переходу на самостійне дихання нами було встановлено (табл. 2), що у пацієнтів 1 групи середня тривалість ШВЛ становила 8,9 ± 0,21 діб, при цьому вентилятор-асоційована пневмонія виявлена в 35,5% випадків. У пацієнтів 2 групи середня тривалість ШВЛ становила 7,4 ± 0,28 доби, вентилятор-асоційована пневмонія виявлена у 32% пацієнтів. Пацієнти 3 групи знаходились на ШВЛ, в середньому, 6,3 ± 0,17 діб та вентилятор-асоційована пневмонія розвивалася у них в 27,6% випадків. Таким чином, нами встановлено, що у пацієнтів, які отримували L-лізину ецинат додатково до стандартної терапії, тривалість ШВЛ була на 16,9% менше, аніж у пацієнтів, що отримували стандартну терапію, частота розвитку пневмонії у них, у зв’язку з цим, була на 9,8% менше, ніж у пацієнтів 1 групи. Пацієнти, що отримували комплекс препаратів L-лізину есцинат та мексидол, знаходились на ШВЛ на 29,2% менше часу (p < 0,05), ніж пацієнти, що отримували стандартну терапію. Частота розвитку пневмонії, у зв’язку з цим, в них була на 22,3% менше, ніж у пацієнтів 1 групи. Це свідчить про ефективність обох варіантів інтенсивної терапії у порівнянні із стандартною терапією та про більшу ефективність у комбінації препаратів L-лізина есцинат та мексидол в порівнянні з L-лізину есцинату без мексидолу.
При аналізі летальності було встановлено, що загальна летальність у пацієнтів, що досліджувались, склала 55,5%. Найбільша кількість пацієнтів (37%) померли впродовж перших 10 діб на фоні набряку головного мозку.
У пацієнтів, що померли після 10 діб, відзначалося зростання поліорганних порушень: пневмонія виявлена у 62% пацієнтів, нефропатія – у 35,5% пацієнтів, ознаки печінкової недостатності – у 19% пацієнтів. Проаналізувавши фактори, що впливають на результати хвороби, ми отримали наступні дані: негативні наслідки залежать від первинного рівня порушень свідомості (r = 0,71), віку пацієнта (r = 0,54) та не залежить від розвитку пневмонії.
Враховуючи, що рівень порушення свідомості при надходженні та вік пацієнтів усіх груп співставимі, летальність визначалася характером та ефективністю інтенсивної терапії, що проводилась.
Летальність в 1 групі становила 59,3%, з яких 71% пацієнтів помер в продовж перших 10 діб, летальність в 2 групі становила 56,9%, з яких 72% пацієнтів померло в строк до 10 діб, а в 3 групі померло 49,2% пацієнтів, з яких 57% в строк до 10 діб.
Таким чином, летальність при тяжкій ЧМТ на 3,1% нижче в групі пацієнтів, що отримували L-лізина есцинат, а також достовірно (p < 0,05) нижче на 10,1% в групі пацієнтів, що отримували комплекс препаратів L-лізину есцинат та мексидол, в порівнянні з пацієнтами, що отримували стандартну терапію. Зниження летальності в 3 групі пов’язане зі зменшенням ранньої летальності, обумовленої набряком головного мозку та вторинною його ішемією. У пізні строки (після 10 діб) у пацієнтів 3 групи рідше відзначалися пневмонія, нефропатія та порушення функцій печінки.
ВИСНОВКИ
В дисертації наведене узагальнення та нове розв’язання актуального наукового завдання – визначення діагностичної ролі нейроспецифічних білків нейронспецифічної енолази та гліофібрилярного кислого протеїну при ушкодженні гематоенцефалічного бар’єру у хворих на тяжку черепно-мозкову травму, - та вирішення актуальної клінічної задачі – удосконалення інтенсивної терапії тяжкої черепно-мозкової травми завдяки уведенню до її складу комплексу препаратів L-лізину есцинату та мексидолу.
1. Ізольована тяжка черепно-мозкова травма найбільш часто зустрічається в осіб, що страждають на хронічний алкоголізм (67,5 %), в результаті падіння з висоти росту (84,8 %). Найбільш характерними її проявом є субдуральна гематома (64,9 %).
2. У сироватці крові умовно здорових донорів виявляються нейроспецифічні білки в концентраціях, що не перевищують: 4,1 нг/мл для гліофібріляторного кислого протеїна та 12,4 нг/мл для нейронспецифічної енолази.
3. У перші 6 годин тяжкої черепно-мозкової травми має місце підвищення концентрації нейроспецифічних білків порівняно з донорським рівнем. Це дозволяє припустити наявність прориву гематоенцефалічного бар’єру у гострому періоді тяжкої черепно-мозкової травми.
Нейронспецифічна енолаза (NSE), що є маркером нейронального ушкодження, підвищується у першу добу в 1,4 рази в порівнянні з верхньою межею норми. Концентрація нейронспецифічної енолази корелює з рівнем порушення свідомості (r = - 0,57), що дозволяє вважати її маркером тяжкості нейротравми.
Гліофібрілярний кислий протеїн (GFAP), що є маркером ушкодження астроглії, підвищується у першу добу в 2,5 рази в порівнянні з верхньою межею норми.
4. У пацієнтів, що отримували стандартний комплекс інтенсивної терапії тяжкої черепно-мозкової травми динаміка концентрації нейроспецифічних білків була такою:
- концентрація нейронспецифічної енолази була максимальною в перші 2-3 доби, що свідчить про найбільший загибель нейронів в цей період, з наступним достовірним (р = 0,005) зниженням до 6-7 доби та нормалізацією на 13-15 добу;
- концентрація гліофібрілярного кислого протеїну найбільш значно підвищувалась після 7 доби, без тенденції до нормалізації до кінця дослідження (13-15 доба), що є свідоцтвом розвитку реактивного астрогліозу в цей період.
5. Раннє (з першої доби) призначення препарату L-лізину есцинату в дозі 20 мл/добу у комплексі інтенсивної терапії тяжкої черепно-мозкової травми дозволяє зменшити елімінацію в кров гліофібрилярного кислого протеїну на 46,9%, а нейронспицефічної енолази на 23%, в порівнянні із стандартною терапією, та припинити надходження NSE у кров до 6-7 доби.
Раннє (з першої доби) призначення препарату L-лізину есцинату в дозі 20 мл/добу одночасно з мексидолом 800 мг/добу в комплексі інтенсивної терапії тяжкої черепно-мозкової травми дозволяє зменшити елімінацію в кров нейронспецифічної енолази на 44,2 %.
6. Включення до складу інтенсивної терапії L-лізину есцинату в дозі 20 мл/добу дозволяє зменшити летальність на 2,4%, прискорити відновлення свідомості на 4,2%, зменшити тривалість ШВЛ на 16,9%, у порівнянні із стандартною терапією. Найбільш істотне зниження летальності відзначалося в період до 10 діб, коли прояви набряку головного мозку є максимальними.
Включення до складу інтенсивної терапії комплексу препаратів L-лізину есцинату в дозі 20 мл/добу та мексидолу 800 мг/добу дозволило зменшити летальність на 10,1%, прискорити відновлення свідомості на 17,4%, зменшити тривалість ШВЛ на 29,2%, у порівнянні зі стандартною терапією.
ПРАКТИЧНІ РЕКОМЕНДАЦІЇ
Для оцінки проникності гематоенцефалічного бар’єру та оцінки ефективності інтенсивної терапії тяжкої черепно-мозкової травми:
- використання методу іммунохімічного аналізу нейроспецифічних білків гліофібрилярного кислого протеїну та нейронспецифічної енолази в сиворотці крові у комплексі. Якщо концентрація GFAP перевищує 4,1 нг/мл, а також концентрація NSE перевищує 12,4 нг/мл діагностують порушення проникності гематоенцефалічного бар’єру при тяжкій черепно-мозковій травмі.
Для підвищення ефективності інтенсивної терапії тяжкої черепно мозкової травми:
- раннє (з перших годин) включення комплексу препаратів L-лізину есцинату в дозі 20 мл/добу одночасно з мексидолом 800 мг/добу до схеми інтенсивної терапії пацієнтів тяжкою черепно-мозковою травмою.
ПЕРЕЛІК ПРАЦЬ, ОПУБЛІКОВАНИХ ЗА ТЕМОЮ ДИСЕРТАЦІЇ
1. Лизогуб Н.В. Возможности исследования нейроспецифических белков в сыворотке крови больных с тяжёлой черепно-мозговой травмой / Н.В. Лизогуб, О.И. Гурина // Матеріали IV з’їзду нейрохірургів України, (Дніпропетровськ, 27-30 травня 2008 р.) // Дніпропетровськ, ТОВ «ЕНЕМ», 2008. – С. 209.
Дисертантом особисто проводилось обстеження хворих, лікування, забір матеріалу для дослідження, узагальнення результатів дослідження, написаний та представлений текст доповіді.
2. Лизогуб М.В. Імуноферментний аналіз нейроспецифічних антигенів у діагностиці важкої черепно-мозкової травми / М.В. Лизогуб, А.А. Хижняк, О.І. Гуріна // Врачебная практика. – 2007. - №5(59). – С. 72-75.
Дисертантом особисто зібраний клінічний матеріал, написаний текст статті.
3. Лизогуб Н.В. Влияние L-лизина эсцината и мексидола на проницаемость гематоэнцефалического барьера при тяжёлой черепно-мозговой травме / Н.В. Лизогуб, А.А. Хижняк, О.И. Гурина // Український журнал екстремальної медицини ім. Г.О. Можаєва. – 2007. –Т.8, №4. – С. 45-47.
Дисертантом особисто визначена мета наукової роботи, зібраний клінічний матеріал, написано розділ, де викладено результати дослідження.
4. Хижняк А.А. Нейроспецифічні білки – перспективні маркери ураження головного мозку при черепно-мозковій травмі /А.А. Хижняк, М.В. Лизогуб // Біль, знеболювання та інтенсивна терапія. – 2006. - №2. – С. 23-28.
Дисертантом особисто проведений літературний пошук, написаний розділ, що присвячений нейроспецифічним білкам.
5. Клініко-імунохімічне визначення впливу препарату L-лізину есцинат на проникність гематоенцефалічного бар’єру при важкій черепно-мозковій травмі / А.А. Хижняк, В.П. Чехонін, О.І. Гуріна, М.В. Лизогуб // Біль, знеболювання та інтенсивна терапія. – 2006. - №1(д). – С. 245-246.
Дисертантом особисто визначена мета наукової роботи, зібраний клінічний матеріал, написано розділ, де викладено результати дослідження.
6. Хижняк А.А. Эффекты глюкокортикоидов и терапия при тяжёлой черепно-мозговой травме / А.А. Хижняк, С.В. Курсов, Н.В. Лизогуб // Біль, знеболювання та інтенсивна терапія. – 2004. - №1. – С. 29-40.
Дисертантом особисто проведений літературний пошук, написаний розділ, що присвячений інтенсивній терапії.
7. Лікування хворих на важку черепно-мозкову травму в умовах відділення інтенсивної терапії / Ієвлева В.І., Курсов С.В., Лизогуб М.В. [та ін.] // Неотложная медицинская помощь: зб. наук. праць. – Харьков: “Основа”, 2004. – С. 278-281.
Дисертантом особисто проводилось обстеження хворих, лікування, написаний розділ, що присвячений інтенсивній терапії.
8. Хижняк А.А. Вторинні ішемічні ушкодження головного мозку та алгоритм боротьби із ними при тяжкій черепно-мозковій травмі : [метод. рекомендації] / А.А. Хижняк, М.В. Лизогуб. – Київ, 2008. – 12 с.
Дисертантом особисто описані результати досліджень та сформульовані висновки та практичні рекомендації.
9. Пат. 32463 Україна, МПК G 01 N 33/00. Спосіб діагностики стану гематоенцефалічного бар’єру при тяжкій черепно-мозковій травмі / Хижняк А.А., Гуріна О.І., Лизогуб М.В.; заявник та патентовласник Харківський національний медичний університет. - № u200801906 ; заявл. 14.02.08 ; опубл. 12.05.08, Бюл. №9
АНОТАЦІЯ
Лизогуб М.В. Клініко-імунохімічна оцінка ефекту «захисту мозку» при тяжкій черепно-мозковій травмі. – Рукопис.
Дисертація на здобуття наукового ступеня кандидата медичних наук за спеціальністю 14.01.30 – анестезіологія та інтенсивна терапія. – Донецький національний медичний університет, Донецьк, 2008.
Дисертація присвячена питанням діагностики пошкодження гематоенцефалічного бар’єру та інтенсивній терапії тяжкої черепно-мозкової травми (ТЧМТ). Проаналізовано результати лікування 191 пацієнта з ТЧМТ, наведені особливості епідеміології та клінічних проявів. Нами був розроблений імуноферментний аналіз нервовоспецифічних білків гліофібрилярного кислого протеїну та нейронспецифічної енолази та було проведене дослідження цих білків у сироватці крові 45 здорових донорів та 46 пацієнтів з ТЧМТ у динаміці. Показано, що у гострому періоді ТЧМТ має місце прорив гематоенцефалічного бар’єру з елімінацією у кров нервовоспецифічних білків, та визначено їх роль у діагностиці ТЧМТ. Була удосконалена схема інтенсивної терапії ТЧМТ за допомогою включення до її складу L-лізину есцинату та мексидолу. Запропонована схема інтенсивної терапії дозволила знизити летальність при тяжкій ЧМТ на 10,1%, прискорити відновлення свідомості на 17,4% та зменшити тривалість ШВЛ на 29,2%, а також зменшити елімінацію у кров нервовоспецифічних білків гліофібрилярного кислого протеїну та нейронспецифічної енолази.
Ключові слова: тяжка черепно-мозкова травма, гліофібрилярний кислий протеїн, нейронспецифічна енолаза, L-лізину есцинат, мексидол.
АННОТАЦИЯ
Лизогуб Н.В. Клинико-иммунохимическая оценка эффекта «защиты мозга» при тяжёлой черепно-мозговой травме. – Рукопись.
Диссертация на соискание учёной степени кандидата медицинских наук по специальности 14.01.30 – анестезиология и интенсивная терапия. – Донецкий национальный медицинский университет, Донецк, 2008.
Диссертация посвящена вопросам диагностики целостности гематоэнцефалического барьера и интенсивной терапии при тяжёлой черепно-мозговой травме (ТЧМТ). В исследование включены 191 пациент с тяжёлой ЧМТ и 45 здоровых доноров. Пациентам проводилось общеклиническое, биохимическое исследование, МРТ головного мозга, иммунохимические (определение концентрации нейроспецифических белков нейронспецифической енолазы (NSE) и глиофибриллярного кислого протеина (GFAP) в сыворотке крови) и статистические методы.
Дизайн исследования – клинико-биохимическое проспективное рандомизированное исследование. Условием включения пациентов являлось наличие тяжёлой черепно-мозговой травмы (уровень нарушения сознания 8 баллов и менее по ШКГ). Условием исключения было наличие у пациента заболеваний и травм нервной системы в анамнезе. В качестве критериев эффективности различных схем интенсивной терапии выбраны следующие показатели: динамика концентрации нейроспецифических белков, позволяющая количественно оценить и проследить структурные повреждение как нейронов, так и астроцитов головного мозга, а также скорость восстановления сознания, длительность ИВЛ и летальность, позволяющие оценить функциональные нарушения повреждённого мозга.
Для оценки эффективности схем интенсивной терапии все больные в момент поступления были разделены при помощи простой фиксированной рандомизации с использованием метода случайных чисел на 3 группы. Пациенты группы 1 (n = 76) получали стандартную интенсивную терапию, согласно существующим рекомендациям. Пациентам 2 группы (n = 58) в комплекс интенсивной терапии включался препарат L-лизина эсцинат, обладающий противоотёчным и ангиопротекторным эффектом, в дозе 20 мл/сут в течение 7-8 суток. Пациентам 3 группы (n = 57) проводилась мультимодальная нейропротекторная терапия путём включения в комплекс интенсивной терапии L-лизина эсцината в дозе 20 мл/сут и мексидола (препарат с установленной антиоксидантной и антигипоксической активностью) в дозе 800 мг/сут. Условно здоровые доноры (n = 45) составили контрольную группу.
Нами были получены высокоочищенные препараты нейроспецифических белков GFAP и NSE и на их основе разработаны диагностические тест-системы для «сэндвич-варианта» иммуноферментного анализа, которые позволяли надежно и воспроизводимо определять уровни GFAP и NSE в сыворотке крови в интервале концентраций от 1 до 128 нг/мл с пределом чувствительности 1 нг/мл.
При исследовании сыворотки крови 45 здоровых доноров нами было выявлено, что концентрация GFAP составляла 3,0 ± 0,12 нг/мл (не превышала 4,1 нг/мл), а концентрация NSE составляла 7,7 ± 0,39 нг/мл (не превышала 12,4 нг/мл).
При исследовании концентраций GFAP и NSE в сыворотке крови пациентов с тяжёлой ЧМТ в течение первых 6 часов после травмы было выявлено, что они достоверно превышали донорский уровень, при этом концентрация NSE коррелировала с уровнем нарушения сознания по шкале ком Глазго.
При исследовании концентрации GFAP и NSE в сыворотке крови пациентов с ТЧМТ в динамике травматической болезни было выявлено, что концентрация GFAP нарастала до 10-11 суток и оставалась выше нормы в течение всего периода наблюдения (15 суток). Концентрация NSE максимально повышалась в течение первых 2-3 суток, а затем резко снижалась к 6-7 суткам. Нормализация концентрации данного белка происходила на 13-15 сутки.
Нами было показано, что раннее (с первых суток) назначение препарата L-лизина эсцинат в дозе 20 мл/сут в комплексе интенсивной терапии тяжёлой черепно-мозговой травмы позволяет уменьшить элиминацию в кровь глиофибрилярного кислого протеина на 46,9%, а нейронспецифической енолазы на 23%, в сравнении со стандартной терапией, и прекратить поступление NSE в кровь к 6-7 суткам. Раннее (с первых суток) назначение L-лизина эсцината в дозе 20 мл/сут совместно с мексидолом 800 мг/сут в комплексе интенсивной терапии тяжёлой черепно-мозговой травмы позволяет уменьшить элиминацию в кровь нейронспецифической енолазы на 44,2%.
При исследовании клинической эффективности предложенных схем интенсивной терапии нами было выявлено, что включение в состав интенсивной терапии L-лизина эсцината в дозе 20 мл/сут позволяет уменьшить летальность на 2,4%, ускорить восстановление сознания на 4,2%, уменьшить длительность ИВЛ на 16,9%, в сравнении со стандартной терапией. Наиболее значимо снижается летальность в период до 10 суток, когда проявления отёка головного мозга максимальны. Включение в состав интенсивной терапии комплекса препаратов L-лизина эсцината в дозе 20 мл/сут и мексидола 800 мг/сут позволяет уменьшить летальность на 10,1%, ускорить восстановление сознания на 17,4%, уменьшить длительность ИВЛ на 29,2%, в сравнении со стандартной терапией.
Ключевые слова: тяжёлая черепно-мозговая травма, нейронспецифическая енолаза, глиофибриллярный кислый протеин, L-лизина эсцинат, мексидол.
SUMMARY
Lyzogub M.V. Clinical and immunochemical assessment of the brain-protective effect in severe traumatic brain injury. – Manuscript.
Thesis for a Candidate of medical science degree on specialty 14.01.30 – anesthesiology and intensive therapy. – Donetsk national medical university, Donetsk, 2008.
The thesis is dedicated to the problem of diagnosing of the blood-brain barrier damage and to the intensive therapy of severe traumatic brain injury (TBI). We analyzed the results of treatment of 191 patients with severe TBI and we showed the epidemiological and clinical features of this type of trauma. We worked up the ELISA for glial fibrillary acid protein and neuronspecific enolase and we examined their blood concentrations in 45 healthy donors and 46 patients with severe TBI in dynamics. We demonsrated the brake of the blood-brain barrier and elimination of the neurospecific proteins to the blood in an acute phase of severe TBI. We showed the role of the neurospecific proteins in diagnosing of severe TBI. We improved the algorithm of severe TBI treatment by adding of L-lisin aescinat and mexidol to intensive therapy. With the help of our algorithm we reduced the mortality, the number of days in coma, the number of days with artificial pulmonary ventilation and we reduced the level of neurospecific proteins in blood in patients with severe TBI.
Key words: severe traumatic brain injury, glial fibrillary acid protein, neuronspecific enolase, L-lisin aescinat, mexidol.
ЛИЗОГУБ МиКОЛА ВІТАЛІЙОВИЧ
Автореферат дисертації на здобуття наукового ступеня
кандидата медичних наук
Відповідальний за випуск А.М. Колесніков
Підписано до друку 14.08.2008. Формат 60х90/16.
Папір офсетний. Друк різографія.
Обсяг 0,90 ум. друк. арк.
Тираж 100 прим. Замовл. № б/н
_____________________________________________
Надруковано ПП Степанов В.В. м. Харків, вул. Ак. Павлова, 311
0 комментариев