Навигация
Генетические факторы предрасположенности и устойчивости к туберкулезу
1.3.2 Генетические факторы предрасположенности и устойчивости к туберкулезу
Понимание важной роли генетических факторов в развитии туберкулеза пришло в первую очередь из эпидемиологических и близнецовых исследований. Так, в нескольких работах было показано, что степень устойчивости к инфекции М. tuberculosis у человека коррелирует с регионом его происхождения - предки более предрасположенных к заболеванию индивидов чаще всего происходили из областей, где туберкулез не распространен. Кроме того, частота клинического туберкулеза особенно высока во время эпидемий в популяциях, ранее не встречавшихся с данной инфекцией, в частности, у американских и канадских индейцев [17]. С середины 80-х годов было проведено множество исследований, пытающихся идентифицировать гены предрасположенности к туберкулезу или доказать уже опубликованные ассоциации. Многие из недавно проведенных исследований (Bellamy 2005, Bellamy 2006, Fernando 2006, Hill 2006, Ottenhoff 2005, Remus 2003) противоречат друг другу, и трудно прийти к единому заключению.
Исследования близнецов показали более высокий уровень конкордантности по клиническому туберкулезу у монозиготных пар по сравнению с дизиготными.
Дальнейшие исследования, проведенные на экспериментальных животных моделях, существенно дополнили имеющуюся информацию о генетических факторах предрасположенности к заболеванию. Исследования на мышах показали, что восприимчивость к инфекции такими родственными М. tuberculosis агентами как M. bovis (BCG), M. lepraemurium, M. intracellulare и М. avium, а также двумя немикобактериальными видами Salmonella typhimurium и Leishmania donovani, контролируется одним геном, локализованным в проксимальном регионе мышиной хромосомы 1. Ген получил три альтернативных названия Lsh, Ity и Bcg. У мышей предрасположенность к инфекции, контролируемая этим геном, является рецессивным признаком по сравнению с устойчивостью. Показано, что ген Lsh/lty/Bcg важен для активации макрофагов ретикулоэндотелиальной системы.
Ген Bcg был изолирован у мышей методом позиционного клонирования в 1993 г. и получил название Nramp (natural-resistance associated macrophage protein; сейчас называется Nramp 1 в связи с открытием гомолога Nramp 2). Анализ последовательности Nramp 1 у 27 инбредных линий мышей показал, что чувствительность к микобактериальной инфекции ассоциирована с миссенс мутацией, приводящей к замене глицина на аспарагиновую кислоту во втором трансмембранном домене белка.
В 1994 г. был клонирован гомолог гена Nramp 1 у человека, названный NRAMP1. Он локализован в локусе 2q35 и содержит 16 экзонов (Cellier 1994). Вклад данного гена в предрасположенность к туберкулезу у человека активно дискутируется. Опубликованы доказательства сцепления региона 2q35 с заболеванием у бразильцев и канадцев. Показано, что данный локус отвечает за скорость прогрессирования заболевания, а не за восприимчивость к инфекции. Кроме того, установлено, что NRAMP1 ассоциирован с проказой и результатами реакции Матсуда (аналог туберкулиновой пробы для проказы) у вьетнамцев. Это свидетельствует о том, что данный ген включен также в контроль инфекции близкородственной М. tuberculosis бактерии М. leprae.
Функция Nramp1 у мышей и NRAMP1 у человека пока неизвестна. Белок Nramp1 у мышей локализован в эндоцитозных компартментах и после фагоцитоза накапливается на мембранах фаголизосом. Эти данные свидетельствуют о том, что Nramp1 может ограничивать воспроизводство внутриклеточных патогенов, изменяя фаголизосомальное содержимое. Родственный ген - Nramp2 контролирует уровень ионов железа, а дрожжевой гомологичный ген SMF1 регулирует концентрацию ионов марганца. Таким образом, возможная функция белка Nrampl состоит в регуляции содержания ионов железа, марганца и других дивалентных катионов в фагосомах.
По данным многих исследований человеческий ген NRAMP1 не вносит существенного вклада в общую подверженность к туберкулезу. Однако его полиморфизм участвует в формировании отличий в подверженности к заболеванию туберкулезом у неинфицированных ранее лиц, а также оказывает влияние на течение уже возникшего заболевания.
Показано, что с туберкулезом связаны три точечные замены в гене белка, связывающего маннозу (MBL). Причем частота этих вариантов была достаточно высока как у европеоидов, так и у африканцев и австралийских аборигенов.
В последнее время получены доказательства связи туберкулеза с полиморфизмом гена рецептора к витамину D (VDR). Показаны ассоциации с туберкулезом полиморфизма генов, кодирующих интерлейкин-1β (IL1B) и его рецепторный антагонист (IL1RA). Ведутся исследования также и других генов, рассматриваемых как кандидаты на роль генов предрасположенности к туберкулезу, исходя из их функции (NOS2, TLR, NAT2, GST и др.).
Также многие исследования направлены на изучение ассоциаций иммуногенетической системы HLA с предрасположенностью к различным инфекциям. Доказано, что аллели HLA ассоциированы с восприимчивостью к таким инфекционным заболеванием, как сложная малярия, с прогрессированием ВИЧ, гепатитов B и C [24]. Исследования HLA также показали ассоциацию HLA-DR2 с лепрой или типами лепры - туберкулоидной или лепроматозной - в семейных и исследованиях типа "случай-контроль" в азиатских, африканских и американских популяциях (Geluk 2006). Многие исследователи искали ассоциации определенных аллелей HLA с восприимчивостью к туберкулезу.
Ранние исследования доказали ассоциации аллелей HLA I класса с восприимчивостью к туберкулезу, хотя было несколько проблем: найденные аллели варьировались в различных исследованиях; исследования, проведенные до начала 90-х годов, были выполнены с помощью лимфоцитотоксического метода, вероятность ошибки которого по сравнению с методом ПЦР составляет около 25% (Rajalingam 1996); не были проведены исправления для многократного исследования (Bland 1995).
Недавно был проведен мета-анализ (Kettaneh 2006), исследующий ранее определенные ассоциации HLA с восприимчивостью к туберкулезу преимущественно у взрослых людей серологическим методом. Мета-анализ показал, что не было никакой существенной ассоциации антигенов HLA I класса (А и C локусов) с предрасположенностью к туберкулезу, но был защитный эффект аллели HLA B13 (OR 0,64; 95% CI 0,50-0,81; P=0,0001). Для II класса локуса DR низкий риск развития туберкулеза был найден у людей, несущих DR3 (OR 0,72; 95% CI 0,59-0,89; P=0,002), DR7 (OR 0,65; 95% CI 0,53-0,80; P<0,0001); высокий риск развития туберкулеза был связан с DR8 (OR 1,72; 95% CI 1,21-2,46; P=0,003). Результаты для DR2 были противоречивыми (OR 1,67; 95% CI 1,16-2,41; P=0,006) (Kettaneh 2006). Мета-анализ очень полезен для исследования ранней литературы о HLA, он подвергает сомнению законность различных ассоциаций, так как не использовался более точный метод для идентификации аллелей HLA - полимеразная цепная реакция.
Ассоциации с аллелями HLA-B13, DR3, DR7 и DR8 в последнее время не получили большого распространения, а пограничная ассоциация с аллелем DR2 требует дальнейшего исследования. Об ассоциации с HLA-DR2 сообщалось в некоторых исследованиях на азиатских популяциях, главным образом от группы исследователей из Нью-Дели. В 1983 году два исследования из Нью-Дели сообщили об ассоциации между DR2 и прогрессированием туберкулеза (Singh 1983, Singh 1983). Исследование методом случай-контроль затем сравнило пациентов с мокротоположительным туберкулезом из Северной Индии с контролем, совпадающим по возрасту, полу и социоэкономическому статусу. Различия в распределении DR2 между пациентами и контролем были несущественными после коррекции в соответствии с числом тестированных антигенов, OR было равно 1,6 (Bothamley 1989). Во время семейного исследования распределения гаплотипов HLA I и II классов в 25 семьях при использовании метода Weitkamp была обнаружена значительно искаженная передача DR2 от родителей с туберкулезом к потомкам с туберкулезом (Weitkamp 1981). Поскольку семейные исследования имеют меньшую выборку, они обладают меньшей статистической достоверностью, чем исследования методом случай-контроль, и для получения надежных данных необходимо минимум 100-200 семей.
Исследования методом случай-контроль в индонезийской популяции показало ассоциацию туберкулеза с HLA-DR2 и DQw1 (Bothamley 1989), но было не ясно, являлись ли контрольные пациенты местными жителями или нет. А также исследование проводилось лимфоцитотоксическим методом, который подвержен ошибкам.
Российские исследования были направлены на изучение различных аллелей HLA у пациентов с туберкулезом в шести этнических группах (Хоменко 1990). В этих этнических группах были найдены разные ассоциации с туберкулезом, но в пяти из них была найдена четкая ассоциация HLA-DR2 с высоким риском развития туберкулеза и протективный эффект аллеля DR3.
Об ассоциации с DR2 также сообщалось и у тувинских детей (Поспелов 1996). Также сообщалось об увеличении частоты HLA-DR2 и DRw53 у детей с туберкулезом по сравнению со здоровыми детьми, но не по сравнению с детьми с другими хроническими болезнями легких. После коррекции Бонферрони существенной оставалась лишь ассоциация с DRw53.
При использовании более точного метода ПЦР для идентификации одиннадцати подтипов HLA-DR2 (Mehra 1995) была отмечена относительно высокая частота встречаемости DRB1*1501 у пациентов с туберкулезом по сравнению с контролем (р<0,05); в последующем сообщалось о том, что в той же группе была обнаружена относительно высокая частота встречаемости DR2 у пациентов с туберкулезом (Rajalingam 1996) по сравнению с контролем (Pc = 0,029, RR=1,8) и более сильная ассоциация при отсутствии лечения с обширным туберкулезом (Pc = 0.0001), но никакой ассоциации с определенным подтипом DR. Недавние исследования сообщают об ассоциации HLA-DRB1*1501 с туберкулезом в Индии (Sriram 2001) и Мексике (OR~8) (Teran-Escandon 1999), и более быстрым началом болезни, вызванной M. avium, у американских пациентов с ВИЧ (LeBlanc 2000). Ассоциация HLA-DR2 с легочным туберкулезом не была найдена в исследовании методом случай-контроль в Южной Индии (Sanjeevi 1992), у афро-американцев (Hwang 1985), в Гонконге (Hawkins 1988), Египте (Hafez 1985), Мексике и Америке (Cox 1988), Камбоджи (Goldfeld 1998) и семейном анализе Северной Бразилии (Blackwell 1998). Трудно собрать всю информацию об ассоциациях с HLA-DR2 и DRB1*1501 воедино. Различия могли быть связаны с этнической картиной, многократностью исследований или самим проектом исследования.
В отличие от сомнительных ассоциаций с DR2 в сельской Камбоджи (Goldfeld 1998) была найдена четкая ассоциация HLA-DQB1*0503 с туберкулезом (р=0,005), ассоциаций с аллелями DR2 и TNF-α обнаружено не было. Исследование было проведено в двух стадиях с отдельными группами пациентов. Во время первой стадии исследования было проверено большое количество аллелей, но ассоциации была обнаружена только с HLA-DRB1*0503. Во время второй стадии исследования проверялся только этот подтип HLA. Кроме того, контролем служили пациенты того же госпиталя, только с незначительными болезнями, поэтому они, скорее всего, являлись представителями той же популяции. Поскольку в данной популяции туберкулез широко распространен, аллель DQ связан не с восприимчивостью к инфекции, а с развитием клинических стадий болезни (Goldfeld 1998).
Ассоциация специфической аллели HLA-DQB1*503 с прогрессивным туберкулезом особенно интересна в связи с тем, что DQB1*503 аллель кодирует изменения в аминокислотной позиции 57 β-цепочки (β57), которая влияет на связывание антигена в кармане Р9 молекулы DQ.
DQB1*503 аллель, которая является частью DQ1 серологической специфичности, кодирует отрицательно заряженную аспарагиновую кислоту в β57 вместо обычной незаряженной и гидрофобной аминокислоты валина. МНС-ограниченная презентация пептидов макрофагами, инфицированными микобактериями может быть изменена у пациентов, которые экспрессируют этот специфический Р9 карман. Отрицательно заряженный Р9-связывающий карман может связывать антигены туберкулезных бактерий менее эффективно или выявляется слабый иммуногенетический ответ.
В последующих исследованиях прогрессирование туберкулеза было связано с гомозиготностью других аллелей HLA-DQB с аспарагиновой кислотой в позиции 57: DQB1*0301, 0303; DQB1*04 (-0401, 0402); DQB1*0503; DQB1*0601,-0602,-0603. По сравнению с аллелью HLA β 57-Ala презентация пептида ESAT-6 HLA β 57-Asp приводит к меньшей продукции IFN-γ CD4+ т-клетками у пациентов с туберкулезом (Delgado 2006).41 аллель HLA-DQB1*0503 был найден среди пациентов с туберкулезом, но аллель не был найден ни у одного из 107 туберкулин-положительных контрольных людей. Этот аллель не ассоциирован с туберкулезом в других популяциях, поэтому считается специфичным для жителей Камбоджи. Однако исследование пациентов в вендской популяции в Южной Африке (Lombard 2006) показало ассоциацию туберкулеза с другими β 57-Asp гаплотипами, идентифицированными в исследовании на пациентах из Камбоджи, DRB1*1302-DQB1*0602, DRB1*1302-DQB1*0603, DRB1*1101-1121-DQB1*0301-0304 и DRB1*1101-1121-DQB1*05. Семь других исследований также доказали ассоциации некоторых из этих гаплотипов с восприимчивостью к туберкулезу (Dubaniewicz 2000, Dubaniewicz 2005, Goldfeld 1998, Kim 2005, Pospelova 2005, Teran-Escandon 1999, Wang 2001), тогда как три других исследования показали защитный эффект гаплотипов (Dubaniewicz 2005, Vejbaesya 2002, Wang 2001).
Было предположено (Lombard 2006), что данные гаплотипы, увеличивающие восприимчивость к туберкулезу, поддерживаются в популяциях, так как часть этих аллелей имеет защитный эффект против малярии (DRB1*1302-DQB1*0501) (Hill 1991), хронического гепатита B (HLA-DRB1*1302) (Thursz 1995) (Hill 2001, Wang 2003) и хронического гепатита C (DRB1*1101 и DQB1*0301) (Hong 2005) [39]. Возможно, что гетерозиготность по этим аллелям HLA может иметь защитный эффект против малярии, туберкулеза и хронических гепатитов для африканских популяций. Наоборот, хотя аллель HLA-DQ β-57-Asp и ассоциирован с восприимчивостью к туберкулезу, он также является протективным для аутоиммунного диабета 1 типа. Поэтому у европейцев, имеющих аллель HLA-DQ β-57-Ala (HLA-DQ2 и - DQ8) вместе с устойчивостью к туберкулезу имеется и восприимчивость к развитию аутоиммунного диабета 1 типа (Delgado 2006).
Молекулярные основы предрасположенности к туберкулезу пока изучены недостаточно. Связь исследованных аллельных вариантов с заболеванием и их клинические проявления слишком слабы, их роль в функциональных нарушениях обоснована недостоверно. Таким образом, молекулярные основы генетического контроля предрасположенности к туберкулезу в больших популяциях остаются пока достаточно туманными.
Вместе с тем существуют четкие причинно-следственные отношения между редкими менделирующими иммунодефицитами по Т-клеткам или фагоцитам и тяжелыми формами туберкулеза. Пациенты с такими заболеваниями в значительной степени чувствительны к инфекции не только M. tuberculosis, но и другими микроорганизмами. Недавно был описан и исследован менделирующий синдром восприимчивости к микобактериалыюй инфекции (OMIM - 209950). Люди с этим синдромом исключительно чувствительны не только к патогенным штаммам, но и к слабовирулентным видам микобактерий, таким как свободноживущие нетуберкулезные формы и BCG. При исследовании этого синдрома обнаружены мутации в генах, связанных с противоинфекционным иммунитетом: IFNG, IFGR1, - 2, TNFA, IL12B, IL12RB1 (интерферон-гамма, два его рецептора, фактор некроза опухолей альфа, ИЛ-12 и бета-1 субъединица его рецептора) (Altare 1998).
На основании имеющихся на сегодняшний день данных сформулировано предположение о непрерывном спектре генетического контроля предрасположенности к туберкулезу у человека: моногенные формы - варианты с эффектом главного гена; олигогенные формы - полигенная подверженность. Может привести к успеху изучение редких менделирующих дефектов иммунитета у отдельных пациентов с тяжелыми нераспространенными клиническими фенотипами, ведущих эффектов в отдельных семьях и в популяциях, лишь недавно столкнувшихся с микобактериальной инфекцией, а также широко распространенных полиморфизмов в популяциях с длительной историей экспозиции М. tuberculosis. Возможно, на всех трех уровнях генетического контроля участвует один ген, имеющий редкие мутации, ответственные за менделирующие тяжёлые фенотипы, относительно редкие варианты, обусловливающие основной эффект, и распространенные в популяциях полиморфизмы, в умеренной степени определяющие риск развития заболевания. Поиск такого гена (генов) - на сегодняшний день актуальная задача. Кроме того, важным представляется изучение функционального полиморфизма известных генов-кандидатов туберкулеза в популяциях различного этнического состава с разной частотой заболевания.
1.4 Ассоциация HLA II класса с микобактериозами в русской популяцииГруппой ученых во главе с Л.В. Сароянц, М.Н. Болдыревой, И.А. Гуськовой было исследовано распределение частот аллелей локусов HLA II класса (DRB1, DQA1, DQB1) и гаплотипов у 113 больных лепрой и 51 больного туберкулезом легких русской национальности, проживающих в Астраханской области. Установлено достоверное повышение частоты встречаемости гаплотипа DRB1-16-DQA1-0102-DQB1-0502/04 при лепре и туберкулезе. Риск возникновения туберкулеза легких ассоциировался с наличием в генотипе гаплотипа DRB1-17-DQA1-0501-DQB1-0201. На основании полученных результатов сделан вывод, что присутствие специфических аллелей генов HLA II класса и их гаплотипов при указанных заболеваниях свидетельствует об их участии в патогенезе данных микобактериозов.
Тяжесть микобактериальных заболеваний скорее связана с Т-клеточным ответом на Mycobacterium leprae и Mycobacterium tuberculosis, чем с непосредственным воздействием бактерий. Поскольку молекулы HLA являются продуктами генов иммунного ответа, значительный полиморфизм в этих генах, возможно, ведет к различиям в восприимчивости и (или) устойчивости к инфекции.
Верификация генетических факторов, обусловливающих предрасположенность или устойчивость к лепре и туберкулезу, имеет большое значение для формирования групп лиц с повышенным риском развития этих заболеваний, что особенно актуально для эндемичных по данным инфекциям регионов. Успехи последних десятилетий в молекулярной генетике позволили перейти на новый уровень прогноза развития указанных болезней.
У больных туберкулезом и у больных лепрой установлена положительная ассоциация с HLA-DRB1-16-специфичностью. В то же, время повышение частоты встречаемости DRB1-17, DQB1-0201 и - 0303 характерно для больных туберкулезом, а DRB1-15, DQA1-0102 - для больных лепрой. У больных туберкулезом установлена отрицательная ассоциация с аллелем DQB1-0301 (таблица 3).
При анализе распределения частот гаплотипов обнаружено достоверное увеличение частоты встречаемости гаплотипа DRBl-16-DQA1-0102-DQB1-0502/04 (р < 0,05) в обеих группах больных.
Кроме того, у больных туберкулезом достоверней чаще по сравнению как с контролем, так и с больными лепрой встречался гаплотип DRB1-17-DQA1-0501-DQB1-0201 (р < 0,01); RR = 3,5. У больных лепрой и туберкулезом с низкой частотой определялся гаплотип DRB1-11-DQA1-0501-DQB1-0301 (таблица 4), однако статистически значимыми различия были только у больных лепрой (р < 0,05).
Таким образом, полученные результаты подтверждают вовлеченность в процессы возникновения и развития лепры и туберкулеза генетических факторов, ассоциированных с аллелями DRB1, DQA1 и DQB1 комплекса HLA. В последние годы стало известно, что полиморфизм системы HLA характерен для каждой конкретной группы населения, что оказывает определяющее влияние на биологическую стабильность данной группы.
Молекула МНС приобретает стабильную форму и соответствующую трехмерную конфигурацию только после того, как в связывающий сайт ее складки встраивается пептид. Пептидное связывание и последующий запуск иммунных реакции решающим образом зависят от аллельных вариантов молекулы HLA. Анализ последовательностей показал, что по одному аминокислотному варианту можно различать продукты DRB1-1501 от DRB1-1502 и DRB1-1601 от DRB1-1602. Можно полагать, что специфичность DRB1-16 или ее аллельные варианты избирательно нацелены на презентацию общих патогенных пептидов Mycobacterium leprae и Mycobacterium tuberculosis Т-клеткам. В то же время выявление DRB1-17-специфичности у больных туберкулезом, вероятно, свидетельствует о наличии патогенных мотивов у HLA-аллеля, стимулирующего Т-клеточные клоны, которые приводят к формированию ответной иммунной реакции, обусловливающей патогенез данного заболевания. Гаплотип DRB1-16-DQA1-0102-DQB1-0502/04 имеет низкую частоту встречаемости во многих популяциях. Так, у здоровых индусов он находится в пределах 4-5% с повышением, хотя и недостоверным (возможно, из-за малого числа наблюдений), у больных лепрой и туберкулезом. В русской популяции эти различия оказались статистически значимыми. Весьма вероятно, что пептиды, принадлежащие Mycobacterium leprae и Mycobacterium tuberculosis, связываются с конкретными эпитопами аллельных вариантов HLA-DRB1-генов и стимулируют Т-клеточные клоны, которые приводят к запуску иммунных ответных реакций, лежащих в основе патогенеза указанных микобактериозов. Возможно, ассоциации с DRB1-16-специфичностью или с ее аллельными вариантами свидетельствуют о предрасположенности к микобактериозам, наличие же в генотипе человека DRB1-17-специфичности (особенно гаплотипа DRB1-17-DQA1-0501-DQB1-0201) увеличивает риск развития туберкулезной инфекции в русской популяции.
Установление молекулярных механизмов распознавания антигенов является необходимой базой для дальнейшей коррекции силы иммунного ответа индивидуума в отношении любого антигенного воздействия. Прогресс на этом пути очевиден, так как уже сейчас показано, что замена всего лишь единственной аминокислоты в последовательности антигенсвязывающего участка молекулы гистосовместимости может приводить к развитию толерантности. Такого рода подходы открывают новые перспективы в борьбе с различными заболеваниями, в том числе с туберкулезом и лепрой.
II. Собственные исследования
2.1 Материалы и методы исследования
2.1.1 Контингент обследуемых лиц
Иммуногенетическое типирование проводилось среди русской этнической группы, постоянно проживающей в Челябинской области. Исследование включает 51 больного туберкулезом, находящегося на стационарном лечении в ГУЗ "Противотуберкулезный диспансер № 3", представителей социально благополучных слоев населения, имеющих родственников русской национальности в трех поколениях. Группу сравнения составили 202 случайно выбранных донора Областной станции переливания крови (г. Челябинск) русской национальности.
2.1.2 Иммуногенетическое типирование
Работа выполнена на базе зональной лаборатории иммуногенетического типирования тканей ОГУП "Челябинской областной станции переливания крови" г. Челябинск.
Генотипирование проводилось методом полимеразной цепной реакции с аллель специфическими праймерами (PCR-SSP) с помощью наборов реагентов, предложенных "НФП ДНК-Технология" (Москва). Идентификацию аллелей HLA II класса проводили методом амплификации с использованием 19 смесей праймеров для DRB1 локуса, 26 для DQB1 локуса и 12 смесей праймеров для DQA1 локуса. Для ПЦР использовался термоциклер МС-2 ("ДНК-технология", Москва, Россия).
Постановка реакции:
Для постановки используется ДНК, выделенная из венозной крови по стандартной методике (разрушение клеток и экстракция ДНК) путем последовательной обработки клеток лизирующим буфером.
В каждую пробирку, содержащую ДНК-pol, дезоксинуклеозид-трифосфаты, хлорид магния, оптимизированную буферную систему для ПЦР вносится по 10 мкл ПЦР растворителя.
Растворенная смесь с помощью автоматического дозатора раскапывается в пробирки по 5 мкл.
В каждую пробирку под масло добавляется по 2,5 мкл определенного праймера и 2,5 мкл раствора выделенной ДНК.
Для проведения амплификации используются последовательно связанные программы, приведенные для амплификатора типа МС-2, запрограммированного на объем 10 мкл. Обычно при проведении ПЦР выполняется 20-35 циклов, каждый из которых состоит из трех стадий: денатурации, отжига и элонгации.
Детекция результатов проводится с помощью гельэлектрофореза в 3% агарозном геле. Для этого в готовые пластины геля в лунки вносится по 5 мкл пробы. Затем пластинка помещается в ванночку и проводится электрофорез в течение 10 мин.
Учет результатов проводится визуально с помощью трансиллюминатора. При этом агарозный гель достается из кюветы и помещается на стекло трансиллюминатора. Продукты реакции амплификации выглядят в виде светящихся полос, наблюдаемых визуально в УФ-свете трансиллюминатора. Результаты фиксируются посредством фотографирования или видеосъемки геля при использовании УФ-фильтров и заносятся в протокол [28].
2.1.3 Методы статистической обработки
В плане наследования антигенов гистосовместимости человеческая популяция является панмиктической и подчиняется закону Харди - Вайнберга, выражающейся формулой наследования для системы с двумя признаками:
p2 + 2рq + q2 = 1,которая отражает количество гомо - и гетерозиготных по соответствующему гену индивидов в выборке.
Часть антигенов рассчитывается как процентное (долевое) соотношение индивидуумов, несущих антигены к общему числу обследованных, а частота гена по указанной выше формуле после ее преобразования:
p2x + 2px (1 - px) + (1 - px) 2 = 1; но так как,
p2x + 2px (1 - px) = Ax,
1 - px = ![]() и
и
px = 1 - ![]() ,
,
где Px - частота гена;
Аx - частота антигена.
Определенная по формуле частота гена должна быть проверена путем сравнения наблюдаемого в выборке распределения гомо - и гетерозиготных индивидуумов с теоретически рассчитанной в соответствии с законом Харди-Вайнберга.
Достоверность различий в частоте встречаемости антигенов у больных туберкулезом и здоровых людей русской национальности, проживающих в Челябинской области, рассчитывается согласно критерию Пирсона:
 ,
,
где N - это число обследованных в двух сравниваемых группах;
а - число индивидуумов несущих исследуемый антиген среди больных туберкулезом;
в - число индивидуумов не несущих исследуемый антиген среди больных туберкулезом;
с - число индивидуумов несущих исследуемый антиген среди здоровых русских;
d - число индивидуумов, не несущих исследуемый антиген среди здоровых русских.
Важным элементом популяционного анализа являются гаметные ассоциации, которые учитывают разницу в теоретически определенной ассоциации между 2-я антигенами разных локусов и истинной ассоциацией, встречающейся в популяции. К необходимости введения данного показателя приводит рассуждение: если бы аллели исследуемых локусов встречались независимо друг от друга, часть их ассоциаций на хромосоме (гаплотип) определялась бы произведением Р1×Р2, где Р1 и Р2 - частота соответствующих генов. Однако в популяции частота отдельных аллелей встречаются более часто или наоборот, более редко, чем это следует из теоретического расчета, то есть данные гены находятся в состоянии неравновесного сцепления (linkage disequilibrium), которое измеряется величиной Δ, отражающее превышение или дефицит гаплотипа в популяции по сравнению с произведением частот двух генов.
Величина Δ подсчитывается из ''сетки'' 2×2 по формуле (P. Mattiusi 1970г)
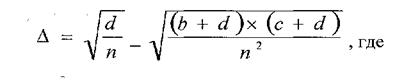
n - число обследованных в выборке
b - число индивидуумов несущих X и не несущих Y
с - число индивидуумов несущих Y, но не несущих X
d - число индивидуумов не несущих ни X ни Y.
Приведенная формула входит составной частью в формулу, используемую для определения частоты гаплотипа в панмиктической популяции
H XY = (PX × PY) + Δ X,Y,
где РX и РY - равны частоте соответствующих генов
ΔX,Y - гаметная ассоциация между генами соответствующими генами.
Для определения частоты трехлокусных гаплотипов методом максимального правдоподобия (maximum-liekelihood) использовалась компьютерная программа "Арлекин", версия 3.1
2.2 Результаты собственных исследований
2.2.1 Анализ распределения частот генов и антигенов HLA II класса у больных туберкулезом представителей русской национальности, проживающих в Челябинской области
В результате проведенного исследования были выявлены основные черты иммуногенетического профиля HLA локусов DR, DQB, DQA у больных туберкулезом русской национальности (рисунок 6, приложения). Анализ распределения аллелей данных локусов представлен в таблице 5.
Таблица 5. Распределение частот генов и антигенов HLA II класса
у больных туберкулезом
| HLA | Больные туберкулезом | ||
| N = 51 | Ax% | Рx% | |
| DR 1 | 14 | 27,45 | 0,15 |
| DR 3 | 8 | 15,69 | 0,08 |
| DR 4 | 12 | 23,53 | 0,13 |
| DR 7 | 15 | 29,41 | 0,16 |
| DR 8 | 3 | 5,88 | 0,03 |
| DR 9 | 2 | 3,92 | 0,02 |
| DR 10 | 0 | 0 | 0,00 |
| DR 11 | 9 | 17,65 | 0,09 |
| DR 12 | 1 | 1,96 | 0,01 |
| DR 13 | 11 | 21,57 | 0,11 |
| DR 14 | 2 | 3,92 | 0,02 |
| DR 15 | 12 | 23,53 | 0,13 |
| DR 16 | 7 | 13,73 | 0,07 |
| DQA 101 | 16 | 31,38 | 0,17 |
| DQA 102 | 19 | 37,25 | 0,21 |
| DQA 103 | 8 | 15,67 | 0,08 |
| DQA 201 | 15 | 29,41 | 0,16 |
| DQA 301 | 14 | 27,45 | 0,15 |
| DQA 401 | 3 | 5,88 | 0,03 |
| DQA 501 | 20 | 39,21 | 0,22 |
| DQA 601 | 0 | 0 | 0,00 |
| DQB 201 | 20 | 39,22 | 0,22 |
| DQB 301 | 15 | 29,41 | 0,16 |
| DQB 302 | 9 | 17,65 | 0,09 |
| DQB 303 | 4 | 7,84 | 0,04 |
| DQB 401/2 | 3 | 5,88 | 0,03 |
| DQB 501 | 13 | 25,49 | 0,14 |
| DQB 502/4 | 7 | 13,73 | 0,07 |
| DQB 503 | 2 | 3,92 | 0,02 |
| DQB 602/8 | 19 | 37,25 | 0,21 |
| DQB 601 | 1 | 1,96 | 0,01 |
Как видно из таблицы, для больных туберкулезом характерна относительно высокая частота антигенов DR 1 (27,45%), DR 7 (29,41%). С низкой частотой встречались DR 8 (5,88%), DR 9 (3,92%), DR 12 (1,96%), DR 14 (3,92%). Антиген DR 10 у больных туберкулезом обнаружен не был.
Самыми распространенными аллелями локуса HLA DQA у больных туберкулезом являются DQA 101 (31,37%), DQA 102 (37,25%), DQA 501 (39,22%). Наиболее низкие частоты имеет DQA 401 (5,88%).
Среди аллелей локуса HLA DQB у больных туберкулезом Челябинской области преобладающими являются DQB 201 (39,21%), DQB 602/8 (37,25%), DQB 501 (25,49%). Редкими являются аллели DQB 303 (7,84%), DQB 401/2 (5,88%), DQB 503 (3,92%), DQB 601 (1,96%). В целом такое распределение типично для большинства популяций европеоидной расы.
2.2.2 Анализ распределения частот генов и антигенов HLA II класса в популяции русских Челябинской области
В результате проведенного исследования были выявлены основные черты иммуногенетического профиля HLA локусов DR, DQB, DQA у здоровых доноров областной станции переливания крови русской национальности, проживающих в Челябинской области. Анализ распределения аллелей данных локусов представлен в таблице 6.
Таблица 6. Распределение частот генов и антигенов HLA II класса
у здоровых русских, проживающих в Челябинской области
| HLA | Здоровые русские | ||
| N = 202 | Ax% | Рx% | |
| DR 1 | 55 | 27,22 | 0,15 |
| DR 3 | 37 | 18,31 | 0,1 |
| DR 4 | 38 | 18,81 | 0,1 |
| DR 7 | 48 | 23,76 | 0,13 |
| DR 8 | 17 | 8,42 | 0,04 |
| DR 9 | 9 | 4,46 | 0,02 |
| DR 10 | 7 | 3,47 | 0,02 |
| DR 11 | 38 | 18,81 | 0,1 |
| DR 12 | 7 | 3,47 | 0,02 |
| DR 13 | 56 | 27,72 | 0,15 |
| DR 14 | 7 | 3,47 | 0,02 |
| DR 15 | 54 | 26,73 | 0,14 |
| DR 16 | 11 | 5,45 | 0,03 |
| DQA 101 | 65 | 32,18 | 0,18 |
| DQA 102 | 62 | 30,69 | 0,17 |
| DQA 103 | 41 | 20,30 | 0,11 |
| DQA 201 | 48 | 23,76 | 0,13 |
| DQA 301 | 48 | 23,76 | 0,13 |
| DQA 401 | 14 | 6,93 | 0,04 |
| DQA 501 | 69 | 34,16 | 0, 19 |
| DQA 601 | 1 | 0,50 | 0,002 |
| DQB 201 | 71 | 35,15 | 0, 19 |
| DQB 301 | 72 | 35,64 | 0, 20 |
| DQB 302 | 29 | 14,36 | 0,07 |
| DQB 303 | 20 | 9,90 | 0,05 |
| DQB 401/2 | 13 | 6,44 | 0,03 |
| DQB 501 | 63 | 31, 19 | 0,17 |
| DQB 502/4 | 13 | 6,43 | 0,03 |
| DQB 503 | 6 | 2,97 | 0,01 |
| DQB 602/8 | 81 | 40,10 | 0,23 |
| DQB 601 | 10 | 4,95 | 0,03 |
Как видно из таблицы, для популяции русских, проживающих в Челябинской области, характерна относительно высокая частота антигенов DR 1 (27,22%), DR 13 (27,22%) и DR 15 (26,73%). С низкой частотой встречались DR 9 (4,46%), DR 10 (3,47%), DR 12 (3,47%), DR 14 (3,47%). Такое распределение аллелей характерно для большинства европеоидных популяций.
Среди аллелей локуса DQA у доноров русской национальности из Челябинской области наиболее частыми являются DQA 101 (32,18%), DQA 102 (30,69%), DQA 501 (34,16%), что типично для большинства популяций европеоидной расы. Редко встречаются аллели DQA 401 (6,93%), DQA 601 (0,50%).
Среди аллелей локуса HLA DQB русских Челябинской области преобладающими являются DQB 201 (35,15%), DQB 301 (35,64%), DQB 501 (31,19%), DQB 602/8 (40,10%), что также характерно для европеоидов. Редкими являются аллели DQB 503 (2,97%), DQB 601 (4,95%).
2.2.3 Сравнительный анализ частот встречаемости антигенов HLA II класса у больных туберкулезом и здоровых представителей русской этнической группы Челябинской областиВ таблице 7 представлены данные о точных популяционных показателях для антигенов и генов (Ах, Рх) локусов DR, DQA, DQB у больных туберкулезом и здоровых представителей русской этнической группы Челябинской области, а также рассчитана достоверность различий (χ2) генов между больными туберкулезом и здоровыми русскими (рисунок 7, приложения).
Таблица 7. Распределение частот аллелей HLA-II класса у больных туберкулезом и здоровых русских Челябинской области
| HLA | Больные туберкулезом | русские Челябинской области | |||||
| N = 51 | Ax% | px% | N=202 | Ax в% | Px | χ² | |
| DR 1 | 14 | 27,45 | 0,15 | 55 | 27,22 | 0,15 | 0,001 |
| DR 3 | 8 | 15,69 | 0,08 | 37 | 18,31 | 0,1 | 0, 193 |
| DR 4 | 12 | 23,53 | 0,13 | 38 | 18,81 | 0,1 | 0,571 |
| DR 7 | 15 | 29,41 | 0,16 | 48 | 23,76 | 0,13 | 0,695 |
| DR 8 | 3 | 5,88 | 0,03 | 17 | 8,42 | 0,04 | 0,359 |
| DR 9 | 2 | 3,92 | 0,02 | 9 | 4,46 | 0,02 | 0,028 |
| DR 10 | 0 | 0 | 0,00 | 7 | 3,47 | 0,02 | 1,818 |
| DR 11 | 9 | 17,65 | 0,09 | 38 | 18,81 | 0,1 | 0,037 |
| DR 12 | 1 | 1,96 | 0,01 | 7 | 3,47 | 0,02 | 0,301 |
| DR 13 | 11 | 21,57 | 0,11 | 56 | 27,72 | 0,15 | 0,792 |
| DR 14 | 2 | 3,92 | 0,02 | 7 | 3,47 | 0,02 | 0,025 |
| DR 15 | 12 | 23,53 | 0,13 | 54 | 26,73 | 0,14 | 0,217 |
| DR 16 | 7 | 13,73 | 0,07 | 11 | 5,45 | 0,03 | 4,224 |
| DQA 101 | 16 | 31,38 | 0,17 | 65 | 32,18 | 0,18 | 0,012 |
| DQA 102 | 19 | 37,25 | 0,21 | 62 | 30,69 | 0,17 | 0,806 |
| DQA 103 | 8 | 15,67 | 0,08 | 41 | 20,30 | 0,11 | 0,554 |
| DQA 201 | 15 | 29,41 | 0,16 | 48 | 23,76 | 0,13 | 0,695 |
| DQA 301 | 14 | 27,45 | 0,15 | 48 | 23,76 | 0,13 | 0,299 |
| DQA 401 | 3 | 5,88 | 0,03 | 14 | 6,93 | 0,04 | 0,071 |
| DQA 501 | 20 | 39,21 | 0,22 | 69 | 34,16 | 0, 19 | 0,457 |
| DQA 601 | 0 | 0 | 0,00 | 1 | 0,50 | 0,002 | 0,253 |
| DQB 201 | 20 | 39,22 | 0,22 | 71 | 35,15 | 0, 19 | 0,292 |
| DQB 301 | 15 | 29,41 | 0,16 | 72 | 35,64 | 0, 20 | 0,701 |
| DQB 302 | 9 | 17,65 | 0,09 | 29 | 14,36 | 0,07 | 0,345 |
| DQB 303 | 4 | 7,84 | 0,04 | 20 | 9,90 | 0,05 | 0, 201 |
| DQB 401/2 | 3 | 5,88 | 0,03 | 13 | 6,44 | 0,03 | 0,021 |
| DQB 501 | 13 | 25,49 | 0,14 | 63 | 31, 19 | 0,17 | 0,629 |
| DQB 502/4 | 7 | 13,73 | 0,07 | 13 | 6,43 | 0,03 | 2,972 |
| DQB 503 | 2 | 3,92 | 0,02 | 6 | 2,97 | 0,01 | 0,120 |
| DQB 602/8 | 19 | 37,25 | 0,21 | 81 | 40,10 | 0,23 | 0,138 |
| DQB 601 | 1 | 1,96 | 0,01 | 10 | 4,95 | 0,03 | 0,875 |
При анализе были выявлены как общие тенденции, так и различия в распределении частот генов HLA DRB1. Так, у больных туберкулезом и здоровых пациентов были выявлены различия в частоте встречаемости антигена HLA DR 16 (14% у больных туберкулезом и 5% у здоровых русских). Результаты являются статистически достоверными, так как χ²=4,224, RR=1,15. Также у больных туберкулезом по сравнению со здоровым контролем выявлена относительно высокая частота встречаемости гена HLA DQB 502/4 (13,73 и 6,43 соответственно). Результаты не достигают статистической достоверности, так как χ²=2,972, RR=0,76.
Частоты некоторых аллелей HLA DR и DQ локусов у здорового контроля были незначительно увеличены по сравнению с частотами HLA у пациентов с туберкулезом (DR 10, DQB 601); это свидетельствует о том, что данные аллели могут вносить вклад в устойчивость к туберкулезу (но результаты не являются статистически значимыми, т.к χ²=2,07 и 0,76, соответственно).
По результатам исследования аллель HLA DR 16 идентифицирован как ген, ассоциированный с прогрессированием туберкулеза. Эти результаты поддерживают гипотезу о том, что изменчивость главного комплекса гистосовместимости играет важную роль в восприимчивости или сопротивлении инфекции.
Данная ассоциация с HLA DR 16 по литературным данным была обнаружена во многих странах мира. В частности, в Польше, Казахстане, Туркмении, Узбекистане, Индонезии и Индии риск развития тяжелых форм туберкулеза также связывают с HLA DR 16.
2.2.4 Анализ трехлокусных гаплотипов HLA у больных туберкулезом русской этнической группы Челябинской областиСведения о частотах наиболее значимых трехлокусных гаплотипов (Н) DR - DQA - и DQB представлены в таблице 8. Полное распределение гаплотипов у больных туберкулезом русской этнической группы Челябинской области представлено в таблице 9 (приложения).
Таблица 8. Частоты трехлокусных гаплотипов (Н) у пациентов, больных туберкулезом
| Гаплотипы | H | Гаплотипы | H |
| DR1-DQA101-DQB501 | 0,1373 | DR11-DQA501-DQB301 | 0,1078 |
| DR1-DQA101-DQB602/8 | 0,0098 | DR12-DQA501-DQB301 | 0,0196 |
| DR3-DQA501-DQB201 | 0,0784 | DR13-DQA501-DQB301 | 0,0196 |
| DR4-DQA301-DQB301 | 0,0294 | DR13-DQA102-DQB602/8 | 0,0196 |
| DR4-DQA301-DQB302 | 0,0882 | DR13-DQA103-DQB602/8 | 0,0784 |
| DR7-DQA201-DQB201 | 0,1373 | DR14-DQA101-DQB503 | 0,0196 |
| DR7-DQA201-DQB303 | 0,0196 | DR15-DQA102-DQB602/8 | 0,1078 |
| DR8-DQA401-DQB402 | 0,0294 | DR15-DQA103-DQB601 | 0,0098 |
| DR9-DQA301-DQB303 | 0,0196 | DR16-DQA102-DQB502/4 | 0,0686 |
Анализируя таблицу видно, что для больных туберкулезом русской этнической группы Челябинской области наиболее высокие Н наблюдаются для гаплотипов DR1-DQA101-DQB501 (0,1373), DR7-DQA201-DQB201 (0,1373), DR11-DQA501-DQB301 (0,1078), DR15-DQA102-DQB602/8 (0,1078). Также с достаточно высокой частотой встречаются гаплотипы DR4-DQA301-DQB302 (0,0882), DR13-DQA103-DQB602/8 (0,0784) и DR16-DQA102-DQB502/4 (0,0686).
2.2.5 Сравнительный анализ частот встречаемости трехлокусных гаплотипов HLA у больных туберкулезом и здоровых представителей русской этнической группы Челябинской областиДанные о наиболее часто встречаемых трехлокусных гаплотипах у больных туберкулезом и здоровых представителей русской этнической группы Челябинской области представлены в таблице 12. Сравнительный анализ представленных данных выявляет наличие общих и индивидуальных особенностей распределения гаплотипов в каждой из исследуемых групп.
Таблица 12. Сравнительный анализ частот гаплотипов у больных туберкулезом и здоровых представителей русской этнической группы
| Гаплотипы | Больные туберкулезом (n=51) | Здоровый контроль (n=202) | Χ2 |
| DR1-DQA101-DQB602/8 | 0,0098 | 0,0248 | 1,115 |
| DR7-DQA201-DQB201 | 0,1373 | 0,0965 | 1,63 |
| DR13-DQA103-DQB602/8 | 0,0784 | 0,0842 | 0,039 |
| DR14-DQA101-DQB503 | 0,0196 | 0,0099 | 0,663 |
| DR15-DQA102-DQB602/8 | 0,1078 | 0,1089 | 0,001 |
| DR15-DQA103-DQB601 | 0,0098 | 0,0248 | 0,875 |
| DR16-DQA102-DQB502/4 | 0,0686 | 0,0272 | 4,224 |
При сравнительном анализе трехлокусных гаплотипов у больных туберкулезом и здоровых представителей русской этнической группы Челябинской области было выявлено, что у больных туберкулезом частота встречаемости гаплотипа DR16-DQA102-DQB502/4 выше, чем у здорового контроля (0,0686 и 0,0272, соответственно, RR=1,15). Это может быть связано с вкладом данного гаплотипа в восприимчивость к туберкулезу (помимо экологических и социоэкономических факторов). Гаплотип DR16-DQA102-DQB502/4 имеет низкую частоту встречаемости во многих популяциях. Так, у здоровых индусов он находится в пределах 4-5% с повышением, хотя и недостоверным (возможно, из-за малого числа наблюдений), у больных лепрой и туберкулезом.
У людей, больных туберкулезом наблюдается относительно низкая частота встречаемости гаплотипов DR1-DQA101-DQB602/8 (0,0098 у больных туберкулезом и 0,0248 у здоровых), DR15-DQA103-DQB601 (0,0098 и 0,0248, соответственно). Эти гаплотипы могут вносить вклад в устойчивость к туберкулезу, но результаты являются спорными, так как не достигают статистической достоверности.
Заключение
Одно из последних направлений иммуногенетики - поиск ассоциаций иммуногенетической системы HLA с предрасположенностью к различным инфекционным заболеваниям. В настоящее время доказано многими исследованиями, что развитие инфекции, вызванной М. tuberculosis и клинический туберкулез обусловлены сложным взаимодействием между биологическими свойствами самого инфекционного агента, средовыми факторами и физиологической индивидуальностью человека.
Понимание важной роли генетических факторов в развитии туберкулеза пришло в первую очередь из эпидемиологических и близнецовых исследований. Дальнейшие исследования, проведенные на экспериментальных животных моделях, существенно дополнили имеющуюся информацию о генетических факторах предрасположенности к заболеванию.
Полиморфные человеческие лейкоцитарные антигены (HLA) были первыми белками, изученными в поисках ассоциаций с восприимчивостью к туберкулезу, которые до сих пор ведутся, что сделало их наиболее исследованными.
Результаты нашего исследования показали, что для больных туберкулезом представителей русской этнической группы Челябинской области характерно распределение генов HLA II класса, сходное с контрольной группой: с относительно высокой частотой встречались DR 1 (27,45%), DR 7 (29,41%), DQB 201 (39,21%), DQB 602/8 (37,25%), DQA 102 (37,25%), DQA 501 (39,22%); с низкой частотой встречались DR 9 (3,92%), DR 12 (1,96%), DR 14 (3,92%), DQA 401 (5,88%), DQB 401/2 (5,88%), DQB 503 (3,92%), DQB 601 (1,96%). Распределение частот аллелей генов HLA DRB1, - DQB1, - DQA1 в русской этнической группе Челябинской области в целом является характерным для большинства европеоидных популяций. Некоторые различия в частоте встречаемости антигенов могут быть связаны с вкладом генетических факторов в восприимчивость к туберкулезу.
Гаплотипические сочетания, вследствие их еще большей вариабельности, лучше отражают разнообразие HLA-системы. У больных туберкулезом русской этнической группы Челябинской области также наблюдалось сходное с контролем распределение гаплотипов: с наибольшей частотой встречались гаплотипы DR1-DQA101-DQB501 (H=0,1373), DR7-DQA201-DQB201 (0,1373), DR11-DQA501-DQB301 (0,1078), DR15-DQA102-DQB602/8 (0,1078). Такое распределение соответствует средним значениям для кавказоидов. У больных туберкулезом частота встречаемости гаплотипа DR16-DQA102-DQB502/4 выше, чем у здорового контроля (0,0686 и 0,0272, соответственно). Это может быть связано с вкладом данного гаплотипа в восприимчивость к туберкулезу (помимо экологических и социоэкономических факторов). Также, у людей, больных туберкулезом наблюдается относительно низкая частота встречаемости гаплотипов DR1-DQA101-DQB602/8 (0,0098 у больных туберкулезом и 0,0248 у здоровых), DR15-DQA103-DQB601 (0,0098 и 0,0248, соответственно). Эти гаплотипы могут вносить вклад в устойчивость к туберкулезу, но результаты являются спорными, так как не достигают статистической достоверности.
Выводы
Установлены точные показатели для антигенов и генов (Ах, Рх, , Н) локусов DR, DQA, DQB и их гаплотических сочетаний у больных туберкулезом представителей русской этнической группы Челябинской области
При сравнительном анализе особенностей распределения специфичностей генов HLA II класса у больных туберкулезом и здоровых представителей русской этнической группы Челябинской области были установлены следующие факты:
у больных туберкулезом и здоровых пациентов были выявлены различия в частоте встречаемости антигена HLA DRB1*16 (14% у больных туберкулезом и 5% у здоровых русских). Результаты являются статистически достоверными, так как χ²=4,224, RR=1,15. Также у больных туберкулезом по сравнению со здоровым контролем выявлена относительно высокая частота встречаемости гена HLA DQB*502/4 (13,73 и 6,43 соответственно). Результаты не достигают статистической достоверности, так как χ²=2,972, RR=0,76;
у больных туберкулезом частота встречаемости гаплотипа DR16-DQA102-DQB502/4 выше, чем у здорового контроля (0,0686 и 0,0272, соответственно, RR=1,15);
у людей, больных туберкулезом наблюдается относительно низкая частота встречаемости гаплотипов DR1-DQA101-DQB602/8 (0,0098 у больных туберкулезом и 0,0248 у здоровых), DR15-DQA103-DQB601 (0,0098 и 0,0248, соответственно). Эти гаплотипы могут вносить вклад в устойчивость к туберкулезу, но результаты являются спорными, так как не достигают статистической достоверности.
По результатам исследования аллель HLA DRB1*16 и гаплотип DR16-DQA102-DQB502/4 идентифицированы как факторы предрасположенности к туберкулезу. Эти результаты поддерживают гипотезу о том, что изменчивость главного комплекса гистосовместимости играет важную роль в восприимчивости или сопротивлении инфекции.
Список использованных источников
1. Авербах М.М., Литвинов В.И., Гергерт В.Я. и др. Иммунологические аспекты легочной патологии. - М.: Медицина, 1980. - 360 с.
2. Акопян А.В., Алексеев Л.П., Хаитов Р.М. Иммунологические и иммуногенетические аспекты периодической болезни // Иммунология. - 1998. - №1. - С.32-35.
3. Алексеев Л.П., Дедов И.И., Болдырева М.Н., Зилов А.В., Хаитов.Р.М. HLA-гены - маркеры инсулин-зависимого сахарного диабета, этнические аспекты // Иммунология. - 2003. - №5. - С.65-68.
4. Алексеев Л.П., Хаитов Р.М. Клиническая иммуногенетика // Цитокины и воспаление. - 2005. - №3. - С.15-19.
5. Арефьев В.А., Лисовенко Л.А. Англо-русский толковый словарь генетических терминов. - Москва: ВНИРО, 1995. - 407 с.
6. Баранов B. C., Баранова Е.В., Иващенко Т.Э., Асеев М.В. Геном человека и гены "предрасположенности". Введение в предиктивную медицину. - СПб.: Интермедиа, 2000. - 271 с.
7. Ботиашвили О.Г. Химиопрофилактика туберкулеза. - Тбилиси: Сабчота Сакартвело, 1980. - 361 с.
8. Гриппи М.А. Патофизиология легких. - M.: Восточная книжная компания, 1997. - 344 с.
9. Есипова И.К. Патологическая анатомия легких. - М.: Медицина, 2000. - 290 с.
10. Зарецкая Ю.М. Клиническая иммуногенетика. - М.: Медицина, 1983. - 365с.
11. Иващенко Т.Э., Сиделева О.Г., Петрова М.А. Генетические факторы предрасположенности к бронхиальной астме // Генетика. - 2001. - №1. - С.65-68.
12. Макаревич А.Э. Заболевания органов дыхания. - М.: Высшая школа, 2000. - 368 с.
13. Маянский Н.А., Маянский А.Н. Номенклатура и функции главного комплекса гистосовместимости человека // Иммунология. - 2006. - №1. - С.45-48.
14. Матракшин А.Г., Цой К.И., Поспелов Л.Б. Туберкулез органов дыхания // Проблемы туберкулеза. - 1993. - №1. - С.61-64.
15. Матракшин А.Г., Месько Е.М., Поспелов Л.Е. Динамика иммунологических показателей у больных туберкулезом легких // Иммунология. - 2002. - №8. - С.26-29.
16. Перельман М.И., Корякин В.А., Богадельникова И.В. Фтизиатрия. - М.: Медицина, 2004. - 467 с.
17. Пузырев В.П. Медико-генетическое исследование населения приполярных регионов. - Томск: Изд-во Томск. унив, 1991. - 200 с.
18. Пузырев В.П. Состояние и перспективы геномных исследований в генетической кардиологии. // Вестник РАМН. - 2000. - № 7. - С.31-37.
19. Ротанова Т.В. Энергозависимый селективный внутриклеточный протеолиз. Cтроение, активные центры и специфичность АТР-зависимых протеиназ // Вопросы медицинской химии. - 2001. - № 1. - С.61-65.
20. Рычков Ю.Г. Генофонд населения России и сопредельных стран // Генофонд и геногеография народонаселения. - СПб.: Наука, 2000, 120с.
21. Сараянц Л.В., Полянская И. С, Алексеев Л.Я. // Вести дерматол. - 1992. - № 4. - С. 19-25.
22. Снелл Дж., Доссе Ж., Нэтенсон С. Совместимость тканей. - М.: Медицина, 1979. - 325 с.
23. Сойфер В.П. Международный проект "Геном человека" // Соросовск. Образ. журн. - 1998. - № 12.
24. Сочнев А.М., Алексеев Л.П., Тананов А.Т. Антигены системы HLA при различных заболеваниях и трансплантации. - Рига: Наука, 1987. - 243 с.
25. Тананов А.Т. Значение системы HLA в оценке степени риска возникновения и прогноза заболеваний: Автореф. дис. канд. биол. наук - М., 1982. - 32 с.
26. Тананов А.Т. HLA и болезни крови. Ассоциация с возрастом начала заболевания, продолжительностью жизни: Матер.7-го междунар. совещ. по тканевому типированию. Тез. докл., 1981. - с.175-175.
27. Тананов А.Т., Абакумов Е.М. HLA антигены и продолжительность жизни больных острым лейкозом. - Тер. арх., 1981,№4, с.77-79.
28. Трофимов Д.Ю. Разработка метода мультипраймерной ПЦР для типирования генов HLA II класса: Дис. канд. биол. наук. - М., 1996. - 36 с.
29. Хаитов Р.М., Алексеев Л.П. Физиологическая роль главного комплекса гистосовместимости человека // Иммунология. - 2001. - №3. - С.37-42.
30. Хаитов Р.М., Алексеев Л.П. Система генов HLA и регуляция иммунного ответа. // Аллергия, астма и клиническая иммунология. - 2000. - № 8. - С.12-18.
31. Хаитов Р.М., Игнатьева Г.А., Сидорович И.Г. Иммунология. - М.: Медицина, 2000. - 583 с.
32. Хоменко А.Г. Туберкулез. Руководство для врачей. - М.: Медицина, 1996. - 493 с.
33. Шевченко Ю.Л. Значение социальных факторов во взаимодействии человека и микроорганизмов. Роль здравоохранения в профилактике и лечении инфекционных заболеваний // Вестн. РАМН. - 2000. - № 11. - С.41-47.
34. Bach F. H., Gose J. F., Alter B. J. et al. Post, present and future aspects of histocompatibility. - Transplant. Proc. - 1979. - vol.11. - №1. - 1207-1211.
35. Brodsky F. M., Lem L., Bresnahan P. A. Antigen Processing and Presentation // Tissue Antigens. - №47 (6). - 464-471.
36. Dausset J., Contu L. MHC in general biologic recognition: its theoretical implication in transplantation. - Transplant. Proc. - 1981. - vol.13. - №13. - 895-899.
37. Endert P. M., Lopez M. T., Patel S. D., Monaco J. J., McDevitt H. O. Genomic polymorphism, recombination, and linkage disequilibrium in human major histocompatibility complex-encoded antigen-processing genes // Proc. Nat. Acad. Sci. - 1992. - 89. - 11594-11597.
38. Kwiatkowski D., Anstey N. M., Twumasi P., Rowe P. A., Bennett S., Brewster D., McMichael A. J., Greenwood B. M.common West African HLA antigens are associated with protection from severe malaria. - Nature 352. - 1991.
39. Larsen C. E., Alper C. A. The genetics of HLA-associated disease. Curr. Opin. Immunol. - 16. - 2004.
40. http://www.en. wikipedia.org/wiki/Human_leukocyte_antigen.
41. http://www.rusmedsever.ru.
42. http://www.rusbiotech.ru.
43. http://www.liveinternet.ru.
44. http://pathology. dn.ua/Lectures/Immune_Anormalities
Приложения
Приложение 1
Таблица 1. Встречаемость аллельных вариантов гена HLA DRB1*04 в различных популяционных группах России
| Аллель HLA DRBI | Русские | Поморы | Саамы | Татары | Мари | Тувинцы | Ненцы |
| 04 | 11,64 | 35,37 | 33,52 | 17,78 | 16,34 | 28,74 | 17,39 |
| 0401* | 3,80 | 16,21 | 9,14 | 5,61 | 12,65 | 12,13 | 0,73 |
| 0402 | 1,66 | 0 | 0,76 | 0,93 | 0 | 0 | 0 |
| 0403** | 0,95 | 1,47 | 8,38 | 1,87 | 1,05 | 5,75 | 7,16 |
| 0404* | 3,09 | 17,69 | 5,33 | 7.9 | 0,53 | 1,28 | 10,14 |
| 0405* | 0 | 0 | 0 | 0 | 0 | 5,75 | 0 |
| 0407 | 1,66 | 0 | 0 | 0 | 0,53 | 0 | 0 |
| 0408 | 1, 19 | 0 | 16,00 | 1,87 | 1,58 | 2,93 | 0 |
| 0410 | 0 | 0 | 0 | 0 | 0 | 1,28 | 0 |
* Ассоциация с предрасположенностью к ИЗСД
** Ассоциация с устойчивостью к тому же заболеванию
Приложение 2
Таблица 2. HLA-антигены, связанные со сходными параметрами иммунного статуса в бурятской и русской популяциях
| Параметр | Буряты | Русские |
| IgM | HLA-A1↑, B15↓, В40↓ | HLA-B5↑ |
| lgG | HLA-A2↓, В7↓ | - |
| Фагоцитоз | HLA-B12↓, B40↑ | HLA-B27↓ |
| РБТЛ-сп | НLA-В16↓, В40↓ | HLA-B7, DR2↓ |
| РБТЛ-ФГА | HLA-A10↓, DR2↓ | HLA-B8↑, DQ2↑ |
| Интерлейкин-2 | HLA-B16↓, DR7↑ | HLA-B7↑, DR4↓, DQ3↓ |
Приложение 3
Таблица 3. Распределение аллелей HLA у больных лепрой, туберкулезом и здоровых
| Специфичность локуса | Здоровые лица (n = 94) | Больные лепрой (n = 133) | Больные туберкулёзом (n = 51) | |||
| DRB1*01 | 14,9 | 21,1 | 11,8 | |||
| DRB1*04 | 20,2 | 21,1 | 25,5 | |||
| DRB1*07 | 31,9 | 22,6 | 31,4 | |||
| DRB1*08 | 4,3 | 6,8 | 1,9 | |||
| DRB1*09 | 5,3 | 1,5 | 2,7 | |||
| DRB1*10 | 3,2 | 0,8 | 1,9 | |||
| DRB1*11 | 32,9 | 27,8 | 25,5 | |||
| DRB1*12 | 3,2 | 2,3 | 1,9 | |||
| DRB1*13 | 38,3 | 31,6 | 29,4 | |||
| DRB1*14 | - | 1,5 | 1,9 | |||
| DRB1*15 | 28,7 | 34,6** | 21,6 | |||
| DRB1*16 | 5,3 | 15,1* | 13,7* | |||
| DRB1*17 | 10,6 | 13,5 | 29,4* | |||
| DQA1*0101 | 18,1 | 19,4 | 13,7 | |||
| DQA1*0102 | 43,6 | 56,7* | 47,1 | |||
| DQA1*0103 | 18,1 | 14,9 | 18,9 | |||
| DQA1*0201 | 29,8 | 22,4 | 31,4 | |||
| DQA1*0301 | 27,7 | 22,4 | 29,4 | |||
| DQA1*0401 | 3,2 | 6,7 | 1,9 | |||
| DQA1*0501 | 58,5 | 50,0 | 62,7 | |||
| DQB1*0201 | 41,5 | 32,3 | 49,0** | |||
| DQB1*0301 | 52,1 | 42,9 | 37,3* | |||
| DQB1*0302 | 12,8 | 14,3 | 15,7 | |||
| DQB1*0303 | 7,5 | 6,0 | 17,6* | |||
| DQB1*0401/02 | 4,3 | 6,8 | 3.9 | |||
| DQB1*0501 | 15,9 | 24,1 | 11,8 | |||
| DQB1*0502/04 | 6,4 | 17,3* | 13,7 | |||
| QB1*0601 | 1,1 | 3,0 | - | |||
| QB1*0602/08 | 55,3 | 54,1 | 47,1 | |||
Приложение 4
Таблица 4. Распределение частот гаплотипов у больных туберкулезом, лепрой и здоровых лиц
| DRB1-DQA1-DQB1 | Здоровые лица (n = 94) | Больные лепрой (n = 133) | Больные туберкулезом (n = 51) |
| 04-0301-0302 | 10,5 | 13,8 | 17,6 |
| 04-0301-0301 | 10,5 | 7,8 | 5,9 |
| 07-0201-0201 | 25,3 | 16,4 | 21,6 |
| 08-0401/2-0401/2 | 4,2 | 5,2 | 1,9 |
| 11-0501-0301 | 33,7 | 21,6* | 25,5 |
| 12-0501-0301 | 1,1 | 1,7 | - |
| 13-0501-0301 | 9,5 | 9,5 | 3,9 |
| 13-0102-0602/8 | 7,4 | 12,1 | 11,8 |
| 13-0103-0602/8 | 20,0 | 12,3 | 13,7 |
| 15-0102-0602/8 | 27,4 | 31,9 | 21,6 |
| 16-0102-0502/4 | 5,3 | 15,1* | 13,7* |
| 17-0501-0201 | 11,6 | 13,5** | 29,4* |
Приложение 5

Рисунок 6. Диаграммы распределения HLA II класса у больных туберкулезом русской этнической группы
Приложение 6



Рисунок 7. Диаграммы распределения генов HLA II класса у больных туберкулезом и здоровых пациентов
Приложение 7
Таблица 5. Частоты трехлокусных сочетаний у больных туберкулезом представителей русской национальности, проживающих в Челябинской области
| Тип гаплотипа | Частота встречаемости (H) |
| DR1-DQA101-DQB501 | 0.137255 |
| DR1-DQA101-DQB602/8 | 0.009804 |
| DR11-DQA501-DQB301 | 0.107843 |
| DR12-DQA501-DQB301 | 0.019608 |
| DR13-DQA102-DQB602/8 | 0.019608 |
| DR13-DQA103-DQB602/8 | 0.078431 |
| DR13-DQA501-DQB301 | 0.019608 |
| DR14-DQA101-DQB503 | 0.019608 |
| DR15-DQA102-DQB602/8 | 0.107843 |
| DR15-DQA103-DQB601 | 0.009804 |
| DR16-DQA102-DQB502/4 | 0.068627 |
| DR3-DQA501-DQB201 | 0.078431 |
| DR4-DQA301-DQB301 | 0.029412 |
| DR4-DQA301-DQB302 | 0.088235 |
| DR7-DQA201-DQB201 | 0.137255 |
| DR7-DQA201-DQB303 | 0.019608 |
| DR8-DQA401-DQB402 | 0.029412 |
| DR9-DQA301-DQB303 | 0.019608 |
Приложение 8
Таблица 6. Частоты трехлокусных сочетаний у здоровых представителей русской национальности, проживающих в Челябинской области
| Тип гаплотипа | Частота встречаемости (H) |
| DR1-DQA101-DQB501 | 0.146032 |
| DR1-DQA101-DQB503 | 0.002475 |
| DR1-DQA101-DQB602/8 | 0.002483 |
| DR10-DQA101-DQB501 | 0.014851 |
| DR10-DQA104-DQB501 | 0.002475 |
| DR11-DQA102-DQB502/4 | 0.002475 |
| DR11-DQA301-DQB301 | 0.002475 |
| DR11-DQA501-DQB301 | 0.089109 |
| DR12-DQA501-DQB301 | 0.017327 |
| DR13-DQA102-DQB602/8 | 0.022277 |
| DR13-DQA103-DQB602/8 | 0.084158 |
| DR13-DQA301-DQB301 | 0.002475 |
| DR13-DQA501-DQB301 | 0.029703 |
| DR14-DQA101-DQB501 | 0.004950 |
| DR14-DQA101-DQB503 | 0.009901 |
| DR15-DQA102-DQB501 | 0.002483 |
| DR15-DQA102-DQB602/8 | 0.108903 |
| DR15-DQA103-DQB601 | 0.024752 |
| DR16-DQA102-DQB502/4 | 0.027228 |
| DR3-DQA501-DQB201 | 0.089109 |
| DR3-DQA501-DQB301 | 0.004950 |
| DR3-DQA501-DQB302 | 0.002475 |
| DR4-DQA301-DQB301 | 0.029703 |
| DR4-DQA301-DQB302 | 0.066832 |
| DR4-DQA301-DQB305 | 0.002475 |
| DR4-DQA401-DQB301 | 0.002475 |
| DR7-DQA201-DQB201 | 0.096534 |
| DR7-DQA201-DQB303 | 0.024752 |
| DR8-DQA301-DQB302 | 0.002475 |
| DR8-DQA401-DQB401/2 | 0.037129 |
| DR8-DQA501-DQB301 | 0.004950 |
| DR9-DQA301-DQB303 | 0.022277 |
0 комментариев