Навигация
Характеристика микобактерий туберкулеза
Микобактерии туберкулеза (МБТ) – факультативные внутриклеточные паразиты.
Микобактерии туберкулеза (МБТ) относятся к семейству бактерий Micobacteriacae, порядку Actinomycetalis, роду Mycobacterium.
Этимологически слово «микобактерия» происходит из греческих слов myces – гриб и bacterium, bactron – палочка, прутик. Компонент названия «гриб» обусловлен тенденцией этих микроорганизмов образовывать нитчатые и ветвящиеся формы, похожие на плесень.
C позиций клинической медицины, микобактерия туберкулеза, открытая немецким ученым Робертом Кохом в 1882 г., является наиболее важным видом микобактерий туберкулеза, которые объединены в комплекс, включающий: M. tuberculosis (МБТ); M.bovis и ее вариант БЦЖ (бацилла Кальметта и Жерена); M.africanum и M.microti. Эта группа микобактерий отличается выраженным генетическим сходством.
Микобактерия туберкулеза (МБТ) является главной причиной заболевания туберкулезом человека. M.bovis и M.africanum вызывают заболевание у человека, клинически не отличающееся от классического туберкулеза.
M.microti считается не патогенной для человека, однако вызывает заболевание у мышей, напоминающее туберкулез. Культура БЦЖ не является патогенной для человека.
Представленные в дальнейшем материалы о туберкулезе имеют отношение только к заболеванию, вызываемому M. tuberculosis (МБТ) – бактерия Коха (БК) Typus humanus.
Естественный резервуар туберкулезной микобактерии – человек, домашние и дикие животные, птицы.
МБТ внешне представляют собой тонкие изогнутые палочки, стойкие к кислотам, щелочам и высыханию. Наружная оболочка бактерии содержит сложные воска и гликолипиды.
МБТ могут размножаться как в макрофагах, так и вне клеток.
МБТ размножаются относительно медленно. Размножение происходит в основном путем простого клеточного деления. На обогащенных питательных средах МБТ размножаются с периодом удвоения от 18 до 24 часов. Для роста в культуре микобактерий туберкулеза, полученных в клинических условиях, необходимо от 4 до 6 недель.
Генетическая структура МБТ установлена. С нуклеотидной последовательностью МБТ можно ознакомиться в международных банках данных. Нуклеотидная последовательность МБТ насчитывает 4,411,529 b.p.
Самостоятельным движением МБТ не обладают. Температурные границы роста на-ходятся между 29 и 42 °C (оптимальная – 37 – 38 °C). МБТ обладают устойчивостью к физическим и химическим агентам; они сохраняют жизнеспособность при очень низких температурах, а повышение до 80°C могут выдерживать в течение 5 мин.
Во внешней среде микобактерия туберкулеза достаточно устойчива. В воде она может сохраняться до 150 дней. Высохшие микобактерии вызывают туберкулез у морских свинок через 1 – 1,5 года, лиофилизированные и замороженные жизнеспособны до 30 лет.
При интенсивном облучении солнцем и при высокой температуре окружающей среды, жизнеспособность МТБ резко снижается; напротив, в темноте и сырости выживаемость их весьма значительна. Вне живого организма они остаются жизнеспособными в течение многих месяцев, в особенности в темных, сырых помещениях.
МБТ выявляются с помощью уникального свойства к окрашиванию (кислотоустойчивостью), отличающего их от многих других возбудителей инфекции. Цилем (Ziehl) и Нильсенем (Neelsen) в 1883 г. был разработан специальный контрастный метод окраски МБТ, основанный на свойстве кислотоустойчивости. Препарат, окрашенный при подогревании карболовым фуксином, обесцвечивается раствором серной кислоты и после промывания водой доокрашивается раствором метиленовой синьки (способ Циля–Нильсена). В отличие от некислотоустойчивых бактерий, туберкулезные микобактерии окрашиваются в красный цвет, не обесцвечиваются при действии раствора кислоты и хорошо видны на синем фоне при микроскопии. Способ Циля–Нильсена до сих пор является одним из основных методов окраски МБТ при микроскопии.
С липидной фракцией внешней оболочки МБТ связывают устойчивость возбудителей туберкулеза к кислотам, щелочам и спиртам.
Изменчивость морфологии МБТ. Морфология и размеры МБТ не постоянны, это зависит от возраста клеток и особенно от условий существования и состава питательной среды.
Корд-фактор. Липиды поверхностной стенки микобактерий определяют ее вирулентность и способность к образованию в культуре скоплений бактерий в виде кос (корд-фактор).
О корд-факторе было сказано еще Кохом в его начальном сообщении относительно МБТ. Первоначально корд-фактор связывали с вирулентностью МБТ. Способность формировать косы наблюдается среди других микобактерий, имеющих низкую или вообще отсутствие вирулентности. Корд-фактор, как было установлено позже, связан с необычным биологическим веществом trehalose 6,6-dimycolate, которое обладает высокой вирулентностью, со смертельным исходом при введении в организм экспериментальных животных. Однако роль этого вещества в патогенезе туберкулеза окончательно не установлена.
L-формы. Одним из важных видов изменчивости МБТ является формирование L-форм. L-формы характеризуются сниженным уровнем метаболизма, ослабленной вирулентностью. Оставаясь жизнеспособными, они могут длительное время находиться в организме и индуцировать противотуберкулезный иммунитет.
L-формы отличаются выраженными функциональными и морфологическими изменениями. Обнаружено, что трансформация МБТ в L-формы усиливается при длительном влиянии антибактериальной терапии и других факторов, которые нарушают их рост и размножение, образование клеточной мембраны.
Установлено, что в мокроте «абациллярных» больных с деструктивными формами туберкулеза могут находиться L-формы МБТ, способные при соответствующих условиях реверсировать (модифицироваться) в палочковидный вариант, вызывая тем самым реактивацию туберкулезного процесса. Следовательно, абациллирование каверн таких больных еще не означает их стерилизацию в отношении МБТ.
МБТ по своей природе нечувствительны ко многим антибиотикам. Это свойство в первую очередь связано с тем, что высоко гидрофобная клеточная поверхность служит своего рода физическим барьером для терапевтических агентов и антибиотиков. Главная причина устойчивости закодирована в структуре генома туберкулезной палочки.
Вместе с тем, МБТ могут вырабатывать устойчивость (резистентность) к противотуберкулезным препаратам. Одновременная лекарственная устойчивость МБТ к нескольким препаратам в последние годы значительно снижает эффективность лечения туберкулеза.
В результате современное здравоохранение имеет дело не просто с опасным возбудителем туберкулеза, а с целым набором его штаммов, устойчивых к разным лекарствам. На практике для организации эффективного лечения туберкулеза важно не только обнаружить МБТ, но и параллельно определить их резистентность, причем достаточно быстро – в течение двух-трех дней, чтобы вовремя назначить эффективную химиотерапию.
В конце 80-х гг. прошлого века появился метод, значительно сокращающий время такого анализа. Новая диагностика основана на избирательной амплификации нуклеиновых кислот (ДНК или РНК) in vitro с помощью полимеразной цепной реакции (ПЦР).
Метод ПЦР имеет большие возможности и лежит в основе точной ДНК-диагностики, которая позволяет идентифицировать любой штамм МБТ и определять первопричину той или иной устойчивости к лекарствам.
Лабораторные исследования показали, что возникновение резистентности у M. tuberculosis связано с нуклеотидными заменами (мутациями) в генах, кодирующих различные ферменты, которые непосредственно взаимодействуют с лекарственными средствами.
Резистентность некоторых штаммов МБТ к изониазиду связана с мутациями в гене katG, приводящими к замене некоторых аминокислот в ферментах – каталазе и пероксидазе.
Нечувствительность МБТ к стрептомицину связана с миссенс-мутацией в гене rpsL, кодирующем S12 митохондриальный белок, или с нуклеотидными заменами в гене rrs, кодирующем 16S РНК.
Представленные некоторые мутации в геноме микобактерии туберкулеза являются лишь ограниченными примерами формирования ее резистентности к противотуберкулезным препаратам. На этом основании можно сделать следующий вывод: по мере внедрения в практику химиотерапии туберкулеза новых лекарств в М. tuberculosis будут происходить мутации, приводящие к резистентности ко всем без исключения используемым препаратам, и это обстоятельство необходимо постоянно учитывать в тактике лечения туберкулеза.
Пути и способы заражения туберкулезом
Источник инфекции. Основным источником МБТ является больной туберкулезом человек, распространяющий МБТ (бацилловыделитель).
Очаг туберкулезной инфекции становится опасным в тех случаях, когда больные страдают открытой формой туберкулеза, т.е. выделяют туберкулезные микобактерии. Особое значение при заражении туберкулезом имеет прямой, длительный и тесный контакт здорового человека с бацилловыделителем. Заражение может происходить чаще всего в семье, в месте проживания или в коллективе долгое время, в которых находится больной туберкулезом, выделяющий микобактерии. Опасность рассеивания заразного начала устраняется, если бацилловыделитель своевременно выявлен и изолирован.
Возникновение и течение инфекции зависят не только от вирулентности возбудителя, но и от состояния устойчивости и реактивности макроорганизма.
Большое значение имеет место проникновения МБТ в организм, где завязывается первичный контакт с микробом (входные ворота инфекции). Различают следующие пути передачи туберкулеза:
1) воздушно-капельный;
2) алиментарный (через пищеварительный тракт);
3) контактный;
4) внутриутробное заражение туберкулезом.
Воздушно-капельный путь заражения туберкулезом
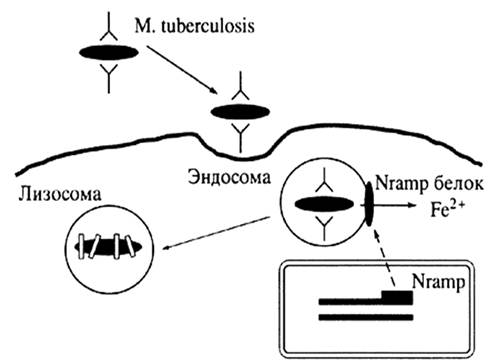
Туберкулезные микобактерии попадают в воздух с капельками при кашле, разговоре и чихании больного с активным туберкулезом. При вдыхании эти зараженные капельки проникают в легкие здорового человека. Этот способ заражения получил название воздушно-капельной инфекции (см. рис. 1).
В зависимости от силы кашлевых импульсов и размеров капелек МБТ распространяются в воздухе на различные расстояния: при кашле – до 2 м, при чихании – до 9 м. В среднем частицы мокроты рассеиваются на расстояние 1 м прямо перед больным.
Пылевая инфекция
Капельки туберкулезной мокроты, осевшие на пол, высыхают и превращаются в пылинки. Находившиеся в них туберкулезные микобактерии некоторое время остаются в пыли жизнеспособными. Установлено, что к 18-му дню в высушенной мокроте остается 1% живых бактерий. При сильном движении воздуха, подметании пола, перемещении людей пылинки, содержащие туберкулезные микобактерии, поднимаются в воздух, проникают в легкие и вызывают заражение.
Алиментарный путь заражения через пищеварительные пути
Специальные эксперименты на животных показывают, что при алиментарном способе требуется значительно большее количество микобактерий, чем при аэрогенном заражении. Если при вдыхании достаточно одной или двух микобактерий, то для заражения через пищу требуются сотни микробов.
Пути распространения туберкулезных микобактерий в организме человека при алиментарном заражении туберкулезной культурой демонстративно показывают секционные материалы, опубликованные в связи с судебным процессом в Любеке. По ошибке 252 грудным детям при вакцинации per os была введена туберкулезная культура (кильский штамм) вместо БЦЖ. Вследствие заражения умерло от туберкулеза 68 детей, заболел 131 ребенок и 53 остались здоровыми.
При вскрытии трупов 20 умерших детей было установлено, что в большинстве случаев процесс локализовался в органах брюшной полости. Входными воротами инфекции были органы пищеварения.
Одной из особенностей этого пути заражения у маленьких детей является частое поражение туберкулезом мезентериальных лимфатических узлов.
Необходимо иметь в виду, что проникновение туберкулезных микобактерий в кишечник может происходить и при заглатывании больными легочным туберкулезом собственной бациллярной мокроты, что подтверждается нахождением бактерий в значительном количестве методом флотации промывных вод желудка.
Контактный путь передачи туберкулеза
Описаны случаи заражения через конъюнктиву глаза маленьких детей и взрослых; при этом иногда обнаруживается острый конъюнктивит и воспаление слезного мешочка.
Заражение туберкулезом через кожу встречается редко. Описаны случаи заболеваний туберкулезом доярок при проникновении МБТ через поврежденную кожу рук от больных туберкулезом коров.
Внутриутробное заражение туберкулезом
Возможность заражения туберкулезом плода в период внутриутробной жизни установлена на секции случаями туберкулеза у детей, умерших в первые дни после рождения. Заражение происходит или при поражении туберкулезом плаценты, или при инфицировании поврежденной плаценты во время родов туберкулезной матерью. Такой путь заражения туберкулезом встречается крайне редко.
Этиология и иммунитет
Морфологические и биохимические компоненты микробной клетки вызывают различные реакции в организме.
Основными биохимическими компонентами МБТ являются:
– белки;
– углеводы;
– липиды.
Белки (туберкулопротеиды) являются основными носителями антигенных свойств МВТ.
Туберкулин – один из туберкулопротеидов, широко используемый в практике для выявления инфицирования МВТ. (Подробнее см. в разделе 2.3. Туберкулинодиагностика.)
Гиперчувствительность замедленного типа (ГЗТ)
Вещества, входящие в состав внешней оболочки МБТ, индуцируют специфическую тканевую воспалительную реакцию макроорганизма и образование гранулемы. Одновременно появляется гиперчувствительность замедленного типа (ГЧЗТ), определяемая по реакции на туберкулиновые пробы, и слабое антителообразование.
В основном ГЧЗТ используется для характеристики иммунного ответа IV типа (наличие индурации, развившейся через 48 часов, на участке внутрикожного введения туберкулина) у индивидов, инфицированных МБТ. Вместе с тем, ГЧЗТ связывают с иммунной реакцией на факторы, повреждающие ткани.
Связь между иммунным ответом и патогенезом
Локальные и генерализованные туберкулезные повреждения в организме определяются защитными реакциями, которые производит иммунная система организма против МБТ. При описании этого сложнейшего процесса ограничимся простым перечислением событий, происходящих с момента первичного проникновения МБТ в альвеолы до результатов естественной борьбы между макроорганизмом и МБТ. Этот процесс определяет судьбу, по крайней мере, трети населения мира, которое инфицировано микобактериями туберкулеза.
Цикл развития туберкулеза от инфициро-вания организма микобактериями туберкулеза до клинических проявлений болезни и распространения МБТ в окружающей среде можно условно разделить на 5 этапов.
Этапы.
1. Распространение инфекции (инфицирование).
2. Начало инфекции, пролиферация и диссеминация в инфицированном организме.
3. Развитие иммунной реакции организма.
4. Казеация и ускоренное размножение МВТ.
5. Вторичное распространение инфекции (способность инфицировать, заражать).
Краткое описание каждого этапа
Этап 1. Распространение инфекции.
1.1. Больной туберкулезом продуцирует аэрозоли, в которых содержатся МБТ.
1.2. Мелкие частицы аэрозоля высыхают и становятся пылевыми частицами.
1.3. Пылевые частицы, содержащие микобактерии, вдыхаются человеком.
1.4. Частицы проникают через бронхи и скапливаются в альвеолах.
1.5. Микобактерии поглощаются альвеолярными макрофагами не иммунизированного организма.
1.6. Если альвеолярные макрофаги способны уничтожить МТБ, инфекция не развивается.
Этап 2. Начало инфекции, пролиферация и диссеминация.
2.1. МБТ выживают и размножаются в альвеолярных макрофагах.
2.2. Размножающиеся МБТ убивают альвеолярные макрофаги, макрофаги распадаются, высвобожденные хемокины и МБТ взаимодействуют с новыми клетками.
2.3. Вновь сформированные макрофаги и моноциты захватывают и переваривают МБТ.
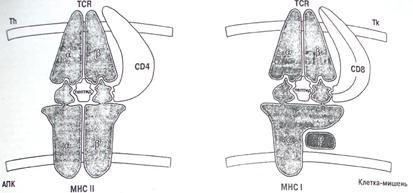
2.4. Киллерные клетки и T-лимфоциты начинают накапливаться в поврежденных участках.
2.5. МБТ продолжают размножаться, убивая клетки макроорганизма, и распространяться локально (в участке своего первоначального внедрения).
2.6. МБТ транспортируются во внутригрудные лимфатические узлы, откуда распространяются в системные органы.
Этап 3. Развитие иммунного ответа макроорганизма. Развитие туберкулезного процесса в течение 3-го этапа может происходить в двух вариантах.
Вариант 1. У большинства пациентов в течение 3-го этапа появляется достаточная устойчивость, чтобы подавлять развитие туберкулеза на протяжении всей жизни.
3.1.1. Размножение МБТ останавливается, а их количество резко уменьшается.
3.1.2. Первичный фокус и его дочерние фокусы оставляют после себя минимальные остаточные проявления.
3.1.3. Туберкулиновый кожный тест становится положительным.
Вариант 2 (неблагоприятный). При недостаточно активной иммунной реакции происходит прогрессирование туберкулезного процесса. Такое прогрессирование чаще наблюдается среди ВИЧ-инфицированных, детей, а также у лиц, предрасположенных к туберкулезу.
У некоторых пациентов возникает реактивация скрытой туберкулезной инфекции. Реактивация может происходить вне легких или в самом легком и закончиться тканевым повреждением, формированием полости распада и вторичным размножением МБТ.
На клеточном уровне неблагоприятный вариант 3-го этапа характеризуется следующими процессами.
3.2.1. Макрофаги передают туберкулезные антигены Т-лимфоцитам; T-лимфоциты высвобождают цитокины.
3.2.2. Цитокины стимулируют продуцирование и активацию макрофагов. В результате формируется защита от повреждения клеток и тканей.
3.2.3. Указанные реакции ограничивают быстрое размножение и/или уничтожают МБТ, заканчиваются формированием первичного легочного фокуса.
3.2.4. Если макроорганизм не способен создать эффективную защиту от МБТ, первичный очаг прогрессирует.
Этап 4. Казеация и ускоренное размножение МБТ.
4.1. Туберкулезный фокус в легком реактивируется, подвергается некротизированию (казеации) с последующим формированием полости.
4.2. В этот период МБТ, находящиеся во внеклеточном пространстве, размножаются экспоненциально.
Этап 5. Вторичное распространение инфекции.
5.1. Пациент откашливает мокроту, содержащую МБТ, другой человек вдыхает их. Таким образом процесс заражения человека в некоторых случаях приводит к выделению МБТ в окружающую среду, тем самым продолжается распространение МБТ среди окружающих.
Заключение. Для развития клинических проявлений туберкулеза необходим комплекс факторов. Известно, что у здоровых людей весьма часто обнаруживаются вирулентные микобактерии туберкулеза, однако заболевают туберкулезом далеко не все их носители. Только при наличии сложной комбинации неблагоприятных внешних и внутренних предрасполагающих факторов, резко снижающих сопротивляемость организма, заражение туберкулезными микобактериями может перейти в заболевание туберкулезом. Вместе с тем, заражение туберкулезными микобактериями может закончиться так называемой скрытой инфекцией без серьезных последствий.
Скрытая инфекция
Скрытой инфекцией принято считать такой инфекционный процесс, при котором отсутствуют клинические проявления болезни при наличии жизнеспособных микробов в организме. Существование процесса при скрытой инфекции может быть установлено посредством патоморфологического исследования или при помощи иммунобиологических реакций.
Скрытая инфекция при туберкулезе является:
1) следствием неразвившейся первичной инфекции, при которой МБТ продолжают оставаться в организме;
2) результатом незаконченного процесса после перенесенного туберкулеза.
В обоих случаях в организме находятся туберкулезные микобактерии, но условия возникновения скрытой инфекции разные. В первом случае скрытая инфекция возникает при наличии некоторой врожденной устойчивости организма, благодаря чему инфекционный очаг не развивается. Во втором – она наступает вследствие приобретения организмом иммунитета в процессе болезни, когда остается латентный очаг. В обоих случаях способность организма недостаточна чтобы уничтожить МБТ.
Следовательно, возникновение скрытой инфекции при туберкулезе зависит как от степени вирулентности туберкулезных микобактерии, так и от состояния сопротивляемости и иммунобиологической реактивности макроорганизма. Имеет значение и влияние внешней среды на организм.
Патологическая анатомия туберкулеза
Легкие – это основной орган, поражаемый при туберкулезе.
Легкие состоят из долей: правое – из трех (верхняя, средняя, нижняя), левое – из двух (верхняя и нижняя). Доли легких делятся на сегменты. В правом легком разделяют 10 сегментов, в левом – 9 (См. рис. 2). Сегменты состоят из долек. Всего в легких содержится около 1000 долек. В среднем размер дольки легкого 1-1,5 см. Совокупность долек составляет субсегмент. Несколько субсегментов образуют сегмент.
Каждый сегмент легкого имеет свой бронх и свою артерию, причем как бронхи, так и артерии почти параллельны. Бронхолегочные сегменты по форме напоминают треугольник, вершиной обращенный медиально, а основанием – к периферической поверхности. Каждый сегмент легкого отделен от соседнего слоем соединительной ткани.
Бронхи. Два главных бронха начинаются от бифуркации трахеи на уровне 4-го грудного позвонка и заканчиваются в соответствующем легком. После входа в легкие бронхи делятся на долевые. Каждый из них дихотомически делится до концевых (конечных, терминальных) бронхиол (bronchulus terminalis) (см. рис. 3.).
Строение легочной паренхимы. Самой мелкой самостоятельной функциональной единицей легочной паренхимы является ацинус (acinus) (см. рис. 3). Это, в известном смысле, легкое в миниатюре диаметром около 1,5 мм.
Ацинус вентилируется конечной брон-хиолой (bronchiolus или bronchulus terminalis) – самым мелким разветвлением бронхиального дерева.
Группа ацинусов образует дольку (lobulus), диаметр которой достигает 1–1,5 см.
Слизистая мембрана, содержащая реснит-чатый, цилиндрический эпителий выстилает внутренние стенки бронхов и конечных структур.
Альвеолярные проходы и альвеолы покрыты тонким слоем прозрачного, чешуйчатого эпителия.
Кровеносные сосуды легких. Легочная артерия транспортирует венозную кровь к легким, ее ветви расположены вдоль бронхиальной сети, делясь, повторяют ветвления бронхов. Терминальные отделы легочной артерии заканчиваются густой сетью капиллярных сосудов, с последующим формированием венозной сети, которая окружает промежуточные стенки альвеолярных проходов и воздушные ячейки. Обогащенная кислородом кровь, возвращается в левое предсердие. Артерии обычно располагаются сверху и сзади бронха, в то время как вены – ниже и впереди его.
Плевра. Каждое легкое окружено серозной оболочкой – плеврой, которая покрывает корень легкого и соответствующие отделы грудной клетки. Та часть мембраны, которая покрывает легкие, называется висцеральной плеврой (pleura visceralis, s. pleura pulmonalis). Она непрерывно переходит на внутренние стенки грудной клетки, где называется париетальной плеврой (pleura parietalis), разделяясь на реберную (pleura costalis), диафрагмальную (pleura diaphragmatica) и медиастинальную (pleura mediastinalis). Висцеральная плевра очень тонкая, упругая, неразрывно связана со структурой легкого. Париетальная плевра сравнительно толще, имеет малую эластичность и может легко отслаиваться от ребер и межреберных мышц, которые она покрывает.
Лимфатическая система легких. На поверхности легкого сформирована тонкая субплевральная сеть лимфатических сосудов, сообщающаяся посредством пор с плевральной полостью. Паренхима легких содержит два вида лимфатических структур, один из которых формирует сложную сеть, расположенную под слизистой мембраной бронхов, а другой начинается в капиллярах между альвеолярными проходами и альвеолярными мешочками.
Лимфатические сосуды обеих структур заканчиваются в бронхиальных лимфатических узлах корня легкого. Эти узлы очень многочисленные и часто больших размеров, расположены вокруг бронхов и бифуркации трахеи (Рис. 4).
Иннервация легких осуществляется симпатическими и парасимпатическими нервами. Симпатические и парасимпатические нервы образуют два сплетения.
Похожие работы
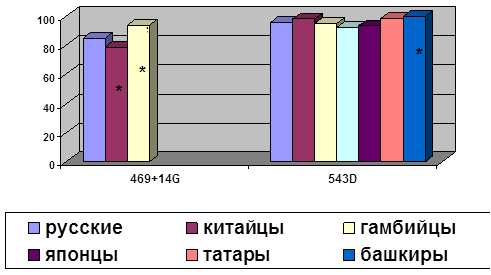
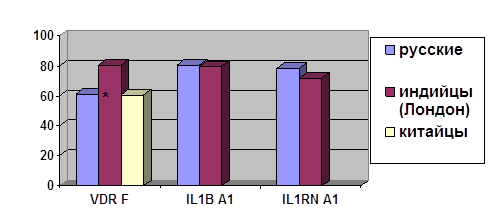
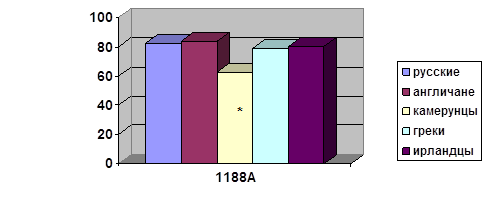
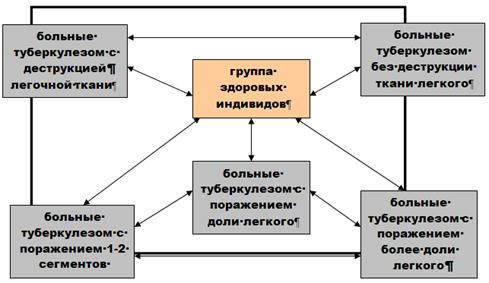
... о связи между частотой аллелей генов-кандидатов ТБ и особенностями распространения этого инфекционного заболевания. Выводы Выявлены особенности в распределении частот аллелей, изученных генов–кандидатов подвержености к туберкулезу, у русских жителей г. Томска по сравнению с другими популяциями мира. При сравнении с тувинцами показаны отличия в распределении генотипов и частот аллелей по всем ...
... с наличием быстро развивающихся каверн, захватывающей 2-3 и более долей легких, остается высокой первичная инвалидность от туберкулеза. ОРГАНИЗАЦИЯ И СИСТЕМА БОРЬБЫ С ТУБЕРКУЛЕЗОМ Центральным звеном в системе борьбы с туберкулезом является противотуберкулезный диспансер. Противотуберкулезный диспансер специализированное лечебно-профилактическое и организационно методическое учреждение, ...
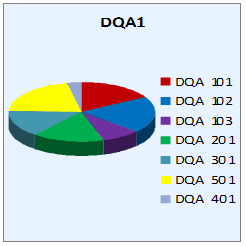
... их гаплотических сочетаний у больных туберкулезом представителей русской этнической группы Челябинской области При сравнительном анализе особенностей распределения специфичностей генов HLA II класса у больных туберкулезом и здоровых представителей русской этнической группы Челябинской области были установлены следующие факты: у больных туберкулезом и здоровых пациентов были выявлены различия в ...
... к 3%-ному щелочному раствору формальдегида и 8%-ной эмульсии феносмолина, особенно M.intracellulare и M.gordonae (Колычев, 1984). 10. Иммунизирующие свойства микобактерий. Со времени открытия возбудителя туберкулеза были проведены многочисленные исследования по изучению иммуногенности живых и убитых туберкулезных и атипичных микобактерий. Иммунопрофилактика туберкулеза с помощью вакцин ...
0 комментариев