МІНІСТЕРСТВО ОХОРОНИ ЗДОРОВ'Я УКРАЇНИ
Український інститут клінічної генетики
Харківського державного медичного університету
Новікова Ірина Володимирівна
УДК: 616-074.614.254.575
Вільні амінокислоти крові в діагностиці спадкових
хвороб обміну у дітей високого генетичного ризику
03.00.15 - генетика
АВТОРЕФЕРАТ
дисертації на здобуття наукового ступеня
кандидата медичних наук
Харків – 2008
Дисертацією є рукопис.
Робота виконана в Харківській медичній академії післядипломної освіти МОЗ України.
Науковий керівник:
член-кореспондент АМН України, доктор медичних наук, професор
Гречаніна Олена Яківна, Харківський державний медичний університет
МОЗ України, завідувач кафедри медичної генетики, Український інститут клінічної генетики Харківського державного медичного університету, директор, м. Харків.
Офіційні опоненти:
доктор медичних наук, професор Гнатейко Олег Зиновійович,
Державна установа “Інститут спадкової патології АМН України”,
директор, м. Львів;
доктор медичних наук, доцент Галаган Віра Олексіївна,
Українська дитяча спеціалізована лікарня “ОХМАТДИТ” МОЗ України, завідувач медико-генетичним центром, м. Київ.
Захист відбудеться “18” лютого 2008 р. о 15.00 годині на засіданні спеціалізованої вченої ради K 64.600.05 в Українському інституті клінічної генетики Харківського державного медичного університету МОЗ України за адресою: 61022, м. Харків, проспект Правди 13.
З дисертацією можна ознайомитись у бібліотеці Харківського державного медичного університету: 61022, м. Харків, проспект Леніна 4
Автореферат розісланий “26” січня 2008 р.
Вчений секретар
спеціалізованої вченої ради, к. мед. н. Л.С. Озерова
Загальна характеристика роботи
Актуальність теми. Спадково обумовлена патологія набуває все більшої питомої ваги серед захворювань людини (Гречаніна О.Я, 2005, Хоффманн Г., 2005, Blau N., 2003, Новіков П.В., 2002). Частота виявлення генетичних захворювань у різних країнах коливається від 82 до 39,7 на 1000 живонароджених (Christianson A., 2006). Навіть при недосконалій системі діагностики в Україні, у 26 з 1000 новонароджених реєструється генетична патологія, а в кожного 7 з 1000 - інвалідність обумовлена генетичними причинами (Моісеєнко Р.О., 2002). Частота окремих нозологічних форм коливається в межах від 0,5 до 1,4% (Богатирьова Р.В., Гречаніна О.Я., 2003). Одночасно із цим відзначається зростання генетичного вантажу в людських популяціях: у 70-і роки обсяг генетичного вантажу з екстраполяцією на весь період життя становив 10,5%; у 2000-му році він збільшився до 74% (Гречаніна О.Я., 2004, Алтухов Ю.П., 2003).
Вивчення вроджених метаболічних захворювань (МЗ) розпочалося з відкриття Гарродом А. алкаптонурії на початку 20-го сторіччя. З того часу була накопичена велика кількість інформації щодо клініки й діагностики МЗ. У 1999 році ВООЗ оголосила генетичні захворювання і МЗ пріоритетним напрямком системи охорони здоров’я майбутнього. Кількість вроджених помилок метаболізму постійно зростає. На початку 21 сторіччя було описано біля 8000 МЗ (Shin Y.S., Podskabi T.,2003). У восьмому виданнi посібника “The Metabolic and Molecular Bases of Inherited Disease” міститься інформація більше ніж про 50000 вроджених помилок метаболізму (Hoffmann J., et al., 2006).
Загальна частота МЗ у європейських популяціях дорівнює 1%. Серед пацієнтів педіатричних клінік МЗ виявляють більше ніж у 5 % (Shin Y.S., Podskabi T.,2003). У період новонародженості проявляється біля 25% МЗ, що не діагностовано й майже всі вони відрізняються тяжкістю стану дитини, нагадуючи нейроінфекції та нейродистрес-синдром (Бєлоусова О.Д, Ніколаєва О.О., 2000). За даними метаболічних центрів Західної Європи різні МЗ виявляють у 0,15-2,5% новонароджених в залежності від рівня діагностики (Stockler-Ipsiroglu S. еt al.,2004, Muntau A., Schulze A.2004, Хоффманн Г, 2005).
Мутації призводять до патохімічних порушень, унаслідок яких формується клінічний і біохімічний фенотип МЗ (Blau N.,1996, 2003, Гречаніна О.Я.,2003, 2004). МЗ проявляються порушеннями з боку різних органів і систем та маніфестують у будь-якому періоді життя, від плода до похилого віку (N.Blau, 2003, Hoffmann G.,2002, Гречаніна О.Я,2007). Більшість МЗ маскуються під зовні легкими формами, але нагадати про себе вони можуть після перенесених травм, інфекцій, операцій, метаболічної кризи, призводячи до важких клінічних наслідків, часто незворотних (Zschocke J., Hoffmann G., 1999, Гречаніна О.Я., 2001, 2004).
У сумі МЗ не є рідкісними, вони стають більш поширеними й усе частіше потребують медичної допомоги, часто впродовж усього життя (N.Blau, M.Duran та ін., 2003). Метаболічна медицина розвинулась із спеціалізованої діяльності лікарів і науковців, спрямованої на науковий пошук та індивідуальний підхід до сім’ї, що включав фахівців різних медичних та “споріднених” спеціальностей (Hoffmann J., et al., 2006). Розробка та впровадження сучасних генетичних технологій є складовою частиною діагностики спадкових захворювань (Гречаніна О.Я, 2002, 2005, Гнатейко О.З., 2002, Бариляк І.Р., 2002, Моісеєнко Р.О, 2002, Кузьмічова Н.О., Калінєнкова С.Г., Новіков П.В., 2002). Науковий і технологічний прогрес та впровадження сучасних досягнень науки в діагностику спадкових помилок метаболізму принесуть велику користь пацієнтам та допоможуть попередити тяжкі ускладнення патології (Hoffmann J.F., Lindner M., Shahbek N., Bariж I., Al Thani G.Hoffmann G.F., 2006).
Спадкові порушення обміну амінокислот (СПО АК) як однієї з ланок патології проміжного обміну, займають провідне місце серед МЗ. Одним з ускладнень СПО АК є затримка розумового розвитку у 20% випадків (Тьоміна П.А., Казанцева Л.З., 2001). Ця обставина змусила вчених розробити новий напрямок у профілактичній медицині – програми масового й селективного скринінгу для виявлення МЗ (Краснопольська К.Д., 1997, 2005, Harvey L., Levy M.D., 2000, Hoffmann G., 2002, 2006). Окремо взяті біохімічні показники не несуть повне інформативне навантаження про наявність тієї або іншої патології, але якщо додати оцінку клінічних ознак, можна розраховувати на визначення кореляції між ними, тобто отримати дані про причетність біохімічних розладів до порушень морфогенезу при МЗ. У більшості випадків тільки поєднана інтерпретація всіх отриманих результатів надасть можливість точно визначити форму захворювання (Краснопольська К.Д. 1997, 2005). ХХ сторіччя було чудовою епохою для вивчення метаболізму й генетики, і ця тенденція підтримується на високому рівні й у нашому сторіччі. Для проникнення в сутність біохімічних порушень необхідно розвивати нові технології, а їх використання вимагає постійного переосмислення одержаної інформації (Hoffmann G., 2005). Визначення патологічних метаболітів у поєднанні з клінічними проявами патології вказує на актуальність запропонованої роботи.
Зв'язок роботи з науковими програмами, планами, темами. Робота виконана відповідно до плану науково-дослідних робіт Харківського державного медичного університету та Харківської медичної академії післядипломної освіти: "Напрямок сучасної діагностики, патогенетичної терапії та трьохрівневої профілактики спадкової патології" № 0106U001640, у рамках міжвідомчої комплексної програми „Здоров’я нації” на 2002-2011 рр., додатку до Національної Програми “Діти України”, затвердженої наказом Президента України №42/2001 від 24.01.2001. У рамках зазначених тем автором проводився аналіз результатів клінічного обстеження дітей з підозрою на спадкові порушення метаболізму, дослідження рівня вільних АК крові методом високоефективної рідинної хроматографії, статистична обробка та аналіз отриманих результатів.
Мета і задачі дослідження. Визначення діагностичної значимості кількісного аналізу вільних амінокислот крові в поєднанні з оцінкою фенотипу у виявленні спадкових порушень обміну в дітей.
Виходячи із загальної мети роботи, були поставлені наступні завдання:
1. Визначити кількісний вміст вільних АК крові у здорових дітей у популяції Харківського регіону.
2. Дослідити рівні вільних АК крові в дітей різного віку з клінічними ознаками МЗ.
3. Провести порівняльну оцінку фенотипу дітей з клінічними ознаками метаболічних порушень та контролю.
4. Провести співставлення біохімічного та клінічного фенотипів дітей з ознаками МЗ.
5. Визначити спектр СПО, які поєднуються з підвищеним рівнем АК крові у дітей з клінічними ознаками МЗ.
Об'єкт дослідження – діти із СПО АК .
Предмет дослідження – рівні вільних АК крові та клінічні маркери СПО АК.
Методи дослідження: біохімічний аналіз АК з використанням високоефективної рідинної хроматографії, клініко-генеалогічний (сомато-генетичне дослідження родини); статистичні методи.
Наукова новизна отриманих результатів. Визначені і кількісно характеризовані рівні вільних АК крові у здорових дітей і дітей з ознаками МЗ у популяції Харківського регіону. Визначено умови проведення аналізу вільних АК крові, включаючи підготовку зразків для дослідження, хроматографічне поділення й аналіз отриманих даних. Вивчено фенотипові особливості в сполученні із вмістом вільних АК крові в дітей з клінічними ознаками МЗ. Визначено спектр СПО АК у дітей, родини яких звернулися за медико-генетичною допомогою до Харківського спеціалізованого медико-генетичного центру (ХСМГЦ). Показано можливість ранньої діагностики СПО АК за умови використання клініко-біохімічного підходу.
Розроблена й впроваджена система клініко-біохімічного підходу в діагностиці СПО АК, що дозволило збільшити кількість верифікованих нозологічних одиниць. На підґрунті комплексної оцінки клінічних і біохімічних показників були виявлені фенотипові особливості в дітей з підвищеним рівнем деяких АК крові: глютамінової кислоти (ГЛУ); гліцину (ГЛІ); аланіну (АЛА); проліну (ПРО). Встановлено особливості фенотипу дітей із СПО АК.
Практичне значення отриманих результатів. Упроваджений кількісний аналіз вільних АК крові з використанням високоефективної рідинної хроматографії (ВЕРХ) в практику медико-генетичного консультування. Урахування результатів дослідження рівнів вільних АК разом з результатами оцінки фенотипу дитини з ознаками МЗ надає можливість підвищити ефективність діагностики МЗ; збільшити кількість верифікованих нозологічних одиниць. Використання рівнів вільних АК крові, що були розраховані на підґрунті кількісного аналізу АК у дітей в популяції Харківського регіону, дозволило підвищити ступінь інформативності отриманих даних. Використання клініко-біохімічного підходу до обстеження дітей групи високого генетичного ризику дозволяє проводити адекватне генетичне консультування на основі лабораторно підтвердженого діагнозу.
Аналіз фенотипу, стану різних органів і систем у поєднанні з кількісним аналізом АК при медико-генетичному консультуванні дозволяє діагностувати не тільки СПО АК, а й підійти до уточнюючої діагностики інших порушень проміжного обміну. Визначення індивідуального вмісту вільних АК надає можливість проводити патогенетичну терапію й контроль за лікуванням.
Результати дослідження використовуються в роботі ХСМГЦ, Криворізького Центру медичної генетики та пренатальної діагностики, відділення дитячої психоневрології та клінічної нейрогенетики інституту неврології, психіатрії та наркології АМНУ; кафедр педіатрії та клінічної генетики, медичної біології, генетики та гістології Буковинського державного медичного університету, Державної установи “Науково-дослідного інституту медико-екологічних проблем” МОЗ України, що підтверджено відповідними актами про впровадження.
За матеріалами дисертації отримано один патент України на винахід (№24837), видано три методичні рекомендації, які використовуються в педагогічному процесі при підготовці лікарів різного фаху.
Особистий внесок здобувача. Дисертантом самостійно складений план дослідження, проведений пошук, збір та аналіз літератури вітчизняних та зарубіжних авторів з питань діагностики спадкових МЗ, проаналізовані існуючі методи досліджень та відібрані найбільш актуальні; проведено дослідження рівнів вільних АК крові в дітей різних вікових категорій з використанням ВЕРХ; проаналізовані результати клініко-генеалогічного обстеження сімей, що мають дітей з ознаками МЗ і знаходяться на обліку в ХСМГЦ. Для оцінки фенотипу дітей з ознаками МЗ і статистичної обробки результатів клінічного обстеження й лабораторного дослідження розроблено карти на базі генетичної, що використовується для медико-генетичного консультування сімей в ХСМГЦ; визначені показання до дослідження рівня вільних АК у дітей з ознаками МЗ. Дисертантом було проведено зіставлення результатів клінічного обстеження й лабораторного дослідження та визначені клінічні ознаки, що поєднуються з підвищеним рівнем деяких АК. Дисертант особисто виконала науковий аналіз отриманих результатів та їх статистичну обробку.
Апробація результатів дисертації. Основні положення й результати дисертації були представлені та обговорені на Міжнародному Форумі “Відродження можливе, якщо…” (Харків, 1998); 2 Конгресі “Плід як частина сім’ї (Харків, 2000); конференції молодих вчених “Медицина третього тисячоліття ” (Харків, 2001), семінарі, присвяченому проблемам дієтотерапії при фенілкетонурії (Київ, 2001), Українсько-Баварському симпозіумі невропатологів (Київ, 2001), 8-му Європейсько-Азіатському об’єднаному Конгресі з метаболічних порушень, (Вільнюс, 2002); 3-му з’їзді медичних генетиків України (Львів, 2002); I та II Українському Конгресі з міжнародною участю “Метаболічні захворювання” (Харків, 2003,2005), міжнародній конференції з медичної генетики “Плід як частина сім’ї” (Харків, 2007); V Європейському Конгресі з неонатального скринінгу ISNS (Рейк’явік, Ісландія, 2007); науково-практичній конференції з міжнародною участю “Актуальні питання медичної генетики” (Київ, 2007); Міжнародному Конгресі з метаболічних захворювань (Гамбург, Німеччина, 2007).
Публікації. За темою дисертації опубліковано 31 наукову працю, з них 12 статей у наукових виданнях, рекомендованих ВАК України, 5 статей написано без співавторів, 1 патент, 18 – тез конгресів, симпозіумів, конференцій.
Структура та обсяг дисертації. Дисертація складається із вступу, огляду літератури, опису методів дослідження, трьох розділів отриманих результатів, заключення, висновків, практичних рекомендацій, списку використаних джерел. Робота викладена на 154 сторінках комп’ютерного друку, ілюстрована 35 таблицями та 18 малюнками. Перелік літературних джерел нараховує 235 джерел: 135 кирилицею, 100 – латиною, що складає 18 сторінок.
Основний зміст роботи
Матеріали та методи дослідження. Для дослідження рівнів вільних АК у дітей, що мешкають у м. Харкові та Харківській області, був безвибірково проведений аналіз вільних АК крові 165 дітей з клінічними ознаками МЗ і 26 дітей, які станом на час обстеження були здоровими.
Для вивчення клінічного й біохімічного фенотипів дітей з ознаками СПО АК проведено обстеження 88 родин – основна група (ОГ). Усі вивчені родини ОГ були поділені на 3 підгрупи. Першу ОГ (1ОГ) склали родини, що мають дітей зі спадковим порушенням обміну АК, N=28 (середній вік - 4,2±0,7 роки); другу ОГ (2 ОГ) - діти із клінічними ознаками МЗ, що супроводжувалась ГААЕ, N=36 (4,3±0,7 роки); третю ОГ (3ОГ) - діти із клінічними ознаками МЗ при відсутності підвищення рівнів вільних АК крові, N=24 (7,7±1,1 років).
Контрольну групу (КГ) склали 20 родин, що мають дітей, які на час обстеження були здоровими (7,4±0,7 років).
Клініко-лабораторне обстеження сімей було проведене на базі ХСМГЦ. Збір інформації проводився лікарями-генетиками ХСМГЦ, відповідно до генетичної карти, прийнятої при медико-генетичному консультуванні. Для клініко-статистичного аналізу результатів обстеження родин на основі генетичної була розроблена карта, що включала 150 ознак. При оцінці фенотипу контролювали наявність патологічних змін і малих аномалій розвитку (МАР). Сума МАР для кожної дитини була представлена як "інтегральний показник", були виділені найбільш інформативні ознаки.
Дослідження рівнів вільних АК крові проводили на амінокислотному аналізаторі (Waters: 486 детектор, 717 аутосамплер, 2 насоси високого тиску Waters 510, хроматографічна колонка із зворотною фазою 3,9х30 см, США). Метод включав доколонну дериватизацію АК з фенілтіоізоціанатом (метод PІCO TAG). Поділення фенілтіокарбамілових похідних АК проводили на аналізаторі з використанням зворотно-фазної ВЕРХ та градієнту концентрацій розчинників (Krugg W.G.1985, Cohen,S.A. et al., 1994). Швидкість потоку розчинників складала 1 мл/хв. Детекцію результатів проводили з використанням абсорбційного детектора при л=254 нм. Кількісний розрахунок рівнів вільних АК проводили на ПЕОМ з використанням програмного забезпечення “Millenium”, США. Відповідні контрольні й стандартні розчини АК включали в кожну серію зразків. Збір зразків крові проводили методом венепункції натщесерце. У дітей першого року життя забір крові проводили через 3-4 години після останнього годування (перед черговим прийняттям їжі).
Статистичний аналіз даних, які отримали, проводили відповідно до інформативних методів розрахунку емпіричних даних, що включав параметричні і непараметричні, а також кореляційний методи аналізу. Вибірки значень, що досліджувались, перевірені на несприятливість результатів спостережень. Результати дослідження підлягали обробці з використанням критеріїв ![]() , Стьюдента, таблиць сукупності ознак. З огляду на те, що ознаки, внесені до карти, були описовими (наприклад, блідість шкірних покривів, м'язова гіпотонія тощо) у роботі застосований ранговий коефіцієнт кореляції Спірмена. Математичну обробку основних показників проводили на ЕОМ БЕСМ-6 обчислювального центру НВО "Хартрон". На підґрунті лінійних комбінацій був використаний дисримінантний аналіз і розраховані класифікаційні коефіцієнти. Ротаційний метод (Варімакс із нормуванням Кайзера) і екстракційний метод (принциповий аналіз компонентів) були використані для зіставлення результатів оцінки фенотипу й дослідження рівня вільних АК крові. Статистичний аналіз з використанням програми SPSS8 був проведений разом з педіатром ХСМГЦ І.Г.Гольдфарбом, пам’яті якого автор низько вклоняється.
, Стьюдента, таблиць сукупності ознак. З огляду на те, що ознаки, внесені до карти, були описовими (наприклад, блідість шкірних покривів, м'язова гіпотонія тощо) у роботі застосований ранговий коефіцієнт кореляції Спірмена. Математичну обробку основних показників проводили на ЕОМ БЕСМ-6 обчислювального центру НВО "Хартрон". На підґрунті лінійних комбінацій був використаний дисримінантний аналіз і розраховані класифікаційні коефіцієнти. Ротаційний метод (Варімакс із нормуванням Кайзера) і екстракційний метод (принциповий аналіз компонентів) були використані для зіставлення результатів оцінки фенотипу й дослідження рівня вільних АК крові. Статистичний аналіз з використанням програми SPSS8 був проведений разом з педіатром ХСМГЦ І.Г.Гольдфарбом, пам’яті якого автор низько вклоняється.
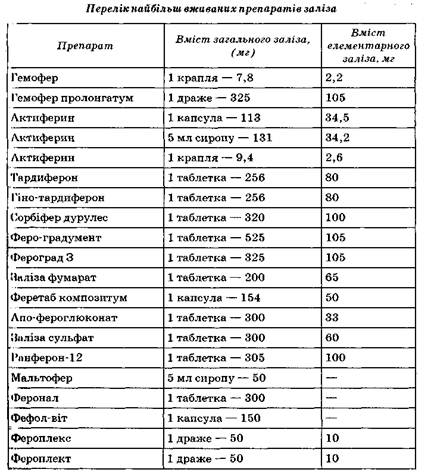
Результати дослідження та їх обговорення. Визначені рівні вільних АК крові дітей з ознаками МЗ і здорових дітей у популяції Харківського регіону (табл.1). На підґрунті результатів дослідження рівнів вільних АК з використанням ВЕРХ було отримано карти розподілу для 34 АК, визначено розбіжності у їх вмісті залежно від віку й виділено 4 вікові категорії. Першу категорію склали діти до 1 місяця життя, середній вік яких становив 0,1±0,01 (4,3 % спостережень); другу категорію - від 1 місяця до 1 року життя, середній вік - 0,44±0,04 (21,6%); третю - від 1 року до 6 років, середній вік - 3,12±0,2 (34,6%); четверту - від 6 до 16 років, середній вік – 10,9±0,4 (28,6%). Вік дітей, які на час обстеження були здоровими, становив старше 6 років, середній вік – 10,2±0,5.
При порівнянні результатів дослідження вільних АК крові здорових дітей і дітей 4 вікової категорії відзначено: зменшення рівня б–аміноадипінової кислоти на 64%, цистіну - на 27,2%; збільшення коефіцієнту співвідношення метіонін/цистін на 69,8%, наявність в-аміноізомасляної кислоти у кількості 7,4±2,6 мкмоль/л (Р<0,05). Ураховуючи, що шлях метаболізму метіоніну через гомоцистін із наступним перетворенням у цистін є піридоксальзалежним, дефіцит піридоксину може бути однією із причин зниження рівня цистіну. З лізину в пероксисомах печінки утворюється піпеколінова кислота, та б–аміноадипінова кислота в присутності вітаміну B6 і б-кетоглутарату. Можна вважати, що зниження рівня б–аміноадипінової кислоти є наслідком недостатнього надходження лізину із їжею або порушення функції пероксисом. Тіамін, що звільнюється при деградації РНК і ДНК, включається в метаболічний шлях утворення в-аміномасляної кислоти. Ці дані свідчать на наявність в-аміно- ізомасляної кислоти в крові дітей з ознаками МЗ можливо, у результаті підвищеної деградації РНК унаслідок порушення епігенетичної регуляції.
Таблиця 1
Рівні вільних АК крові здорових дітей і дітей з ознаками МЗ старше 6 років (М±m, мкмоль/л)
| Амінокислота | Здорові діти, N=26 | Діти з ознаками МЗ N=53 | Критерій t |
| 1 | 2 | 3 | 4 |
| Глутамат | 35,2±4,0 | 37,9±5,6 | 0,39 |
| Аспартат | 6,2±0,98 | 7,5±1,0 | 0,93 |
| б –аміноадипінова кислота | 1,9±0,6 | 0,7±0,2 * | 1,99 |
| Гідроксипролін | 26,9±2,9 | 26,9±2,2 | 0 |
| Аспарагін | 55,4±3,7 | 54,1±3,1 | 0,27 |
| Серин | 109,0±10,0 | 99,7±4,6 | 0,84 |
| Гліцин | 304,0±48,0 | 297,0±30,0 | 0,12 |
| в-аланін | 3,7±0,95 | 3,6±0,9 | 0,08 |
| Таурин | 51,6±5,1 | 49,5±2,9 | 0,36 |
| Гістидин | 55,9±5,6 | 49,6±3,2 | 0,98 |
| Треонін | 78,4±8,7 | 64,4±4,7 | 1,42 |
| Аланін | 285,0±23,0 | 302,9±17,1 | 0,63 |
| Аргінін | 51,3±6,2 | 58,3±3,5 | 0,98 |
| Пролін | 167,0±23,0 | 148,0±12,0 | 0,73 |
| б-аміномасляна кислота | 7,5±0,9 | 5,4±0,8 | 1,77 |
| Тирозин | 48,2±3,0 | 42,4±2,4 | 1,51 |
| Валін | 191,0±12,0 | 185,0±8,1 | 0,41 |
| Метіонін | 16,2±1,4 | 18,2±1,3 | 1,05 |
| Цистін | 35,7±3,6 | 26,0±2,9 * | 2,10 |
| Цистатіонін | 5,6±2,2 | 3,9±1,2 | 0,68 |
| Ізолейцин | 52,1±4,3 | 51,6±3,5 | 0,09 |
| Лейцин | 102,0±7,0 | 96,1±5,0 | 0,69 |
| Гідроксилізин | 3,7±1,2 | 3,4±1,1 | 0,18 |
| Фенілаланін | 42,9±3,8 | 39,8±2,1 | 0,71 |
| Триптофан | 19,5±1,8 | 17,3±1,3 | 0,99 |
| Орнітин | 55,8±5,0 | 51,5±3,0 | 0,74 |
| Лізин | 124,0±8,0 | 116,0±6,0 | 0,8 |
| Фосфосерин | 3,6±1,1 | 5,3±1,5 | 0,25 |
| Цистатіонін 1 | 1,1±0,5 | 2,0±0,5 | 0,13 |
| Цитрулін | 18,1±2,6 | 16,4±1,8 | 0,25 |
| в-аміноізомасляна кислота | 0,0±0,0 | 7,4±2,6 * | 2,85 |
| Метилгістидин | 0,2±0,2 | 0,7±0,4 | 0,07 |
| Глютамін | 341,0±21,0 | 435,0±64,0 | 1,40 |
| Сума незамінних АК | 733,0±42,0 | 698,0±31,0 | 0,67 |
| Сума замінних АК | 1306,0±65,0 | 1080,0±65,0 * | 2,46 |
| Сума білок утворюючих АК | 2039,0±101,0 | 1779,0±88,0 | 1,94 |
| 1 | 2 | 3 | 4 |
| Загальна сума АК | 2316,0±98,0 | 2080±94 | 1,74 |
| Співвідношення незамінні/замінні | 0,6±0,02 | 0,7±0,03 * | 2,36 |
| Незамінні АК,% | 35,9±0,9 | 40,4±1,0 * | 3,34 |
| Замінні АК,% | 64,1±0,9 | 59,6±1,0 * | 3,34 |
| Співвідношення Глу/Про | 0,3±0,07 | 0,3±0,04 | 0,25 |
| Співвідношення Лей/Іле | 2,1±0,1 | 2,1±0,1 | 0 |
| Співвідношення Aла/Aсп | 0,02±0,0 | 0,03±0,0 | 0,001 |
| Співвідношення Фен/Тир | 0,9±0,1 | 1,0±0,05 | 0,02 |
| Співвідношення Mет/Цис | 0,5±0,06 | 0,9±0,1 * | 3,17 |
Примітка:-* різниця статистично значима (P<0,05)
Зважаючи на те, що розрахунок коефіцієнтів співвідношення деяких АК підтверджує існування механізму метаболічних змін (Гречаніна Ю.Б., 2005, Zschocke J., Hoffmann G., 1999, Коломоєць М.Ю., 1994), був проведений порівняльний аналіз коефіцієнтів співвідношення АК, що поєднані загальним “метаболічним шляхом”. Різниці для коефіцієнту фенілаланін/тирозин у дітей старше 6 років не виявлено, але значення більше 1,2 у дітей з клінічними ознаками МЗ виявлено в 21,7% спостережень, що надає можливість диференціювати вторинні порушення обміну (Коломоєць М.Ю., 1994). Коефіцієнт замінні/незамінні АК склав 0,65 у порівнянні із 0,56 у здорових дітей (збільшення на 15,2%), унаслідок порушень метаболізму (Р<0,05). Коефіцієнт метіонін/цистін у дітей 4 вікової категорії склав 0,9 у порівнянні з 0,53 здорових дітей (збільшення на 69,8 %), що вказувало на наявність порушень в обміні сіркоутримуючих АК (Р<0,05).
Установлені рівні вільних АК здорових дітей (сума АК дорівнювала 2316±98 мкмоль/л) і дітей 4 вікової категорії (2080±94 мкмоль/л), свідчать про відсутність статистично значимої різниці сумарного рівня АК. Виявлені статистично значимі розходження відносного числа незамінних АК, коефіцієнтів співвідношення АК, що включені в загальний метаболічний шлях і рівнів індивідуальних АК, підтверджують необхідність дослідження окремих АК при наявності клінічних ознак МЗ.
Сума вільних АК крові дітей першої (3338±422 мкмоль/л) та другої (2995±239мкмоль/л) вікових категорій вірогідно перевищувала загальну кількість вільних АК крові дітей старшого віку (2278±144 мкмоль/л) (Р<0,05). У дітей 2 та 3 вікових категорій відзначене зниження загальної кількості вільних АК крові в порівнянні з рівнем АК дітей 1 категорії на 10,3% і 29,9% відповідно. що підтверджувало більш високу активність метаболізму в дітей раннього віку й погоджувалося з даними літератури (Blau N., 2003, Тіц Н.У., 1997).
Вивчаючи клініко-генеалогічні особливості сімей, що мали дітей з ознаками МЗ, було встановлено, що ранні патологічні ознаки не розцінювались як прояв СПО, а трактувалися стандартно як "перинатальне ураження ЦНС" (23,9%), "затримка психомоторного розвитку" (29,6%), "лікворно-гіпертензійний синдром" (14,8%) тощо. За цими діагнозами можуть "приховуватись" різні МЗ, що потребує дослідження стану метаболізму.
У результаті дослідження основних характеристик родин ОГ у порівнянні з КГ визначена наявність передчасних пологів у 12,5%±3,5 (0,0% у контролі) матерів пробандів (Р<0,05). При аналізі родоводів сімей ОГ у порівнянні з контролем виявлено обтяженість психоневрологічною патологією - 22,7%±4,5 (4,8% у контролі); уроджені аномалії розвитку - 27,3%±4,7 (0,0%) (Р<0,05). Можливо, психічні порушення в родинах пробандів зі СПО можуть бути пов'язані з гетерозиготним носійством і його впливом на психіку.
На підгрунті аналізу історій розвитку відзначено, що у 83,0 % дітей ОГ на першу добу життя ознаки патології були відсутніми, у 78,6% дітей 1ОГ мала місце тенденція до ранньої маніфестації захворювання (у 1-ому півріччі). У дітей 3ОГ переважала маніфестація патології у віці старше 6 років (33,3%±9,63, Р=0,011). При оцінці етапів раннього розвитку у 26,1% дітей ОГ (17,9% у 1ОГ, 38,9% - у 2ОГ, 16,7 % - у 3 ОГ) навички ходіння були відсутніми (Р=0,010), що відбиває істотні порушення з боку нервової системи дитини із СПО й може рекомендуватися при спрямуванні на медико-генетичне консультування.
Проведено оцінку фенотипових особливостей дітей ОГ і КГ. Урахування особливостей шкіри, волосся й нігтів дозволяють звузити коло діагнозів, що передбачаються (Здибська О.П., 1994). Сумарно особливості шкіри виявлені у 96,4% дітей 1ОГ, 91,7% - 2 ОГ, 95,8% - 3ОГ і 75,0 % - КГ (Р<0,05). У дітей ОГ переважно виявлено більше 2 ознак шкіри, в контролі – до 2 МАР (сухість шкіри, телеангіектазії). Аналіз стану підшкірної клітковини виявив зменшення у 36,4% дітей ОГ (28,6% в 1ОГ, 36,1% - 2ОГ, 45,8% - 3 ОГ, 0,0% - КГ). Можна припустити, що зменшення підшкірної клітковини формується при недостатньому надходженні АК унаслідок дефекту переносника АК та порушення процесів кишкового всмоктування. Це припущення підтверджується зниженням суми вільних АК крові в дітей 3ОГ (1560,3±137,9 ммоль/л) на 29,7% у порівнянні із КГ (2215,9±139,8) (Р<0,05). Сумарно зміни з боку м'язів виявлені в 64,8% дітей ОГ (91,4% в 1ОГ, 66,7% в 2 ОГ, 54,2% в 3 ОГ, 5,0%в КГ) (Р<0,05), що погоджується з даними літератури про наявність змін з боку м'язової системи у 25% - 83% дітей з різними формами СПО АК (Hoffmann G., 2002, Вєльтищев Ю.Є., Бочков М.П., 1992). Серед черепно-лицьових дизморфій у дітей ОГ найчастіше зустрічались: виступаюче чоло (44,3%); брахіцефалія (20,5%), виступаюча потилиця (19,3%), сплощена потилиця (17,0%), низька лінія росту волосся (10,2%) (Р<0,05). Прояви тих чи інших черепно-лицьових дизморфій можуть бути пов'язані з різним впливом проміжних метаболітів при МЗ у період внутрішньоутробного розвитку. МАР очей та очного яблука відзначені в 82,1% дітей 1ОГ, 72,2% - 2ОГ, 95,8% -3ОГ, серед них: блакитні склери, епікант, гіпертелоризм; коротка очна щілина; антимонголоїдний розріз очей. В 40% дітей КГ відмічено ознаку “блакитні склери”.
На підґрунті даних оцінки фенотипу ми виявили, що в дітей 1 ОГ переважали: діатези, екзематозні висипання (32,1±8,8%); сухість шкірних покривів (39,3±9,2%); світле волосся (17,9±7,2%); зміни з боку м'язової системи (71,4±8,5%) з перевагою м'язової гіпотонії (35,7±9,1%). Серед "черепно-лицьових дизморфій", які виявлено у 78,6±7,7% дітей, переважали: брахіцефалія (25,0±8,2%), широке обличчя (17,9±7,2%); МАР вушних раковин (78,6±7,7%), переважно деформованих (17,9±7,2%); МАР очей і очного яблука (82,1±7,2%), переважно "блакитні склери" (53,6±9,4%); МАР носа (78,6±7,7%) "увігнута спинка носа" (35,7±9,1%); високе піднебіння (75,0±8,2%). При вивченні МАР шиї, "коротка шия" виявлена в 57,1±9,3% пробандів. Серед МАР грудної клітки переважав "гіпертелоризм сосків" (64,3±9,1%). МАР нижніх кінцівок ми виявили у 85,7±6,6% пробандів, “плоску стопу” - 35,7±9,1%. МАР передньої черевної стінки й тазу виявлені в 67,9±8,8% обстежених у порівнянні з 44,4±8,3% 2ОГ і 29,2±9,3% 3ОГ. При цьому, "широке пупкове кільце" відзначене в 25,0±8,2%, "пупкова кила" - 17,9±7,2%. При аналізі змін з боку нервової системи відзначена максимальна кількість порушень: ЗПМР - 46,4%±9,4 (у порівнянні 19,4%±6,6 в 2ОГ і 8,3%±5,6 - в 3ОГ); судоми - 32,1%±8,8 (у порівнянні з 27,8%±7,5 в 2 ОГ і 4,2%±4,1 - 3 ОГ). Сумарно порушення з боку ЦНС виявлені у 82,1%±7,2 дітей 1ОГ, у 66,7%±7,9 - 2 ОГ і у 41,7%±10,1 - 3 ОГ.
Представлений "фенотиповий портрет" дітей 2 ОГ: зміни з боку м'язової системи (66,7%±7,9) з перевагою м'язової гіпотонії (47,2%±8,3); "черепно-лицьові дизморфії" (75,0%±7,2), переважно "виступаюча потилиця" (25,0%±7,2); сума МАР вушних раковин (72,2%±7,5), переважно низько розташованих (33,3%±7,9) і відстовбурчених (19,4%±6,6); МАР очей та очного яблука (72,2%±7,5), з перевагою "короткої очної щілини" (22,2±6,9%); сума МАР носу (80,6%±6,6), з них "увігнута спинка" (27,8±7,5%); високе піднебіння (75,0%±7,2); сума МАР нижніх кінцівок (72,2%±7,5).
Для спостережень 3 ОГ були характерними: телеангіектазії (66,7%±9,6); тонке волосся (29,2%±9,3); зниження підшкірної клітковини (45,8%±10,2), що сполучалося зі зниженням суми вільних АК крові (1560,3±137,9 мкмоль/л) на 29,7% у порівнянні з КГ (2215,9±139,7 мкмоль/л);. зміни з боку м'язової системи (54,2%±10,2). Сумарно "черепно-лицьові дизморфії" виявлені у 87,5%±6,8 дітей, переважно "виступаюче чоло" (54,2%±10,2); "низька лінія росту волосся" (16,7±7,6%); МАР вушних раковин (70,8%±9,3); МАР очей і очного яблука (95,8±4,1%); сума МАР носа (70,8%±9,3), найбільш часто - "широка спинка носа" (33,3±9,6%); "довгий фільтр" (50,0±10,2%); сума МАР нижніх кінцівок (75,0%±8,8).
На підґрунті аналізу результатів обстеження й отриманих даних патологічні зміни і МАР з боку різних органів і систем були нами підсумовані й представлені як інтегральний показник. У 85% дітей КГ відзначалося до 10 МАР, у 15% - до 15 дизморфій. Інтегральний показник МАР більше 10 виявлений у 96,4%±3,5 спостережень 1 ОГ; 91,7%±4,6 - 2 ОГ; 100% - 3 ОГ. У дітей ОГ зареєстровано більше 30 МАР у 15 (17,0±4,0%) дітей; від 20 до 30 дизморфій - у 32 (36,4±5,1%) пробандів ОГ; від 10 до 20 МАР - у 37 (42,0±5,3%); менше 10 змін - у 4 (4,5±2,2%) випадках. Високий показник аномалій дизембріогенезу (більше 10 МАР) у 95,5% дітей ОГ підтверджує факт впливу патологічних метаболітів на розвиток МАР у період ембріонального розвитку організму. Поєднання високого "інтегрального показника" МАР із збільшенням рівнів вільних АК, дає підстави вважати, що первинний біохімічний продукт починає накопичуватися в організмі хворого, швидше за все, у період ембріогенезу, призводячи до формування різних морфо-генетичних порушень.
Результати сомато-генетичного дослідження були зіставлені з рівнями вільних АК крові дітей ОГ і КГ. Виявлені фенотипові особливості дітей ОГ, що сполучаються з підвищенням рівнів деяких АК. Збільшення глу було виявлене в 40,9±5,2% дітей ОГ і сполучалось з: дизморфічними рисами обличчя й голови (78%); високим піднебінням (67%); МАР грудної клітки (58%); змінами з боку ЦНС (53%); деформацією вушних раковин (64%) у сполученні з аномаліями верхніх кінцівок (52%). ГЛУ характеризується високою метаболічною активністю в головному мозку. Ці дані свідчать на користь нейротоксичної дії високих рівнів ГЛУ. Можна думати, що неврологічні порушення, зміни з боку шкірних покривів, печінки, нирок, імунологічні порушення спостерігаються в пацієнтів з підвищенням рівня ГЛУ з урахуванням експресії генів і тканинної локалізації, ферментів, що беруть участь у метаболізмі глутамата (мозок, печінка, нирки, лімфоцити, лімфобласти, фібробласти) (Зайчик А.Ш., Чурилов Л.П., 2000).
Збільшення рівня ГЛІ було виявлене в 13 (14,8%±3,8) дітей ОГ, у яких відзначені: зміни з боку ЦНС (91%), черепно-лицьові дизморфії (86%), зміни з боку щелепного апарату (83%), МАР нижніх кінцівок (84%), МАР грудної клітки (66%), верхніх кінцівок, піднебіння, деформація вушних раковин, у сполученні зі зміною шкірних покривів (50%). Множинність клінічних проявів при порушенні обміну ГЛІ може бути обумовлена тим, що він є однією з найпоширеніших АК в організмі: відіграє важливу роль у якості нейротрансмітера й донора метильних груп у реакціях біосинтезу; може використовуватися як енергетичне джерело; входить до складу колагену; через біосинтез пуринів включається в утворення РНК або ДНК; бере участь у синтезі глутатіону, жовчних кислот тощо.
При дослідженні рівня АЛА крові дітей ОГ було виявлене підвищення в 9 (10,2%±3,2) пробандів з: малими аномаліями хребта (78%), МАР грудної клітки й піднебіння (по 77% кожне), МАР шкіри і її придатків (70%), лицьовими дизморфіями в сполученні зі змінами з боку м'язів (70%), деформаціями вушних раковин, МАР верхніх і нижніх кінцівок (біля 50%). АЛА відбиває концентрацію пірувату й, побічно, лактату крові. Підвищена концентрація АЛА крові може спостерігатися при деяких порушеннях обміну: уроджених гіперамонієміях; порушеннях метаболізму вуглеводів; порушеннях енергетичного метаболізму в мітохондріях; органічних ацидуріях тощо (Oznand G., 1992, N. Blau, M.Duran, et.al, 2003)
Підвищення рівня ПРО відзначене в 8 (9,1%±3,1) дітей ОГ, що супроводжувалось: МАР хребта (72%), МАР нижніх кінцівок (67%); МАР грудної клітки (64%), зміни волосся (63%); МАР м'язового апарату (63%) у сполученні з дизморфічними рисами обличчя й голови (44%). Про є основним компонентом колагену, широко використовується для білкового синтезу й метаболізується в гідроксипролін - важливий компонент сполучної тканини. Отже, зміна рівня про може відбивати неадекватний синтез сполучної тканини.
Cума білок утворюючих АК крові в дітей 1ОГ (2580,6±329,9 мкмоль/л) у порівнянні із сумою АК дітей КГ (2215,9±139,7 мкмоль/л) була більше на 16,5% (Р<0,05), у 2 ОГ (2376,3±229,4 мкмоль/л) - на 7,2% (Р<0,05) переважно за рахунок незамінних АК; і менше на 29,6% в 3 ОГ (1560,3±137,9 мкмоль/л) (Р<0,05) переважно за рахунок замінних АК. Були виявлені статистично значимі (Р<0,05) зміни рівнів наступних АК крові у дітей 1ОГ у порівнянні із КГ: підвищення рівню ГЛУ на 144,3%; аспартату - на 115,2%; аспарагіну - на 56,8%; ГЛІ - на 63,6%; аргініну - на 391,0%.
У дітей 2 ОГ відзначено підвищення рівнів (Р<0,05) наступних АК: ГЛУ на 196,6%; аспартату - на 183,2%; гідроксипроліну - на 39,4%; аспарагіну - на 34,5%; ГЛІ - на 45,9%; треоніну - на 44,0%; тирозину - на 48,5%; валіну - на 36,6%; метіоніну - на 53,1%; орнітину - на 38,7%; лізину - на 28,5%.
У дітей 3 ОГ у порівнянні із КГ виявлені статистично значимі (Р<0,05) зміни: зменшення рівня ТРП на 26,7% і наявність в-АМК, яка в дітей КГ була відсутня. в-АМК утворюється на шляху катаболізму тиміну при деградації РНК і ДНК. Можна припустити, що наявність в крові в-АМК пов'язана із прискореною загибеллю клітин і деструкцією ДНК.
На підґрунті аналізу результатів клініко-генетичного обстеження й кількісного дослідження рівнів АК крові діагностували аміноацідопатії. У 14 дітей ОГ рівень про крові перевищував верхню межу норми у 2 та більше рази (більше 594 мкмоль/л). Зважаючи на дані клінічного обстеження і лабораторного дослідження, а саме, ізольоване підвищення рівню про, пролінемію було діагностовано у 5 (5,7%±2,5) дітей. Рівень ГЛІ, що перевищував верхній інтервал (більше 880 мкмоль/л), виявлений у 6 дітей. Гліцінемію було діагностовано в 6 (6,8%±2,7) пробандів. Порушення обміну АК з розгалуженим ланцюгом характеризуються підвищенням рівнів валіну (ВАЛ), ізолейцину (ІЛЕ), лейцину (ЛЕЙ). Перевищення верхнього інтервалу нормальних значень ВАЛ було виявлено у 2 дітей (більше 572,4 мкмоль/л); ІЛЕ - у 2 (більше 175,0 мкмоль/л); ЛЕЙ - у 2 (більше 324,4 мкмоль/л), таким чином, порушення обміну АК з розгалуженим ланцюгом було діагностовано у 2 (2,3%±1,6) дітей. Рівень ала більше 922,8 мкмоль/л визначався в 3 осіб, однак ізольована гіпераланінемія була виявлена у 2 дітей (2,3%±1,6). Порушення обміну ароматичних АК - ізольована гіперфенілаланінемія виявлена в 1 (1,14%±1,1) дитини. Рівень фенілаланіну склав 735 мкмоль/л. Підвищення рівня лізину більш ніж в 2 рази (більше 388,0 мкмоль/л) виявлене у 2 дітей, однак лізинемію діагностовано в 1 (1,14%±1,1) дитини. Більш ніж двохкратне підвищення рівня гістидину (більше 187,8 мкмоль/л), виявлене у 1 (1,14%±1,1) пробанда, у якого зміни сполучалися із клінічними ознаками гістидинемії. Порушення обміну інших АК відзначене в 9 (10,3%±3,2) дітей. Недиференційоване підвищення рівнів АК крові відзначалося в 17 (19,3%±4,0) випадках, вторинні аміноацидопатії - у 19 (21,6%±4,2). Органічну ацидемію було діагностовано в 1 (1,14%±0,9) пробанда. Загальна кількість спостережень, серед яких відзначені первинні й вторинні зміни рівнів АК крові були виявлені в 64 (72,7%±4,7) дітей. У 27,3%±4,8 спостережень не було виявлено підвищення рівнів АК, що вказувало на необхідність пошуку СПО іншої етіології. Таким чином, проведений клініко-біохімічній аналіз дозволив визначити спектр СПО АК, що супроводжувався морфо-генетичними порушеннями та поєднувався з підвищеним рівнем АК у 30,7%±4,9 обстежених.
Висновки
1. Визначено показники кількісного вмісту вільних АК крові в здорових дітей у популяції Харківського регіону, що склали: глутамат (35,2±16,6 мкмоль/л, M±S), аспартат (6,2±3,9), аспарагін (55,4±15,1), серин (109±40,6), гліцин (304±68,0); таурин (51,6±21), гістидин (55,9±19), треонін (78,4±35,9), аргінін (51,3±23,6), аланін (285±88,2), пролін (167±65), тирозин (48,2±12,4), валін (191±47,7), метіонін (16,2±5,7) цистин (35,7±14,6), ізолейцин (52,1±17,7), лейцин (102±30,1), фенілаланін (42,9±15,6), триптофан (19,5±7,3), орнітин (55,8±20,5), лізин (124±30,5), гідроксипролін (26,9±12,1), цитрулін (18,1±10,7).
2. Визначено рівні вільних АК крові в дітей старше 6 років з клінічними ознаками МЗ; виявлено зменшення рівнів б–аміноадипінової кислоти на 64,0%, цистину – на 27,2% та наявність в-аміномасляної кислоти (7,4±2,6 мкмоль/л) у порівнянні з рівнями АК крові здорових дітей, які свідчать на користь метаболічних порушень. Сумарна кількість вільних АК крові склала: у новонароджених - 3338±422 мкмоль/л, дітей першого року життя - 2995±239 мкмоль/л, дітей від 1 до 6 років життя - 2278±144 мкмоль/л, що може вказувати на більш високу активність метаболічних процесів у дітей раннього віку.
3. Порівняльна оцінка фенотипу дітей із клінічними ознаками метаболічних порушень виявила зміни з боку шкірних покривів, опорно-рухової системи, черепно-лицьові МАР. З боку нервової системи відзначена максимальна кількість змін, серед яких, ЗПМР та судоми: у дітей із СПО АК - 46,4% та 32,1%, відповідно; у дітей з гіпераміноацидеміями: 19,4% та 27,8%, відповідно; у дітей з відсутністю підвищеного рівня АК, але з клінічними ознаками метаболічних порушень: 8,3% та 4,2%, відповідно, на відміну від контролю. Встановлено, що велика кількість дизморфій (більше 10 МАР) супроводжується підвищеним рівнем вільних АК крові у 95,5% дітей. Це може свідчити про вплив патологічних метаболітів на ембріональний розвиток організму.
4. Оцінка фенотипу дітей із СПО АК встановила наявність: діатезів, екзематозного ураження - 32,1% (в контролі 0,0%); сухості шкіри - 39,3% (20,0%); світлого волосся - 17,9% (5,0%), м’язових порушень - 71,4% (15,0%), черепно-лицьових МАР - 78,6% (5,0%) з перевагою брахіцефалії - 25,0% (5,0%), широкого обличчя - 17,9% (0,0%), деформованих вушних раковин - 17,9% (5,0%), “увігнутої спинки носу” - 35,7% (5,0%), високого піднебіння – 75,0% (5,0%), “короткої шиї” - 57,1% (0,0%), “гіпертелоризму сосків” - 64,3% (5,0%), “плоскої стопи” - 35,7% (10,0%), “пупкової кили”- 17,9% (0,0%), що поєднуються із порушеннями з боку нервової (82,2%), травної (39,3%) і сечовидільної (57,1%) систем, які були відсутніми у контролі, потребують дослідження рівня вільних амінокислот з використанням апаратних методів.
5. Аналіз співставлення клінічного та біохімічного фенотипів дітей з ознаками МЗ виявив морфогенетичні особливості, що поєднуються з підвищенням рівнів індивідуальних АК крові: ГЛУ - з дизморфічними рисами обличчя і голови; високим піднебінням; МАР грудної клітки; змінами з боку ЦНС; деформацією вушних раковин у сполученні з аномаліями верхніх кінцівок; ГЛІ - із змінами з боку ЦНС, щелепного апарату, черепно-лицьовими дизморфіями, МАР верхніх та нижніх кінцівок, МАР грудної клітки, піднебіння, деформацією вушних раковин у сполученні зі зміною шкірних покривів; ПРО – з МАР хребта, грудної клітки, нижніх кінцівок та м'язового апарату; змінами волосся у сполученні з дизморфічними рисами обличчя і голови; АЛА - з МАР хребта, грудної клітки й, шкіри та її придатків, верхніх і нижніх кінцівок, лиця, вушних раковин і піднебіння у сполученні зі змінами м'язів.
6. Визначено спектр СПО (30,7%), що поєднуються з підвищеним рівнем АК крові, серед яких: пролінемія (5,7%), гліцінемія, (6,8%), гіпераланінемія (2,3%), гіперфенілаланінемія (1,1%), лізинемія (1,1%), гістидинемія (1,1%), порушення обміну АК з розгалуженим ланцюгом (2,3%) та інших АК (10,3%). Недиференційовані ГААЕ виявлені у 19,3% обстежених; вторинні аміноацідопатії - у 21,6%; органічні ацидемії - 1,14%.
Практичні рекомендації
1. У діагностиці СПО АК рекомендований системний генетичний підхід до обстеження пробанду та його сім’ї з урахуванням оцінки фенотипу і дослідження кількісного рівню вільних АК.
2. Наявність у дитини більше 10 мікроаномалій вказує на необхідність дослідження стану метаболізму.
3. При проведенні медико-генетичного консультування дітей з клінічними ознаками МЗ наявність у фенотипі аномалій дизембріогенезу (черепно-лицьові МАР з перевагою брахіцефалії, широкого обличчя, деформованих вушних раковин, “увігнутої спинки носу”, високого піднебіння, “короткої шиї”, “гіпертелоризму сосків”, “плоскої стопи”, “широкого пупкового кільця” “пупкової кили”), що поєднуються із діатезами, екзематозним ураженням, сухістю шкіри; світлим волосся, м’язовою гіпотонію, порушеннями з боку нервової (ЗПМР, судоми) травної і сечовидільної систем потребують дослідження рівня вільних амінокислот.
4. Наявність у дитини дизморфічних рис обличчя і голови; високого піднебіння; МАР грудної клітки; змін з боку ЦНС; деформації вушних раковин у сполученні з аномаліями верхніх кінцівок може поєднуватися з підвищеним рівнем ГЛУ; для підвищеного рівня ГЛІ є характерними зміни з боку ЦНС, щелепного апарату, черепно-лицьової дизморфії, МАР верхніх та нижніх кінцівок, МАР грудної клітки, піднебіння, деформація вушних раковин у сполученні зі зміною шкірних покривів; підвищення рівню ПРО поєднується з МАР хребта, грудної клітки, нижніх кінцівок та м'язового апарату; змінами волосся у сполученні з дизморфічними рисами обличчя і голови; АЛА - з МАР хребта, грудної клітки й, шкіри та її придатків, верхніх і нижніх кінцівок, лиця, вушних раковин і піднебіння у сполученні зі змінами м'язів. Наявність комплексу мікроаномалій можна вважати маркерними ознаками підвищеного рівня вказаних АК.
Список праць, опублікованих за темою дисертації
1. Новикова И.В. Наследственные болезни обмена амінокислот // Проблемы современной генетики. - Под ред. Е.Я.Гречаниной. – Харьков: КВАДРАТ. - 2003. – С. 361-419.
2. Гречаніна О.Я., Здибська О.П., Новікова І.В., Москалець Н.О. Фенілкетонурія. Клініка, діагностика, лікування //Проблемы современной генетики. - Под ред. Е.Я.Гречаниной. – Харьков: КВАДРАТ. - 2003.– С.113-171.
3. Новикова И.В., Песочина Э.А., Тикоцкая А.Г. Итоги 10 лет массового скрининга новорожденных на фенилкетонурию//Ультразвуковая перинатальная диагностика. - 1997. - № 8-9. - С. 197-208.
4. Новикова И.В. Высокоэффективная жидкостная хроматография в диагностике наследственных болезней аминокислотного обмена: Зб. наукових праць співробітників КМАПО ім. П.Л. Шупика .- Київ.- Вип.8, кн.2.- 1999. - С.151-159.
5. Новікова І.В. Вільні амінокислоти біологічних рідин у дітей з передбачуваним порушенням метаболізму в залежності від віку // Ультразвукова перинатальна діагностика. - Харків. - 1999. - №11. - С. 50-55.
6. Новикова И.В. Содержание свободных аминокислот в сыворотке крови // Ультразвукова перинатальна діагностика. - Харків. - 2000. - №.13 - С.54-58.
7. Новикова И.В. Нарушения обмена аминокислот. Обзор литературы // Ультразвукова перинатальна діагностика. - Харків. - 2001. - №.14 - С.84-95.
8. Новикова И.В., Булавина А.А., Чудная И.В., Москалец Н.А. Диагностика наследственных болезней обмена //Ультразвукова перинатальна діагностика. – Харків, 2001. - №.14 - С.119-124.
9. Гречанина Е.Я., Добродецкая А.Л., Степанец А.П., Новикова И.В., Здыбская Е.П., Гречанина Ю.Б., Гольдфарб И.Г., Гречанин Б.Е., Варенко В.А. Наследственные нарушения метаболизма //Ультразвукова перинатальна діагностика. – Харків, 2003. - №.16 - С. 3-41.
10. Гречаніна О.Я., Новікова І.В., Здибська О.П., Гольдфарб І.Г., Гречаніна Ю.Б. Порушення обміну амінокислот. Проблеми діагностики: Зб. наукових праць співробітників КМАПО ім.П.Л.Шупика. - Київ.- Вип.13, кн.5. - 2004. - С.270-277.
11. Гречаніна О.Я., Здибська О.П., Гречаніна Ю.Б., Гольдфарб І.Г., Новікова І.В. Діагностика органічних ацідурій у дітей: Зб. наукових праць співробітників КМАПО ім. П.Л. Шупика. - Київ.- Вип.13, кн.5. - 2004. - С.262-269.
12. Гречанина Е.Я., Маталон Р., Акопян Г.Р., Холмс Б., Жукс С., Реди П.Л., Новикова И.В., Гречанина Ю.Б., Тайринг С., Мясоедов В.В., Гусар В.А., Моисеенко Р.А. Неиспользованные возможности пренатальной эхографии: дефекты закрытия невральной трубки как маркер эпигенетических нарушений // Ультразвукова перинатальна діагностика. – Харків, 2006. - №.22 - С.26 – 51.
13. Пат. № 24837 Україна Спосіб діагностики спадкової тромбофілії, що обумовлена порушенням перетворення метіоніну на цистин //Гречанина О.Я., Гречанина Ю.Б., Бугайова О.В., Новікова І.В., Васильєва О.В., Полуботко Т.О., Прасол В.О, Васильєва О.В. (Україна) Опубл. 10.07.07, Бюл. № 10
14. Гречанина Е.Я., Прасол В.А, Троян В.И, Васильєв Д.В., Бугаева Е.В., Молодан Л.В., Новикова И.В. Случай синдрома Элерса-Данлоса, сопровождающийся распространенной венозной мальформацией // Ультразвукова перинатальна діагностика. – Харків, 2006. - №.21 - С.23 – 25.
15. Гречанина Е.Я., Новикова И.В. Клинико-биохимические особенности детей с нарушением обмена амінокислот //Актуальні питання медичної генетики: матеріали науково-практичної конференції з міжнародною участю КМАПО ім.. П.Л. Шупика. – Київ, - 2007. - С.42-45.
16. Гречанина Е.Я., Сасс Д.О., Здыбская Е.П, Новикова И.В., Федосеева Н.П. Случай метилмалоновой ацидурии у мальчика 4-х лет//Актуальні питання медичної генетики: матеріали науково-практичної конференції з міжнародною участю КМАПО ім. П. Л. Щупика. – Київ. - 2007. - С.46-48.
17. Гречанина Е.Я., Песочина Э.А., Новикова И.В. Случай гомоцистинурии III типа у ребенка 6 лет // Плід як частина родини. Додаток до журналу “Ультразвукова перинатальна діагностика”. - Харків. - 2000. –Том 1.- С.35-37.
18. Булавина А.А., Москалец Н.А., Новикова И.В. Программы уточняющей диагностики наследственных аминоацидопатий // Плід як частина родини. Додаток до журналу “Ультразвукова перинатальна діагностика” - Харків.- 2000. –Том 2.- С.331-332.
19. Гречанина Е.Я., Песочина Э.А., Ткачева Т.М., Христич А.В., Новикова И.В. Возможности диагностики наследственных синдромов в раннем неонатальном периоде с помощью классических методов и новых технологий // Плід як частина родини. Додаток до журналу “Ультразвукова перинатальна діагностика”.- Харків. - 2000. – Том 2.- С.346-347.
20. Новикова И.В., Здыбская Е.П., Молодан Л.В. Исследование свободных аминокислот биологических жидкостей // Плід як частина родини. Додаток до журналу “Ультразвукова перинатальна діагностика”.- Харків. - 2000. – Том 2.- С.369-370.
21. Федосеева Н.П., Новикова И.В. Клинический полиморфизм и генетическая гетерогенность перинатальной энцефалопатии у детей с болезнями обмена веществ // Плід як частина родини. Додаток до журналу “Ультразвукова перинатальна діагностика”.- Харків. - 2000. –Том 2.- С.378-380.
22. Гречаніна О.Я., Новікова І.В., Гречаніна Ю.Б. Роль аналізу вільних амінокислот в діагностиці метаболічних порушень при спадково обумовлених неврологічних захворюваннях //Соціальна педіатрія: Матеріали V міжнародного Українсько-Баварського симпозіуму. - Вип. I. - Київ, 2001. -С.74-79.
23. Гречаніна О.Я., Москалець Н.О., Новікова І.В., Федосєєва Н.П. Оздоровче харчування для дітей, хворих га фенілкетонурію // Педіатрія, акушерство та гінекологія.– 2001. - №2.– С.63-64.
24. Новікова І.В., Чудна І.В. Діагностика спадкових аміноацідопатій // Медицина третього тисячоріччя: Матеріали конференції молодих вчених Харківського державного медичного університету. – Харків. - 2001. – С.30.
25. Новікова І.В., Ткачова Т.М., Христич А.В., Чудна І.В., Гречаніна Ю.Б. Характер обмінних порушень при структурних хромосомних абераціях// Медицина третього тисячоріччя: Матеріали конференції молодих вчених Харківського державного медичного університету. Харків. - 2001. – С. 29.
26. Новікова І.В, Гречаніна О.Я. Порушення обміну амінокислот у дітей та дорослих // III з‘їзд медичних генетиків України: Матеріали з‘їзду. – Львів. - 2002. – С.23.
27. Grechanina O.Ya., Novikova I.V., Moskalets N.O., Grechanina Ju.B., Gusar V.A. Detection of inherited metabolic disorders in the region of Kharkiv/Ukraine //Laboratorine Medicina: 8th Annual Asian-Europ. Workshop on Inborn Errors of Metabolism – Vilnius, Lithuania, 2002. – Р.60.
28. Озерова Л.С., Здыбская Е.П., Гречанина Ю.Б., Федосєєва Н.П., Новикова И.В. Случай интермиттирующей формы лейциноза // Ультразвукова перинатальна діагностика. – Харків. - 2006. - №.21 - С.37– 38.
29. Grechanina E., Novikova I., Fedoseeva N., Gusar V. PKU screening in Kharkiv, Poltava, Chernigiv and Sumy regions of Ukraine // The 5th European ISNS Congress in Newborn Screening. – Reykjavik, 2007. – P.49.
30. Grechanina E., Matalon R., Novikova I.,. Fedoseeva N., Zdybskaya E., Grechanina Ju. The experience with Large Neutral Amino Acids in Ukraine // Journal of Inherited Metabolic Disease. – Vol.30. – Hamburg, 2007. - P.13.
31. Grechanina E., Matalon R., Brandon B., Holmes Е., Novikova I., Grechanina Ju., Gusar V. Genetic Polymorphisms of Methylenetetrahydrofolate Reductase (MTHFR), Methionine Synthase Reductase (MTRR), and Reduced Folate Carrier-1 (RFC-1) in a High Neural Tube Defect Risk Population // Journal of Inherited Metabolic Disease. – Vol.30. – Hamburg, 2007. - P.30.
Анотація
Новікова І.В. Вільні амінокислоти крові в діагностиці спадкових хвороб обміну в дітей високого генетичного ризику. – Рукопис
Дисертація на здобуття наукового ступеня кандидата медичних наук за спеціальністю 03.00.15 - генетика. - Український інститут клінічної генетики Харківського державного медичного університету, Харків, 2007.
Дисертація присвячена дослідженню особливостей сімей, що мають дітей з ознаками МЗ. Вивчені фенотипові ознаки дітей з порушенням обміну АК, досліджені рівні вільних АК крові здорових дітей і дітей з клінічними ознаками МЗ в популяції Харківського регіону. Доведено, що зміни в кількісному вмісті вільних АК крові поєднуються з високим рівнем дизморфій (більше 10) у 95,5% дітей. Установлені морфогенетичні особливості дітей, що сполучаються з підвищенням рівня окремих АК крові. Визначено спектр СПО (30,7%), що поєднуються з підвищеним рівнем АК крові, серед яких: пролінемія, гліцінемія, гіпераланінемія, гіперфенілаланінемія, лізинемія, гістидинемія, порушення обміну АК з розгалуженим ланцюгом. Недиференційовані ГААЕ виявлені у 19,3% обстежених; вторинні аміноацідопатії - у 21,6%.
Ключові слова: спадкові порушення обміну, амінокислоти, спадкові метаболічні захворювання, дизморфії, фенотип, біохімічне дослідження, високоефективна рідинна хроматографія.
Аннотация
Новикова И.В. Свободные аминокислоты крови в диагностике наследственных болезней обмена у детей высокого генетического риска. - Рукопись
Диссертация на соискание ученой степени кандидата медицинских наук по специальности 03.00.15 - генетика. - Украинский институт клинической генетики Харьковского государственного медицинского университета, Харьков, 2007.
Диссертация посвящена исследованию особенностей семей, которые имеют детей с клиническими признаками наследственных нарушений обмена аминокислот (АК).
Проведено исследование клинических, клинико-генеалогических и биохимических (исследование уровней свободных АК крови с использованием высокоэффективной жидкостной хроматографии) характеристик пробандов с признаками наследственных метаболических заболеваний (МЗ). Изученные фенотипические признаки детей, направленных на медико-генетическое консультирование с подозрением на нарушения обмена АК.
Исследованы уровни свободных АК крови здоровых детей и детей с клиническими признаками МЗ разных возрастных категорий. Исследованы образцы крови детей популяции Харьковского региона. Установлено, что клинические проявления патологии, которые сочетаются с повышением уровней свободных АК крови, у 78,6% детей манифестировали в 1-ом полугодии жизни. Доказано, что изменения в количественном содержимом свободных АК крови сочетаются с высоким уровнем дизморфий (больше 10) у 95,5% детей. Высказано предположение о влиянии патологических метаболитов (аминокислот и их производных) на развитие микроаномалий. Установлены морфогенетические особенности детей, которые сочетаются с повышением уровня глицина, глютаминовой кислоты, аланина и пролина крови.
Среди детей с признаками МЗ выявлен спектр НБО (30,7%), которые сочетаются с повышенным уровнем АК крови, среди которых: пролинемия, глицинемия, гипераланинемия, гиперфенилаланинемия, лизинемия, гистидинемия, нарушения обмена АК с разветвленной цепью. Недифференцированные гипераминоацидемии выявлены у 19,3% обследованных; вторичные аминоацидопатии - у 21,6%.
При проведении медико-генетического консультирования детей с клиническими признаками МЗ наличие в фенотипе аномалий дизэмбриогенеза (черепно-лицевые МАР с преобладанием брахицефалии, широкого лица, деформированных ушных раковин, “вогнутой спинки носа”, высокого неба, “короткой шеи”, “гипертелоризма сосков”, “плоской стопы”, “широкого пупочного кольца”), которые сопровождаются диатезами, экзематозными поражениями, сухостью кожи, мышечной гипотонией, нарушениями со стороны нервной (ЗПМР, судороги) пищеварительной и мочевыделительной систем являются показаниями к оценке состояния метаболизма.
Ключевые слова: наследственные нарушения обмена, аминокислоты, наследственные метаболические заболевания, дизморфии, фенотип, биохимическое исследование, высокоэффективная жидкостная хроматография.
Summary
Novikova I.V. Blood’s free amino acids in the diagnostics of the inherited metabolic diseases in children of high genetic risk. – Manuscript.
Candidate Dissertation on the scientific degree competition in medical sciences on speciality 03.00.15 –genetics – The Ukrainian Institute of Clinical Genetics of the Kharkiv State Medical University, Kharkiv, 2007.
The thesis is devoted to research of phenotype pictures of patients with clinical indications of the amino acid’s (AA) metabolic diseases in combination with quantitative blood’s free AA’s analysis.
There were investigated clinical, genealogical and biochemical (blood’s free AА’s levels with using HPLC) patient’s attributes with the signs of inherited metabolic diseases. The author is made phenotype signs of children, which were directed on the medical-genetic advising and had attributes of AA’s metabolic diseases. There were detected levels of the blood’s free AA of the children in different age categories for Kharkiv subpopulation.
The clinical signs of the pathologies with combination of increasing of the blood’s free AA’s level are manifested at the 1 half-year of life for 78,6% children. It is proved that increasing blood’s free AA level go with high level of dysmorphias (more than 10) in 95,5% children. We supposed that pathological metabolites influence on dismorphy formation. There were detected morphogenetic children’s features which were combined with increasing levels of some blood’s AA.
There were exposed: inherited AA diseases (30,7%), undifferential hyperaminoacidaemias (19,3%); secondary aminoaminoacidopathias (21,6%); on the base of the clinical inspection and laboratory research. The calculation of some AA’s coefficients was conducted.
The keywords: inherited metabolic diseases, free amino acid, dysmorphia, phenotype, biochemical research, high performance liquid chromatography.
Похожие работы
... з достатньою кількістю білка, усунення дисбактеріозу кишечнику, замісна ферментна терапія, полівітаміни, у тяжких випадках внутрішньовенно вводять плазму, альбумін. 2. Хронічні розлади харчування в дітей раннього віку 2.1 Витримка внутрішньоутробного розвитку Затримку внутрішньоутробного розвитку діагностують у дітей, які іій момент народження мають недостатню масу тіла або недостатні ...
... актуальним. Також діти з розумовою неповносправністю потребують спілкування в колі ровесників, вчителів, батьків та друзів. Діти з особливими потребами становлять об’єкт соціальної роботи з надзвичайно складною структурою. 1.2 Особливості релігійного виховання підлітків з особливими потребами в сім’ї Людина є сотворена Богом, її покликання – відкрити своє синівство та усім серцем і душею ...


0 комментариев