Навигация
Строение атомов и их ядер
Содержание
Введение. 2
1. Ядерные реакции. 3
2. Радиоактивность. 3
3. Деление ядер. 6
4. Стpоение многоэлектpонных атомов. Пеpиодический закон Менделеева. 9
Заключение. 15
Список литературы.. 16
Введение
Как известно, все в мире состоит из молекул, которые представляют собой сложные комплексы взаимодействующих атомов. Молекулы - это наименьшие частицы вещества, сохраняющие его свойства. В состав молекул входят атомы различных химических элементов.
Химические элементы состоят из атомов одного типа. Атом, мельчайшая частица химического элемента, состоит из "тяжелого" ядра и вращающихся вокруг электронов.
Ядра атомов образованы совокупностью положительно заряженных протонов и нейтральных нейтронов. Эти частицы, называемые нуклонами, удерживаются в ядрах короткодействующими силами притяжения, возникающими за счет обменов мезонами, частицами меньшей массы.
Ядро элемента X обозначают как ![]() или X-A, например уран U-235 -
или X-A, например уран U-235 - ![]() ,
,
где Z - заряд ядра, равный числу протонов, определяющий атомный номер ядра, A - массовое число ядра, равное суммарному числу протонов и нейтронов.
Ядра элементов с одинаковым числом протонов, но разным числом нейтронов называются изотопами (например, уран имеет два изотопа U-235 и U-238); ядра при N=const, z=var - изобарами[1].
Цель работы – рассмотреть строение атомов и их ядер.
Задачи работы – изучить ядерные реакции; охарактеризовать сущность реактивности; проанализировать особенности деления ядер; обозначить стpоение многоэлектpонных атомов.
1. Ядерные реакции
Ядра водорода, протоны, а также нейтроны, электроны (бета-частицы) и одиночные ядра гелия (называемые альфа-частицами), могут существовать автономно вне ядерных структур. Такие ядра или иначе элементарные частицы, двигаясь в пространстве и приближаясь к ядрам на расстояния порядка поперечных размеров ядер, могут взаимодействовать с ядрами, как говорят участвовать в реакции. При этом частицы могут захватываться ядрами, либо после столкновения - менять направление движения, отдавать ядру часть кинетической энергии. Такие акты взаимодействия называются ядерными реакциями. Реакция без проникновения внуть ядра называется упругим рассеянием.
После захвата частицы составное ядро находится в возбужденном состоянии. "Освободиться" от возбуждения ядро может несколькими способами - испустить какую-либо другую частицу и гамма-квант, либо разделиться на две неравные части. Соответственно конечным результатам различают реакции - захвата, неупругого рассеяния, деления, ядерного превращения с испусканием протона или альфа-частицы.
Дополнительная энергия, освобождаемая при ядерных превращениях, часто имеет вид потоков гамма-квантов.
Вероятность реакции характеризуется величиной "поперечного сечения" реакции данного типа ![]() [2]
[2]
2. Радиоактивность
Радиоактивность вошла в сознание человечества всего лишь примерно 100 лет тому назад. Лишь в 1986 году А. Бекерель обнаружил некие х-лучи, засвечивавшие фотопластинки.
Затем было установлено, что радиоактивность - это свойство испускать потоки заряженных aльфа, бета и нейтральных гамма частиц. Усилиями многих ученых было обнаружено,что aльфа-частицы представляют собой ядра гелия, бета-частицы - электроны, а гамма-частицы - поток квантов света. Было установлено, что многие вещества являются естественными излучателями частиц, из которых некоторые, как например радий, оказались очень интенсивными источниками радиации.
Различные комбинации нуклонов в ядрах управляются законами ядерных взаимодействий, взаимное положение и движения внутри ядер определяется действием короткодействующих ядерных сил. Известно,что существует некоторая зависимость между числом протонов и нейтронов в ядрах, в рамках которой реализуется стабильность ядер. Эта зависимость для устойчивых ядер имеет вид:
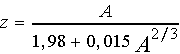
Из этой формулы следует,что при малых массовых числах 1<A<10 число протонов, определяемое атомным номером - числом z, примерно равно числу нейтронов, а при больших массовых числах A>>10 число протонов растет как корень кубический из числа А. Отклонение от этой "линии устойчивости ядер ", избыток числа нуклонов приводит к тому, что ядра атомов претерпевают радиоактивные превращения стремясь уменьшить степень отклонения и перейти к более стабильной конфигурации нуклонов.
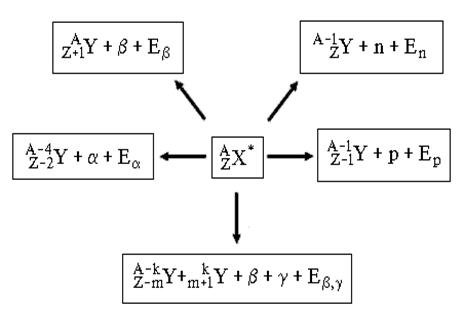
Различные виды радиоактивных превращений можно описать:
![]()
 ,
,
где X* - составное ядро,
A=A1+A2, Z=Z1+Z2,
E - выделенная энергия.
Дочерние продукты радиоактивных процессов могут также претерпевать распад - так возникают цепочки радиоактивных превращений. Важной разновидностью радиоактивных превращений является т.н. спонтанное деление тяжелых ядер, открытое Флеровым и Петржаком в 1942 году. Радиоактивный распад это процесс статистический, т.е. управляемый вероятностными законамиi. Однако, в среднем, за времена большие времен характерных внутренних процессов - это вполне детерминированное явление. Так, можно записать уравнение радиоактивного распада, имеющее вид
![]() или
или ![]()
где Аi- число ядер изотопа Аi в единице обьема, ![]() - константа радиоактивного распада изотопа Аi.
- константа радиоактивного распада изотопа Аi.
Величина ![]() определяет другую, часто используемую характеристику радиоактивного распада изотопов - период полураспада T1/2:
определяет другую, часто используемую характеристику радиоактивного распада изотопов - период полураспада T1/2:
![]()
время в течение которого количество вещества за счет радиоактивного распада уменьшается в два раза.
Интенсивность радиоактивного распада измеряется в единицах, называемых "беккерель" (1 Бк = 1 распад / 1 сек). Важная единица интенсивного радиоактивного распада - кюри (1 кюри = 3,7*1010 Бк = 37 ГБк)[3].
Похожие работы
... : 1,60*10 Кл. Подставив это значение в найденное Томсоном отношение заряда электрона к его массе, можно было вычислить массу электрона: 1,60*10 Кл/1,76*10 Кл/г = 9,11*10 г. 4. Ядерная модель строения атома Изучение строения атома практически началось в 1897-1898 гг., после того как была окончательно установлена природа катодных лучей как потока электронов и были определены величина заряда и ...
... их в таблице. В связи с открытием закона Мозле современная формулировка периодического закона следующая: свойство элементов, а так же формы и свойства их соединений находятся в периодической зависимости от заряда ядра их атомов. Связь периодического закона и периодической системы со строением атомов. Итак, главной характеристикой атома является не атомная масса, а величина ...
... массой, большей урана. В наши дни такие «трансурановые» элементы были получены искусственно. Вполне можно утверждать, что предела таблицы не существует и получение или нахождение других трансурановых элементов – это дело будущего. Таково, в общих чертах, учение об атомах химических элементов, созданное Дальтоном и определившее все дальнейшее развитие химии в XIX столетии. , с помощью ...
... ; ↓↑ ↓↑ Количество неспаренных электронов на внешнем уровне определяет валентность элемента, т.е. способность образовывать химические связи с другими атомами. В большинстве случаев, но не всегда. 5 4 4 3 3 2 2 1 1 Периодический закон (1869 г): свойства простых тел, а также свойства ...

0 комментариев