Навигация
1. Преципитация
| Реагенты | Опытные пробы, (мл.) | Калибровочные пробы, (мл.) | Контрольные пробы, (мл.) |
| Сыворотка или плазма | 0,15 | _ | _ |
| H2O | _ | _ | 0,15 |
| Осаждающий реагент | 0,3 | 0,3 | 0,3 |
| Раствор холестерина | _ | 0,15 | _ |
Хорошо перемешать и оставить на 10 мин при комнатной температуре. Опытные пробы отцентрифугировать в течение 10 мин при 4000g или 1-2 мин 1000g. Прозрачный супернатант использовать для определения концентрации HDL. Калибровочные и контрольные пробы центрифугировать не нужно. Определение холестерина во всех пробах в течение часа.
2. Определение концентрации HDL
| Реагенты | Опытные пробы, (мл.) | Калибровочные пробы, (мл.) | Контрольные пробы, (мл.) |
| Супернатант | 0,2 | _ | - |
| H2O+ реагент №1 | _ | _ | 0,2 |
| Рабочий реагент для определ. холестерина | 0,2 | 0,2 | 0,2 |
| Раствор холестерина+реагент №1 | _ | 0,2 | _ |
Реакционную смесь тщательно перемешивают и инкубируют не менее 10 мин при комнатной температуре (20-25°С) или 5 мин при 37°С и измеряют оптическую плотность опытных и калибровочных проб против контрольной пробы в кювете с толщиной поглощающего слоя 5 см (1 см.) при длине волны 500 нм (ФЭК- 490 нм). Окраска стабильна не менее 2-х часов после окончания инкубации при предохранении от прямого солнечного света.
Расчет концентрации (С) холестерина HDL проводят по формуле:
С = Ео/Ест * 1,29 (ммоль/л) или С = Ео/Ест * 50 (мг/100 мл) Ео и Ест – экстинция образца и стандарта, измеряется относительно контрольной пробы.
2.3.6. Определение ХС-ЛОНП (холестерина-липопротеидов очень низкой плотности) расчетным методомУровень ХС-ЛОНП находят путем деления показателя концентрации триацилглицеринов на 2,2 (ТГ/2,2). Вывод этой формулы расчетов базируется на том, что, во-первых, при отсутствии в крови хиломикронов (а они после 12-часового голодания у большинства пациентов не выявляются) практически все количество ТГ крови сосредоточено в ЛОНП и ,во-вторых, при не слишком высокой концентрации в крови (когда содержание ТГ не привышает 4,4 ммоль/л) в частицах ЛОНП на 22 молекулы ТГ приходится 10 молекул холестерола [12].
2.3.7. Определение ХС-ЛНП (холестерина липопротеидов низкой плотности) расчетным методом
Зная уровень ХСобщ плазмы, ХС-ЛВП и ХС-ЛОНП, нетрудно определить содержание ХС-ЛНП по формуле [12]:
ХС-ЛНП = ХС - (ХС-ЛВП + ХС-ЛОНП)
2.3.8. Определение индекса атерогенности (ИА) расчетным методомРасчет индекса атерогенности призводят по формуле:
ХСпл – £-ХС /£-ХС Х (ЭХС/СХС)
ХСпл – общий холестерол плазмы
£-ХС (альфа-ХС) – холестерол супернатанта (ЛПВП)
ЭХС/СХС – отношение содержания эфиросвязанного и свободного холестерола супернатанта плазмы [12] .
2.3.9. Определение содержания диеновых коньюгатов(ДК) в эритроцитах
За основу взят классический метод Placer в модификации Гаврилова В. Б. [9] для эритроцитов. 0,5 мл гемолизата эритроцитов (1:1) смешивают в пробирках с притертой крышкой с 4 мл чистоперегнанных растворов изопропанол : гептан (1:1). Смесь встряхивают постоянно не менее одного часа затем добавляют 1 мл HCl (pH=2) после чего еще раз встряхивают две минуты, добавляют 2 мл чисто перегнанного гептана и снова встряхивают 10-15 мин. Примерно через 1-2 часа отбирают верхнюю фазу и фотометрируют при 232нм против контрольной пробы (Афон) где вместо гемолизата взято 0,5 мл H2O. Коэффициент экстинции при 233 нм –
2,2 * 10 -5 см-1 М-1. Формула для расчета: С(нмоль/мл эр)= (Аоп - Афон) * 36,4
2.3.10. Определение содержания ДК в плазме крови и гомогенате печениЗа основу взят классический метод Гаврилова В.Б. и соавт [9], Владимирова Ю.А. и соавт. [7]. 0,4 мл плазмы вносят в пробирку с плотной крышкой и добавляют 4 мл чисто перегнанной смеси изопропанол : гептан (1:1). Смесь встряхивают в течение 20-30 мин затем добавляют 1 мл HCl (pH=2) после чего еще раз встряхивают две минуты, добавляют 2 мл чисто перегнанного гептана и снова встряхивают 10-15 мин. Примерно через час отбирают верхнюю фазу и фотометрируют при 232 нм против контрольной пробы где вместо гемолизата взято 0,2 мл H2O. Коэффициент экстинции 2,2 * 10 -5 см-1 М-1. Формула для расчета (при l=1 см):
С(нмоль/мл пл) = [(∆А* 106)/(2,2*105*1)]*[4/Vпроб], где: ∆А = Аоп - Афон, 2,2*105 – коэффициент экстинции, 1 (см) = L (толщина кюветы), 2 (мл) = Vгепт (объем гептана)
2.3.11. Определение содержания малонового диальдегида (МДА) в эритроцитах
За основу взят классический метод Ernster et al [25] в модификации для эритроцитов. 0,5 мл гемолизата эритроцитов (1:1) смешивают с 1 мл охлажденной 5% ТХУ и тщательно растирают смесь стеклянной палочкой. После выдерживают при 0±5 °С не менее 1-2 часов смесь центрифугируют при 4000 g 30 мин. Далее тщательно отбирают 0,4мл надосадка в пробирки для кипячения и добавляют 1,0 мл 0,5% тиобарбитуровой кислоты. Смесь инкубируют в кипящей воде более 10 мин после чего охлаждают и фотометрируют при 532 нм против соответствующего контроля. В расчет принимают коэффициент молярной экститнции – 1,56*105 см-1 М-1. С(нмоль/мл эр) = ∆А * 115,8
2.3.12. Определение содержания МДА в плазме крови и печени
За основу взят классический метод Mihara et al. [30]. 0,4 мл плазмы крови смешивают с 4 мл охлажденной 1,4% ортофосфорной кислоты и 2 мл 0,5% тиобарбитуровой кислоты. Смесь инкубируют в кипящей бане 45 мин после чего охлаждают и добавляют 4 мл н-бутанола. Смесь встряхивают до образования белой суспензии, после чего центрифугируют при 4000 g 20 мин. Верхнюю фазу фотометрируют при 532 нм против контрольной пробы. Коэффициент экстинции – 1,56*105 см-1 М-1. Формула для расчета (при L=1 см). С (нмоль/мл )= ∆А * 64,2
2.3.13. Определение жирнокислотного состава масел методом газожидкостной хроматографии (метод внутренней нормализации)
1 мл масла смешивают с 5 мл метанола, добавляют 1 мл метилирующего агента (раствор гидроксида тетраметиламмония) и 3 мл эфира серного (диэтиловый). Выдерживают в течение 10-15 мин при комнатной температуре, аликвотную часть отбирают для анализа (3-5 мкл) и хроматографируют.
Режим разделения: Температура колонки 170-190°С, Температура впрыскивающей камеры 250°С, Колонка насадочная 3 м, Содержание колонки: 5% диэтиленгликольсукцинат нанесенный на хроматон N-AW. Анализ проводят относительно количества жирных кислот.
2.3.14. Гистологический анализВыполняли для подтверждения наличия атеросклеротических изменений в опытных группах. Для гистологического исследования брали грудную и брюшную аорту, фиксировали 10% нейтральным формалином. Гистологическое исследование выполняли сотрудники гистологической лаборатории.
3. РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ 3.1. ИССЛЕДОВАНИЯ АНТИОКСИДАНТНЫХ СВОЙСТВ СЕЛЕНОПИРАНА
Данные исследования антиоксидантных свойств СП по сравнению с БОТ, ТФ и СП при термическом окислении подсолнечного масла (Таблица 1) свидетельствуют о том, что антиоксидантная активность СП не уступает активности БОТ, и даже превосходит ее.
Рисунок 1
Динамика накопления пероксидов в смеси нерафинированных растительных масел в присутствии бутилокситолуола, селенопирана и токоферола
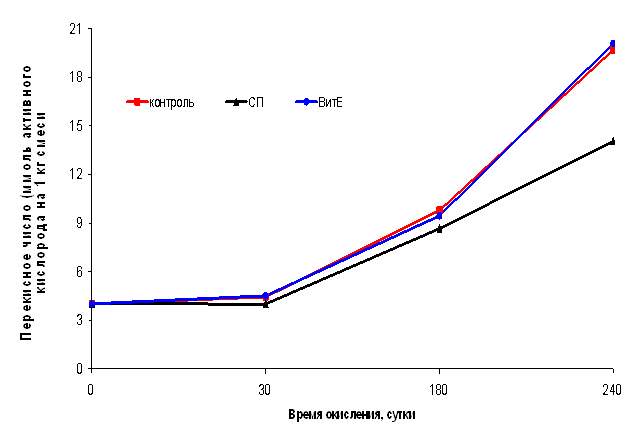
Преимущество СП становится заметным уже в течение 1-го часа окисления. Отмечено, что введение в смесь СП приводило к снижению концентрации пероксидов, и только к 6 часу их накопление достигло величин, превышающих исходные. К 26 часу окисления концентрация пероксидов в системе с БОТ составляла 95,65%, с СП – 85,51%, с ТФ – 111,6% по отношению к контролю.
Таблица 1
Динамика накопления пероксидов в подсолнечном масле в присутствии бутилокситолуола, селенопирана и токоферола
| Часы | Концентрация пероксидов, ммоль/г | |||
| контроль | БОТ | СП | ТФ | |
| 0 | 0,0060 | 0,0060 | 0,0060 | 0,0060 |
| 1 | 0,0090 | 0,0070 | 0,0045 | 0,0060 |
| 3 | 0,0100 | 0,0080 | 0,0055 | 0,0100 |
| 6 | 0,0131 | 0,0130 | 0,0090 | 0,0170 |
| 11 | 0,0300 | 0,0250 | 0,0210 | 0,0280 |
| 18 | 0,0480 | 0,0460 | 0,0380 | 0,0520 |
| 26 | 0,0690 | 0,0660 | 0,0590 | 0,0770 |
При щадящем режиме окисления смеси растительных масел СП в качестве АО также имел преимущества перед ТФ (Рис. 1), что позволило выбрать его для стабилизации итогового продукта – композиции нерафинированных масел льна и расторопши.
3.2. ИЗМЕНЕНИЯ БИОХИМИЧЕСКИХ ПОКАЗАТЕЛЕЙ ТКАНЕЙ ЭКСПЕРИМЕНТАЛЬНЫХ ЖИВОТНЫХ
Результаты комплексного биохимического и гистологического анализа биоматериала, полученного от экспериментальных животных, свидетельствуют о существенном торможении развития атеросклеротических процессов при введении СМЛР в качестве добавки к ВЖР.
Достоверные различия между опытными группами обнаруживались как в количестве липидов плазмы крови, так и в их соотношении (Таблица 2). В первой опытной группе наблюдались характерные признаки нарушения липидного обмена: повышение ХСобщ на 54% и ХС-ЛНП на 350 % по сравнению с контрольной группой, на фоне снижения содержания ХС-ЛВП на 57 %. При этом ИА повышался до 6,29 по сравнению с 1,03 в контроле. Введение в ВЖР животных второй опытной группы СМЛР привело к торможению накопления в плазме ХС, снижение на 38 % и снижение концентрации ХС атерогенных ЛП: ХС-ЛНП на 272% и ХС-ЛОНП на 55% по сравнению с контролем, а также к повышению содержания ХС-ЛВП 42%, что отразилось на величине ИА – 3,91.
Таблица 2
Липидограмма плазмы экспериментальных животных
| Группа | ТГ ммоль/л | ХС общ., ммоль/л | ХС-ЛВП, ммоль/л | ХС-ЛНП, ммоль/л | ХС-ЛОНП, ммоль/л | Индекс Атероген., у.е. |
| Контроль n=10 | 0,906± 0,031 | 1,74± 0,052 | 0,858± 0,024 | 0,459± 0,049 | 0,421± 0,019 | 1,03± 0,069 |
| Опытная 1 n=10 | 0,512# ± 0,044 | 2,68# ± 0,083 | 0,372#± 0,01 | 2,07#± 0,08 | 0,240#± 0,018 | 6,29#± 0,393 |
| Опытная 2 n=10 | 0,442#± 0,015 | 2,40#* ± 0,083 | 0,496#* ± 0,025 | 1,71#* ± 0,077 | 0,191#* ± 0,007 | 3,91#* ± 0,235 |
Примечание: * - p<0,05 относительно опытной группы 1
# - p<0,05 относительно контрольной группы
Было также установлено, что применение СМЛР существенно влияло на процессы ПОЛ. Выявлено достоверное снижение ДК плазмы на 12% , МДА эритроцитов на 37% и печени на 11% животных второй опытной группы по сравнению с животными, не получавшими СМЛР (Таблица 3).
Таблица 3
Содержание ДК и МДА в плазме, эритроцитах и печени экспериментальных животных
| Группа | ДК плазмы, нмоль/мл | ДК эритроц., нмоль/мл | ДК печени, нмоль/г | МДА плазмы, нмоль/мл | МДА эритроц., нмоль/мл | МДА печени, нмоль/г |
| Контроль n=10 | 3,06± 0,097 | 13,2± 0,482 | 47,0± 1,14 | 11,6± 0,068 | 53,8± 0,914 | 36,7± 0,656 |
| Опытная 1 n=10 | 3,24± 0,101 | 14,3#± 0,168 | 85,5#± 3,21 | 13,4#± 0,107 | 54,2± 3,30 | 50,6#± 1,52 |
| Опытная 2 n=10 | 2,68 #* ± 0,127 | 16,3#* ± 0,655 | 87,9± 2,32 | 13,1± 0,051 | 33,9 #* ± 1,48 | 32,8# *± 0,362 |
Примечание: * - p<0,05 относительно опытной группы 1
# - p<0,05 относительно контрольной группы
3.3. ГИСТОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ ПРЕПАРАТОВ АОРТЫ ЭКСПЕРИМЕНТАЛЬНЫХ ЖИВОТНЫХ
Результаты гистологического исследования препаратов аорты представлены в таблице 4. При макроскопическом исследовании аорты у 100% животных первой опытной группы наблюдали умеренно выраженные уплотнения в брюшном и грудном отделе аорты и снижение эластичности стенки аорты.
При микроскопическом исследовании аорты животных первой опытной группы во всех образцах обнаружен склероз ветвей брюшной отдела у 100% с наложением фибрина у 100% и частичной облитерацией их просвета у 40 %. При исследовании грудного отдела аорты выявлены слабо выраженные очаговые утолщения стенки у 50 %. В целом в препаратах аорты наблюдали признаки атеросклероза в стадии сформированной фиброзной бляшки (Рис. 2).
Таблица 4
Макро- и микроскопические изменения стенки аорты экспериментальных животных
| Признаки | Опытная 1 | Опытная 2 | |||
| % | степень | % | степень | ||
| МАКРО-скопическое исследование | Уплотнения в брюшном отделе | 100 | ++ | 70 | + |
| Уплотнения в грудном отделе | 100 | ++ | - | - | |
| Снижение эластичности стенки | 100 | ++ | 70 | + | |
| МИКРО- скопическое исследование | Очаговые утолщения стенки в брюшном отделе | 100 | ++ | 70 | + |
| Очаговые утолщения стенки в грудном отделе | 50 | + | - | - | |
| Наложения фибрина | 100 | ++ | - | - | |
| Склероз ветвей брюшной аорты | 100 | +++ | 70 | ++ | |
| Облитерация просвета ветвей брюшной аорты | 40 | ++ | - | - | |
Примечание: +++ сильно выражены, ++ умеренно выражены, + слабо выражены
У животных второй опытной группы при микро- и макроскопическом исследовании аорты все указанные изменения были выражены в меньшей степени.
Рисунок 2
Фиброзная бляшка в стенке брюшного отдела аорты (из препаратов 1 опытной группы), окраска гематоксилин-эозин х 250.
![]()

1- грубая соединительная ткань, сформированная фиброзная бляшка
2 – нарушение целостности эндотелия.
Обнаруживались лишь начальные признаки повреждения интимы и специфические «завихрения» в слое гладкомышечных волокон, ни в одном препарате не находили сформированных «бляшек», просвет ветвей аорты свободен, а в 30% случаев (у 3-х животных) признаков атеросклероза аорты вообще не выявлено.
4. ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Введение СП в сочетании с ПНЖК в атерогенный рацион оказало существенное влияние на развитие атеросклеротических процессов и на процессы ПОЛ. Вероятнее всего, это связано с антиоксидантными свойствами СП.
Липидограмма плазмы эксперементальных животных более наглядно показала действие СП, так как отличия второй опытной группы от первой было значительным. Концентрация ХСобщ, ХС-ЛНП и ХС-ЛОНП второй опытной группы была достоверно ниже, чем у животных первой опытной группы. Данные изменения в липидограмме, в совокупности с повышением ХС фракции ЛВП, можно трактовать как положительные, так как ЛНП и ЛОНП являются атерогенными, а ЛВП - антиатерогенными частицами. ЛВП осуществляют обратный транспорт ХС из периферических органов и тканей в печень для окисления в желчные кислоты и выведения с желчью [14]. Этим можно объяснить более низкую концентрацию ХСобщ у животных второй опытной группы в отличие от первой. Понижение концентрации ТГ объясняется снижением количества ЛОНП, которые являются транспортной формой эндогенных ТГ [14].
При исследовании продуктов ПОЛ было выявлено достоверное увеличение концентрации ДК в эритроцитах и печени, и снижение ДК в плазме у животных, получавших СМЛР. Это объясняется тем, что вдыхание кислорода приводит к десятикратному увеличению количества перекисей в печени [18], эритроциты же осуществляют транспорт кислорода и содержат мощный катализатор ПОЛ – гемоглобин [7]. Между тем, большинство тканей в норме содержит некоторое количество липидных перекисей [17]. Так, по данным Нейфаха и Кагана в печени, мозге, сальнике крыс обнаруживается от 15 до 80 нмолей перекисей на 1 г липидов или от 1 до 4,5 нмоль перекисей на 1 г ткани [18]. Следовательно, концентрация ДК, как первичных продуктов ПОЛ, высока именно в печени и эритроцитах. Накопление ДК в клетках приводит к тому, что в мембранах появляются участки («поры»), через которые наружу выходит содержимое самих клеток и органелл, а в эритроцитах возрастает перекисный и осмотический гемолиз. ДК являются неустойчивыми и через образование липоперекисей превращаются в МДА [12]. СП взаимодействует именно с перекисями жирных кислот, причем это взаимодействие имеет двойной характер. Во-первых, в нашем исследовании была показана способность СП тормозить накопление перекисей жирных кислот, а ранее автором соединения [3] было показано, что увеличение содержания перекисей в системе приводит к рециклизации соединения, протоны расходуются на инактивацию перекисей и обрыв цепи свободнорадикального окисления. При дальнейшем разрыве ковалентных связей в системе микросомального окисления с участием ферментов цитохрома р-450 из состава СП высвобождается восстановленный селен, который участвует в образовании селеноцистеина и таким образом стимулирует синтез глутатионпероксидазы [4] – главного внутри- и внеклеточного фермента, обезвреживающего липопероксиды. Таким образом, при обрыве цепи и инактивации липопероксидов, следующая степень повреждения жирных кислот – образование МДА – не наступает, чем и объясняется достоверно более низкое содержание МДА в печени и эритроцитах у животных второй опытной группы.
По результатам гистологического анализа у животных первой опытной группы были обнаружены сформировавшиеся фиброзные бляшки в отличие от второй опытной группы, у которой были найдены только липидные пятна. Большинство морфологов считают, что развитие атеросклероза протекает по схеме: липидные пятна или полоски Ò фиброзные бляшки Òосложненные поражения (изъязвления, кальциноз, тромбоз), хотя отдельные авторы не исключают возможности образования фиброзных бляшек без предварительного формирования липидных пятен [5], но так же известно и то, что липидные пятна могут исчезнуть, если произойдет значительное и длительное снижение уровня ХС и ЛНП в плазме крови, и достигнутый уровень будет поддерживаться на протяжении полутора-двух лет у людей [14]. Важную роль в регрессии играют так же ЛВП, благодаря их способности осуществлять транспорт ХС в печень [14]. Можно предположить, что время опыта было слишком мало для того, чтобы увидеть, какие изменения произойдут с липидными пятнами во второй опытной группе, но даже полученные данные подтверждают положительное действие СМЛР. Возможно, СМЛР в сочетании с физическими нагрузками имела бы более выраженный положительный эффект, так как из-за малой подвижности у экспериментальных животных наблюдалось ожирение [14].
ВЫВОДЫ
1. В исследованиях in vitro доказано, что селенопиран, благодаря электроно- и водорододонорным свойствам, обладает способностью тормозить накопление пероксидов в системе нерафинированных растительных масел с различным содержанием полиненасыщенных жирных кислот в большей степени, чем бутилокситолуол и токоферол.
2. Введение в высокожировой рацион экспериментальных животных смеси масел льна и расторопши с селенопираном способствует торможению атеросклеротических процессов: снижению концентрации холестерина и атерогенных липопротеидов в плазме крови, повышению содержания антиатерогенных липопротеидов.
3. Полученные данные свидетельствуют о стабилизации перекисных процессов в липопротеидах низкой и очень низкой плотности, что подтверждается положительной корреляцией между показателями содержания диеновых конъюгатов плазмы и холестерина в липопротеидах низкой и очень низкой плотности.
4. Гистологический анализ препаратов аорты подтверждает полученные биохимические данные, и свидетельствует о значительном торможении развития морфологических изменений, вызванных атерогенной диетой, при внесении в нее испытуемой смеси масел льна и расторопши с селенопираном.
СПИСОК ЛИТЕРАТУРЫ
1. Абрамова Ж.И., Оксенгендлер Г.И. Человек и противоокислительные вещества. – Л.: Наука, 1985.-232с.
2. Биохимические основы патологических процессов / Под ред. Е.С. Северина / – М.: Медицина, 2000. –304 с.
3. Боряев Г.И., Жуков О.И., Блинохватов А.Ф., Древко Б.И. Оценка антиоксидантной активности селен органических соединений // Сб. науч. трудов Саратовского университета. – Саратов, 1996. – С.199.
4. Боряев Г.И., Галочкин В.А., Блинохватов А.Ф. Функциональная активность монооксигеназной системы печени цыплят – бройлеров при введение в рацион селеноорганического соединения СП-1 // Бюлл.ВНИИФБиП с.-х. животных. – 1990. – Вып.3 (99). – С.70-73.
5. Вихтер А. М. Атеросклероз // Руководство по кардиологии / Под ред. Е. И.Чазова. – М.: Медицина, 1982. – Т. 1. – С. 417 - 443.
6. Владимиров Ю.А., Азизова О.А., Деев А.И. и др. Свободные радикалы в живых системах // Итоги науки и техники. Сер. Биофизика. - Т.29. - М., 1991. - С.1-249.
7. Владимиров Ю.А., Арчаков А.И. Перекисное окисление липидов в биологических мембранах. - М.: Наука, 1972. - С.237-238.
8. Владимиров Ю.А. Свободные радикалы в биологических системах // Соросовский образовательный журнал. - 2000. - Т.6. - №12. - С.13-19
9. Гаврилов В.Б., Мишкорудная М.И. // Лаб. дело. - 1983. -№3. - С.33-35.
10. Гильмиярова Ф.Н. Патент РФ № 2131672, кл. А 23 D 9/00, 1998.
11. Зенков Н.К., Ланкин В.З., Меньщикова ЕБ. Окислительный стресс: Биохимический и патофизиологический аспекты. – М.:МАИК «Наука\Интерпереодика», 2001.-343 с.
12. Камышников В.С. Справочник по клинико-биохимической лабораторной диагностике. В 2 т. – Минск: Беларусь, 2000. - Т.1-2
13. Климов А.Н., Никульчева Н.Г Липиды и липопротеиды и атеросклероз. – СПб.: Питер, 1995.–298с.
14. Климов А.Н., Никульчева Н.Г. Обмен липидов и липопротеидов и его нарушения. - С-Пб: « Питер – Ком », 1999.–512с.
15. Кравченко Ю.В. Экспериментальное исследование системы антиоксидантной защиты на этапах онтогенеза при токсическом и алиментарном воздействии: // Дис. к.б.н.-М., 2005
16. Ланкин В.З., Вихерт А.М., Тихазе А.К. и др. Роль перекисного окисления липидов в этиологии и патогенезе атеросклероза // Вопр. мед. химии. - 1989. -№3. - С.18-24.
17. Нейфах ЕА Биофизика. – 1971. - С.16-560.
18. Нейфах ЕА., Каган ВЕ. Биохимия. – 1969. - С.34-511.
19. Соколовский В.В. Тиолдисульфидное соотношение крови как показатель состояния неспецефической резистентности организма: Учебное пособие. – С-Пб., 1996.-30 с.
20. Aviram M. Modified forms of low-density lipoprotein and atherogenesis // Atherosclerosis.-1993. - Vol.98.- P.1-9.
21. Brown M.S., Goldstein J.L. Lipoprotein metabolism in the macrophage: implication for cholesterol deposition in atherosclerosis // Annu. Rev. Biochem. - 1983. - Vol.52.- P.223-261.
22. Burton G., Ingold K. Vitamin E: application of the principles of physical organic chemistry to the exploration of its structure and function. // Acc. Chem. Res. – 1986. - Vol.19.- P.194 -201
23. Cthcart M.K., Menally A.K., Morel D.W., Chisolm G.M. Superoxid anion participation in human monocyte-mediated oxidation of low-density lipoprotein and conversion of low-density lipoprotein to a cytotoxin // J. Immunol. - 1989. -Vol.142. - P1963-1969.
24. Doba T., Burton G., Ingold K. Antioxidant and co- antioxidant activity of vitamin C. The effect of vitamin C, either alone or in the presence of vitamin E analogue, upon the peroxidation of agueous multilamellarphospholipid liposomes. // Biochem. biophys. аcta .- 1985. - Vol.835. - P.298 -303.
25. Ernster L, Nordenbrandt K. Microsomal lipid peroxidation // Methods Enzymol., 1967. - Vol. 10. - P. 575-576.
26. Fan Y.Y., Chapkin R.S. Importance of Dietory γ-Linolenic Acid in Human Health and Nutrition // The Journal of Nutrition. – 1998. – Vol.128. – P.1411-1414.
27. Frenoux J-M.R., Prost E.D., Belleville J.L., Prost J.L. A Polyunsaturated Fatty Acid How us Blood Pressure and Improves Antioxidant Status in Spontaneously Hypertensive Rats // The Journal of Nutrition – 2001. – Vol.131. – Р.39-45.
28. Halliwel B. Oxidation of low-density lipoproteins: guestions of initiation, propagation, and the effect of antioxidants // Amer. J. Clin. Nutr. - 1995. - Vol.61 (suppl). - P.670S-677S.
29. Henning B., Chow C.K. Lipid peroxidation and endothelial cell injury: Implications in atherosclerosis. Review // Free Radical Biol. and Med. - 1988. - Vol.4. - P.99-105.
30. Michara M., Uchiyama M., Fukuzava K. Thiobarbituric acid value on fresh homogenate of rat as a parameter of lipid peroxidation in aging, CCL4 intoxication, аnd vitamin E deficiency // Biochem. Med. 1980. - Vol. 23 (3). P. 302-311.
31. Nair S.D., Leitch J.W., Falconer J., Gard M.L. Prevention of Cardiac Arrhythmia by Dietory (n-3) Poly un saturated Fatty Acid and Their Mechanism of Action // The Journal of Nutrition – 1997. – Vol.127. – Р.383-393.
32. Park E., Thomas J. The mechanisms of reduction of protein mixed disulfides (dethiolation) in cardiac tissue. // Arch. Biochem. Biophys. – 1989. - Vol.274 (1). - P.47 -54.
33. Parthasarathy S., Steiberg D., Witzturm J.L. The role of oxidized low-density lipoprotein in the pathogenesis of atherosclerosis // Annu. Rev. Med. - 1992. - Vol.43. - P.219-225.
34. Pitas R.E. Expression of the acetyl low-density lipoprotein receptor by rabbit fibroblasts and smooth muscle cells. Up-regulation by phorbol esters // J. Biol. Chem. -1990. - Vol.265. - P.12722 -12727.
35. Sakai M., Miyazaki A., Hakamata H. et al. The scavenger receptor serves as a route for internalization of lysophospatidilcholine in oxidized low density lipoprotein - induced macrophage proliferation // J. Biol. Chen. – 1996. - Vol.271. - P.27346 -27352.
36. Schwarz K., Porter L.A., Fredga A. Some regularities in the structure-function relationship of organoselenium compounds effective against dietary liver necrosis // Ann.N.Y.Acad.Sci. – 1972. – Vol.14. – Р.192-200.
37. Steinbrecher U.P., Zang H.F., Lougheed M. Role of oxidatively modified LDL in atherosclerosis // Free Radical Biol. and Med. - 1990. - Vol.9. - P.155-168.
38. Yla-Herttuala S. Macrophages and oxidized low-density lipoprotein in the pathogenesis of atherosclerosis // Ann. Med. - 1991. - Vol.23. - P.561 -566.
0 комментариев