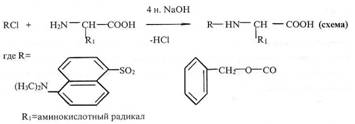
Биосинтез 2h-меченого инозина высокого уровня дейтерированности
О. В. МОСИН*
*Московская государственная академия тонкой химической технологии им. М. В. Ломоносова, 117571 Москва, просп. Вернадского, 86.
Осуществлен биосинтез 2Н-меченого пуринового рибонуклеозида инозина (выход 3.9 г c 1 л ростовой среды) с использованием адаптированного к дейтерию штамма Bacillus subtilis в тяжеловодородной среде высокого уровня дейтерированности (89-90 ат.% 2Н) с 2% гидролизатом биомассы метилотрофной бактерии Brevibacterium methylicum как источника 2Н-меченых ростовых субстратов (условия синтеза: синтетическая среда М9 с 98% 2Н2О и 2% [U-2H]метанолом, инкубационный период 5-6 сут при 370С). Исследование уровня дейтерированности биосинтетического инозина методом масс-спектрометрии FAB выявило полиморфизм включения дейтерия в молекулу (изотопный состав инозина: 4 ат. 2Н, 20%; 5 ат. 2Н, 38%; 6 ат. 2Н, 28%; 7 ат. 2Н, 14%) с включением дейтерия в рибозный и гипоксантиновый фрагменты молекулы.
Ключевые слова: Bacillus subtillis; 2Н-меченый инозин; биосинтез; масс-спектрометрия FAB.
ВВЕДЕНИЕВ настоящее время во всем мире растет интерес к получению природных биологически активных соединений (БАС), меченных стабильными изотопами (2Н, 13С, 15N, 18О и др), которые необходимы для многочисленных биохимических и диагностических целей [1], структурно-функциональных исследований [2], а также для изучения клеточного метаболизма [3]. Тенденции к предпочтительному использованию стабильных изотопов по сравнению с радиоактивными аналогами обусловлены отсутствием радиационной опасности и возможностью определения локализации метки в молекуле спектроскопией 1Н ЯМР [4, 5], ИК- и лазерной спектроскопией [6], а также масс-спектрометрией [7]. Развитие технической и компъютерной оснащенности аналитических методов позволило существенно повысить эффективность проведения биологических исследований de novo, а также изучать структуру и механизм действия БАС на молекулярном уровне [8]. Большое научно-прикладное значение в этом аспекте имеют соединения нуклеиновой природы, содержащие дейтериевую метку в углеродном скелете молекулы [9]. В частности, 2Н-меченые рибонуклеозиды в ближайшем будущем смогут найти применение в матричных синтезах молекул дейтерированных РНК для изучения их пространственной структуры и конформационных изменений [10].
Важным моментом в исследованиях с применением изотопно меченых БАС является их доступность. Дейтериймеченые БАС могут быть синтезированы с использованием химических, ферментативных и биосинтетических методов [11, 12]. Однако химические синтезы часто многостадийны, требуют больших расходов ценных реагентов и меченых субстратов и приводят к конечному продукту, представляющему собой рацемическую смесь D- и L-форм, для разделения которых требуются специальные методы [13]. Более тонкие синтезы меченых БАС связаны с комбинацией химических [14] и ферментативных подходов [15, 16]. Стратегия синтеза изотопно-меченых БАС более подробно освещена в работе ЛеМастера [17].
Для многих научно-практических целей биотехнология предлагает альтернативный химическому синтезу биосинтетический метод получения дейтериймеченых БАС, который приводит к высоким выходам синтезируемых продуктов, к эффективному включению дейтерия в молекулы и к сохранению природной конфигурации синтезируемых соединений [18]. Традиционным подходом при этом остается предложенный Креспи метод выращивания штаммов-продуцентов в средах с максимальными концентрациями дейтерия [19]. Однако основным препятствием является недостаток 2Н-меченых ростовых субстратов с высоким уровнем дейтерированности. Прежде всего это связано с ограниченной доступностью и дороговизной самого высокоочищенного дейтерия, выделяемого из природных источников. Природная распространенность дейтерия составляет лишь 0.015% (относительно общего количества элемента), однако несмотря на невысокое содержание дейтерия в пробах разработанные в последние годы методы обогащения и очистки позволяют получать 2Н-меченые субстраты высокого уровня изотопной чистоты [20].
Начиная с первых экспериментов Даболла и Кокса по выращиванию природных объектов в тяжелой воде, разрабатываются подходы с использованием гидролизатов 2Н-меченой биомассы как ростовых субстратов для синтеза штаммов-продуцентов БАС [21, 22]. Однако эксперименты обнаружили бактериостатический эффект 2Н2О, заключающийся в ингибировании жизненно-важных функций клетки, оказываемой 40% 2Н2О на растительные клетки [23] и 80-90% 2Н2О на клетки простейших и бактерий [24]. Попытки использовать для синтеза в 2Н2О природных объектов различной таксономической принадлежности, включая бактерии, микроводоросли [25] и дрожжи [26] предпринимались в течение длительного времени. Однако широкого распространения в биотехнологии они не получили ввиду трудности синтеза, использования сложных комплексных ростовых сред, сложности технологической схемы синтеза и т. п. Поэтому целый ряд практических вопросов биосинтеза 2Н-меченых БАС в 2Н2О остается не выясненным.
Более перспективны схемы синтеза с использованием в качестве 2Н-меченых ростовых субстратов биомассы метилотрофных бактерий, ассимилирующих метанол по рибулозо-5-монофосфатному (РМФ) и сериновому пути фиксации углерода, интерес к которым возрастает благодаря интенсивному развитию технологии химического синтеза метанола [27, 28]. Уровень ассимиляции биомассы метилотрофов клетками простейших организмов и эукариот составляет 85-98%, а их производительность, измеренная по уровню биоконверсии метанола в клеточные компоненты, достигает 50% [29]. Как было показано нами раннее, метилотрофные бактерии очень неприхотливые объекты, растут на минимальных средах с 2-4% метанолом, в которых другие контаминантные бактерии не размножаются и достаточно легко адаптируются к максимальным концентрациям 2Н2О, что существенно для синтеза 2Н-меченых БАС [30, 31]. Большой научно-практический интерес к использованию дейтерированной метилотрофной биомассы для синтеза продуцентов рибонуклеозидов определил цель настоящей работы, связанной с изучением принципиальной возможности биосинтеза 2Н-меченого инозина штаммом Bacillus subtilis за счет использования гидролизата факультативных метилотрофных бактерий Brevibacterium methylicum.
Таблица 1. Изотопный состав ростовых сред и биосинтетические характеристики B. methylicum
|
| Компоненты среды, об.% H2O 2H2O Метанол [U-2H] Метанол | Лаг-период, ч | Выход микробной биомассы, % от контроля | Время генерации, ч | |||
| 1 | 98 | 0 | 2 | 0 | 20 | 100 | 2.2 |
| 2 | 98 | 0 | 0 | 2 | 30 | 92.3 | 2.4 |
| 3 | 73.5 | 24.5 | 2 | 0 | 32 | 90.6 | 2.4 |
| 4 | 73.5 | 24.5 | 0 | 2 | 34 | 85.9 | 2.6 |
| 5 | 49.0 | 49.0 | 2 | 0 | 40 | 70.1 | 3.0 |
| 6 | 49.0 | 49.0 | 0 | 2 | 44 | 60.5 | 3.2 |
| 7 | 24.5 | 73.5 | 2 | 0 | 45 | 56.4 | 3.5 |
| 8 | 24.5 | 73.5 | 0 | 2 | 49 | 47.2 | 3.8 |
| 9 | 0 | 98.0 | 2 | 0 | 58 | 32.9 | 4.4 |
| 10 | 0 | 98.0 | 0 | 2 | 60 | 30.1 | 4.9 |
| 10’ | 0 | 98.0 | 0 | 2 | 40 | 87.0 | 2.8 |
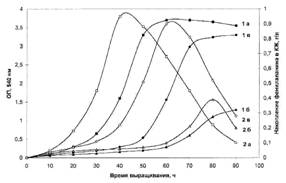
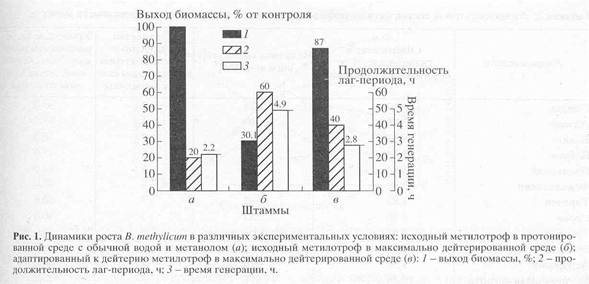
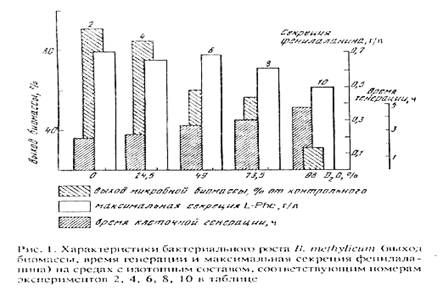
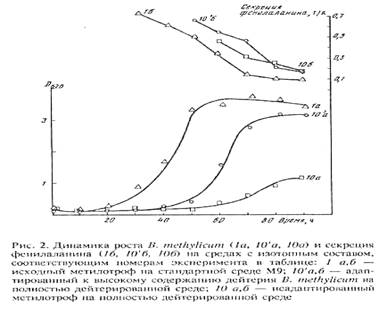
Для синтеза 2Н-меченого инозина использовали мутантный штамм грамположительных бактерий Bacillus subtilis (предварительно адаптированный к дейтерию скринингом до отдельных колоний), который из-за нарушения метаболических путей регуляции биосинтеза пуриновых рибонуклеозидов синтезирует в стандартных условиях выращивания (дрожжевая среда, поздний экспоненциальный рост, 32-340С) 17 г инозина на 1 л культуральной жидкости (КЖ) [32]. Максимальный выход инозина достигался при использовании природной протонированной среды, содержащей в качестве в качестве источников ростовых факторов и аминного азота 2% БВК дрожжей, а в качестве источника углерода и энергии глюкозу (не менее 12 мас.%). При проведении синтеза требовалось заменить протонированные ростовые субстраты их дейтерированными аналогами, а также использовать 2Н2О высокого уровня изотопной чистоты. Для решения поставленной задачи использовали адаптированный к дейтерию штамм факультативных метилотрофных бактерий Brevibacterium methylicum с 50% уровнем биоконверсии метанола (при эффективности конверсии 15.5-17.3 г сух. биомассы на 1 г потребленного субстрата) [33]. Проведение адаптации для B. methylicum определялось необходимостью улучшить ростовые характеристики штамма в максимально дейтерированной среде, поэтому использовали ступенчато-увеличивающийся градиент концентрации 2Н2О в ростовых средах в присутствии 2% метанола (табл. 1). Для изучения влияния уровня дейтерированности источника углерода на ростовые параметры штамма в опытах (1, 3, 5, 7 и 9) использовали протонированный метанол, а в опытах (2, 4, 6, 8 и 10) [U-2Н]метанол. Согласно полученным данным замена протонированного метанола его дейтерированным аналогом в условиях одинаковой концентрации 2Н2О в среде приводила к небольшим уменьшениям ростовых характеристик штамма (табл. 1, опыты 2, 4, 6, 8 и 10). Поэтому в дальнейших опытах использовали среды с 2Н2О и [U-2Н]метанолом. На контрольной протонированной среде (1) с водой и метанолом продолжительность лаг-периода и времени клеточной генерации B. methylicum составили 20 и 2.2 ч, а выход микробной биомассы 200 г с 1 л КЖ (табл. 1, опыт 1). В промежуточных опытах (2-10) биосинтетические параметры изменялись пропорционально концентрации 2Н2О. Найденная закономерность заключалась в увеличении продолжительности лаг-периода и времени клеточной генерации при уменьшении выходов микробной биомассы с фиксированием самых низких значений этих параметров в максимально дейтерированной среде с 98% 2Н2О и 2% [U-2H]метанолом (табл. 1, опыт 10). За ходом адаптации, условия которой показаны в опыте 10’ (табл. 1) наблюдали, снимая динамики роста исходного (б) и адаптированного к дейтерию (в) штамма в максимально дейтерированной среде М9 (рис. 1, контроль (а) получен в протонированной среде), а также по изменению продолжительности лаг-периода, времени генерации и выходов микробной биомассы (рис. 2). В отличие от адаптированного штамма (в), ростовые динамики исходного штамма (б) в максимальной дейтерированной среде ингибировались дейтерием (рис. 1).
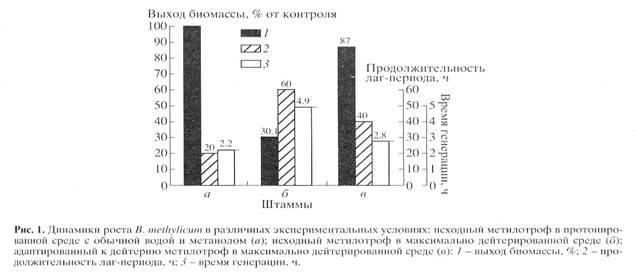
Выход микробной биомассы у адаптированного штамма (в) уменьшался на 13% по сравнению с контрольными условиями (рис. 2, а) при увеличении времени генерации до 2.8, а продолжительности лаг-периода до 40 ч (рис. 2, в). Адаптированный штамм возвращался к нормальному росту при переносе в протонированную среду после пролонгированного лаг-периода, что доказывает фенотипическую природу феномена адаптации, хотя теоретически не исключается, что эффект реверсии стабильно сохраняется при росте в 2Н2О, но маскируется при переносе клеток в протонированную среду. Улучшенные ростовые характеристики адаптированного метилотрофа существено упрощают схему синтеза 2Н-меченой биомассы, оптимальным условиям которой удовлетворяет максимально дейтерированная среда М9 с 98% 2Н2О и 2% [U-2Н]метанолом с инкубационным периодом 5-6 сут при 370С.

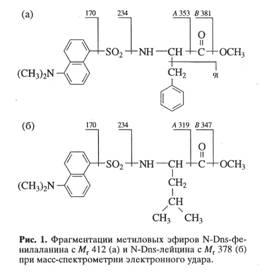
Схема синтеза 2Н-меченого инозина разрабатывалась с учетом способности метилотрофных бактерий синтезировать большое количество белка (выход 50% от веса сухого вещества), 15-17% полисахаридов, 10-12% липидов (в основном, фосфолипиды) и 18% зольных веществ [34]. Гидролиз биомассы проводили автоклавированием в 0.5 н. 2НCl (в 2Н2O), чтобы обеспечить высокие выходы этих соединений и минимизировать реакции обратного (1Н-2Н) обмена в аминокислотных остатках молекул белков. Качественный и количественный состав ароматических аминокислот метилотрофного гидролизата изучали в дейтерированной среде М9 на катионообменной колонке Biotronic LC-5001 (ФРГ) с сульфированной смолой UR-30, а уровни дейтерированности молекул масс-спектрометрией электронного удара метиловых эфиров N-диметиламинонафталин-5-сульфонильных производных аминокислот. Гидролизат представлен пятнадцатью идентифицированными аминокислотами (за исключением пролина, который детектировался при 440 нм) при выходах аминокислот, сопоставимом с потребностями штамма в источниках углерода и аминного азота (табл. 2). При этом индикатором, определяющим высокую эффективность включения дейтерия в синтезируемый продукт служит высокий уровень дейтерированности молекул аминокислот, который варьирует от 49% для лейцина/изолейцина до 97.5% для аланина (табл. 2).
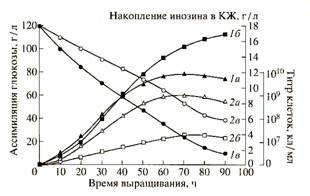
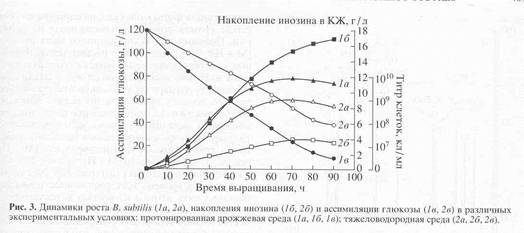
Биосинтетические характеристики штамма B. subtilis снимали в протонированной дрожжевой среде с обычной водой и синтетической тяжеловодородной среде с 2Н2О и 2% 2Н-меченым метилотрофным гидролизатом B. methylicum (рис. 3). Отмечена корреляция в характере изменения ростовых динамик (рис. 3, 1а, 2а), выхода инозина (рис. 3, 1б, 2б) и ассимиляции глюкозы (рис. 3, 1в, 2в). Максимальный выход инозина (17 г/л) зафиксирован в опыте 1б (рис. 3, 1б) на протонированной среде при уровне ассимилируемой глюкозы 10 г/л (рис. 3, 1в). На тяжеловодородной среде выход инозина снижался в 4.4 (3.9 г/л) (рис. 3, 2б), а уровень ассимиляции глюкозы в 4 раза, о чем свидетельствует 40 г/л неассимилируемой глюкозы в КЖ (рис. 3, 2в).
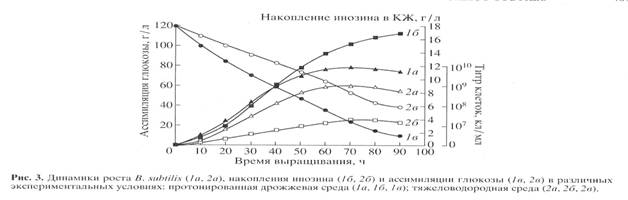
Таблица 2. Аминокислотный состав метилотрофного гидролизата и уровни дейтерированности молекул
| Аминокислота | Выход, % от сухого веса 1 г биомассы | Величина молекулярного иона Мr | Количество включенных атомов дейтерия в углеродный скелет молекулы | Уровень дейтерированности молекул, % от общего количества атомов водорода | |
| Глицин | 9.69 | 324 | 2 | 90.0 | |
| Аланин | 13.98 | 340 | 4 | 97.5 | |
| Валин | 3.74 | 369 | 4 | 50.0 | |
| Лейцин | 7.33 | 383 | 5 | 49.0 | |
| Изолейцин | 3.64 | 383 | 5 | 49.0 | |
| Фенилаланин | 3.94 | 420 | 8 | 95.0 | |
| Тирозин | 1.82 | 669 | 7 | 92.8 | |
| Серин | 4.90 | 355 | 3 | 86.6 | |
| Треонин | 5.51 | не детектировался | - | - | |
| Метионин | 2.25 | не детектировался | - | - | |
| Аспарагин | 9.59 | 396 | 2 | 66.6 | |
| Глутаминовая кислота | 10.38 | 411 | 4 | 70.0 | |
| Лизин | 3.98 | 632 | 5 | 58.9 | |
| Аргинин | 5.27 | не детектировался | - | - | |
| Гистидин | 3.72 | не детектировался | - | - |
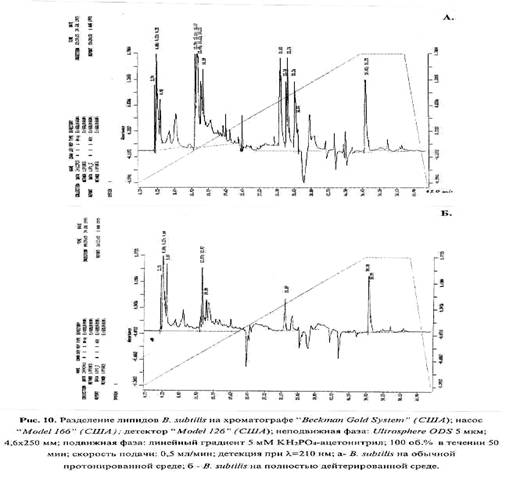
Полученный результат требовал изучение содержания глюкозы в биомассе штамма после гидролиза, осуществленное методом обращенно-фазовой ВЭЖХ (табл. 3). Смесь гидролизных сахаров в табл. 3 (нумерация приведена по последовательности их элюции с колонки) составляли моно-(глюкоза, фруктоза, рамноза, арабиноза), ди-сахариды (мальтоза, сахароза), а также четыре других неидентифицированных сахара с временами удерживания 3.08 (15.63%), 4.26 (7.46%), 7.23 (11.72%) и 9.14 (7.95%) мин (не показаны). Выход глюкозы в дейтерированном гидролизате составляет 21.4% от сух. веса, то есть выше, чем фруктозы (6.82%), рамнозы (3.47%), арабинозы (3.69%) и мальтозы (11.62%). Их выхода существенно не отличались от контроля на Н2О, за исключением сахарозы, не детектируемой в дейтерированном гидролизате.
Таблица 3. Состав сахаров гидролизата штамма-продуцента
| Сахар Выход, % от сухого веса 1 г биомассы протонированная среда тяжеловодородная среда | ||
| Глюкоза | 20.01 | 21.4 |
| Фруктоза | 6.12 | 6.82 |
| Рамноза | 2.91 | 3.47 |
| Арабиноза | 3.26 | 3.69 |
| Мальтоза | 15.3 | 11.62 |
| Сахароза | 8.62 | - |
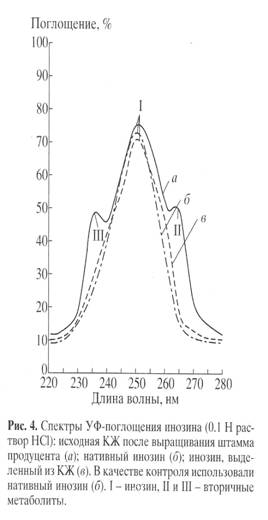
Применение сложных физико-химических методов для выделения биосинтетически 2Н-меченого инозина из КЖ диктовалось необходимостью получать инозин высокой степени хроматографической чистоты. Поскольку в КЖ наряду с синтезируемым продуктом присутствуют примеси неорганических солей, белков и полисахаридов, а также сопутствующие вторичные метаболиты нуклеиновой природы (аденозин, гуанозин) и непрореагировавшие субстраты (глюкоза, аминокислоты), проводили ступенчатое фракционирование КЖ. Повышенная чувствительность инозина к кислотам и щелочам и его нестабильность при выделении диктовали использование кислотных и щелочных растворов низкой концентрации, а также по-возможности проводить выделение при низких температурах, избегая длительного перегрева реакционной смеси. Фракционирование КЖ заключалось в низкотемпературном осаждении высокомолекулярных примесей органическими растворителями ацетоном и метанолом, твердофазной адсорбции/десорбции на поверхности активированного угля, экстрактивного извлечения продукта, перекристаллизации и ионообменной хроматографии. Белки и полисахариды удаляли низкотемператрным осаждением ацетоном при -40С, проводя последующую адсорбцию суммы рибонуклеозидов активированным углем на холоду. Десорбированные рибонуклеозиды извлекали из прореагировавшей твердой фазы элюцией этанольно-аммиачным раствором при 600С, а сам инозин экстракцией 0.3 М NH4-формиатным буфером (рН 8.9) с последующей перекристаллизацией в 80% этаноле. Окончательная стадия очистки заключалась в колоночной ионообменной хроматографии на катионообменнике AG50WX 4, уравновешенным 0.3 М NH4-формиатным буфером с 0.045 М NH4Cl с ТСХ контролем при Rf 0.5. Данные по выделению инозина из КЖ штамма-продуцента представлены в виде спектров УФ-поглощения на рис. 4, а-в. Наличие в синтетическом образце (в) основной полосы поглощения I, соответствующей нативному инозину (lmax 249 нм, e249 7100 М-1 см-1) и отсутствие вторичных метаболитов II и III неоспоримо доказывает его однородность и тем самым эффективность разработанного метода выделения со степенью хроматографической чистоты 92%.
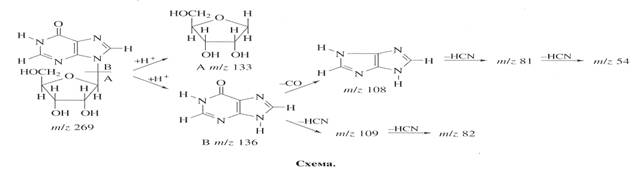
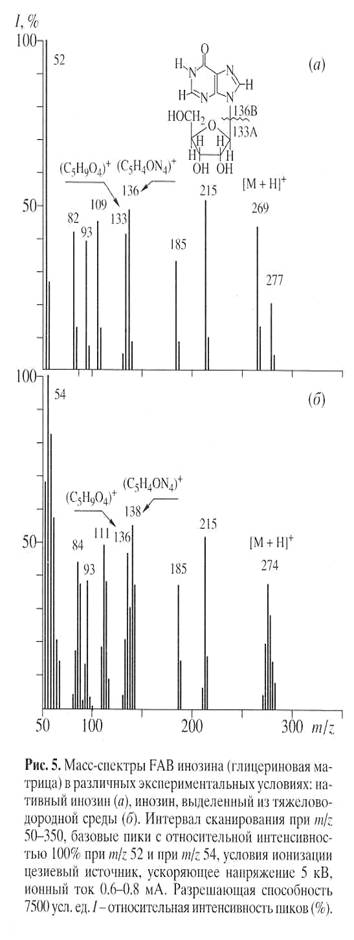
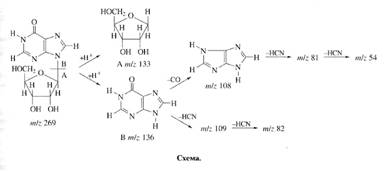
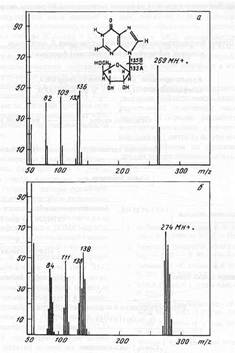
Уровень дейтерированности инозина исследовали методом масс-спектрометрии FAB из за высокой чувствительности, позволяющей детектировать 10-8-10-10 моль вещества в пробе, что существенно выше чем при использовании 1Н ЯМР-спектроскопии [7]. Пути фрагментации молекулы методом FAB приводят к распаду инозина на фрагмент рибозы А с Мr при массовом соотношении m/z 133 и гипоксантиновый фрагмент Б c Мr m/z 136 (их распад сопровождался миграцией протона Н+), который в свою очередь расщепляется на ряд менее низкомолекулярных осколочных фрагментов В, Г, Д, Е и Ж при m/z 109, 108, 82, 81 и 54 за счет элиминирования НСN и СО из гипоксантина (схема).
Биосинтетический 2Н-меченый инозин (масс-спектр приведен на рис. 5, б относительно контроля (а)), представлен смесью изотопнозамещенных форм молекул с различным количеством атомов водорода, замещенных на дейтерий. Подсчет уровня дейтерированности молекулы инозина определяли, сравнивая величины пиков молекулярных ионов Мr инозина дейтерированного и протонированного образцов (формирование пика молекулярного иона инозина сопровождалось миграцией протона Н+). Пик (М+Н)+ полиморфно расщеплялся на отдельные кластеры с примесью молекул со статистическим набором массовых чисел m/z с различным вкладом в суммарный уровень дейтерированности с включением четырех (m/z 273, 20%), пяти (m/z 274, 38%), шести (m/z 275, 28%) и семи атомов дейтерия (m/z 276, 14%) (табл. 4).
Суммарный уровень дейтерированности молекулы (УД), вычесленный по приводимой ниже формуле составил 61% от общего количества атомов водорода в углеродном скелете молекулы.
Mr1 C1 + Mr2 C2 + ....... +Mrn Cn
УД = ______________________________
S Cn
(Mr - величины пиков молекулярных ионов инозина; Сn - вклад в уровень дейтерированности, мол.%).
Анализ масс-спектра FAB выявил включение атомов дейтерия в рибозный и гипоксантиновый фрагменты молекулы, что подтверждено присутствием двух “тяжелых” пиков фрагментов рибозы А m/z 136, 46% (вместо m/z 133, 41%) и гипоксантина Б m/z 138, 55% (вместо m/z 136, 48%), а также пиков низкомолекулярных фрагментов, продуктов распада гипоксантина В m/z 111, 49% (вместо m/z 109, 45%) и Г m/z 84, 43% (вместо m/z 82, 41%) (рис. 5).
Таблица 4. Величины пиков (М+Н)+ в масс-спектрах FAB и уровни дейтерированности инозина
| Величина пика (М+Н)+
| Вклад в уровень дейтерированности, мол.% | Количество атомов дейтерия | Уровень дейтерированности, % от общего количества атомов водорода |
| 273 | 20 | 4 | 20.0 |
| 274 | 38 | 5 | 62.5 |
| 275 | 28 | 6 | 72.5 |
| 276 | 14 | 7 | 87.5 |
Эффект множественного мечения определяется способом получения дейтерированных молекул и свидетельствует о недостаточно высокой селективности биосинтетической схемы, повысить которую возможно контролем изотопного состава синтетической ростовой среды и исключения источников дополнительных протонов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Исследования проводили с генетически маркированным штаммом грамположительных бактерий Bacillus subtilis ВКПМ В-3157, продуцентом инозина, адаптированным к дейтерию рассевом до отдельных колоний на 2% агаре с 2Н2О и последующей селекции по признаку устойчивости к 2Н2О.
В работе использовали 2Н2О (99.9 ат.% 2Н), 2НСl (95.5 ат.% 2Н) и [U-2H]метанол (97.5 ат.% 2Н) (ЗАО Изотоп, Санкт-Петербург, РФ). Неорганические соли и D, L- глюкозу (Reanal, Венгрия) предварительно перекристаллизовывали в 2Н2О, 2H2O дистиллировали над перманганатом калия с последующим контролем изотопной чистоты 1Н ЯМР-спектроскопией на приборе Brucker WM-250 (ФРГ) (Частота 70 МГц). Масс-спектры электронного удара ЭУ получены на приборе МB-80A (Hitachi, Япония) с двойным фокусированием (энергия ионизирующих электронов 70 эВ, ускоряющее напряжение 8 кВ, температура катодного источника 180-2000С) после модификации в метиловые эфиры N-диметиламинонафталин-5-сульфонильных производных аминокислот по разработанной раннее методике [7]. Масс-спектры FAB получены на импульсном масс-спектрометре VG-70 SEQ (Fisons, VG Analitical, США), снабженным цезиевым источником Cs+ на глицериновой матрице с ускоряющем напряжением 5 кВ и ионным током 0.6-0.8 мА. УФ-спектры регистрировали на программируемом спектрофотометре Beckman DU-6 (США) в диапазоне длин волн 220-280 нм. Центрифугирование осуществляли на центрифуге Т-24 (ФРГ) с охлаждением при -40С. Аналитическую обращенно-фазовую ВЭЖХ проводили на жидкостном хроматографе Knauer (ФРГ), снабженным насосом Gilson (ФРГ) и рефрактометром Waters K-401 (ФРГ) на колонке Separon С18 (250 x10 мм), элюция смесью ацетонитрил : вода, 75 : 25, об.%, скорость элюирования 0.6 мл/мин. Ионообменную хроматографию осуществляли на катионообменной колонке Biotronic LC-5001 (ФРГ) (230 x 3.2) с сульфированной стирольной (7.25% сшивки) смолой UR-30 (Beckman-Spinco, США); рабочее давление 50-60 атм; скорость подачи Na+-цитратного буфера 18.5; нингидрина 9.25 мл/ч; детекция при 570 нм. Уровень биоконверсии углеродного субстрата определяли, используя глюкозооксидазу (КФ 1.1.3.4) как описано в работе [35].
Биосинтетический 2Н-меченый инозин. Получен с выходом 3.9 г/л на синтетической тяжеловодородной среде (89-90% ат. 2Н), используя в качестве источника 2Н-меченых ростовых субстратов гидролизат биомассы метанол-ассимилирующего штамма факультативных метилотрофных бактерий Brevibacterium methylicum ВКПМ B-5662 (условия получения: автоклавирование в 0.1 н. 2НСl30-40 мин при 08 ати), выделенный скринингом в условиях многостадийной адаптации на твердой среде М9 (2% агар) с 2% [U-2Н]метанолом со ступенчато увеличивающимся градиентом концентрации тяжелой воды (от 0 до 98% 2Н2О). Состав синтетической тяжеловодородной среды (мас.%): глюкоза - 12; 2Н-меченый гидролизат B. methylicum - 2; NH4NO3 - 2; MgSO4. 7H2O - 1; Са2СО3 - 2. Синтез проводили в колбах Эрленмейера вместимостью 500 мл (наполнение средой 100 мл) в течение 5-6 сут при 30-320С в условиях интенсивной аэрации реакционной смеси на орбитальном шейкере S-380 (Венгрия).
Очистка 2Н-меченого инозина. Пробы КЖ центрифугировали при 2000 g, 10 мин, концентрировали при 10 мм рт. ст., добавляли ацетон при 00С (3 x 5 мл). Смесь выдерживали 14-15 ч при -40С, осадок отделяли центрифугированием при 1200 g, 5 мин. К супернатанту добавляли 10 г активированного угля, выдерживали 2 сут при 40С. Водную фракцию отделяли фильтрованием, к твердой фазе добавляли 20 мл 50% этанола в 25% аммиаке (1 : 1, об.%), кипятили при 600С с обратным водяным холодильником. Через 2-3 ч смесь фильтровали и упаривали при 10 мм рт. ст. Продукт экстрагировали 0.3 М NH4-формиатным буфером (рН 8.9), промывали ацетоном (2 x 10 мл), сушили над безводным СaCl2. Инозин перекристаллизовывали из 80% этанола, очищали методом ионообменной хроматографии на откалиброванной колонке Biorad (150 x 10 мм) с катионообменной смолой АG50WX 4 (Pharmacia, США), уравновешенной 0.3 М NH4-формиатным буфером (рН 8.9) c 0.045 М NH4Cl в условиях изократической элюции (хроматографическая чистота 92%). Контроль чистоты проводили методом ТСХ с использованием стандартного набора рибонуклеозидов фирмы Beckman-Spinco (США) на хроматографических пластинках (150 x 150 мм) с закрепленным слоем флуоресцентного носителя Silufol UV-254 (Чехословакия) в системе растворителей: H-бутанол : уксусная кислота : вода, 2 : 1 : 1, об.%. Выход 2.5 г/л (64%). Т. пл. 68-700С. [a]D20 1.610 (с 1.5 этанол). Rf 0.5. рКa1.2 (фосфатный буфер, рН 6.87). УФ-спектр (0.1 н. НСl) (lmax 249 нм, e249 7100 М-1 см-1); FAB-спектр (глицериновая матрица Cs+, ускоряющее напряжение 5 кВ, ионный ток 0.6-0.8 мА): (M+H)+ m/z (I,%): 273, 20% (4 ат. 2Н); 274, 38% (5 ат. 2Н); 275, 28% (6 ат. 2Н); 276, 14% (7 ат. 2Н), (А + H)+ 136, 46%; (Б + Н)+ 138, 55%; (Б - НCN)+ 111, 49%; (В - HCN)+ 84, 43%.
СПИСОК ЛИТЕРАТУРЫ
1. Young V.R., Yu Y.M., Krempf M. Protein and amino acid turnover using the stable isotopes 15N, 13C, and 2H as probes. in: New techniques in nutritional research // Whitehead R. G. (ed). Acad. Press. N. Y. 1990. V. 9. Р. 17-72.
2. Hruby V.J. // Synth. and Appl. Isot. Label. Compounds. 1985. V. 4. ¹1. Р. 287-292.
3. Nelson J.E., Ruo T.I. // Clinica Chemica Acta. 1988. V. 175. ¹ 3. Р. 59-65.
4. Stockman B.J., Reily M.D., Westler W.M., Ulrich E.L., Markley J.L. // Biochemistry. 1989. V. 28. ¹ 7. Р. 230-236.
5. McIntosh L.P., Dahlquist F.W. // Quart. Rev. Biophys. 1990. V. 23. ¹ 1. Р. 1-38.
6. Argade P.V., Rothschild K.J., Kawamoto A.H., Herzfeld J., Herlihy W. C. // Proc. Natl. Acad. Sci. USA. 1981. V. 78. № 3. P. 1643-1646.
7. Мосин О.В., Складнев Д.А., Егорова Т.А., Швец В.И. // Биоорган. химия. 1996. Т. 22. ¹ 10-11. С. 856-869.
8. Darmaun D., Robert J. J., Bier D.M., Mathews D.E., Young V.R. // Annales-d’ Endocrinologie. 1985. V. 46. ¹ 4. Р. 355-356.
9. Shvets V.I., Yurkevich A.M., Mosin O.V., Skladnev D.A. // Karadeniz Journal of Medical Sciences, 1995. V. 8. ¹ 4. P. 231.
10. Fesik S.W., Zuderweg E.R.P. // Quart. Rev. Biophys. 1990. V. 23. № 2. Р. 97-131.
11. Мосин О. В., Складнев Д. А., Егорова Т. А., Швец В. И. //Биотехнология. 1996. № 10. С. 24-40.
12. Пшеничникова А.Б., Карнаухова Е.Н., Звонкова Е.Н., Швец В.И. // Биоорган. химия. 1995. Т. 21. ¹ 3. С. 163-178.
13. Daub G. H. Syntheses with stable isotopes. in: Stable Isotopes, Proc. of the 3d Intern. Conference // Klein E. R. (ed). Academic Press. N. Y. 1979. Р. 3-10.
14. van der Berg E.M.M., van Liemt, Willem B.S // Recl. Trav. Chim. Pays-Bas. 1989. V. 108. ¹ 9. Р. 304-313.
15. Walker T. E., Matheny C. // J. Org. Chem. 1986. V. 51. Р. 1175-1179.
16. Фалеев Н.Г., Рувинов С. В., Сапоровская Н. В., Беликов В. М., Закомырдина Л.Н. // Изв. Ан. СССР. Сер. хим. 1989. Т. 10. Вып. 3. С. 2341-2343.
17. LeMaster D. // Quart. Rev. Biophys. 1990. V. 23. ¹ 2. Р. 133-174.
18. Mosin O.V., Skladnev D.A., Shvets V.I. // Bioscience, biotechnology, and biochemistry. V. 62. ¹ 2. P. 225-229.
19. Crespi H.L., Marmur J., Katz J.J. // Nature. 1962. V. 84. ¹ 1. Р. 3489-3491.
20. Crespy H.L. Stable Isotopes in the Life Sciences. International atomic energy agency Press. Vienna. 1977. Р. 111-121.
21. Daboll H.F., Crespi H.L., Katz J.J. // Biotechnol. Bioengineer. 1962. V. 4. ¹ 5. Р. 281-297.
22. Cox J., Kyli D., Radmer R. // Trends Biotechnol. 1988. V. 6. № 12. Р. 279-282.
23. Мосин О.В., Складнев Д.А., Швец В.И. // Изв. РАН. Сер. биол. ¹ 3. С. 1-10.
24. Thomson J. F. Biological effects of deuterium. Pergamon Press. N. Y. 1963. P. 1-133.
25. Еремин В.А., Чекулаева Л.Н., Харатьян Е.Ф., Островский Д.Н. // Микробиология. 1978. Т. 32. Вып. 4. С. 629-636.
26. Busujima U.K., Shimiba S., Narita K., Okada S. // Chem. Pharm. Bull. 1988. V. 36. ¹ 4. P. 1828-1832.
27. Colby J, Dalton H. // Ann. Rev. Microbiol. 1979. V.33. ¹ 6. P.481-517.
28. Karnaukhova E.N., Reshetova O.S., Semenov S.Y., Skladnev D.A., Tsygankov Y.D. // Amino Acids. 1994. V.6. ¹ 2. P.165-176.
29. Skladnev D.A., Tsygankov Y.D. Convertion of stable isotope labeled methanol to components of bacterial biomass, in: 6 th Eur. Conf. of Biomass for Energy. Athens. Greece, 1991. P. 234.
30. Мосин О.В., Складнев Д.А., Егорова Т.А., Швец В.И. // Биотехнология. 1996. № 3. С. 3-12.
31. Складнев Д.А., Мосин О.В., Егорова Т.А., Еремин С.В., Швец В.И. // Биотехнология. 1996. № 5. С. 25-34.
32. Мосин О.В., Казаринова Л.А., Преображенская К.А., Складнев Д.А., Чеботаев Д.В., Юркевич А.М., Швец В.И. // Биотехнология. 1996 г. № 4. C. 19-27.
33. Мосин О.В., Карнаухова Е.Н., Пшеничникова А.Б.,Складнев Д.А., Акимова О.Л. // Биотехнология. 1993. № 9. С. 16-20.
34. Зорина А.В, Бабусенко Е.С. Химический состав биомассы метилотрофных бактерий. Современные проблемы биотехнологии микроорганизмов. // Тезисы докл. молодых ученых. Рига. 1987. Т. 1. № 2. С.35-40.
35. Полюдек-Фабини Р., Бейрих Т. Органический анализ. Руководство по анализу органических соединений. Л.: Химия, 1981. 514 c.
THE BIOSYNTHESIS OF 2H-LABLED INOSINE WITH HIGH LEVEL OF DEUTERIUM ENRICHMENT
О. V. MOSIN
Мoscow State Academy of Fine Chemical Technology named after М.V. Lomonosov, 117571 Moscow, Vernadskogo Pr., 86;
The biosynthesis of 2Н-labeled purine ribonucleoside inosine (yeald 3/9 g/l) with using an adapted to deuterium strain of Bacillus subtilis on heavy water medium with highly level of deuteration (89-90 at.% 2H2O), containing 2% hydrolyzate of biomass of methylotrophic bacterium Brevibacterium methylicum as a source of 2H-labeled growth substrates (the biosynthetic conditions: synthetic medim M9 with 98% 2Н2O and 2% [U-2Н]methanol, the incubation period 5-6 days at 370C) was carried out. The studyng of the level of deuterium enrichment of inosine by a method of FAB mass-spectrometry found out the polymorhysm of isotopic introduction into the molecule (isotopic composition of inosine: 4 at. 2H, 20%, 5 at. 2H, 38%, 6 at. 2H, 28%, 7 at. 2H, 14%) with deuterium introduction to ribose and hypoxantinefragments of the molecule.
Похожие работы
... . Так, в Phe детектировалось 80,5 % метки, в Ala - 95 %, в Gly - 90% (см. табл. 6). Во всех экспериментах степени включения дейтерия и изотопа углерода 13С в метаболически связанных аминокислотах обнаружили определённую коррелляцию. Так, степени изотопного обогащения валина и лейцина (семейство пирувата), фснилаланина и тирозина (семейство ароматических аминокислот} совпадают (табл. 6). Степени ...
... . Преимущества разработанного метода получения высокодейтерированного инозина заключаются в следующих аспектах: -1. В способности штамма B. subtilis к росту и биосинтезу инозина на среде, содержащей максимальные концентрации тяжелой воды. -2. Замене необходимых для роста бактерий субстратов на гидролизаты дейтерий-меченной биомассы метилотрофных бактерий Brevibacterium methylicum. При ...
... Methylobacillus flagellatum, галофильные бактерии Halobacterium methylicum и бациллы Bacillus subtilis. Целью настоящей работы было исследование процесса физиологической адаптации этих продуцентов БАС при росте на средах, содержащих максимальные концентрации тяжёлой воды. Поскольку биосинтетический потенциал используемых штаммов при росте на тяжелой воде к началу проведения данной работы ...
0 комментариев