Навигация
Типы химических связей. Электростатическая, ковалентная связь. Ковалентная связь в органических соединениях. Строение метана. Строение молекул с N, O-атомами с неподеленной парой электронов. Строение и физико-химические свойства органических соединений.
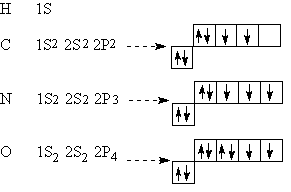
Связь между частицами лучше всего определять через энергию, которую система теряет при образовании соединения - аддукта.
1. Электростатическая связь
1.1 Ионная связь
1.2 Ион-дипольное взаимодействие
1.3 Диполь-дипольное взаимодействие
ИОННАЯ СВЯЗЬ
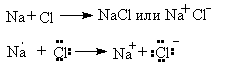
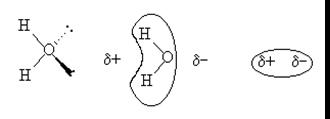
Ион-дипольное взаимодействие
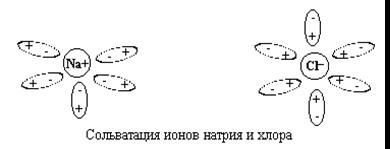
Диполь-дипольное взаимодействие
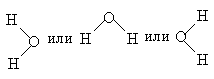
2. КОВАЛЕНТНАЯ СВЯЗЬ - связь, образованная двумя электронами
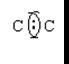
Переход от ковалентной связи к ионной
| ковалентная связь | полярная ковалентная связь | ионная связь |
| А:А | d+В:Аd- | М+ А- |
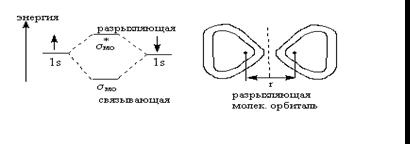
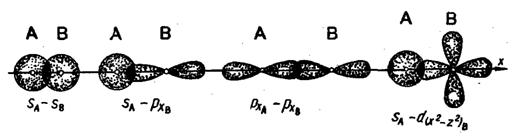
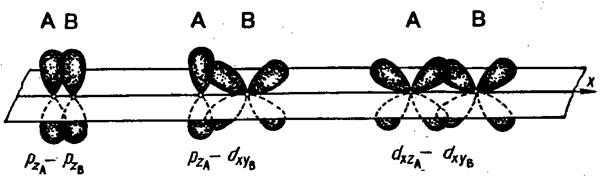
2.1 Молекулярные орбитали - атомные орбитали
Молекула водорода Н2
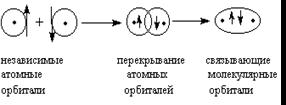
Длина связи
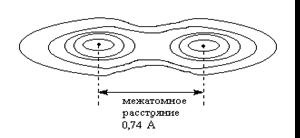
Энергетическая диаграмма для разрыхляющей и связывающей орбиталей
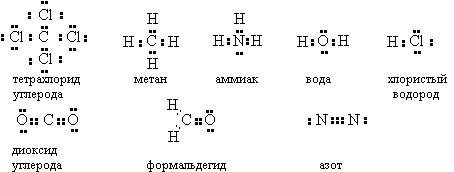
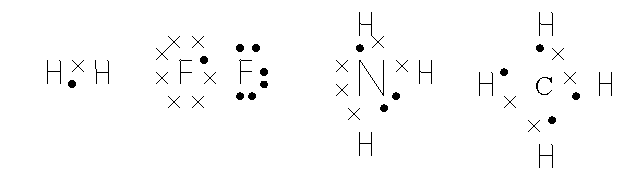
3. Структуры Льюиса
Связь между атомами обеспечивается электронными парами (американский химик Джилберт Льюис)
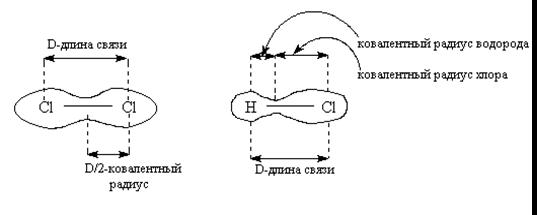
4. Некоторые свойства ковалентных связей (длина связи, полярность связи и энергия связи)
4.1 Длина связи
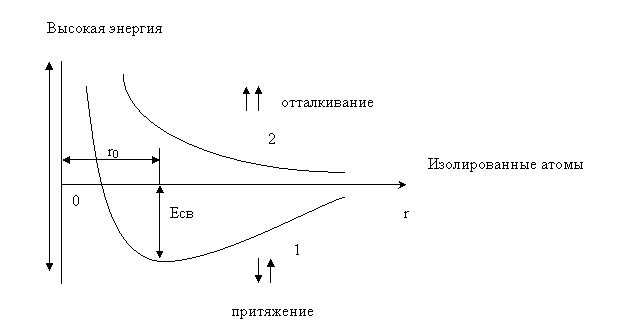
Минимальное расстояние между атомами отвечает минимальной потенциальной энергии системы.
Кривая потенциальной энергии (энергетический профиль)
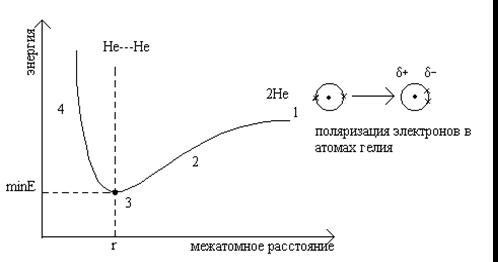
2 - участок притяжения, вызванного индуцированной поляризацией (дисперсионые силы Лондона).
Половина расстояния, разделяющего атомы в точке 3, соответствует вандерваальсову радиусу.
Вандерваальсовы радиусы
| Атом или группа | Вандерваальсов радиус, Е |
| Br | 1,35 |
| CH2 | 2,0 |
| CH3 | 2,0 |
| Cl | 1,8 |
| F | 1,35 |
| H | 1,2 |
| I | 2,15 |
| N | 1,15 |
| O | 1,4 |
Похожие работы
... воздействие. Принцип Ле Шателье – Брауна является одним из следствий второго начала термодинамики и применим к любым макроскопическим системам, находящимся в состоянии истинного равновесия. Типы химических связей На этой концептуальной основе была разработана стройная атомно-молекулярная теория того времени, которая впоследствии оказалась не в состоянии объяснить многие экспериментальные ...
... а в группах – их падения. Элементы по электроот-рицательностям располагают в ряд, на основании которого можно сравнить электроотрицательности элементов, находящихся в разных периодах. Тип химической связи зависит от того, насколько велика разность значений электроотрицательностей соединяющихся атомов элементов. Чем больше отличаются по электроотрицательности атомы элементов, образующих связь, тем ...
... кислот. Это свидетельствует о наличии специфического взаимодействия между молекулами Н2О, молекулами HF. Такое взаимодействие должно затруднять отрыв молекул друг от друга, т.е. уменьшать их летучесть, а, следовательно, повышать температуру кипения соответствующих веществ. Вследствие большой разницы в ЭО химические связи H–F, H–O, H–N сильно поляризованы. Поэтому атом водорода имеет положительный ...
... научных подходов для объяснения химической связи – метода валентных связей и метода молекулярных орбиталей. Оба метода не взаимоисключают, а дополняют друг друга и позволяют трактовать процесс формирования химической связи и выяснить внутреннее строение веществ. Различают три основных (модельных) типа химической связи: ковалентную, ионную и металлическую связи. Эти типы химической связи не ...

0 комментариев