Навигация
Разработка способа снижения концентрации серы в силикомарганце
3. Разработка способа снижения концентрации серы в силикомарганце
3.1 Источники серы и титана при выплавке силикомарганца
Основным источником серы при выплавке силикомарганца является кокс из донецких углей. Массовая доля серы в них составляет 1,5-1,8%. В концентратах II сорта, используемых в производстве силикомарганца массовая доля серы по анализам Марганцевого и Ордженикидзевского ГОКов находится в пределах 0,046-0,053%. При агломерации концентратов содержание серы в готовом продукте достигает 0,17-0,20%. Доля концентратов в этой общей сумме составляет около 25%, оставшиеся 75% приходятся на коксовую мелочь.
При использовании одного агломерата в качестве марганцевого сырья количество серы, вносимое шихтой на тонну силикомарганца, составляет около 12,5-13,0 кг.
На Запорожском заводе вследствие использования смеси агломерата и концентрата в соотношении 1:1 эта масса вносимой серы уменьшается до 10,0-10,5 кг. По содержанию двуокиси титана в шихтовых материалах и продуктах их плавки информация весьма ограничена. Ее содержание в лучшем случае определяется в среднегодовых пробах материалов.
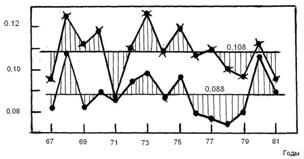
Рис.3.1 Динамика изменения содержания двуокиси титана в концентратах II сорта двух рудников марганцевого ГОКа
По марганцевым ГОКам массовая доля TiO2 в концентратах определялась до 1982 г. Динамика ее изменения по двум рудникам марганецкого ГОКа приведена на рис.3.1. по Орджоникидзевскому ГОКу результаты предыдущих анализов не сохранились.
На основании приведенных данных можно заключить, что существует значительное расхождение до 20-22% массовой доли двуокиси титана в концентратах различных рудников. При этом по годам не наблюдалось тенденции ее повышения в концентратах.
Негативной стороной качества марганцевых концентратов является понижение в них концентрации марганца и особенно в последние годы с 1991 по 1995 г.
По среднегодовым усредненным по двум ГОКам анализам понижение содержания марганца в прокаленных концентратах II сорта за эти годы вполне удовлетворительно описывается зависимостью:
![]() , (3.1)
, (3.1)
с коэффициентом корреляции близким единице.
Вследствие этого изменения происходит увеличение количества двуокиси титана на единицу марганца, вносимого в шихту силикомарганца, и, следовательно, на тонну получаемого сплава.
Кроме марганцевого сырья, титан в шихты вносится коксом и кварцитом. По данным УХИНа массовая доля TiO2 в золе кокса составляет 0,6-0,8%, в кварцитах – 0,08-0,10% [29].
С учетом расхода марганцевых концентратов и коксовой мелочи на тонну агломерата II сорта массовая доля TiO2 должна составлять 0,12-0,14%.
На базе приведенных данных и удельных расходов шихтовых материалов расчетный баланс титана выглядит следующим образом. На тонну силикомарганца в условиях НЗФ вносится шихтовыми материалами 3,6-4,3 кг двуокиси титана. Из них 75-77% – агломератом, 13-15% – коксом, остальное (около 10-11%) – кварцитом.
В условиях ЗФЗ на тонну силикомарганца шихтой вносится 3,2-4,1 кг TiO2.
Распределяется титан преимущественно в два продукта плавки: в сплав 50-55% и в шлак 45-50%.
Различия в количествах серы и двуокиси титана, вносимых шихтовыми материалами на тонну силикомарганца на НЗФ и ЗФЗ, отражаются на качестве сплава. На Запорожском заводе случаи получения силикомарганца с массовой долей серы до 0,03% существенно реже, чем на Никопольском.
3.2 Вероятная модель взаимодействия серы с оксидами
Наиболее вероятно взаимодействие серы с восстанавливаемыми оксидами происходит через газовую фазу. Такое предположение основано на результатах проведенных экспериментов. При нагреве кокса (а им вносится основная масса серы в шихты) происходит уменьшение содержания в нем серы:
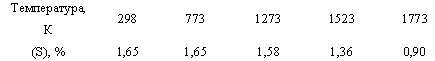
Причем заметное удаление серы наблюдается при температурах выше 1000○С, что закономерно, поскольку в коксовых батареях смесь углей коксуется при 1000-1100○С с максимально возможным удалением серы.
По результатам опытов относительное уменьшение серы в коксе удовлетворительно описывается зависимостью:
![]() ; (3.2)
; (3.2)
где Т – температура, К.
По ней практически полное удаление серы из кокса должно завершаться к 2039К (1766○С). По инструментальным замерам [30] этот уровень температур 1700-1800○С достигается в нижних горизонтах силикомарганцевых печей.
В процессе нагрева в коксе термодинамически возможны реакции перехода серы в газовую фазу:
C + 2S(т) = CS2 (3.3)
![]() G3.3 = 27740 – 40,20Т
G3.3 = 27740 – 40,20Т
2S(T) = S2(Г) (3.4)
![]() G3.4 = 30477 – 39,24Т
G3.4 = 30477 – 39,24Т
CO + S(T) = COS (3.5)
![]() G3.5 = - 6663 – 0,47Т
G3.5 = - 6663 – 0,47Т
Одновременно с этим процессом газификации серы в шихте происходит плавление марганцевого сырья [31]. Образующийся рудный сплав к 1250-1300○С приобретает высокую жидкоподвижность и вытекает из шихты. При этом в нем почти полностью растворяется кварцит [32].
Двуокись титана может переходить в рудный сплав в виде соединения с марганцем Mn2TiO4 с температурой плавления 1455○С [33].
Восстановление оксидов с образованием силикомарганца протекает из жидкой фазы на поверхности кокса. Поэтому и взаимодействие серы с восстанавливаемыми оксидами происходит в присутствии углерода.
Для оценки возможности образования сульфидов и карбидов титана и марганца воспользуемся приближенным методом расчета равновесия реакций [34]. Более точные расчеты невозможны из-за отсутствия установленных теплот плавления сульфидов и карбидов титана.
Результаты расчетов приведены на рис.3.2 и 3.3.
Из сульфидов титана термодинамически более вероятны реакции образования TiS2, нежели TiS. На рис.3.2 приведено изменение константы равновесия только реакции:
TiO2 + COS + 2C = TiS + 3CO (пунктир) (3.6)
Относительно образования TiS2 с участием сероокиси (реакция 1) одинаковая величина lnКр достигается для реакции образования TiS при более высокой температуре. Аналогичные смешения получаются по другим возможным реакциям.
В то же время образование TiS2 является, по-видимому, суммарной реакцией:
TiO2 + COS + 2C = TiS + 3CO (3.7)
TiS + COS = TiS2 + CO .
TiO2 + 2COS + 2C = TiS2 + 4CO
Термодинамически невозможна реакция образования сульфида титана без участия углерода (реакция 4). Также маловероятно протекание реакции образования карбида титана при участии сернистых соединений в качестве восстановителей (реакция 4). При температурах ниже 1500 К газообразные соединения серы могут разрушать карбид титана с образованием сульфидов (реакция 7). Однако при более высоких температурах может протекать реакция с одновременным образованием сульфида и карбида титана (реакция 6).
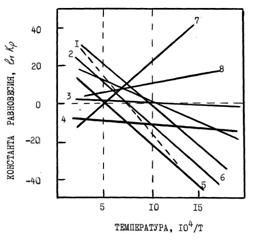
Рис.3.2 Равновесие реакций образования сульфидов и карбидов титана
Вертикальные пунктирные линии – интервал температур выделения серы из кокса
1. TiO2 + 2COS + 2C = TiS2 + 4CO;
2. TiO2 + S2 + 2C = TiS2 + 2CO;
3. TiO2 + 2CS2 = TiS2 + 2COS;
4. TiO2 + 3/2S2 = TiS2 + SO2;
5. TiO2 + CS2 + 2C = TiC + 2COS;
6. TiO2 +1/2CS2 + 2C = 1/2TiC + 1/2TiS2 = 2CO;
7. TiC + CS2 = TiS2 + 2C;
8. MnO + 1/2TiS2 = MnS + 1/2TiO2.
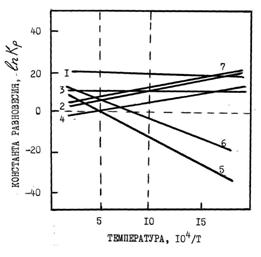
Рис.3.3 Равновесие реакций образования сульфидов и карбидов марганца
Вертикальные пунктирные линии – интервал температур выделения серы из кокса
0 комментариев