Навигация
Дихотомический распад глюкозы до стадии ПВК, полностью совпадающий с реакциями гликолиза
1. Дихотомический распад глюкозы до стадии ПВК, полностью совпадающий с реакциями гликолиза.
2. Окислительное декарбоксилирование ПВК, завершающееся образованием ацетил-КоА.
3. Цикл Кребса, в котором ацетил-КоА расходуется на образование СО2 и субстратов тканевого дыхания, используемых дыхательной цепью митохондрий.
Подчеркнем, что, в отличие от первого этапа, остальные два требуют аэробных условий и протекают в митохондриях.
Окислительное декарбоксилирование пирувата
Пируват, образовавшийся в реакциях гликолиза (в цитоплазме), должен быть транспортирован в митохондрии. Транспорт осуществляется специальной «челночной» системой. В матриксе митохондрии, прикрепившись к ее внутренней мембране, находится сложный полиферментный комплекс – пируватдегидрогеназа.
Пируватдегидрогеназа состоит из 60 полипептидных цепей, которые можно разделить на 3 основных фермента: Е1 – собственно пируватдегидрогеназа (состоит из 24 субъединиц); Е2 – дигидролипоилтрансацетилаза (также 24 субъединицы); Е3 – дигидролипоилдегидрогеназа (12 субъединиц).
Е1 катализирует декарбоксилирование ПВК с участием кофермента тиаминпирофосфата (ТПФ). Образовавшийся продукт реакции (гидроксиэтильное производное ТПФ) при участии Е2 реагирует с окисленной липоевой кислотой(ЛК). Липоевая кислота – низкомолекулярное азотсодержащее соединение – является коферментом Е2.
![]() CH2
CH2
СН2 СН – (СН2)4 – СООН
S – S
Липоевая кислота.
Дисульфидная группа ЛК способна восстанавливаться и ацетилироваться. В реакции, катализируемой дигидролипоилтрансацетилазой (Е2 ), образуется ацетиллипоевая кислота. Далее это соединение реагирует с коэнзимом А (КоА-SH не является собственным коферментом Е2) – при этом образуется восстановленная форма ЛК (дигидролипоевая кислота) и ацетил-КоА.
Наконец, начинает функционировать Е3 , коферментом которого является ФАД: кофермент окисляет дигидролипоевую кислоту и сам при этом восстанавливается (ФАДН2) . Восстановленный флавиновый кофермент реагирует с митохондриальным НАД+, в свою очередь, восстанавливая его (НАДН ·Н+).
Таким образом, в окислительном декарбоксилировании ПВК участвует фактически три фермента, составляющих единый пируватдегидрогеназный комплекс, и 5 коферментов: ТПФ, ЛК и ФАД – собственные коферменты комплекса, КоА-SH и НАД+ – внешние, приходящие “извне”. Образующийся ацетил-КоА затем окисляется в цикле Кребса, а водород с НАДН ·Н+ поступает в дыхательную цепь митохондрий.
Пируватдегидрогеназа отличается большим отрицательным редокс-потенциалом, который способен обеспечить не только восстановление НАД+, но и способствовать образованию высокоэнергетической тиоэфирной связи в ацетил-КоА (СН3-СО~ SкоА).
При недостаточном содержании в диете входящих в состав пируватдегидрогеназы витаминов, в первую очередь тиамина, активность фермента снижается. Это приводит к накоплению в крови и тканях пирувата и лактата и развитию метаболического ацидоза. При выраженном дефиците тиамина развивается некомпенсированный ацидоз, который без лечения приводит к летальному исходу.
Регуляция активности пируватдегидрогеназы
Пируватдегидрогеназный комплекс может существовать в активной и неактивной формах. Переход одной формы в другую осуществляется путем обратимого фосфорилирования с участием киназы и дефосфорилирования с участием фосфатазы. При этом фосфорилированная форма является неактивной, а дефосфорилированная – активной .
При низкой концентрации инсулина и высоком уровне энергообеспеченности клетки (↑АТФ, ↑ ацетил-КоА и ↑ НАДН·Н+) этот комплекс находится в неактивном состоянии. Активирование пируватдегидрогеназного комплекса индуцируется инсулином, КоА-SН, пируватом, АДФ и ионами магния.
Цикл Кребса – центральный путь обмена веществ
Этот метаболический путь назван именем открывшего его автора – Г.Кребса, получившего (совместно с Ф. Липманом) за данное открытие в 1953 г. Нобелевскую премию. В цикле лимонной кислоты улавливается большая часть свободной энергии, образующейся при распаде белков, жиров и углеводов пищи. Цикл Кребса – центральный путь обмена веществ.
NB! Функции цикла трикарбоновых кислот многообразны
· Интегративная – цикл Кребса является центральным метаболическим путем, объединяющим процессы распада и синтеза важнейших компонентов клетки.
· Анаболическая – субстраты цикла используются для синтеза многих других соединений: оксалацетат используется для синтеза глюкозы (глюконеогенез) и синтеза аспарагиновой кислоты, ацетил-КоА – для синтеза гема, α-кетоглутарат – для синтеза глютаминовой кислоты, ацетил-КоА – для синтеза жирных кислот, холестерола, стероидных гормонов, ацетоновых тел и др.
· Катаболическая – в этом цикле завершают свой путь продукты распада глюкозы, жирных кислот, кетогенных аминокислот – все они превращаются в ацетил-КоА; глутаминовая кислота – в α-кетоглутаровую; аспарагиновая – в оксалоацетат и пр.
· Собственно энергетическая – одна из реакций цикла (распад сукцинил-КоА) является реакцией субстратного фосфорилирования. В ходе этой реакции образуется одна молекула ГТФ (реакция перефосфорилирования приводит к образованию АТФ).
· Водороддонорная – при участии трех НАД+-зависимых дегидрогеназ ( дегидрогеназ изоцитрата, α-кетоглутарата и малата) и ФАД-зависимой сукцинатдегидрогеназы образуются 3 НАДН∙Н+ и 1 ФАДН2. Эти восстановленные коферменты являются донорами водорода для дыхательной цепи митохондрий, энергия переноса водородов используется для синтеза АТФ.
· Анаплеротическая – восполняющая. Значительные количества субстратов цикла Кребса используются для синтеза разных соединений и покидают цикл. Одной из реакций, восполняющих эти потери, является реакция, катализируемая пируваткарбоксилазой.
NB! Скорость реакция цикла Кребса определяется энергетическими потребностями клетки
Скорость реакций цикла Кребса коррелирует с интенсивностью процесса тканевого дыхания и связанного с ним окислительного фосфорилирования – дыхательный контроль. Все метаболиты, отражающие достаточное обеспечение клетки энергией являются ингибиторами цикла Кребса. Увеличение соотношения АТФ/АДФ –показатель достаточного энергообеспечении клетки и снижает активность цикла. Увеличение соотношения НАД+/ НАДН, ФАД/ ФАДН2 указывает на энергодефицит и является сигналом ускорения процессов окисления в цикле Кребса. Основное действие регуляторов направлено на активность трех ключевых ферментов: цитратсинтазы, изоцитратдегидрогеназы и a-кетоглутаратдегидрогеназы. Аллостерическими ингибиторами цитратсинтазы являются АТФ, жирные кислоты. В некоторых клетках роль ее ингибиторов играют цитрат и НАДН. Изоцитратдегидрогеназа аллостерически активируется АДФ и ингибируется при повышении уровня НАДН+Н+.
Последний является ингибитором и a-кетоглутаратдегидрогена, активность которой снижается также при повышении уровня сукцинил-КоА.
Активность цикла Кребса во многом зависит от обеспеченности субстратами. Постоянная “утечка” субстратов из цикла (например, при аммиачном отравлении) может вызывать значительные нарушения энергообеспеченности клеток.
NB! Пентозофосфатный путь окисления глюкозы обслуживает восстановительные синтезы в клетке.
Как видно из названия, в этом пути образуются столь необходимые клетке пентозофосфаты. Поскольку образование пентоз сопровождается окислением и отщеплением первого углеродного атома глюкозы, то этот путь называется также апотомическим (apex – вершина).
Пентозофосфатный путь можно разделить две части: окислительную и неокислительную. В окислительной части, включающей три реакции, образуются НАДФН∙Н+ и рибулозо-5-фосфат. В неокислительной части рибулозо-5-фосфат превращается в различные моносахариды с 3, 4, 5, 6, 7 и 8 атомами углерода; конечными продуктами являются фруктозо-6-фосфат и 3-ФГА.
· Окислительная часть. Первая реакция–дегидрирование глюкозо-6-фосфата глюкозо-6-фосфатдегидрогеназой с образованием δ-лактона 6-фосфоглюконовой кислоты и НАДФН∙Н+ (НАДФ+ – кофермент глюкозо-6-фосфатдегидрогеназы).
Вторая реакция – гидролиз 6-фосфоглюконолактона глюконолактонгидролазой. Продукт реакции – 6-фосфоглюконат.
Третья реакция – дегидрирование и декарбоксилирование 6-фосфоглюконолактона ферментом 6-фосфоглюконатдегидрогеназой, коферментом которого является НАДФ+. В ходе реакции восстанавливается кофермент и отщепляется С-1 глюкозы с образованием рибулозо-5-фосфата.
· Неокислительная часть. В отличие от первой, окислительной, все реакции этой части пентозофосфатного пути обратимы
Транскетолаза (кофермент – тиаминпирофосфат) отщепляет двухуглеродный фрагмент и переносит его на другие сахара (см. схему). Трансальдолаза переносит трехуглеродные фрагменты.
В реакцию вначале вступают рибозо-5-фосфат и ксилулозо-5-фосфат. Это – транскетолазная реакция: переносится 2С-фрагмент от ксилулозо-5-фосфата на рибозо-5-фосфат.
Затем два образовавшиеся соединения реагируют друг с другом в трансальдолазной реакции; при этом в результате переноса 3С-фрагмента от седогептулозо-7-фосфата на 3-ФГА образуются эритрозо-4-фосфат и фруктозо-6-фосфат.Это F-вариант пентозофосфатного пути. Он характерен для жировой ткани.
Однако реакции могут идти и по другому пути. Этот путь обозначается как L-вариант. Он протекает в печени и других органах. В этом случае в трансальдолазной реакции образуется октулозо-1,8-дифосфат.
Общее уравнение окислительной и неокислительной частей пентозофосфатного пути можно представить в следующем виде:
![]() 6 Глюкозо-6-Ф + 7Н2О + 12 НАДФ+ 5 Пентозо-5-Ф + 6СО2 + 12 НАДФН∙Н+ + Фн.
6 Глюкозо-6-Ф + 7Н2О + 12 НАДФ+ 5 Пентозо-5-Ф + 6СО2 + 12 НАДФН∙Н+ + Фн.
Значение пентозофосфатного пути окисления глюкозы
Частью анаболических процессов являются так называемые восстановительные синтезы. В этих реакциях синтез вещества сопровождается потреблением восстановительных эквивалентов, ведущую роль среди которых, играет НАДФН+Н+. Роль донора данной формы восстановительных эквивалентов и выполняет пентозофосфатный путь. Синтез жирных кислот, аминокислот, стероидных гормонов - вот неполный перечень таких потребителей водородов НАДФН+Н+. В тканях, где интенсивно протекают данные реакции, активны и ферменты пентозофосфатного пути. К таким тканям относятся: надпочечники, печень, жировая ткань, лактирующая молочная железа. Особую функцию несет пентозофосфатный путь в эритроцитах, где водороды НАДФН+Н+ используется для защиты этих клеток от повреждающего действия активными формами кислорода (супероксидным анион-радикалом и пероксидом водорода).
Недостаточность глюкозо-6-фосфатдегидрогеназы является наиболее частым дефектом ферментативных систем эритроцита. Насчитывается около 100 миллионов жителей нашей планеты с недостаточностью этого фермента. Многие из этих случаев вызваны генетическими изменениями структуры фермента (изоферменты с различной активностью). Проявления зависят от степени повреждения фермента: люди могут испытывать постоянный окислительный стресс, но бывает и безсимптомное течение. В тяжелых случаях заболевание проявляется в форме гемолитической анемии и хронического течения инфекционных заболеваний.
Некоторые лекарственные препараты, обладающие свойствами окислителей, могут усиливать окислительный стресс, так как стимулируют образование активных форм кислорода. У людей с недостаточностью глюкозо-6-фосфатдегидрогеназы лечение этими препаратами может сопровождаться усиленным гемолизом.
Если в эритроцитах НАДФН+Н+ используется для борьбы с активными формами кислорода, то фагоцитирующие клетки используют НАДФН+Н+ для получения супероксидных анион-радикалов и других активных форм кислорода, которые играют основную роль в разрушении поглощенных бактериальных клеток. Образование супероксидного анион-радикала катализирует НАДФН-оксидаза. Эта реакция сопровождается образованием “осколка молекулы кислорода” (О2.-) и запускается, когда фагоцитирующая клетка заглатывает бактерию. Кислород, поглощаемый фагоцитами, используется на генерацию О2.-.
НАДФН + 2О2 ¾® 2 О2.- + НАДФ+ + Н+
Хронический грануломатоз - наследственное заболевание, возникающее по причине дефицита НАДФН-оксидазы. Фагоциты таких людей не способны в достаточном количестве генерировать О2.- для разрушения поглощенных микроорганизмов.
Велико значение пентозофосфатного пути как поставщика рибозы-5-фосфата, необходимого для построения мононуклеотидов (АМФ, АДФ, АТФ, ГМФ и т.д.), олигонуклеотидов, коферментов (ФМН, ФАД, НАД, НАДФ), нуклеиновых кислот.
Следует заметить, что НАДФН∙Н+, в отличие от НАДН∙Н+, не является донором водородов для митохондриальной цепи ферментов. Для передачи его водородов в дыхательную цепь используются специальные трансдегидрогеназные реакции.
Регуляция. Главными регулируемыми (ключевыми) ферментами пентозофосфатного пути являются две дегидрогеназы его окислительной части: глюкозо-6-фосфатдегидрогеназа и дегидрогеназа 6-фосфоглюконата. Индукторами биосинтеза этих ферментов является инсулин. Активность дегидрогеназ увеличивается при поступлении углеводов в организм и снижается при голодании и диабете.
Глюкуроновый путь обмена глюкозы
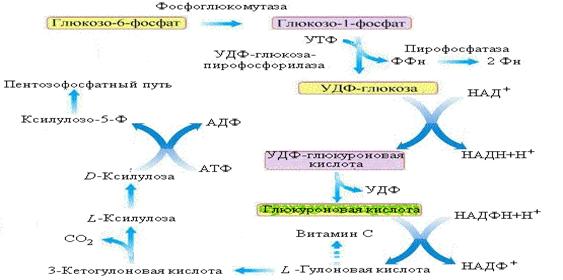
Рис. Глюкуроновый путь обмена глюкозы
Начальный этап пути аналогичен реакциям синтеза гликогена. Далее УДФ-глюкоза окисляется дегидрогеназой в УДФ-глюкуроновую кислоту, которая, теряя УДФ, превращается в глюкуроновую кислоту. В следующей реакции глюкуроновая кислота восстанавливается НАДФ-зависимой дегидрогеназой до L-гулоновой кислоты. Последняя в организме человека, приматов, морских свинок и некоторых птиц окисляется до 3-кетогулоновой кислоты, которая, декарбоксилируясь, превращается в L-ксилулозу. В организме большинства животных гулоновая кислота служит предшественником витамина С.
Ксилулоза может включаться в пентозофосфатный путь обмена углеводов, однако только в виде D-изомера. Изомеризация L-формы в D-форму осуществляется НАДФ-зависимыми дегидрогеназами через стадию образования спирта ксилитола. При отсутствии этих ферментов в моче резко увеличивается концентрация L-ксилулозы – синдром идиопатической пентозурии (довольно редкое наследственное заболевание).
Значение глюкуронового пути. В клетках организма глюкуроновая кислота используется для синтеза глюкозаминогликанов (гиалуроновой кислоты, хондроитинсульфатов, гепарина). УДФ-глюкуроновая кислота, связывая продукты метаболизма (например, стероидные гормоны) и чужеродные вещества (лекарственные препараты и другие ксенобиотики) в виде водорастворимых глюкуронидов легко экскретируется с желчью и мочой.
NB! Фруктоза и галактоза превращаются в глюкозу
Фруктоза образуется в кишечнике при гидролизе сахарозы сахаразой; кроме того, в состав фруктов и меда входит свободная фруктоза, которая легко всасывается. Поступая с током крови в различные органы, фруктоза подвергается следующим превращениям.
1. Фосфорилируется гексокиназой с образованием фруктозо-6-фосфата, который изомеризуется в глюкозо-6-фосфат – центральный метаболит обмена глюкозы. У человека фруктоза в свободном, т.е. нефосфорилированном виде, находится только в семенной жидкости.
Похожие работы
... α,d – глюкоза глюкозо – 6 – фосфат С образованием глюкозо – 6 – фосфата пути гликолиза и гликогенолиза совпадают. Глюкозо – 6 – фосфат занимает ключевое место в обмене углеводов. Он вступает в следующие метаболические пути: глюкозо – 6 – фосфат глюкоза + Н3РО4 фруктозо – 6 – фосфат пентозный путь распада (поступает в кровь и др. ...
... . Динамика химических превращений, происходящих в клетках, изучается биологической химией. Задачей физиологии является определение общих затрат веществ и энергии организмом и того, как они должны восполняться с помощью полноценного питания. Энергетический обмен служит показателем общего состояния и физиологической активности организма. Единица измерения энергии, обычно применяемая в биологии и ...
... образом, углеводы необходимы для рационального использования белков. Они также способны стимулировать окисление промежуточных продуктов обмена жирных кислот. Этим, однако, не исчерпывается роль углеводов. Они являются составной частью молекул некоторых аминокислот, участвуют в построении ферментов, образовании нуклеиновых кислот, являются предшественниками образования жиров, иммуноглобулинов, ...
... хирургического лечения, иногда в сочетании с введением радиоактивного йода. Этот вид рака чаще встречается у лиц, перенесших облучение головы и шеи. Особенности гормональной регуляции обмена углеводов при мышечной деятельности. На любой процесс жизнедеятельности организма расходуется энергия. Эта энергия образуется в результате распада различных химических веществ - углеводов, жиров (реже - ...

0 комментариев