Навигация
Расчёт теплового эффекта реакции
2.1 Расчёт теплового эффекта реакции
Расчёт теплового эффекта реакции в изобарном процессе в стандартных условиях
ΔНr˚ (298) = (ΔНf˚ (298)CdSO4 + ΔНf˚ (298)H2O) – (ΔНf˚ (298)CdO + ΔНf˚ (298)H2SO4)
ΔНr˚ (298) = (-934,41 – 241,81) – (-258,99 – 813,99) = -103,24 кДж.
Вывод: При реакции в стандартных условиях ,произошло выделение тепла в количестве 103,24 кДж как следствие реакция является экзотермической.
Расчёт теплового эффекта реакции в изобарном процессе при заданной температуре
ΔH(T) = ΔНr˚ (298) + ![]() ;
;
Δa = ( ΔaCdSO4+ ΔaH2O)- ( ΔaCdO+ ΔaH2SO4)
Δa = (77,32+30,00) – (48,94+156,90) = -97,82 ;
Δb = (Δb CdSO4+ Δb H2O)- (Δb CdO+ Δb H2SO4)
Δb = (77,40+10,71) – (6,38+28,30) = 53,43 * 10-3
Δc΄ =( Δc΄CdSO4+ Δc΄H2O)- (Δc΄CdO+ Δc΄H2SO4)
Δc΄ = (0 + 0.33) – (-4,90-23,46) = 28,69 * 105
Δc = 0, т.к. все вещества неорганические.
ΔH(511) = -103,24 * 103 + ![]() =
=
= -103,24 * 103 + (-97,82) * (511-298) + ![]() * (5112 – 2982) +
* (5112 – 2982) + ![]() -103240 – 20835,66 + 4603,45 + 4050,80 = -115,42 kДж.
-103240 – 20835,66 + 4603,45 + 4050,80 = -115,42 kДж.
Вывод: Увеличение температуры привело к увеличению количества теплоты выделившегося в следствии реакции.
Расчёт теплового эффекта реакции в изохорном процессе в стандартных условиях
ΔU = ΔН – ΔnRT
Δn = Δnкон. – Δnнач
Δn=1-0=1
Газовая постоянная R = 8.314 Дж/моль*К
ΔU(298)= ΔНr˚ (298) –Δn*R*T
ΔU(298) = -103,24 * 103 -1 * 8,314 * 298 = -103240 – 2477,57 = -105,72 кДж.
Вывод: Внутренняя энергия реакции в изохорном процессе составила 100,76 килоджоуля.
Расчёт теплового эффекта реакции в изохорном процессе при заданной температуре
ΔU(511)= ΔНr˚ (511) –Δn*R*T
ΔU(511) = -115,42 * 103 - 1 * 8,314 * 511 = -115420– 4248,45= - 119,67 кДж.
Вывод: Как и в изобарном процессе увеличение температуры приводит к увеличению внутренней энергии реакции на 18,91 кДж.
2.2 Определение направления протекания химического процесса
Определение направления протекания данной реакции в изолированной системе
Определение направления протекания реакции в стандартных условиях
ΔS˚ (298) = (S(298)Cd SO4 + S(298)H2O) – (S(298)Cd O + S(298)H2SO4)
ΔS˚ (298) =(123,05+188,72)-( 54,81+156,90)= 100,06 ![]()
Вывод: Так как энтропия S больше ноля 100,06>0 то процесс реакции в изолированной системе протекает самопроизвольно без внешнего воздействия. Определение направления протекания реакции при заданной температуре.
ΔS(T) = ΔS˚ (298) + ![]() ;
;
ΔS(511) = 100,06 + ![]() = 100,06 – 97,82
= 100,06 – 97,82![]() + 53,43 * 10-3
+ 53,43 * 10-3![]() + 28,69 * 105
+ 28,69 * 105 ![]() = 100,06 – 97,82
= 100,06 – 97,82 ![]() + 53,43 * 10-3 * (511-298) +
+ 53,43 * 10-3 * (511-298) + ![]() *
* ![]() = 121,66
= 121,66 ![]()
Вывод: Изменение температуры привело к увеличению энтропии по сравнению с процессом при стандартных условиях . Следовательно повышение температуры ведёт к увеличению неупорядоченности и увеличению количества соударений молекул при реакции.
Определение направления протекания химического процесса в закрытой системе
Расчёт изобарно – изотермического потенциала в стандартных условиях
ΔGr˚ (298) = (G(298)Cd SO4 + G(298)H2O) – (G (298)Cd O + G(298)H2SO4)
ΔGr˚ (298)= (-823,88 – 228.61) – (-229,33 – 690.14) = -133,02 кДж/моль.
Вывод: Изобарно – изотермический потенциал показывает что процесс в закрытой системе идёт самопроизвольно ΔGr˚ < 0 ; -133,02<0 .
Произведем расчет изобарно – изотермического потенциала по другой формуле:
ΔGr˚ (298) = ΔНr˚ (298) - Т* ΔS˚ (298)
ΔGr˚ (298) = -103,24 * 103 – 298 * 100,06 = -133,06 кДж/моль.
Найдем процент ошибки:
% ошибки = ![]()
Расчет можно производить любым способом, т.к. процент ошибки не существенен. Расчёт изобарно – изотермического потенциала при заданной температуре
ΔGr˚ (511) = ΔНr˚ (511) - Т* ΔS˚ (511)
ΔGr˚ (511) = -119,46 * 103 – 511 * 121,66 = -181,63 кДж/моль.
Вывод: Увеличение температуры никак не повлияло на процесс реакции в закрытой системе, она по прежнему идёт самопроизвольно ΔGr˚ < 0; -181,63<0. Расчёт изохорно – изотермического потенциала в стандартных условиях.
ΔF(298) = ΔU(298) – T* ΔS˚ (298)
ΔF(298) = -105,72 * 103 – 298 * 100,06 = -135,53 кДж.
Вывод: Изохорно – изотермический потенциал показывает что процесс в закрытой системе идёт самопроизвольно ΔF< 0 ; -135,53<0
Расчёт изохорно – изотермического потенциала при заданной температуре
ΔF(511) = ΔU(511) – T* ΔS˚ (511)
ΔF(511) = - 123,70 * 103 – 511 *121,66 = -185,87кДж.
Вывод: Изменение температуры привело к уменьшению потенциала по сравнению с процессом при стандартных условиях, а это означает что глубина реакции в закрытой системе увеличилась ΔF< 0 ; -185,87>0.
Вывод
Рассмотренная реакция оксида кадмия и серной кислоты идёт самопроизвольно на это указывают все характеристики реакции, а рассмотренное увеличение температуры реакции её ничуть не замедляет. Всё это позволяет сделать вывод о том что увеличение температуры реакции позволяет увеличить её глубину и полноту. При этом реакция останется самопроизвольной.
| T, K | ΔH, кДж | ΔU, кДж | ΔS, | ΔG, кДж/моль | ΔF, кДж |
| 298 | -103,24 | -105,72 | 100,06 | -133,02 | -135,53 |
| 511 | -115,42 | -119,67 | 121,66 | -181,63 | -185,87 |
Похожие работы
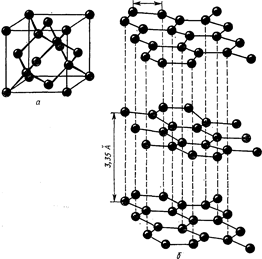
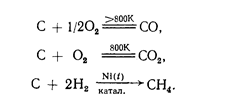
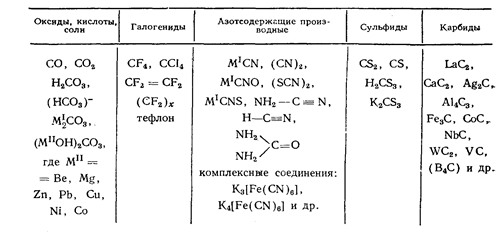
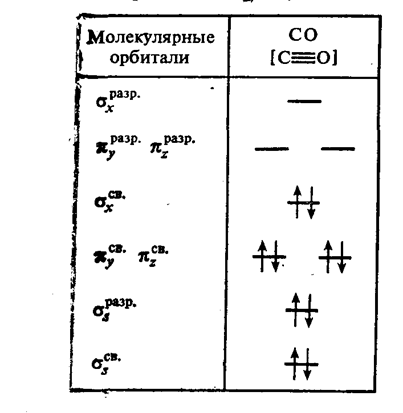
... химия и др. Как уже было сказано выше, химия рассматривает химические элементы и образуемые ими вещества, а также законы, которым подчиняются эти превращения. Один из этих аспектов (а именно, химические соединения на основе кремния и углерода) и будет рассмотрен мной в данной работе. Глава 1. Кремний и углерод - химические элементы 1.1 Общие сведения об углероде и кремнии Углерод (С) ...
... металлов с белками, нуклеиновыми кислотами, липидами. Её практическое применение связано с синтезом фарамакологических препаратов, действие которых обусловленно комплексными ионами металлов. Биоорганическая Химия Изучает связь между строениями органических веществ и их биологическими функциями, использующих в основном методы органической и физической химии, а также физики и математики. ...
... (II), (II)-(III) и(III). Гидроксиды и соли железа(II) и(III). Ферраты(III) и(VI). Комплексные соединения железа. Соли и комплексные соединения кобальта(II) и никеля(II). Органическая химия Характеристика каждого класса органических соединений включает: особенности электронного и пространственного строения соединений данного класса, закономерности изменения физических и химических свойств в ...
... конце столетия в самостоятельную отрасль оформилась физическая химия.Результаты химических исследований всё шире стали использоваться в практике,а это повлекло за собой развитие химической технологии. О пользе химии. Химическое искусство возникло в глубокой древности,и его трудно отличить от производства,потому что,подобно сёстрам-близнецам,оно одновременно рождалось у горна ...
0 комментариев