Все вещества состоят из крошечных частиц - атомов. Атомы соединяются в молекулы, крупнейшие из которых имеют сложное строение, состоящее из тысяч атомов.
О том, что все сущее состоит из частиц, знали еще древние греки. Около 420 г. до н. э. философ Демокрит поддержал гипотезу, что материя состоит из крошечных, неделимых частиц. По-гречески atomos означает "неделимый", поэтому эти частицы назвали атомами.
Другие философы придерживались иной точки зрения, и в IV веке до н. э. Аристотель высказался в поддержку мнения, согласно которому материя состоит из различных сочетаний так называемых четырех стихий - земли, воздуха, огня и воды. Эта идея получила широкое распространение и легла в основу алхимии - примитивной формы химии, господствовавшей в науке до XVII века.
Одной из главных задач алхимии было создание "эликсира жизни" - снадобья, которое позволило бы человеку жить вечно. Другая заключалась в создании богатств путем превращения обычных металлов в золото. Многие алхимики утверждали, что решили эти задачи, однако никто из них так и не добился реального успеха.
Переворот в науке
Некоторые ученые продолжали придерживаться мнения, что материя состоит из атомов, но только в начале XIX века были получены экспериментальные данные, подтверждающие эту теорию. Английский химик и писатель Джон Дальтон проводил опыты с газами и изучал пути их соединения. Так, он обнаружил, что кислород и водород, образуя воду, всегда соединяются в одних и тех же пропорциях по массе. Другие ученые также сталкивались с подобными данными, но именно Дальтон впервые осознал их значение. Он сделал вывод, что вещества состоят из атомов, и что все атомы простого вещества имеют одинаковую массу. При соединении простых веществ количества соединяющихся атомов находятся в определенной неизменной пропорции. Атомистика Дальтона объясняла, почему вещества соединяются в неизменной массовой пропорции, а также явилась основой для детального изучения материи. Вещества состоят из атомов, а из чего состоят атомы? Первые ключи к разгадке этой тайны появились в конце XIX века, когда исследователи изучали прохождение электричества через разрядные трубки, содержащие разреженный воздух. Иногда стенки трубки излучали зеленый свет при подаче высокого напряжения на две металлические пластины - электроды. Свечение возникало при попадании невидимых лучей от отрицательного электрода, или катода, на стенки трубки.
В 1890-х годах английский физик Дж. Томсон доказал, что эти катодные лучи (как их тогда называли) - не что иное, как потоки отрицательно заряженных частиц. Предполагалось, что эти частицы исходят из атомов, хотя их расположение внутри атомов оставалось неясным. Томсон высказал предположение, что атом может быть похож на рождественский пудинг, в котором большая, но легкая по массе положительно заряженная сфера усеяна многочисленными отрицательно заряженными частицами (электронами). Однако различные опыты по изучению строения атома доказали, что это - безусловно ошибочная теория.
Строение атома
В 1911 году Эрнест Резерфорд, британский физик, уроженец Новой Зеландии, работавший вместе с Томсоном, предложил строение атома, реально объясняющее его поведение во время экспериментов. Резерфорд предположил, что центр (или ядро) атома имеет положительный заряд и относительно большую массу, а вокруг ядра вращаются крайне легкие и отрицательно заряженные электроны.
Однако Резерфорд не осознавал, что обычно в ядре атома находятся как положительно заряженные, так и нейтральные частицы. Существование положительно заряженных частиц было признано в 1920 г., и они получили название протоны. В 1932 г. английский физик Джеймс Чэдвик открыл незаряженные частицы и назвал их нейтронами. В результате картина строения атома была завершена и с тех пор является основой нашего понимания материи.
Элементы
Любое вещество, в котором все атомы имеют одинаковое количество протонов, называется элементом. Число протонов в каждом атоме - атомный номер элемента. Существуют 92 природных элемента, их атомы имеют от 1 до 92 протонов. Кроме того, некоторые другие элементы с еще большим числом протонов в атоме можно получить с помощью устройства под названием ускоритель элементарных частиц. К природным элементам относятся железо, ртуть и водород.
| Профессиональная химчистка диванов в Москве |
Во многих веществах атомы объединяются в группы, называемые молекулами. Так, газ водород состоит из молекул, каждая из которых содержит два атома водорода. Часто, однако, молекулы вещества состоят из атомов более одного элемента. Такие вещества называются соединениями. Например, вода является соединением, где каждая молекула состоит из двух атомов водорода и одного атома кислорода. Во многих молекулах насчитывается гораздо большее количество атомов. Некоторые белковые молекулы представляют собой сложные соединения из нескольких тысяч атомов. Некоторые природные элементы встречаются только в соединениях. Так, натрий - это металл, настолько легко соединяющийся с другими веществами, что его нельзя обнаружить в чистом виде. Он широко известен в сочетании с хлором в виде хлорида натрия - поваренной соли.
Связи
Атомы в молекулах связываются различными путями, при этом они разделяют между собой электроны или обмениваются ими. Двумя простыми видами химической связи являются ковалентная и ионная.
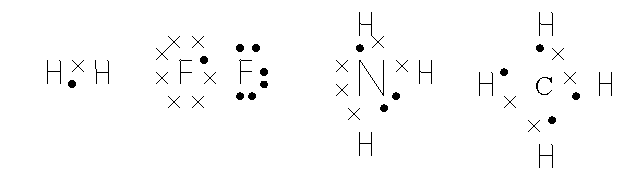
Ковалентная связь возникает, когда атомы имеют общие электроны. Так, молекула водородного газа состоит из двух атомов водорода, связанных ковалентной связью. Единственный электрон каждого атома водорода вращается вокруг ядер обоих атомов, связывая их воедино.
В случае ионной связи один атом передает электроны другому атому. В результате возникает электрическая сила, связывающая атомы воедино. Как правило, количество положительно заряженных протонов и отрицательно заряженных электронов в атоме одинаково. Их положительные и отрицательные заряды уравновешивают друг друга, и поэтому атом не имеет общего заряда. Однако в атоме, отдающем электроны, создается избыток положительного заряда, а атом, получающий электроны, приобретает общий отрицательный заряд. Такие заряженные атомы называются ионами. Ионы противоположных зарядов притягиваются друг к другу, и именно это электрическое притяжение удерживает атомы вместе при ионной связи. Например, молекула поваренной соли формируется с помощью ионной связи, когда атом натрия передает электрон атому хлора.
Все атомы одного вещества имеют одинаковое количество протонов, но различное количество нейтронов. Так, в углероде ядро большинства атомов содержит шесть нейтронов, но примерно в каждом сотом из них имеется семь нейтронов. Эти различные типы атомов одного и того же элемента называются изотопами. Все изотопы данного элемента обладают одинаковыми химическими свойствами - все они соединяются с другими веществами и образуют одни и те же химические соединения. Но отдельные физические свойства изотопов различаются - например, они имеют разные точки замерзания или кипения.
Говоря о конкретном изотопе того или иного элемента, ученые называют его массовое число. Например, углерод-12 - это обычный природный изотоп углерода. Его атом содержит шесть протонов и шесть нейтронов. Более редкий природный изотоп, в ядре каждого атома которого находится лишний нейтрон, называется углерод-13.
Атомный вес
Протон и нейтрон имеют почти одинаковую массу, которая более чем в 1800 раз превышает массу электрона. Поэтому когда речь идет о массе атома, как правило, не будет ошибкой ссылаться на его массовое число.
Атомный вес элемента, или его относительная атомная масса, обычно представляет собой среднюю массу смеси изотопов, встречающихся в природе. Молекулярный вес вещества, или его относительная молекулярная масса, - это сумма атомных весов всех атомов в одной молекуле данного вещества.
Многосложный атом
С тех пор экспериментировавшие с ускорителями ученые открыли сотни других видов частиц в атомах. Но, к счастью, простая модель атома достаточна для того, чтобы объяснить большую часть свойств материи.
Список литературы
Для подготовки данной работы были использованы материалы с сайта http://www.sciencetechnics.com/
Похожие работы
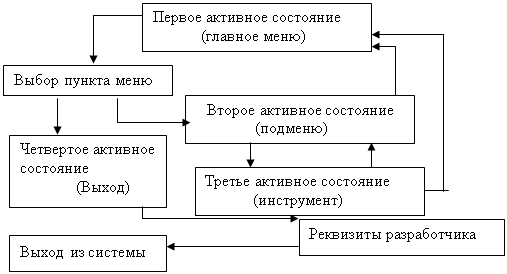
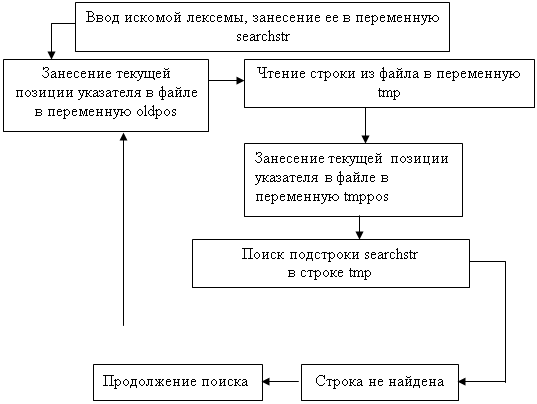
... из программы. Б.3 Описание основных возможностей системы Основное меню позволяет получить доступ к основным обучающим возможностям, которыми располагает система. Пункт меню “Теория” содержит информацию по теме: “Атомно-молекулярная теория. Доказательство существования атомов и молекул” и состоит из подпункта: – Поиск: содержит инструменты, позволяющие пользователю получать информацию в ...
... кислот. Это свидетельствует о наличии специфического взаимодействия между молекулами Н2О, молекулами HF. Такое взаимодействие должно затруднять отрыв молекул друг от друга, т.е. уменьшать их летучесть, а, следовательно, повышать температуру кипения соответствующих веществ. Вследствие большой разницы в ЭО химические связи H–F, H–O, H–N сильно поляризованы. Поэтому атом водорода имеет положительный ...
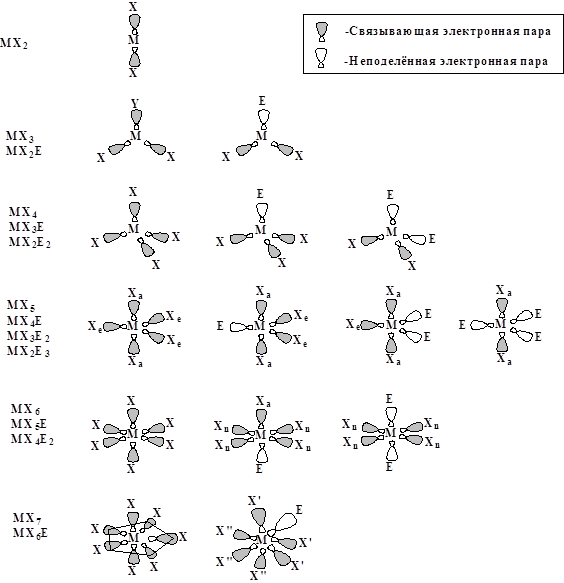
... электронных пар в оболочке атома целое, оно ограничено, оно определяется валентным состоянием атома. Обратимся к примерам, иллюстрирующим прогнозы теории ЛЭП. Рассмотрим соединения разных групп Периодической Системы. 1)У молекул соединений элементов 2-й группы реализуется самая простая структура, порождаемая валентной конфигурацией центрального атома вида MX2. У самого центра 2 валентных ...
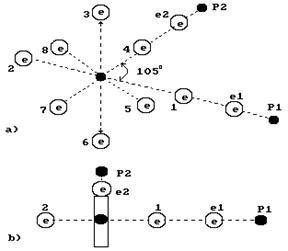
... электронов в молекуле воды, так как валентные электроны атомов, вступающих в связь, могут соединяться не только с протонами соседнего атома, но и с его валентными электронами. С учетом этого структура молекулы воды может отличаться количеством электронов в ней, и возникает необходимость дать названия этим структурам. Структуру молекулы воды с полным набором электронов назовем первой моделью (рис. ...





0 комментариев