ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ
ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
"НОВОСИБИРСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ"Кафедра технологии и организации пищевых производств
Контрольная работа
по дисциплине "Технология продукции общественного питания"
Новосибирск 2011
Содержание
Денатурация фибрилярных белков, постденатурационные изменения
Крахмальные полисахариды и их свойства
Способы стабилизации витаминов
Изменение цвета продуктов под воздействием ферментов
Денатурация фибриллярных белков, постденатурационные изменения
Белки, или протеины, - сложные высокомолекулярные органические соединения (сложные полипептиды), построенные из остатков аминокислот, соединенных между собой амидными связями. В состав одного и того же белка входят различные аминокислоты. При полном гидролизе белок превращается в смесь аминокислот. Молекулярная масса белков весьма велика: так, молекулярная масса альбумина сыворотки крови человека 61 500, у глобулина сыворотки крови 153 000, гемоцианина улитки 600 000. Белки пищевых продуктов по строению молекулы подразделяются на два класса – фибриллярные и глобулярные. Они различаются по строению молекулы, аминокислотному составу, биологической ценности, выполняемой функции и функционально-технологическим свойствам. Глобулярные белки содержатся в подавляющем большинстве пищевых продуктов, а фибриллярные – в мясе, субпродуктах, птице, рыбе, костях.
Многие белки растворимы в воде, в разбавленных растворах солей, в кислотах. Почти все белки растворяются в щелочах, и все они нерастворимы в органических растворителях. Из растворов белки легко осаждаются органическими водорастворимыми растворителями (спиртом, ацетоном), растворами солей, особенно солей тяжелых металлов, кислотами и т. д. Осаждением растворами солей различной концентрации белки могут быть очищены и разделены. При осаждении некоторые белки меняют конформацию цепей и переходят в нерастворимое состояние. Этот процесс называется денатурацией. Денатурация многих белков может быть вызвана и нагреванием.
При кулинарной обработке денатурацию белков вызывает чаще всего нагревание. Процесс этот в глобулярных и фибриллярных белках происходит по-разному. В глобулярных белках при нагревании усиливается тепловое движение полипептидных цепей внутри глобулы, водородные связи, которые удерживали их в определенном положении, разрываются и полипептидная цепь развертывается, а затем сворачивается по-новому. Такое изменение структуры в корне меняет и свойства белков: уменьшается число полярных групп на поверхности, уменьшается или пропадает заряд частицы, резко уменьшается способность к гидратации. В результате денатурации белки теряют устойчивость (молекулы их слипаются, уплотняются, белок свертывается), окраску, ферментативную устойчивость, способность растворяться.
Свертывание белков в результате денатурации бывает двух видов. Если концентрация белка была низкая (до 1%), то свернувшийся белок образует хлопья (пена на поверхности бульонов). Если концентрация белка была высокой, то образуется студень и влага не отделяется (белки яйца). Денатурацию может вызвать не только нагревание, но и ряд других причин: действие солей тяжелых металлов, дубильных веществ; взбивание и др. При взбивании образуется пена с очень тонкими прослойками жидкости между пузырьками воздуха. Поверхность жидкости при этом сильно увеличивается. На поверхности всякой жидкости действуют силы поверхностного натяжения. Они способны механически развернуть полипептидные цепи в молекуле, изменить их конфигурацию и вызвать этим денатурацию. Например, при взбивании яичных белков в поверхностом слое денатурирует белок овомукоид, тормозящий действие трепсина, и усвояемость белков повышается.
Из содержащихся в пищевых продуктах фибриллярных белков (коллаген, эластин, миозин, актин и др.) наибольшее влияние на качество кулинарных изделий и блюд оказывают изменения в процессе тепловой кулинарной обработки белка коллагена. При нагревании в воде отдельных коллагеновых волокон или их пучков вначале они несколько набухают, а затем деформируются. Упорядоченная структура коллагена (вытянутые параллельные цепи) плавится, и коллаген переходит в аморфное состояние. В расплавленном состоянии из-за ослабления внутри- и межмолекулярного взаимодействия цепи за счет разрыва части поперечных связей, стабилизирующих структуру коллагенового волокна, принимают произвольную конфигурацию, что приводит к усадке (сокращению) коллагенового волокна. Длина волокон может уменьшиться до 60% от первоначальной, а их диаметр увеличивается, что приводит к увеличению объема волокна по сравнению с первоначальным. Это происходит при температуре 40-50°С. При дальнейшем повышении температуры разрушение структуры волокон значительно усиливается, и при достижении температуры 55-65°С для коллагенов различного происхождения происходит резкое и мгновенное сокращение длины волокон и увеличение их объема. Этот процесс называется свариванием коллагена. Наряду с изменением линейных размеров коллагеновых волокон происходит нарушение их фибриллярной структуры, и волокна становятся стекловидными. При сваривании коллагена тройные, плотно свитые спирали нативного коллагена переориентируются в беспорядочно свернутые молекулы. Волокна становятся эластичными, более доступными действию ферментов желудочно-кишечного тракта (трипсина), их прочность значительно снижается.
Нагревание коллагеновых волокон выше температуры сваривания вызывает дальнейшее разрушение их структуры, обусловленное последовательным разрывом поперечных связей между молекулами тропоколлагена и внутримолекулярных поперечных связей между цепями тропоколлагена, что приводит в конечном счете к необратимой дезагрегации структуры молеуклы тропоколлагена. Этот процесс резко ускоряется при температурах выше 80°С. В результате этих изменений из коллагена образуется растворимый в горячей воде продукт – глютин.
Стадии перехода коллагена в глютин:
1) Плавление трехспиральной структуры до аморфного состояния;
2) Гидролиз поперечных (межмолекулярных) связей между тропоколлагеновыми единицами;
3) Гидролиз внутримолекулярных поперечных связей;
4) Гидролиз пептидных связей главной цепи.
Для образования глютина необязательно наличие всех четырех стадий, а также необязательно, чтобы каждая стадия прошла полностью.
Образовавшийся глютин, в отличие от нативного коллагена не только хорошо набухает, но при температуре 40°С и выше неограниченно растворяется в воде. Растворы глютина при охлаждении образуют студни, прочность которых зависит от концентрации и продолжительности нагрева. Студни при концентрации глютина более 2,5% хорошо сохраняют форму. При длительном нагреве глютина студнеобразующая способность его снижается вследствие дальнейшей деструкции глютина.
Крахмальные полисахариды и их свойства
Полисахариды – это высокомолекулярные соединения, содержащие сотни и тысячи остатков моносахаридов. Общим для строения полисахаридов является то, что остатки моносахаридов связываются за счет полуацетального гидроксила одной молекулы и спиртового гидроксила другой и т.д. Каждый остаток моносахарида связан с соседними остатками гликозидными связями. Полигликозиды могут содержать разветвленные и неразветвленные цепи. Остатки моносахаридов, входящие в состав молекулы, могут быть одинаковыми или разными. Наибольшее значение из высших полисахаридов имеют крахмал, гликоген (животный крахмал), клетчатка (или целлюлоза). Все эти три полисахарида состоят из молекул глюкозы, по-разному соединенных друг с другом. Состав всех трех соединений можно выразить общей формулой: (С6Н10О5)n
Крахмал относится к полисахаридам. Молекулярная масса этого вещества точно не установлена, но известно, что очень велика (порядка 100000) и для разных образцов может быть различна. Поэтому формулу крахмала, как и других полисахаридов, изображают в виде (С6Н10О5)n. Для каждого полисахарида n имеет различные значения.
Крахмал представляет собой полимеры α-D-глюкозы, находящейся в двух молекулярых формах: линейной (амилоза)
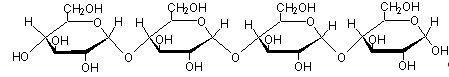
И разветвленной (амилопектин)
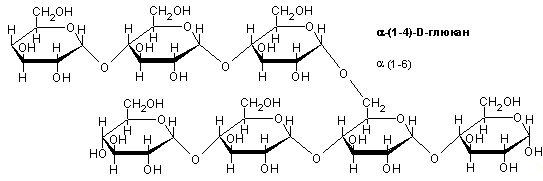
Соотношение этих полисахаридов различное в разных крахмалах (амилозы 18-30%, амилопектина 70-82%).
Амилоза имеет молекулярную массу от 105 до 106. Длина цепи находится в пределах от 500 до 6000 глюкозных остатков. Полимерная цепь амилозы закручивается в спираль. Амилоза способна образовывать комплексные соединения с йодом, которые окрашиваются в синий цвет. Благодаря длинным линейным цепям молекулы амилозы могут объединяться друг с другом и осаждаться из раствора. Этот процесс называется ретроградацией.
Цепочка амилопектина состоит лишь из 20-25 глюкозных остатков. Молекулярная масса превышает 108. Из-за множества ответвлений амилопектин имеет молекулярную массу в 1000 раз большую, чем амилоза. Амилопектиновые цепи собираются в кластерную структуру. Амилопектин не растворяется в воде и образует вязкие стабильные растворы. С йодом амилопектин дает фиолетовое с красноватым оттенком окрашивание.
Физические свойства
Крахмал представляет собой безвкусный порошок, нерастворимый в холодной воде. В горячей воде набухает, образуя клейстер. Крахмал широко распространен в природе. Он является для различных растений запасным питательным материалом и содержится в них в виде крахмальных зерен. Наиболее богато крахмалом зерно злаков: риса (до 86%), пшеницы (до 75%), кукурузы (до 72% ), а также клубни картофеля (до 24% ). В клубнях картофеля крахмальные зерна плавают в клеточном соке, а в злаках они плотно склеены белковым веществом клейковиной. Крахмал является одним из продуктов фотосинтеза.
Химические свойства
При действии ферментов или при нагревании с кислотами (ионы водорода служат катализатором) крахмал, как и все сложные углеводы, подвергается гидролизу. При этом сначала образуется растворимый крахмал, затем менее сложные вещества — декстрины. Конечным продуктом гидролиза является глюкоза. Можно выразить суммарное уравнение реакции следующим образом:
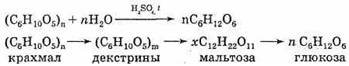
Происходит постепенное расщепление макромолекул. Гидролиз крахмала — его важное химическое свойство.
Крахмал не дает реакции "серебряного зеркала", но ее дают продукты его гидролиза. Макромолекулы крахмала состоят из многих молекул циклической α-глюкозы. Процесс образования крахмала можно выразить так (реакция поликонденсации):
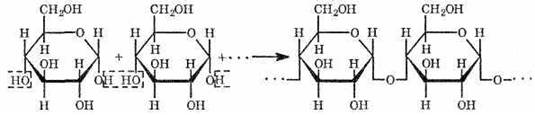
Характерной реакцией является взаимодействие крахмала с растворами йода. Если к охлажденному крахмальному клейстеру добавить раствор йода, то появляется синее окрашивание. При нагревании клейстера оно исчезает, а при охлаждении появляется вновь. Этим свойством пользуются при определении крахмала в пищевых продуктах. Так, например, если каплю йода нанести на срез картофеля или ломтик белого хлеба, то появляется синее окрашивание.
Применение
Крахмал является основным углеводом пищи человека, он в больших количествах содержится в хлебе, крупах, картофеле, овощах. В значительных количествах крахмал перерабатывается на декстрины, патоку, глюкозу, которые используются в кондитерской промышленности. Крахмал используется как клеящее средство, применяется для отделки тканей, накрахмаливания белья. В медицине на основе крахмала готовят мази, присыпки и т.д.
Способы стабилизации витаминов
Витамины участвуют во множестве биохимических реакций, выполняя каталитическую функцию в составе активных центров большого количества разнообразных ферментов либо выступая информационными регуляторными посредниками, выполняя сигнальные функции экзогенных прогормонов и гормонов. Они не являются для организма поставщиком энергии и не имеют существенного пластического значения. Однако витаминам отводится важнейшая роль в обмене веществ. Известно около полутора десятков витаминов. Исходя из растворимости, витамины делят на жирорастворимые — A, D, E, F, K и водорастворимые — все остальные. Жирорастворимые витамины накапливаются в организме, причём их депо являются жировая ткань и печень. Водорастворимые витамины в существенных количествах не депонируются, а при избытке выводятся. Витамины отличаются от других органических пищевых веществ тем, что не включаются в структуру тканей и не используются организмом в качестве источника энергии (не обладают калорийностью).
При надлежащем хранении витамины в их исходной форме сохраняют свою биологическую активность в течение ряда лет. Хорошая сохранность отмечается также в сухих продуктах. Однако в более сложных условиях витамины подвергаются воздействию ряда физических и химических факторов, которые необходимо принимать во внимание перед выбором обогащающих компонентов: температура, тепловая энергия, срок хранения, влажность, неблагоприятная величина рН, кислород и другие газы, свободные Радикалы, свет, облучение, катализаторы (например, ионы меди и железа), ферменты.
Физические и химические факторы, оказывающие влияние на стабильность витаминов:
В целом, холекальциферол, токоферола ацетат, биотин, ниацин, никотинамид, пиридоксин и рибофлавин могут рассматриваться как стабильные витамины, тогда как витамин А, витамин К, аскорбиновая кислота, цианокобаламин, фолиевая кислота, пантотеновая кислота, пантенол и тиамин могут создавать некоторые сложности, связанные с их стабильностью, возникающих при обработке и/или хранении продуктов. Переработка продуктов питания наиболее сильно воздействует на стабильность витаминов в готовых продуктах. Применение стабилизированных и микрокапсулированных форм витаминов значительно повышает их устойчивость в продуктах при различных условиях переработки и хранения. Исследования показывают, что витамин А стабилен в обогащенной муке (после шести месяцев хранения при температуре ниже 25°С сохранность витамина А составляет 95% от исходного уровня). При выпечке хлеба из обогащенной муки наблюдаются незначительные потери витамина А: 10-20%, при использовании для жарки обогащенного растительного масла потери витамина А могут составить порядка 40%. Витамин Е наиболее стабилен в форме d,l-alfa-токоферола ацетата. Природный витамин Е, присутствующий в пищевом сырье в форме аlfa-токоферола, медленно окисляется под воздействием кислорода воздуха. Однако стабильность витамина Е, внесенного в форме d,l-alfa-токоферола ацетата, очень высока и его потери появляются только при продолжительном нагревании, например, кипячении или жарке. Тиамин (витамин В1) - один из наименее стабильных витаминов. Выпечка, пастеризация или кипячение продуктов, обогащенных тиамином, может привести к его потерям до 50%. Стабильность тиамина при хранении зависит от влажности продукта. При хранении муки с влажностью 12% в течение пяти месяцев потери тиамина могут составить до 20%, при 6% влажности муки потерь не наблюдается. Тиамин, рибофлавин и ниацин стабильны при выпечке хлеба: потери составляют от 5 до 10%. Рибофлавин (витамин В2) очень стабилен во время термообработки, хранения и приготовления пищи. Однако рибофлавин подвержен разрушению под воздействием света. Этого можно избежать при использовании светозащитной упаковки. Ниацин - один из наиболее стабильных витаминов и основные потери возникают из-за выщелачивания в воде для приготовления пищи. Пиридоксин (Витамин В6): его потери зависят от типа термической обработки. Например, наибольшие потери в витамина В6 возникают в процессе стерилизации жидкого детского питания, и наоборот, В6 в обогащенной муке стоек к температуре выпекания. В6 чувствителен на свету, вызывающем расщепление и выдерживание в воде может вызвать выщелачивание и привести к значительным потерям. Однако витамин В6 стабилен при хранении, в пшеничной муке, хранящейся при комнатной температуре или при 45°С сохраняется около 90% от внесенного В6. Фолиевая кислота нестабильна и теряет свою активность в присутствии света, окислителей или восстановителей, в кислой или щелочной средах. Однако она относительно стабильна к нагреванию и влажности; так выпечка и зерновые хлопья сохраняют до 100% от добавленного количества фолиевой кислоты после шести месяцев хранения. Свыше 70% ее сохраняется в процессе выпечки хлеба. D-пантотенаткальция стабилен при нагревании в слабых кислотах и нейтральной среде, но его стабильность снижается в щелочной среде. Биотин чувствителен как к кислотам, так и к основаниям. Аскорбиновая кислота (витамин С) легко разрушается в ходе технологической обработки или хранении из-за действия металлов таких как медь или железо. Длительное воздействие воздуха и продолжительное нагревание в присутствии кислорода разрушает аскорбиновую кислоту, таким образом стабильность витамина С в обогащенном продукте будет зависеть от самого продукта, технологии его производства, типа используемой упаковки. В витаминизированном продукте или напитке сохраняется от 75 до 97% витамина С при хранении 12 месяцев при комнатной температуре. Для увеличения стабильности некоторые витамины могут быть также подвержены химической модификации, специальной технологической обработке с целью получения более стабильных форм, позволяющих их использовать в различных отраслях пищевой промышленности. Основные параметры, учитывающиеся при разработке форм продуктов:
- стабильность (в процессе обработки и при хранении)
- удобство при использовании (например, минимальное пылеобразование, минимальное расслоение в конечном продукте, устойчивость к слеживанию, хорошая сыпучесть и однородность)
- растворимость (получение вододиспергируемых форм жирорастворимых витаминов и каротиноидов)
- биодоступность
- органолептические характеристики (например, маскирование неприятных запахов за счет встраивания или инкапсулирования действующего вещества в защитную матрицу)
Выбор оптимальной упаковки в значительной степени определяется сроком хранения и стоимостью. Витамин А необходимо защищать от кислорода и света, витамин С - от кислорода, а рибофлавин и пиридоксин - от света. В напитках, молоке и масле кислород может вызывать быстрое разложение витаминов А и С. Упаковка из стекла - хороший выбор для защиты от кислорода, но с точки зрения удобства использования, утилизации и других причин пластмассовая является более подходящей. Правильно подобранные упаковочные материалы совместно с соответствующими передозировками витаминов - путь преодоления проблем, вызываемых взаимодействием с кислородом. Светозащитная упаковка (темное стекло, темный пластик, асептические коробки) - также способствуют сведению к минимуму воздействие света и, следовательно, сведению к минимуму разложения светочувствительных витаминов.
Изменение цвета продуктов под воздействием ферментов
Ферменты - (от латинского слова "ферментум" - закваска) - это вещества белковой природы, вырабатываемые живой клеткой. Известно около 1000 ферментов, и каждый из них обладает исключительной специфичностью действия, т.е. катализирует только одну определённую реакцию. Все ферменты делятся на 6 классов:
оксиредуктазы - катализируют окислительно-восстановительные процессы;
трансферазы - перенос химических групп;
гидролазы - гидролиз;
лиазы - расщепление негидролитическим путём с образованием воды или диоксида углерода;
изомеразы - внутримолекулярное перемещение различных групп;
лигазы - синтез.
Оптимальная температура для действия растительных ферментов 50-60 °С, животного происхождения – 40-50 °С.
В сырье, собранном для консервирования, дыхательные процессы не прекращаются, а находятся в равновесии, что не дает происходить явным изменениям вещества. Но любое механическое мероприятие, например, резание, чистка, измельчение, помол материала приводят к дезорганизации ферментативной системы, разрушению витамина С и других веществ и вследствие окисления некоторых органических материалов приводят к окрашиванию в коричневый цвет. При обработке фруктов с белой мякотью на компот можно замочить готовые плоды в слабом растворе лимонной кислоты, таким вмешательством можно ограничить доступ кислорода к продуктам и тем самым снизить скорость ферментативных реакций. Добавка лимонного сока к тому же приводит к предохранению от быстрого окисления витамина С, что могло бы привести к коричневой окраске продуктов. В измельченных фруктах, предназначенных для приготовления мармелада, инактивация (снижение активности) ферментов достигается своевременным и быстрым нагревом. Окрашивание некоторых видов нарезанных овощей (сельдерея, петрушки), предназначенных для дальнейшей стерилизации или сушки снижается быстрым обвариванием в кипящей воде.
Изменение цвета очищенных клубней картофеля. Потемнение на воздухе очищенного картофеля вызвано деятельностью фермента полифенолоксидазы (комплекс фенолазы, полифенолазы, катехолазы, тирозиназы и крезолазы), катализирующей первые две ступени сложной реакции превращения моно-, ди - или полифенолов в темноокрашенный меланин. При хранении очищенного картофеля на воздухе появляются розовые пятна, постепенно темнеющие и переходящие в черные. Пигмент, окрашивающий поверхность очищенного картофеля, называется меланином. Склонность к потемнению не является устойчивым сортовым признаком. У одного и того же сорта картофеля она может сильно варьировать в зависимости от почвенных и климатических условий. Наблюдается прямая зависимость между активностью ферментной системы картофеля и скоростью его потемнения. Так, в быстро темнеющем сорте Вольтман активность тирозиназы в 2,7 раза больше, чем в сорте 8670, не склонном к потемнению. Для предохранения очищенного картофеля от потемнения применяются способы, основанные на инактивации полифенолоксидазы.
В мясоперерабатывающей практике существует так называемый "загар мяса" - автолиз мяса — процесс самопроизвольного изменения химического состава, структуры и свойств мясного сырья после убоя животного под воздействием собственных ферментов мяса. В связи с отсутствием поступления кислорода в организм ресинтез гликогена в мясе после убоя идти не может, и начинается его анаэробный распад, который протекает по пути фосфоролиза и амилолиза с образованием молочной кислоты и глюкозы. Скорость гликолиза можно регулировать: введение хлорида натрия в парное мясо подавляет процесс; применение электростимуляции — ускоряет. Интенсивный прижизненный распад гликогена может вызываться стрессовыми ситуациями у животных. Процесс этот сопровождается изменением цвета (в зависимости от интенсивности процесса — коричнево-красный, медно-красный, желто- или серо-красный) и удушливо кислым запахом мяса.
При кулинарной обработке может происходить изменение естественной окраски продуктов животного (мясо и мясопродукты) и растительного происхождения (щавель, крыжовник и др.) и образование другой окраски (очищенные клубни картофеля). Основными причинами изменения цвета продуктов являются окислительные и другие превращения полифенольных соединений, которые в них содержатся, происходящие при участии ферментов и неферментативным путем; полимеризация продуктов окисления полифенолов; сахаро-аминные (меланоидиновые) реакции между сахаром со свободными карбонильными группами и аминокислотными соединениями; карамелизация сахаров, интенсивно проходящая при температурах их плавления и связанная с реакциями дегидратации; окисление соединений железа и т. д.
Литература
1. Баранов В.С., Мглинец А.И., Алешина Л.М. и др. Технология производства продукции общественного питания. – М: Экономика, 1986.
2. Мацейчик И.В., Габелко С.В. Методические указания по курсу Технология продукции общественного питания. – Н: НГТУ, 2000
3. Интернет – портал www.publiccatering.ru
4. Интернет – портал www.meatinfo.ru
5. Интернет – портал www.wikipedia.ru
6. Интернет – портал http://ido.tsu.ru/schools/chem/data/res/org/uchpos/text/Untitled3.html?sphrase_id=33558
7. Мглинец А.И. Технология продукции общественного питания. – СПб: Троицкий мост, 2010
Похожие работы
... эффективность исполнения оборудования, осуществить поточность производства, применить прогрессивную технологию, значительно улучшить организацию труда. Технологическая схема централизованного производства крупнокусковых, порционных, мелкокусковых, рубленных полуфабрикатов практически та же, что и на предприятиях общественного питания, работающих на сырье, но дополнительно включает охлаждение ...
... контингентом питающихся (столовые при больницах, санаториях, домах отдыха, ремесленных училищах и др.). Данные, приведенные в приложениях 15,19-24. дают возможность определить количество продуктов для проектируемого предприятия общественного питания в зависимости от контингента потребителей. При расчете сырья по физиологическим нормам норму продуктов на одного человека в день умножают на ...
... в настоящее время и в перспективе; во-вторых, чем товары (услуги) фирмы отличаются от товаров (услуг) конкурентов. Далее считаем уместным, рассмотреть задачи формирования имиджа организации общественного питания. Имидж формируется как на основе реального поведения индивида, так и под влиянием оценок и мнений других людей. На формирование имиджа организации на рынке труда влияют как объективные ( ...
... работник, и автоматизированные, где контроль за безопасной работой и режимом тепловой обработки обеспечивает сам тепловой аппарат при помощи приборов автоматики. На предприятиях общественного питания тепловое оборудование может использоваться как несекционное или секционное, модулированное. Несекционное оборудование, это оборудование, которое различно по габаритам, конструктивному исполнению и ...
0 комментариев