Навигация
Определение диаметра молекул
Муниципальное общеобразовательное учреждение
«Основная общеобразовательная школа №10»
Определение диаметра молекул
Лабораторная работа
Исполнитель: Масаев Евгений
7 класс «А»
Руководитель: Резник А. В.
Гурьевский район
2010
Введение
В этом учебном году я начал изучать физику. Я узнал, что тела, которые нас окружают, состоят из мельчайших частиц – молекул. Меня заинтересовало, каковы размеры молекул. Из-за очень малых размеров молекулы нельзя увидеть невооруженным глазом или с помощью обыкновенного микроскопа. Я прочитал, что молекулы можно увидеть только с помощью электронного микроскопа. Ученые доказали, что молекулы разных веществ отличаются друг от друга, а молекулы одного и того же вещества одинаковы. Мне захотелось на практике измерить диаметр молекулы. Но к сожалению, в школьной программе не предусматривает изучение проблем такого рода, а рассмотреть её одному оказалось нелёгкой задачей и пришлось изучать литературу о методах определения диаметра молекул.
Глава I. Молекулы
1.1 Из теории вопроса
Молекула в современном понимании – это наименьшая частица вещества, обладающая всеми его химическими свойствами. Молекула способна к самостоятельному существованию. Она может состоять как из одинаковых атомов, например кислород О2, озон О3, азот N2, фосфор P4, сера S6 и т. д., так и из различных атомов: сюда относятся молекулы всех сложных веществ. Простейшие молекулы состоят из одного атома: это молекулы инертных газов – гелия, неона, аргона, криптона, ксенона, радона. В так называемых высокомолекулярных соединениях и полимерах каждая молекула может состоять из сотен тысяч атомов.
Экспериментальное доказательство существования молекул первым наиболее убедительно дал французский физик Ж. Перрен в 1906 г. при изучении броуновского движения. Оно, как показал Перрен, является результатом теплового движения молекул – и ничем иным.
Сущность молекулы можно описать и с другой точки зрения: молекула – устойчивая система, состоящая из ядер атомов (одинаковых или различных) и окружающих электронов, причем химические свойства молекулы определяются электронами внешних оболочек в атомах. Атомы объединяются в молекулы в большинстве случаев химическими связями. Обычно такая связь создается одной, двумя или тремя парами электронов, которыми владеют сообща два атома.
Атомы в молекулах соединены друг с другом в определенной последовательности и определённым образом распределены в пространстве. Связи между атомами имеют различную прочность; она оценивается величиной энергии, которую необходимо затратить для разрыва межатомных связей.
Молекулы характеризуются определёнными размером и формой. Различными способами было определено, что в 1 см3 любого газа при нормальных условиях содержится около 2,7x1019 молекул.
Чтобы понять, насколько велико это число, можно представить, что молекула – это «кирпич». Тогда если взять количество кирпичей, равное числу молекул в 1 см3 газа при нормальных условиях, и плотно уложить ими поверхность суши всего земного шара, то они покрыли бы поверхность слоем высотой 120 м, что почти в 4 раза превосходит высоту 10-этажного дома. Огромное число молекул в единице объёма указывает на очень малые размеры самих молекул. Например, масса молекулы воды m=29,9 x 10-27 кг. Соответственно малы и размеры молекул. Диаметром молекулы принято считать минимальное расстояние, на которое им позволяет сблизиться силы отталкивания. Однако понятие размера молекулы является условным, так как на молекулярных расстояниях представления классической физики не всегда оправданы. Средний размер молекул порядка 10-10м.
Молекула как система, состоящая из взаимодействующих электронов и ядер, может находиться в различных состояниях и переходить из одного состояния в другое вынужденно (под влиянием внешних воздействий) или самопроизвольно. Для всех молекул данного вида характерна некоторая совокупность состояний, которая может служить для идентификации молекул. Как самостоятельное образование молекула обладает в каждом состоянии определенным набором физических свойств, эти свойства в той или иной степени сохраняются при переходе от молекул к состоящему из них веществу и определяют свойства этого вещества. При химических превращениях молекулы одного вещества обмениваются атомами с молекулами другого вещества, распадаются на молекулы с меньшим числом атомов, а также вступают в химические реакции других типов. Поэтому химия изучает вещества и их превращения в неразрывной связи со строением и состоянием молекул.
Обычно молекулой называют электрически нейтральную частицу. В веществе положительные ионы всегда сосуществуют вместе с отрицательными.
По числу входящих в молекулу атомных ядер различают молекулы двухатомные, трехатомные и т.д. Если число атомов в молекуле превосходит сотни и тысячи, молекула называется макромолекулой. Сумма масс всех атомов, входящих в состав молекулы, рассматривается как молекулярная масса. По величине молекулярной массы все вещества условно делят на низко- и высокомолекулярные.
Похожие работы
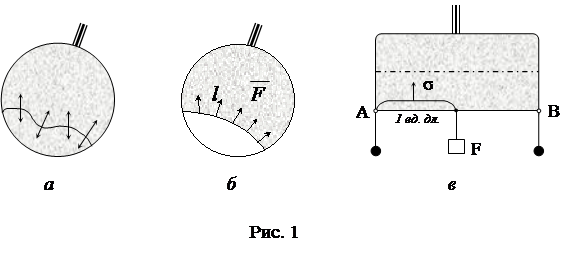
... , и начинаем отпускать его до момента образования плёнки. Отмечая новую тягу Р2, мы найдём для поверхностного натяжения s значение: . (8) §3. Определение коэффициента поверхностного натяжения методом компенсации давления Лапласа Молекулы жидкости взаимодействуют между собой силами притяжения и отталкивания, которые проявляются заметно в ...
... (47) Величина, обратная t, характеризует скорость прироста при данной температуре концентрации триплетных молекул акцептора энергии, q = 1/t , и называется константой скорости процесса [161]. Итак, прирост в результате отжига образца числа молекул, участвующих в излучении сенсибилизированной фосфоресценции происходит по экспоненциальному закону. Константа скорости этого ...
... к решению соответствующего интегрального уравнения, при этом могут быть использованы численные методы - аналитические зависимости в этом случае получить не удается. Еще сложнее описать процессы испарения и конденсации частиц, в среде, состоящей из нескольких летучих компонентов [23]. Предполагалось, что процесс стационарный, испаряющиеся компоненты химически инертны, пары представляют собой ...
... основе "Зеленой тетради". Шредингер был хорошо знаком с авторами этой работы по совместным семинарам физиков-теоретиков (и частично - радиационных генетиков) копенгагенской школы. Это и стало следующим "касанием" создателей великой идеи. Прежде всего Шредингер развил модель гена-молекулы (модель Дельбрюка, как он ее часто называл): "Предположим, что по своей структуре ген является гигантской ...





0 комментариев