Навигация
Дегазация воды
1. Классификация методов дегазации воды, теоретические основы процесса
Удаление из воды растворенных в ней или образующихся в процессе ее обработки газов называют ее дегазацией. Обычно из воды приходится удалять углекислоту, сероводород, кислород и реже метан. Первые три коррозионно-активных газа обусловливают либо катализируют процессы коррозии металла, а диоксид углерода(IV) вызывает коррозию бетона. Метан, выделяющийся из воды в процессе ее обработки, образует с воздухом в помещении водоочистного комплекса взрывоопасную смесь, а сероводород придает воде неприятный запах. Кроме того, при водород-катионитовом умягчении и ионитовом обессоливании воды, а также при обезжелезивании и деманганации подземных бикарбонатных вод приходится решать задачу удаления свободной углекислоты. При подготовке питательной воды, а также воды теплоцентралей необходимо удалять из нее кислород в целях предотвращения коррозии металла. Отсюда становится очевидной необходимость возможно полного удаления из воды растворенных в ней газов. Существующие методы дегазации воды подразделяют на физические и химические. Сущность физических методов дегазации заключается в следующем: вода, содержащая удаляемый газ, приводится в соприкосновение с воздухом, если парциальное давление этого газа в воздухе близко к нулю; создаются условия, при которых растворимость газа в воде становится ничтожно малой. С помощью первого приема, аэрации воды, обычно удаляют свободную углекислоту и сероводород, поскольку парциальное давление этих газов в атмосферном воздухе близко к нулю. Ко второму приему обычно прибегают при обескислороживании воды. В этом случае ввиду значителнього парциального давления кислорода в атмосферном воздухе аэрацией воды кислород удалить нельзя, поэтому воду доводят до кипения, тогда растворимость всех газов в ней падает до нуля. Для этого применяют либо нагревание воды, либо понижение давления до величины, при которой вода кипит без дополнительного подогрева в вакуумных дегазаторах. В настоящее время наиболее распространенной теорией, объясняющей механизм передачи вещества между жидкой и газообразной фазами в процессе десорбции, является теория двухслойного поглощения, согласно которой десорбция сводится к последовательной диффузии удаляемого газа через два пограничных слоя — жидкостный и газовый. При диффузии газа из жидкой фазы в газообразную концентрация его и парциальное давление изменяются в диффузионных пленках. Концентрация газа в жидкой фазе равна концентрации его на границе между жидкостной пленкой и основной массой жидкости; в жидкостной пленке происходит снижение концентрации от величины С1 до С2, отвечающей парциальному давлению р2 диффундирующего газа на границе раздела фаз; в газовой пленке парциальное давление диффундирующего газа изменяется от величины р2 до величины р1 имеющей место на границе газовой пленки и основной массы газа, в которой парциальное давление диффундирующегго газа также равно величине р1.
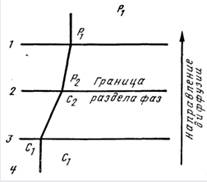
Рис. 19.1. Схема изменения давлений и концентраций газа на границе раздела фаз: 1,4 — газообразная и жидкостная фазы; 2, 3 — газовая и жидкостная диффузионная пленка
По теории двухслойного поглощения, общее сопротивление десорбции R равно сумме сопротивлений, оказываемых пограничными диффузионными слоями:
R = R1+ R2(19.1)
где R1 — сопротивление жидкостного пограничного слоя; R2 — сопротивление газового пограничного слоя.
Величины, обратные сопротивлениям в пограничных слоях, называют частными или пленочными коэффициентами десорбции:
![]() (19.2)
(19.2)
Численно частный коэффициент десорбции равен количеству удаляемого (десорбируемого) газа, передаваемого через единицу площади соприкосновения фаз в единицу времени при движущей силе в диффузионной пленке, равной единице.
Скорость процесса десорбции растворенного в воде газа в воздух определяется из выражения
![]() (19.3)
(19.3)
где Т — время, ч; А — площадь соприкосновения жидкой и газообразной фаз, м2; G — количество десорбируемого газа, кг/ч.
При малой концентрации десорбируемого газа в воде скорость процесса десорбции определяется средней движущей силой ΔСср и сопротивлением процессу диффузии в пленке жидкости Кж
![]() (19.4)
(19.4)
Согласно теории двухслойного поглощения, количество десорбируемого газа
![]() (19.5)
(19.5)
где Ко — общий коэффициент десорбции, м/ч, который для случая десорбции труднорастворимых газов может быть приравнен к пленочному коэффициенту в жидкостной пленке Кж, А — площадь соприкосновения жидкой и газообразной фаз, м2; ΔСср — средняя движущая сила процесса десорбции, кг/м3, которую для случаев десорбции из малоконцентрированных растворов газов подсчитывают по уравнению
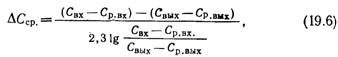
здесь Свх и Свых — концентрации удаляемого газа в воде соответственно на входе ее в аппарат и на выходе из него; Ср.Вх и Ср.вых — равновесные концентрации удаляемого газа в воде соответственно при входе ее в аппарат и на выходе из него.
Таким образом, величина ΔСср зависит от разности концентраций удаляемого газа в воде и воздухе.
Основное расчетное уравнение аппаратов для извлечения из воды растворенных газов десорбцией записывается в следующем виде:
![]() (19.7)
(19.7)
![]()
где q — производительность аппарата, м3/ч.
Коэффициент сопротивления процессу диффузии в пленке жидкости Km возрастает с увеличением относительной скорости движения воды и воздуха в десорбере, с повышением температуры и увеличением коэффициента диффузии удаляемого газа.
Из величин, входящих в общее уравнение десорбции, G и ΔССр, могут быть подсчитаны по заданным условиям работы дегазатора, величина Km вычислена опытным путем или с помощью теории подобия. Это уравнение является основным для расчета десорбционных аппаратов. Из него находят необходимую поверхность соприкосновения жидкой и газообразной фаз для обеспечения заданного эффекта дегазации, а, следовательно, и размер проектируемых аппаратов.
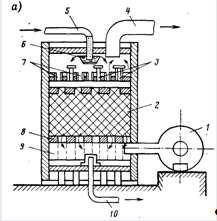
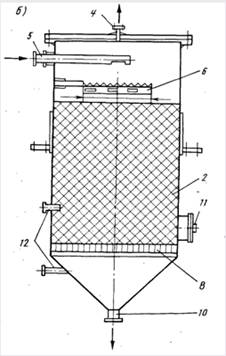
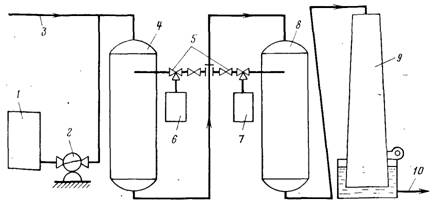
Для удаления из воды растворенных газов применяют несколько типов дегазаторов: пленочные с различного рода насадками, работающие в условиях противотока дегазируемой воды и воздуха, подаваемого вентилятором, барботажные, пенные, вакуумно-эжекционные, вакуумные.
Похожие работы
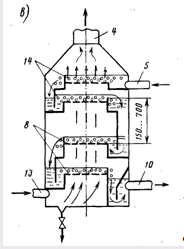
... — ввод воздуха; 14 — пенный слой Концентрация свободной углекислоты в воде, подлежащей дегазации, не всегда указывается в анализе. Ее можно определить следующим образом. При дегазации воды после Н-катионитовых фильтров суммарное количество углекислоты будет равно: где Жк — карбонатная жесткость исходной воды, мг-экв/л; Снач — содержание свободной углекислоты в исходной воде, мг/л, ...
... поверхности различных горизонтов; составление карт изотерм по срезам на различных глубинах; построение обобщенного графика изменения температуры с глубиной для района в целом. РОЛЬ ПОДЗЕМНЫХ ВОД В ФОРМИРОВАНИИ И РАЗРУШЕНИИ ЗАЛЕЖЕЙ НЕФТИ И ГАЗА Ведущая роль подземных вод в процессах миграции УВ и формирования их залежей признается большинством исследователей. Еще в первых работах М. Менна ...
... %. Количество осадка после механической очистки - 1,5 л/м3. Осадок удаляется раз в 5-7 суток перекачкой его в начало очистных сооружений. Сооружения обеззараживания и обезвреживания осадков Химическое обеззараживание осадков проводится известью, аммиаком, тиазоном, формальдегидом или мочевиной. Одновременно повышается удобрительная ценность осадков. Требуемая для обеззараживания известью ...
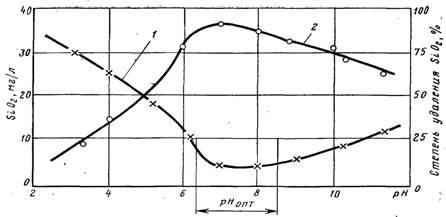
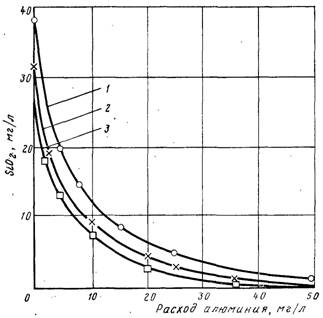
... кислота или фторид натрия переводят кремниевую кислоту в сильную кремнефтористоводородную, которая достаточно полно поглощается слабоосновными анионитами: Электрохимическое декремнизирование воды Обескремнивание воды при электролизе растворимым алюминиевым анодом основано на способности образующегося в процессе электролиза гидроксида алюминия сорбировать соединения кремния. Как показали ...
0 комментариев