Навигация
Показатель эффективности процесса - расход Q
2. Показатель эффективности процесса - расход Q.
3. Цель управления процессом Q=Qзд.
4. Анализ типовой схемы как объекта управления:
Основные элементы, подлежащие анализу - трубопровод 3 и насос 2.
Основные параметры трубопровода как объекта управления.
внутренний диаметр d:
![]() ,
,
где Q –расход, м^3/с, v - скорость потока, м/с.
Скорость потока v = 0.5 – 2.5м/с.
Гидравлическое сопротивление трубопровода:
pгс = pск + pтр + pмс
потери давления на сообщение потоку скорости:
![]()
потери давления на преодоление трения потока о стенки трубопровода:
![]()
где = f(Re,l) - коэффициент трения.
потери давления на преодоление местных сопротивлений:
pмс = мс*pск,
где мс - коэффициент местного сопротивления.
Сопротивление, затрачиваемое на подъем жидкости на высоту h:
pпод = *g*h
Дополнительное сопротивление:
pдоп = p2 – p1
Полное сопротивление:
![]()
Мощность ,которую необходимо затратить на перекачивание:
N = pобщ*Q/(10^3*),
= н*п*д,:
где - полный к.п.д., насоса; н - к.п.д. насоса; п - к.п.д. передачи;
д - к.п.д. двигателя.
Схема трубопровода как объекта управления
для типовой схемы процесса перемещения жидкости.
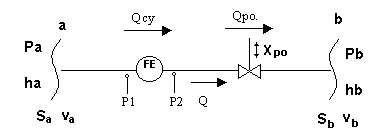
Рис.1.
Математическое описание статики объекта.
Материальный баланс для трубопровода (рис.1) на основании условия неразрывности струи:
Sa*va = Sb*vb (1)
Из (1) получим :
va = Sb*vb/ Sa (1б).
Обозначим Sb/ Sa = m (1в).
Энергетический баланс - уравнение Бернулли:
![]() (2)
(2)
Подставим в (2) выражение для скорости потока в сечении «а» на основании (1б):
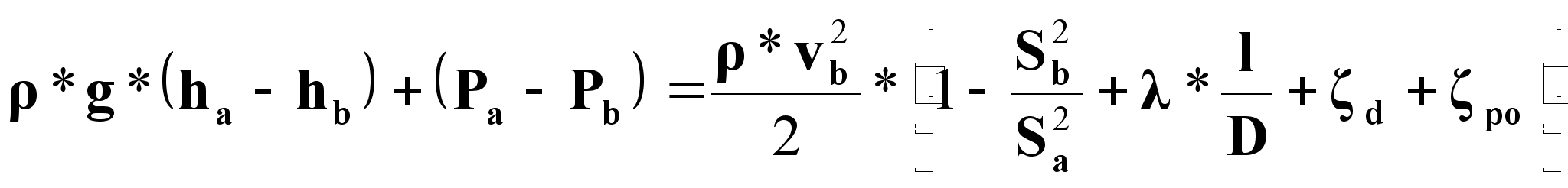 (3)
(3)
Подставим в (3) вместо vb его выражение из соотношения для объемного расхода в сечении «b»:
Qb = vb*Sb;
откуда
vb =Qb / Sb:
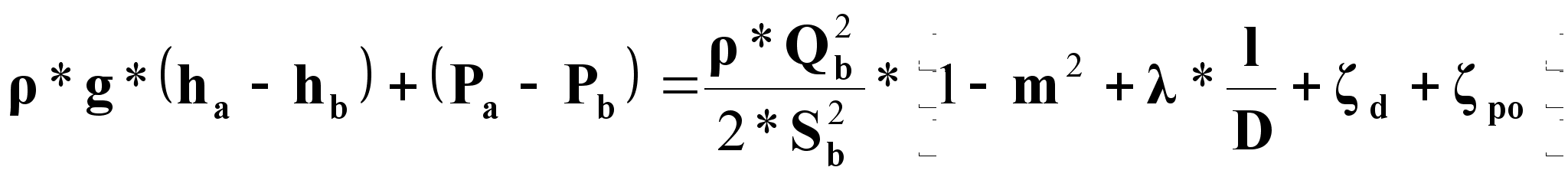 (4)
(4)
Преобразуем выражение (4) с учетом (1в) к виду:
![]() (5)
(5)
Решим выражение (5) относительно Qb:
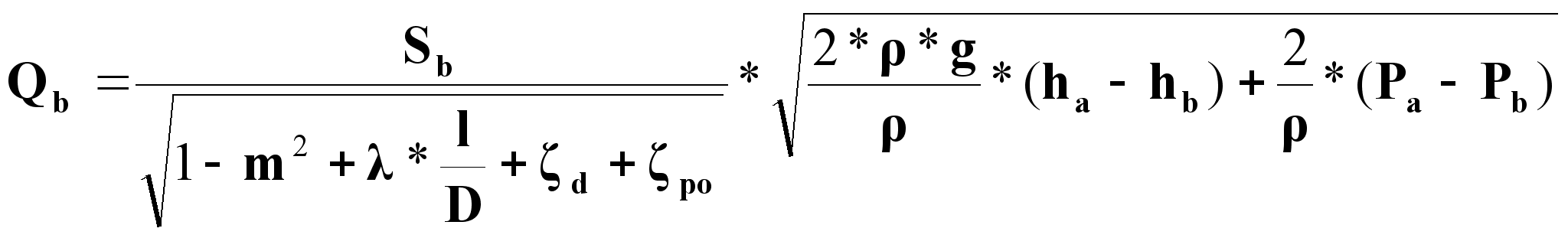 (6)
(6)
Линеаризованные выражения мат. модели статики
на основании разложения в ряд Тейлора:
1.Через приращения и частные производные:
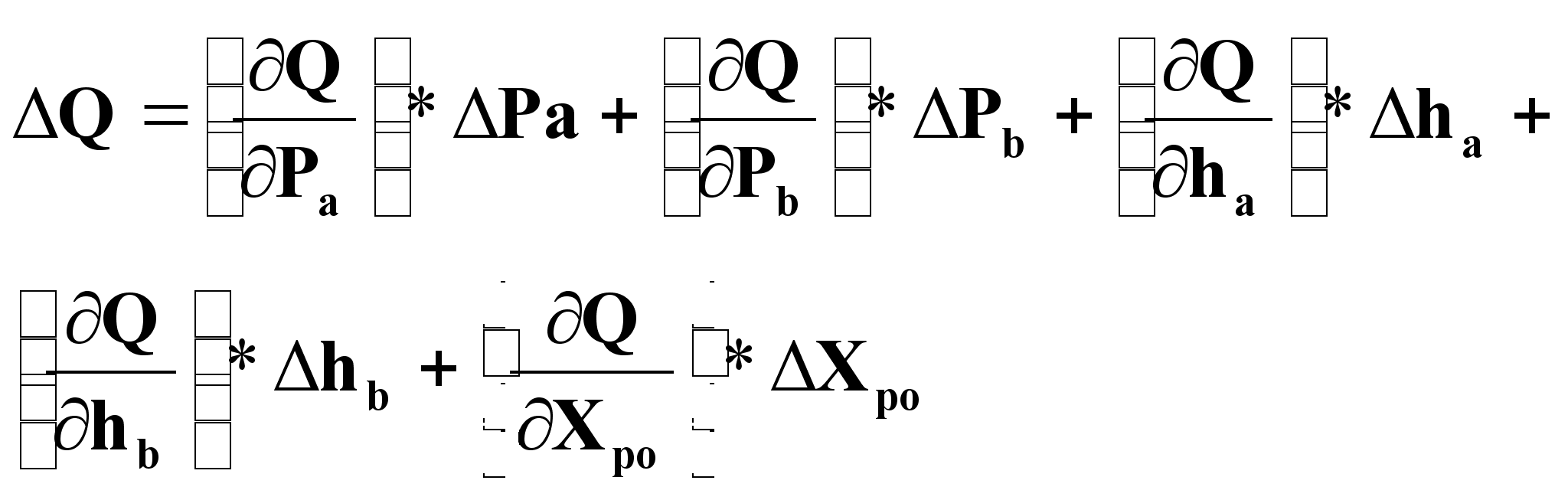
2.Через приращения и коэффициенты усиления:
![]()
Информационная схема объекта управления.
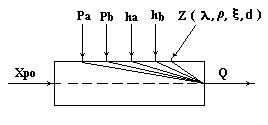
Рис.2.
Хро - возможное регулирующее воздействие;
Рa , ha , Pb , hb - возможные контролируемые возмущающие воздействия;
Z - возможные неконтролируемые возмущающие воздействия.
Математическое описание динамики объекта.
Структурная схема объекта.
Рис.3
Уравнение динамики:
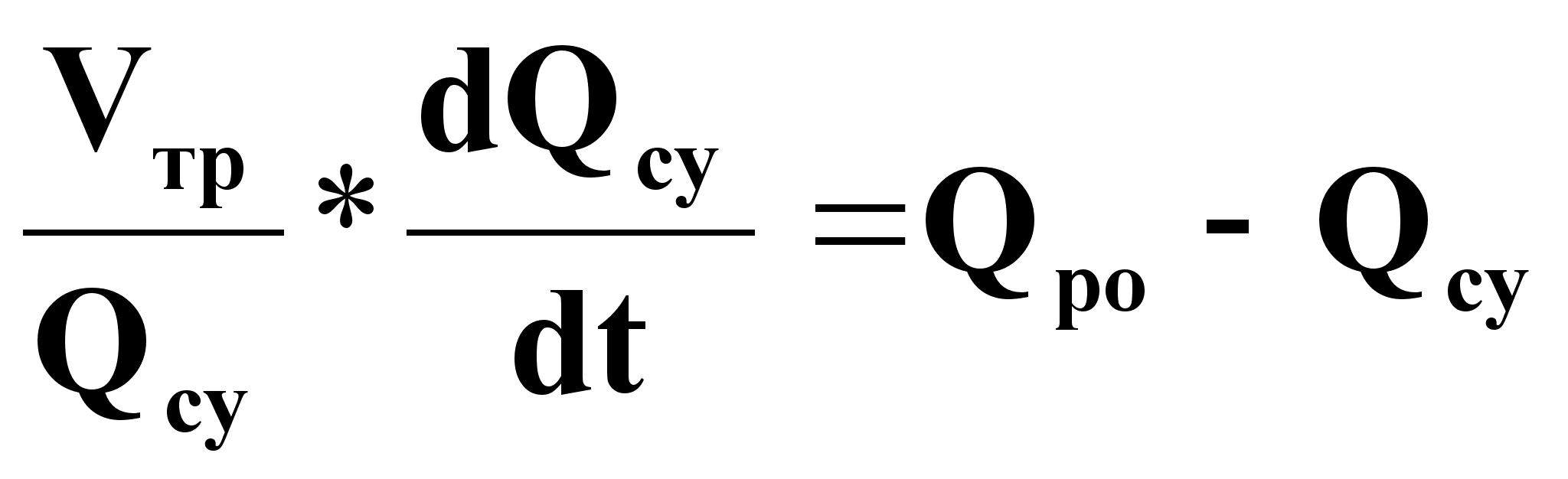 (1).
(1).
Уравнение статики:
![]() (2).
(2).
Уравнение динамики во временной области на основе метода безразмерных переменных:
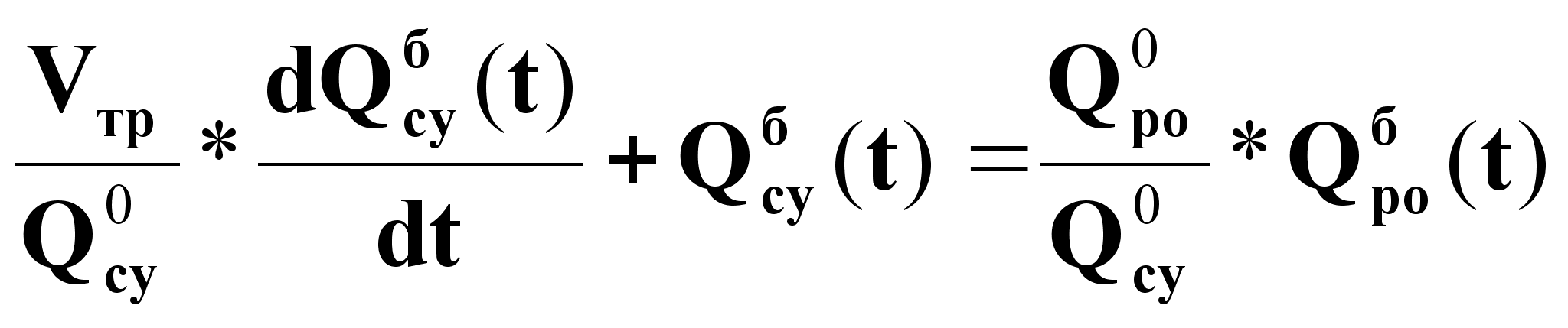 (3).
(3).
Уравнение динамики с учетом запаздывания:
![]() (5).
(5).
Передаточная функция для выражения (5) будет иметь вид:
![]() (6),
(6),
где
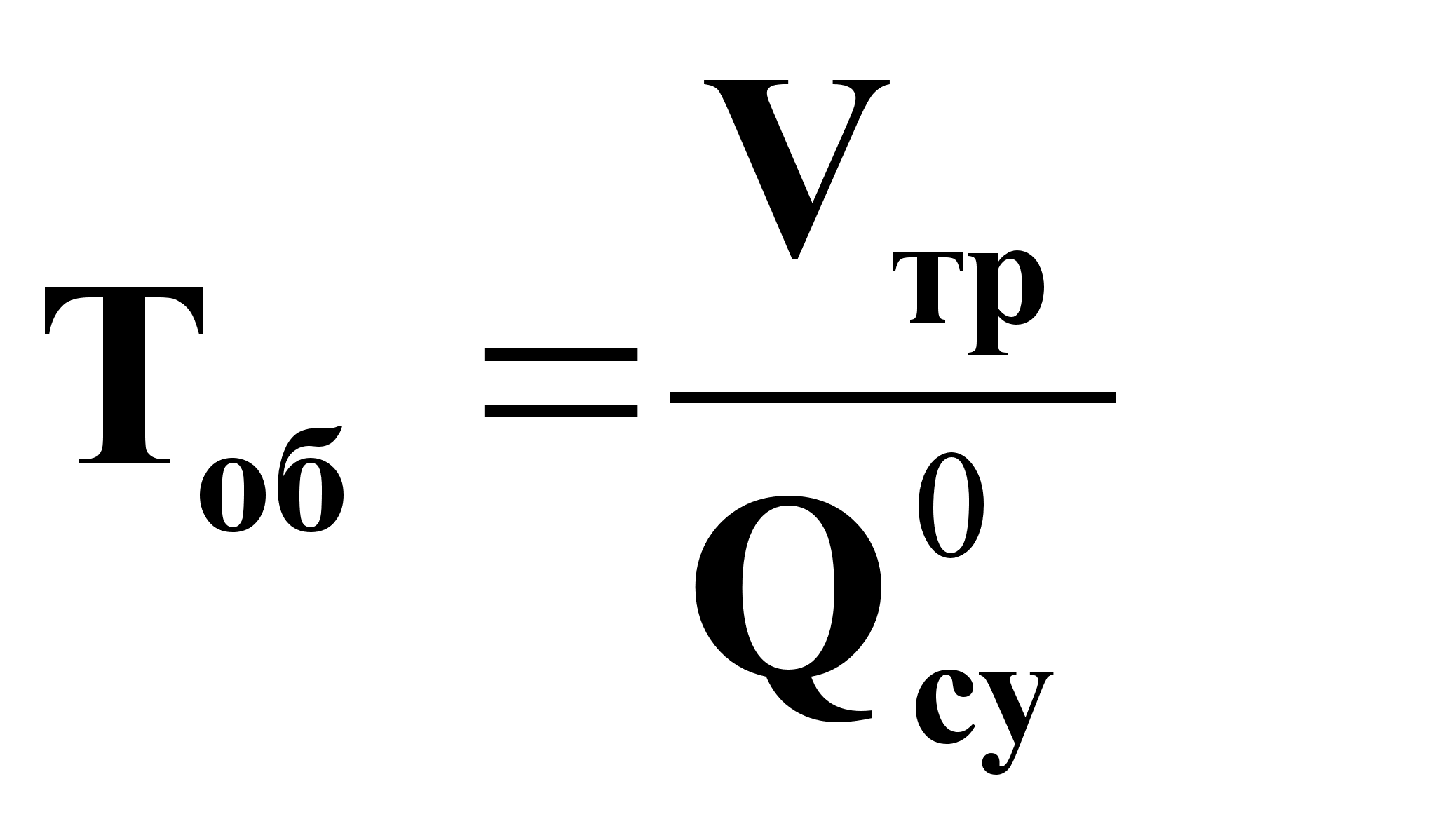
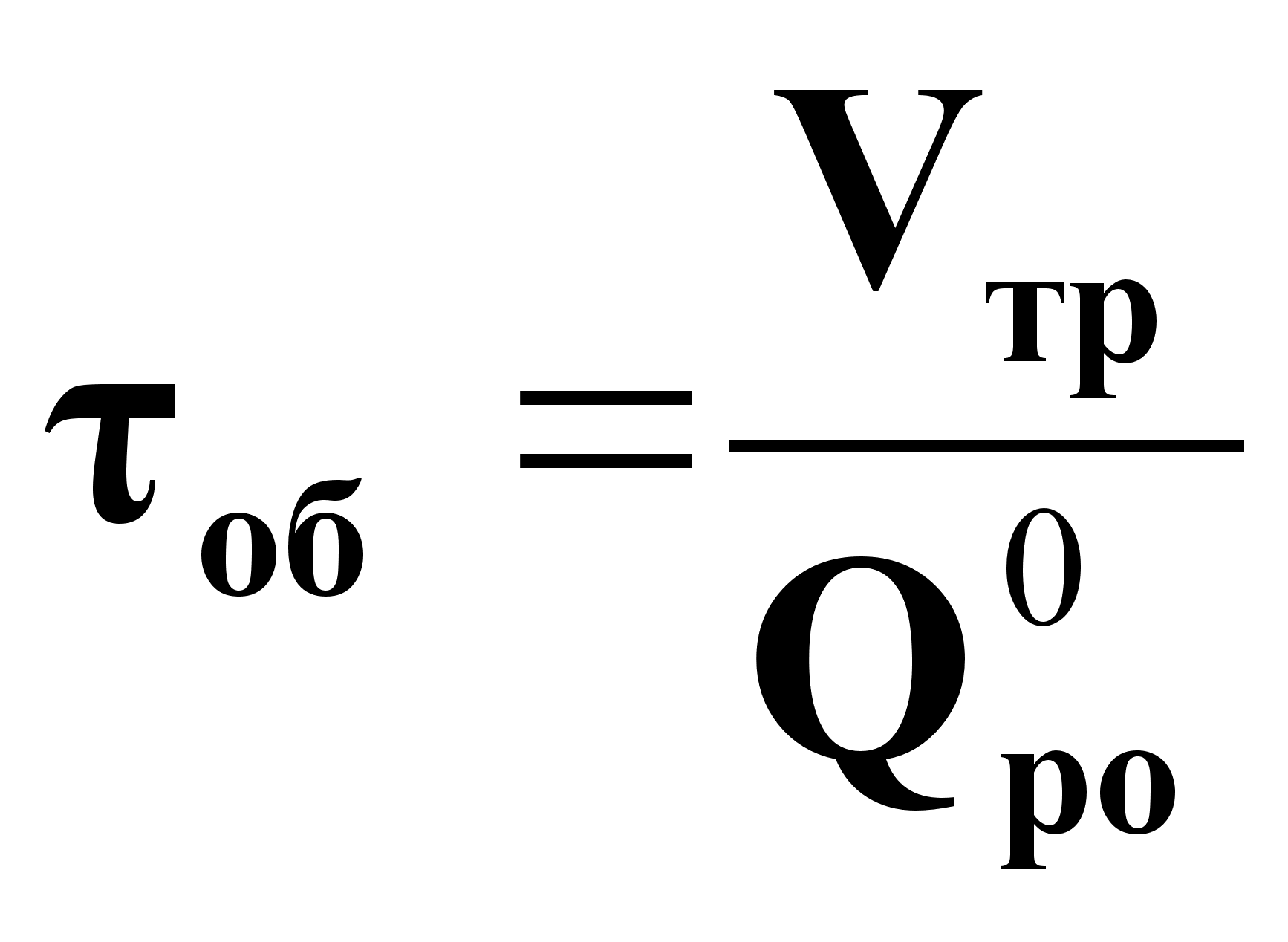 .
.
Автоматизация центробежных насосов
Основные показатели работы насосов
Производительность, или подача, Q (м3/ceк) - объем жидкости, подаваемой насосом в нагнетательный трубопровод в единицу времени.
Напор Н (м) - удельная энергия, сообщаемая насосом единице веса перекачиваемой жидкости.
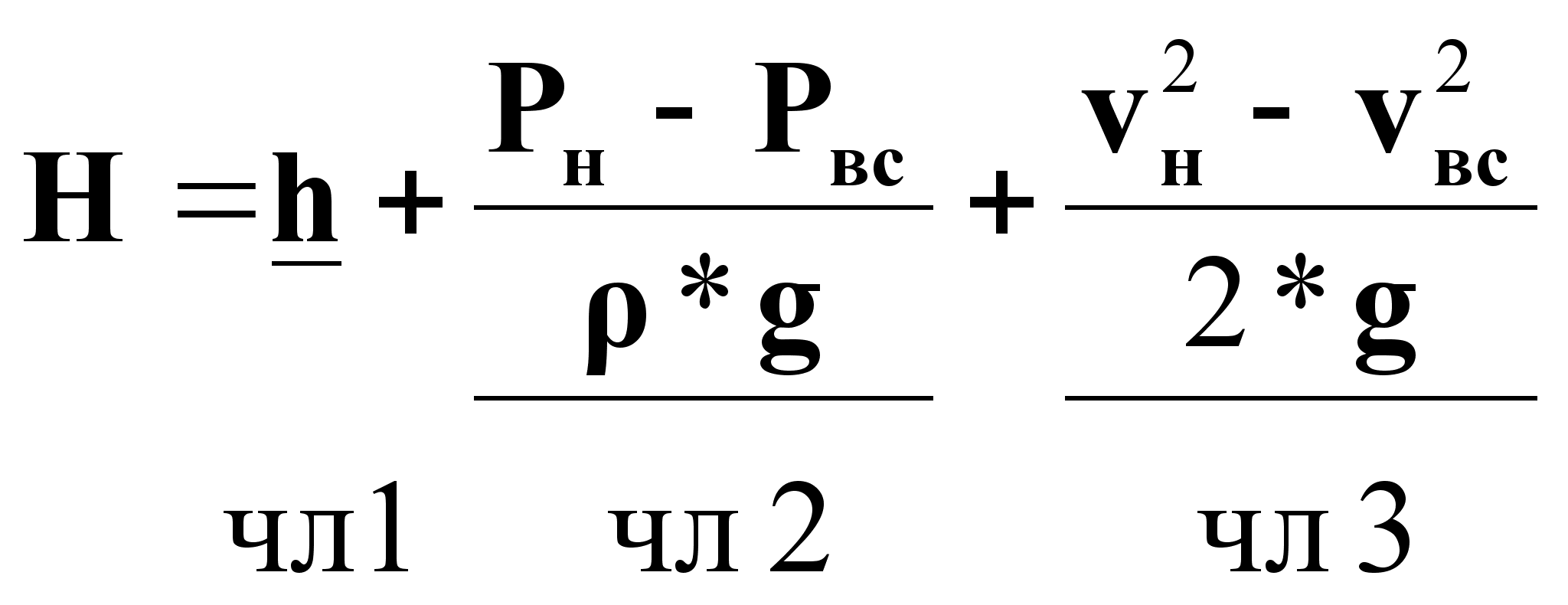 (1)
(1)
где чл.1 - высота подъема жидкости в насосе;
чл.2 - разность пьезометрических напоров;
чл.3 - разность динамических напоров.
Полезная мощность Nn - это мощность, затрачиваемая насосом на сообщение жидкости энергии:
![]() (2).
(2).
Мощность на валу насоса Ne – это отношение полезной мощности Nn к к.п.д. насоса:
![]() (3).
(3).
Коэффициент полезного действия насоса ηн
![]() (4).
(4).
где ηv = Q/QТ - объемный к.п.д.;
![]() - гидравлический
к.п.д.
- гидравлический
к.п.д.
ηмех - механический к. п. д.
Основная цель управления насосами - обеспечить эффективную работу насоса на сеть.
Насосы как объекты управления классифицируются по принципу действия на:
центробежные;
поршневые.
Схема центробежного насоса.
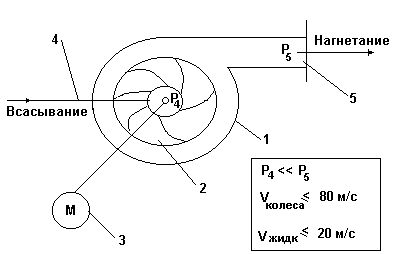
- корпус;
- рабочее колесо;
- привод насоса;
- линия всасывания;
– патрубок нагнетания.
Рис.1.
Принцип действия центробежных насосов - основан на создании центробежных полей давления при вращении рабочего колеса в жидкости.
Работа схемы.
В корпусе 1 вращается рабочее колесо 2 от привода 3.
При этом залитая в корпус жидкость также вращается и возникает центробежное поле давлений
с максимальным давлением на периферии (давление Р5)и минимальным давлением по оси потока (давление Р4) т.е. создается Р4 tпред;
давления - P < Pпред;
расходы - Q < Qмин (наличие потоков масла и охлаждающей жидкости).
Система защиты.
По сигналам «В схему защиты» - отключается действующий насос и включается резервный.
Материалы к лекции №5Автоматизация поршневых компрессоров
Вид теоретической индикаторной диаграммы
поршневого компрессора.
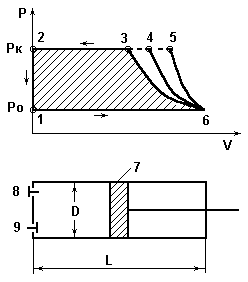
Рис.3.1.
Схема Пз-регулирования подачи поршневого компрессора
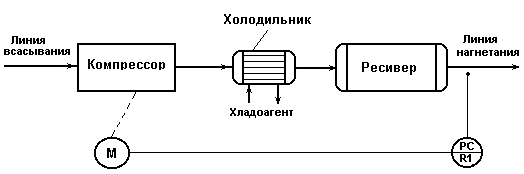
Рис.5.1
Схема регулирования подачи поршневого компрессора
путем изменения частоты вращения привода компрессора.
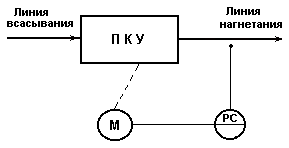
ПКУ - поршневая компрессорная установка.
Рис.5.2.
Схема регулирования подачи поршневого компрессора
путем дросселирования потока на линии всасывания.
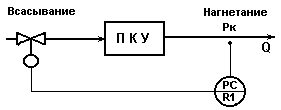
Рис.5.3.
Схема регулирования подачи поршневого компрессора
путем отжима клапанов.
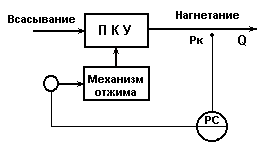
Рис.5.4.
Схема регулирования подачи поршневого компрессора
путем перевода компрессора на холостой ход.
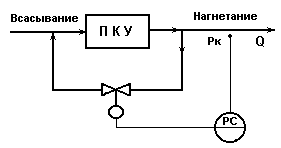
Рис.5.5.
Схема регулирования подачи 2х-ступенчатого компрессора
с воздействием на ИМ каждой ступени.
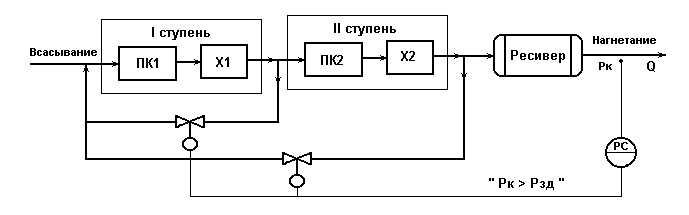
Рис.6.1.
Схема регулирования подачи 2х-ступенчатого компрессора
с воздействием на ИМ первой ступени.
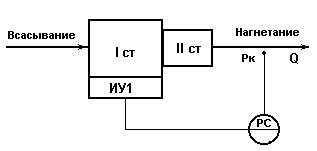
Рис.6.2.
Схема трехступенчатого компрессора.
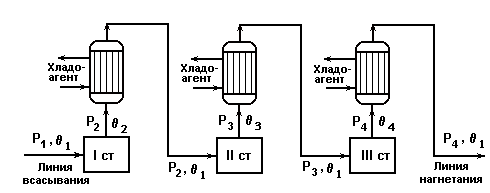
Рис.4.1.
Теоретическая индикаторная диаграмма
трехступенчатого сжатия.
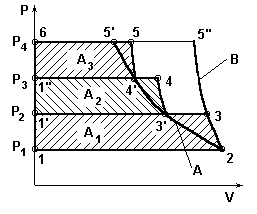
Рис.4.2.
Схема регулирования подачи 4х-ступенчатого компрессора с включением технологического оборудования после 2-ой и 4-ой ступеней.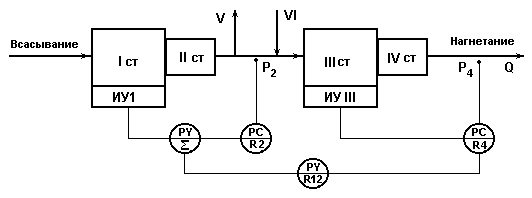
I II III IV - ступени компримирования;
V - линия промежуточного отбора среднего давления Р2 в технологическую схему;
VI - линия возврата газа из аппарата высокого давления.
Рис.6.3
Схема регулирования подачи 4х-ступенчатого компрессора с подключением технологического оборудования на входе 1-ой ступени, после 2-ой и 4-ой ступеней.
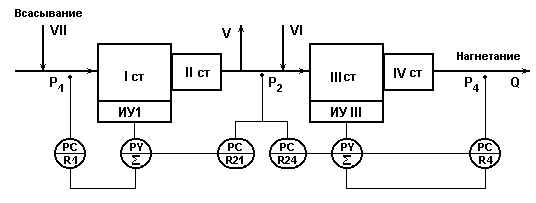
I II III IV - ступени компримирования;
V - линия промежуточного отбора среднего давления Р2 в технологическую схему;
VI - линия возврата газа из аппарата высокого давления.
VII - линия возврата газа из аппарата среднего давления.
Рис.6.4.
Структурная схема системы регулирования подачи
4-х ступенчатого компрессора для рис.6.3.
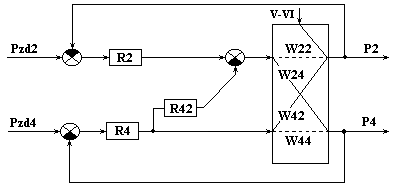
Рис. 6.3б
Структурная схема системы регулирования подачи
4-х ступенчатого компрессора для рис.6.4.
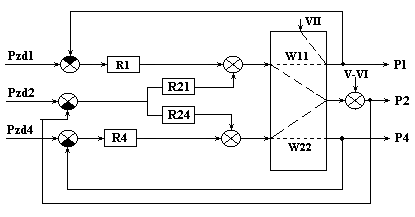
Рис.6.4б
Типовая схема автоматизации установки
с двухступенчатым поршневым компрессором.
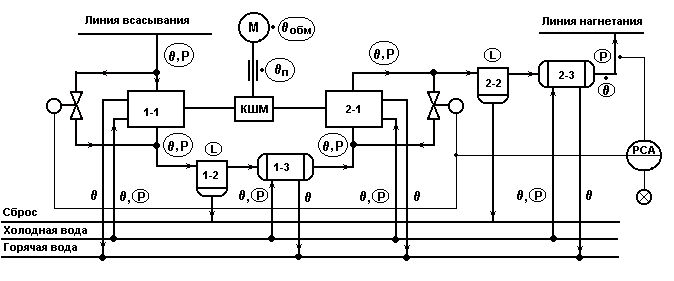
Обозначения на схеме:
1-1, 2-1 - цилиндры ступеней 1и 2; 1-2, 2-2 - масловлагоотделители;
1-3, 2-3 - холодильники.
![]() Р - сигнализируемый
и контролируемый
параметр;
Р - сигнализируемый
и контролируемый
параметр;
Р - контролируемый параметр.
Рис.7.1.
Типовое решение автоматизации установки
с двухступенчатым поршневым компрессором.
Показателем эффективности процесса является подача компрессорной установки.
Регулирование подачи осуществляется по давлению в линии нагнетания.
Регулирование.
В данной схеме используется метод регулирования подачи по давлению Р в линии нагнетания на выходе компрессорной установки путем перевода компрессора на холостой ход в результате открытия запорных клапанов РО1 и РО2 на линиях байпаса 1 и 2 ступеней компрессора.
Контроль.
Контролю в любой компрессорной установке подлежат температура, давление, уровень, потребляемая мощность.
Контроль температуры:
температура газа в линии нагнетания;
газа на входе и выходе каждой ступени;
п смазки в различных точках подшипников;
воды на входе и выходе холодильников;
обм обмоток электропривода.
Контроль давления:
Р газа на входе и выходе каждой ступени;
Р воды на входе в холодильники;
Р масла в магистрали (система смазки на схеме не показана);
Давление обладает меньшей инерционностью, чем температура при изменении технологических режимов, поэтому его используют для сигнализации, блокировок и защиты.
Контроль уровня:
Н конденсата в масловлагоотделителях;
Н масла в масляных баках (на схеме не показаны);
Н воды в гидрозатворах и газгольдерах (не показаны).
Контроль мощности:
мощность, потребляемая приводом - Nпр ;
контроль осуществляется измерительным устройством, установленным на валу привода.
Nпр определяет экономичность установки.
Сигнализация.
Сигнализации подлежат:
существенные отклонения давления газа в линии нагнетания;
повышение температуры и давления газа на входе и выходе каждой ступени - ↑, Р ↑;
повышение температуры подшипников - п ↑;
повышение температуры обмоток - обм ↑;
понижение уровня Н во всех контролируемых точках;
понижение давления воды на входе холодильников - Р ;
понижение давления масла - Рм ;
перегрузка привода Nпр ↑ .
Система защиты.
При существенном отклонении сигнализируемых параметров от заданных значений ,
когда в результате срабатывания блокировок и вмешательства обслуживающего персонала не удается восстановить заданный технологический режим,
отключается действующий привод и включается резервный.
Материалы к лекции №6Общая характеристика тепловых процессов
Фазовое равновесие теплоносителей.
Правило фаз:
s=k-f+2 (1),
где s - число степеней свободы данной системы;
f - число фаз системы;
k - число компонентов системы.
для трехфазной однокомпонентной системы:
s=1-3+2=0.
для двухфазной однокомпонентной системы:
s=1-2+2=1.
для однофазной однокомпонентной системы:
s=1-1+2=2.
Фазовые переходы в однокомпонентных системах.
Уравнение Клапейрона-Клаузиуса ![]() (2),
(2),
где Р - давление;
r - молярная теплота фазового перехода;
Т - температура фазового перехода (испарения, плавления, возгонки);
∆V - изменение объема 1 моля вещества при переходе его из одной фазы в другую.
Фазовые переходы в многокомпонентных системах.
Закон Генри: ![]() (3),
(3),
где mi - молекулярная доля газа в растворе;
ψ - константа Генри;
pi - парциальное давление газа над жидкостью.
Закон Рауля: ![]() (4),
(4),
где рА - парциальное давление компонента А в парах;
РА - давление паров чистого компонента А;
![]() - молекулярная
доля этого
компонента
в растворе.
- молекулярная
доля этого
компонента
в растворе.
Закон распределения: ![]() (5),
(5),
где К - молярный коэффициент распределения;
mCA - концентрация вещества С в жидкости А
в г-моль/л;
mCВ - концентрация вещества С в жидкости B.
Связь основных параметров
теплоносителей в газовой фазе.
Закон Бойля:
P*V=const при T=const (1).
Закон Гей-Люссака:
![]() (2а),
(2а),
или на основании (2а) можно получить при Р=const:
![]() (2б),
(2б),
На основании (1) и (2б) можно также получить:
![]() при Р=const (3),
при Р=const (3),
или
![]() при V=const (4).
при V=const (4).
На основании (1)и (2) получают также формулу для приведения объема газа к нормальным условиям:
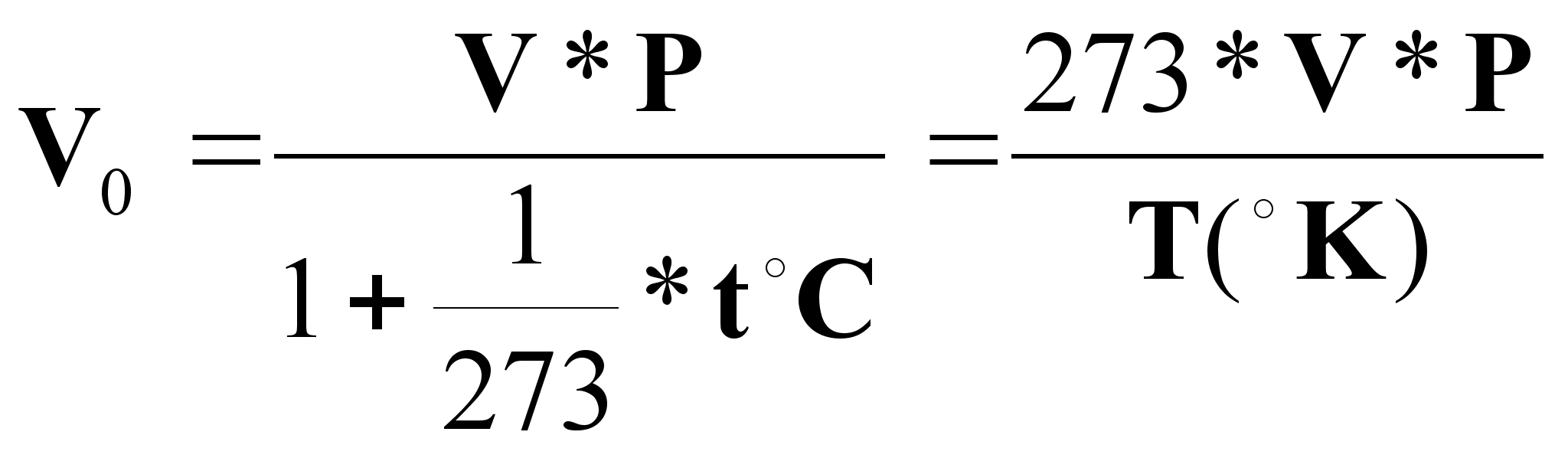 (5),
(5),
Закон Авогадро: в одинаковых объемах газа при одинаковых температуре и давлении содержится одно и то же количество молекул.
1г-мол. любого вещества в газообразном состоянии занимает 22,4л.;
1кг-мол. → 22,4 м3 и содержит 6,03*1023 молекул.
Уравнение Менделеева – Клапейрона.
для 1 г-моля газа:
P*V=R*T (6)
для n г-молей газа:
P*V = n*R*T (7)
Если количество газа выражается в граммах:
![]() (8)
(8)
откуда: ![]() (9)
(9)
или ![]() (10).
(10).
Закон Дальтона:
![]() (11).
(11).
Следствие из законов Дальтона и Бойля:
![]() (12),
(12),
где рi - парциальное давление компонента в газовой смеси;
vi /Vсм - парциальный объем компонента в единице объема газовой смеси;
Pсм - общее давление смеси.
Физические параметры и скорости движения теплоносителей.
Удельные теплоемкости.
Размерности удельных теплоемкостей с:
![]() ;
;
![]() ;
;
![]() .
.
Зависимости удельных теплоемкостей от температуры:
для заданной температуры Т:
c=a1+b1*T+c1*T2 (1),
где a1, b1, c1 - коэффициенты для данного вещества.
для заданного диапазона температур:
![]() (2),
(2),
где Т1 и Т2 - заданный интервал температур.
Молярная удельная теплоемкость твердого тела:
![]() (3),
(3),
где n - число атомов в молекуле.
Теплоемкости газов:
cp - при p = const или cv при V=const.
![]() (4),
(4),
где М - масса 1моля газа (кг/моль);
R - универсальная газовая постоянная, R=1,985 ккал/((кг/моль)*град).
Для воздуха : cp=1,4*cv.
Теплота испарения
Эмпирические формулы для расчета молекулярной теплоты испарения (в ккал/кг или кал/г):
rисп= 21*Tкип; (5а)
rисп= Tкип*(9,5*lgTкип-0,007*Ткип); (5б)
rисп= Tкип(8,75+4,571*lgТкип) (5в).
Эмпирическая формула для расчета теплоты испарения rисп2 для температуры Т2 ,:
![]() (6),
(6),
где rисп2 - искомая теплота испарения при температуре Т2;
rисп1 - известная теплота испарения при температуре Т1;
к - поправочный коэффициент, k=f(T1,T2,Tкрит).
Определение теплоты испарения по энтропийным диаграммам:
rисп=iжидк- iгаз (7),
где iжидк, iгаз - теплосодержание, дж/кг (или ккал/кг).
Плотности для жидких и газовых теплоносителей.
Эмпирическая формула для определения плотности жидкости ρtпри заданной температуре tср:
ρt = ρ0-βt*(tср-20○С) (8),
где ρ0 - плотность жидкости при t0=20○С;
βt - температурная поправка на 1○С
Для чистых жидкостей ρt можно найтипо формуле:
![]() (9),
(9),
где - коэффициент объемного расширения жидкости, град-1;
t=tср-t0 - разность между температурой среды и t=20C.
Плотность газов при 0°С и 760 мм рт ст. на основании закона Авогадро:
![]() (10)
(10)
или
![]() (11),
(11),
где М – молекулярный вес газа.
Плотность смеси см при заданных температуре и давлении:
см=b1*1+ b2*2+… *n (12),
где b1… bn - объемные доли компонентов;
1 n - плотности компонентов, кг/м3.
Коэффициенты теплопроводности.
Коэффициент теплопроводности для жидкостей при отсутствии справочных данных:
![]() (13),
(13),
где
А=3,58*10-8 - для ассоциированных жидкостей;
А=4,22*10-8 - для неассоциированных жидкостей;
с - удельная теплоемкость жидкости, Дж/(кг*град);
- плотность жидкости, кг/м3;
М - молярная масса, кг/кмоль.
Коэффициент теплопроводности смеси жидкостей:
![]() (14),
(14),
где а1…аn - массовые доли компонентов в смеси;
1…n - коэффициенты теплопроводности компонентов, вт/(м*град).
Вязкость теплоносителей.
Зависимость вязкости газов t от температуры:
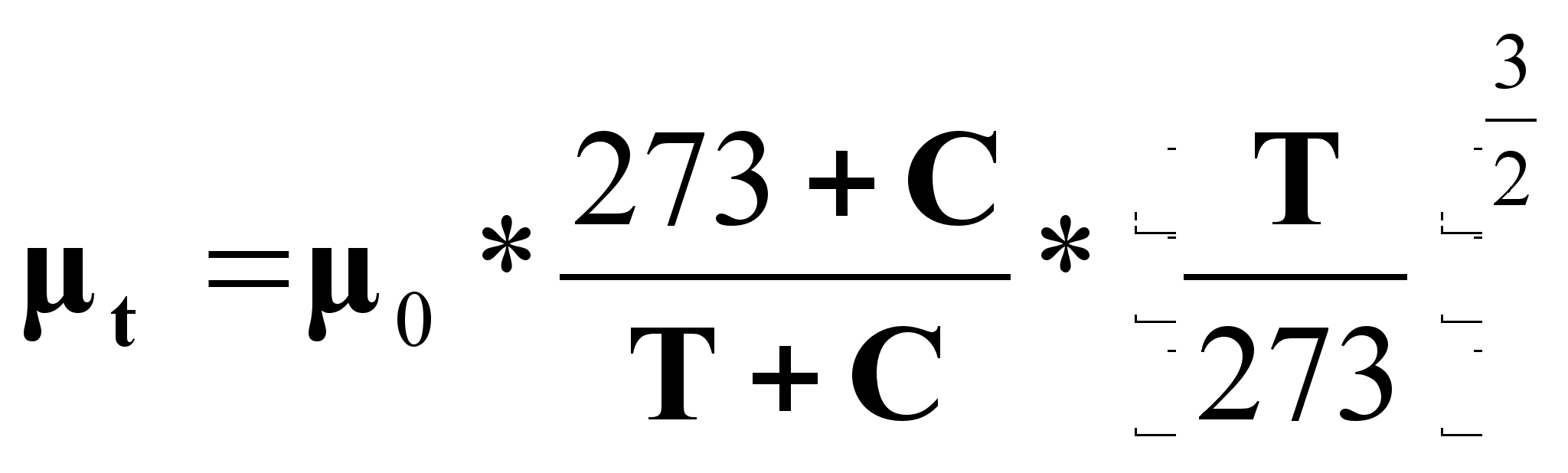 (15),
(15),
где 0 - вязкость при 0С;
Т - температура в К;
С - константа.
Вязкость газовых смесей см:
![]() (16),
(16),
где Мi - молярные массы компонентов смеси, кг/кмоль;
i - динамические вязкости компонентов, Па*с;
![]() - объемные
доли компонентов
в смеси.
- объемные
доли компонентов
в смеси.
Вязкость смеси неассоциированных жидкостей:
![]() (17),
(17),
где i - вязкости компонентов смеси, Па*с;
mi - молярные доли компонентов в смеси, кг/кмоль.
Вязкость разбавленных суспензий:
![]() (18),
(18),
где ж - вязкость чистой жидкости, Па*с;
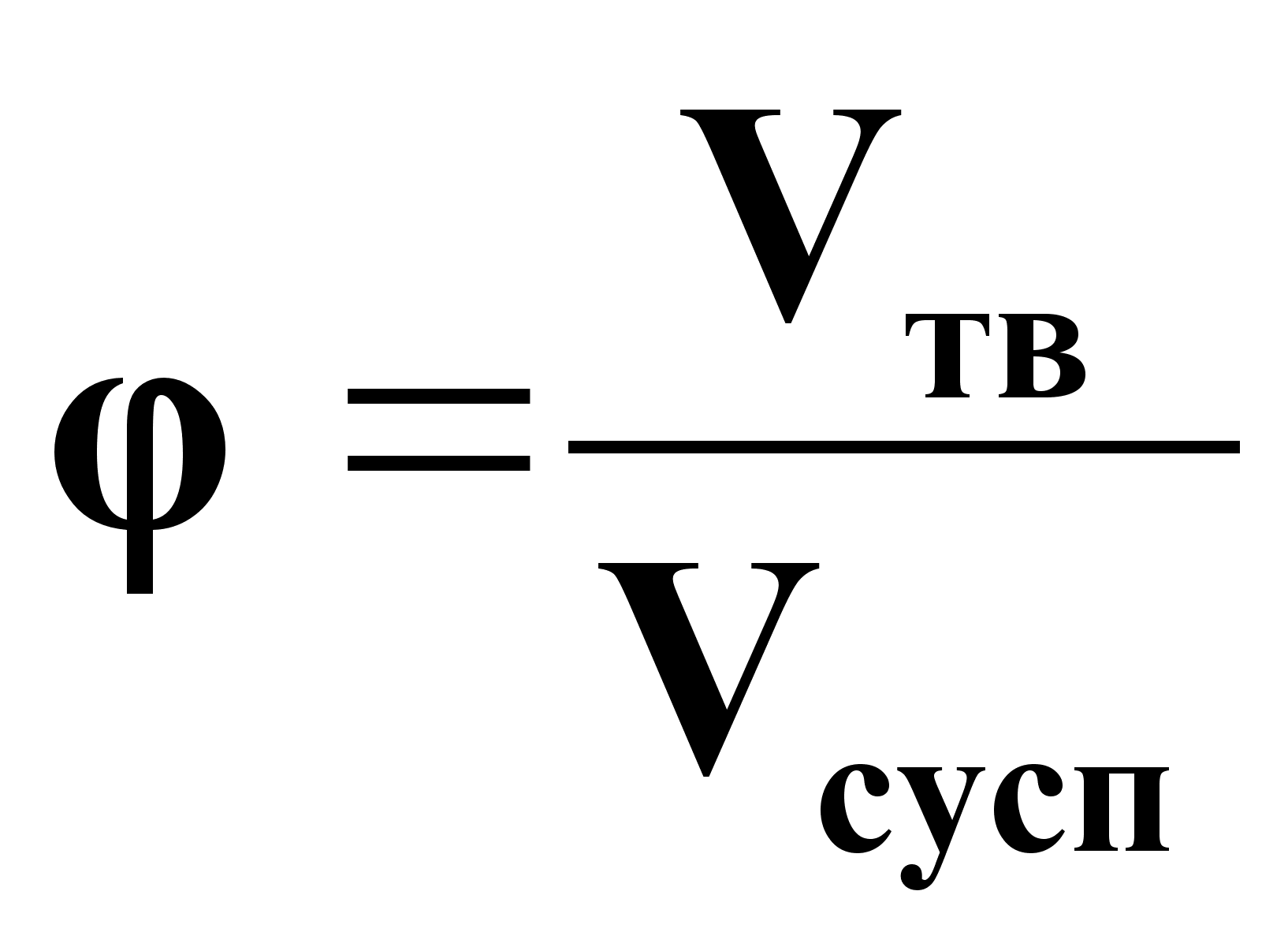 - объемная
доля твердой
фазы в суспензии.
- объемная
доля твердой
фазы в суспензии.
Скорости теплоносителей.
Средние скорости движения среды:
![]() (19),
(19),
где линср - средняя линейная скорость, м/с;
мср - средняя массовая скорость, кг/(м2*с);
Q - объемный расход, м3/с;
G - массовый расход, кг/с;
S - площадь сечения потока, м2.
Зависимость между массовой и линейной скоростью:
![]() (20),
(20),
где - плотность среды.
Рекомендуемые скорости:
для жидкостей в трубах диаметром 25-57мм от (1,5-2) м/c до (0,06-0,3) м/с.
Средняя рекомендуемая скорость для маловязких жидкостей составляет 0,2-0,3 м/с.
Для газов при атмосферном давлении допускаются массовые скорости от 15-20 до 2-2,5 кг/(м2*с), а линейные скорости до 25м/с;
для насыщенных паров при конденсации рекомендуются до 10 м/с.
Тепловая нагрузка аппарата.
Тепло, отдаваемое более нагретым теплоносителем Q1, затрачивается на нагрев более холодного теплоносителя Q2 и на потери в окружающую среду Qпот.:
Q1= Q2+ Qпот. (1)
Так как Qпот= 2-3%, то им можно пренебречь и считать:
Q1 = Q2 = Q (2),
где Q – тепловая нагрузка аппарата.
Уравнение теплового баланса аппарата.
Q = G1*(I1Н-I1К) = G2*(I2К-I2Н) (3),
где G1 и G2 - массовые расходы теплоносителей, кг/с;
I1Н и I2Н - начальные энтальпии теплоносителей, дж/кг;
I1К и I2К и - конечные энтальпии теплоносителей, дж/кг.
Энтальпии теплоносителей:
Ii=ci*i (4).
Тепловой баланс аппарата при использовании теплоносителей, не изменяющих агрегатного состояния:
Q = G1*с1*(1Н-1К) = G2*с2*(2К-2Н) (6),
где с1 и с2 - средние удельные теплоемкости.
Тепловые балансы теплоносителя
при изменении его агрегатного состояния.
Теплоноситель – насыщенный пар, который конденсируется и конденсат не охлаждается: т = нп =кт .
Gт (iт – iкт ) = Gт * срт *т - Gт * сркт *кт = Gт *rт.
Теплоноситель – пересыщенный пар, который конденсируется и конденсат не охлаждается: т > нп =кт
Q=Qт –Qкт =Gт *(iт – iкт )= Gт * срт *(т - нп)+Gт *rт =
= Gт * срт *нп - Gт * срт *нп + Gт * срт *нп - Gт * сркт*кт=
= Gт * срт *т - Gт * сркт*кт .
Теплоноситель – пересыщенный пар, который конденсируется и конденсат охлаждается: т > нп > кт:
Q=Qт –Qкт =Gт *(iт – iкт )=
Gт * срт *(т - нп)+Gт *rт + Gт * сркт *(нп - кт) =
= Gт * срт *т - Gт * срт *нп + Gт * срт *нп -
- Gт * сркт*нп + Gт * сркт*нп - Gт * сркт*кт=
= Gт * срт *т - Gт * сркт*кт .
Основное уравнение теплопередачи.
Q = K*F*tср* (1),
где
F - поверхность теплообмена;
tср - средний температурный напор;
- время теплообмена;
К - коэффициент теплопередачи:
![]() (2).
(2).
Выражения для определения коэффициента К
в зависимости от способа передачи тепла.
При передаче тепла теплопроводностью К - это коэффициент теплопроводности , определяемый на основе закона Фурье:
![]() (3)
(3)
При конвективном теплообмене К - это коэффициент теплоотдачи , определяемый на основе закона Ньютона:
![]() (4),
(4),
При передаче тепла путем излучения К - коэффициент взаимного излучения с1-2 излучающих тел:
K=с1-2
= пр*K0*108
= ![]() (5),
(5),
где
К0 - константа лучеиспускания;
пр = 1 *2 - приведенная степень черноты;
1 и 2 - степени черноты излучающих тел.
Движущая сила при прямотоке теплоносителей.
Схема прямоточного движения теплоносителей.

Рис.1.
График изменения температуры среды при прямотоке.
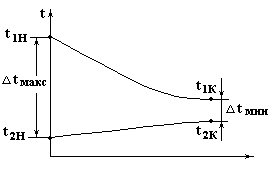
Рис.2
![]() (1),
(1),
При (Δtмакс/Δtмин) ![]() (2).
(2).
При ![]() :
: 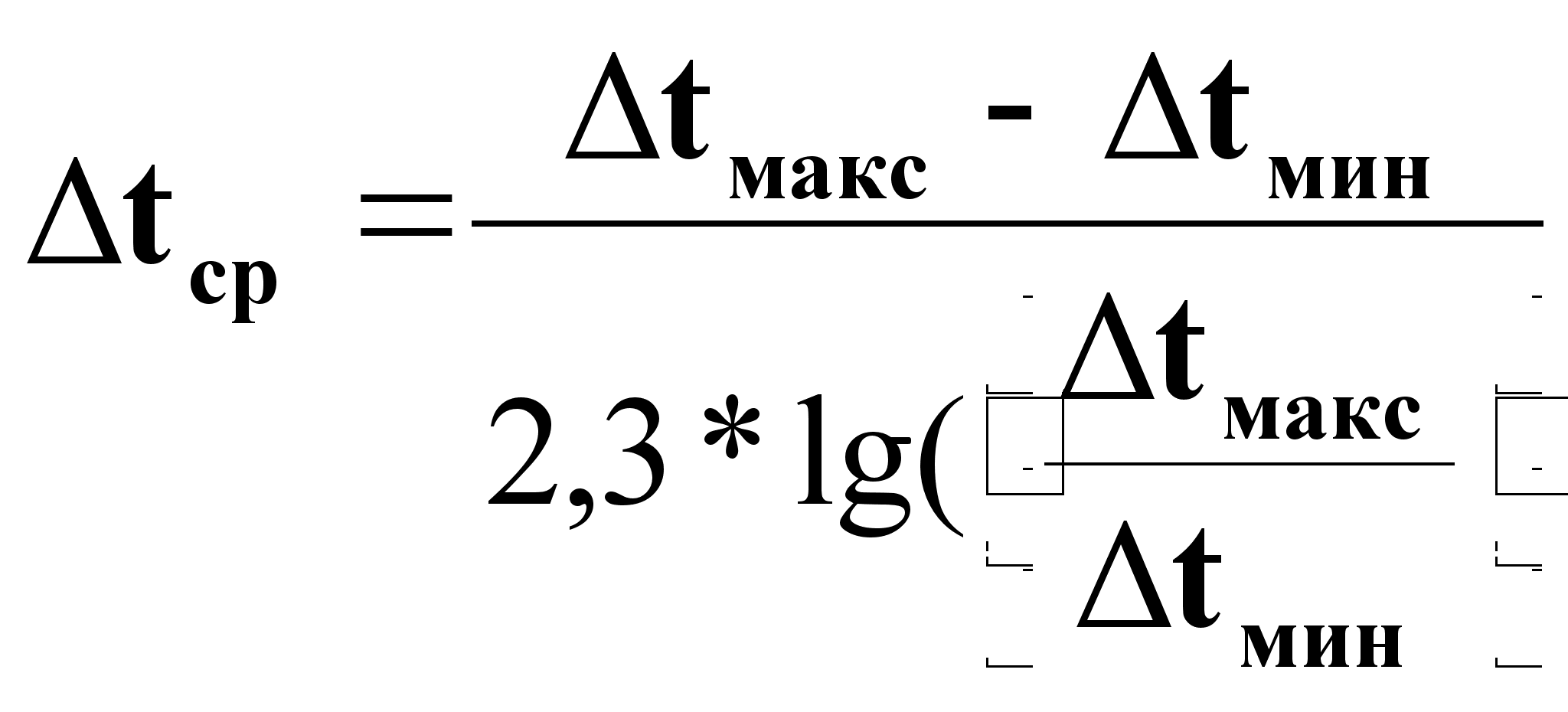 (3).
(3).
Движущая сила при противотоке теплоносителей.
Схема противоточного движения теплоносителей.

Рис.3.
График изменения температур при противотоке.
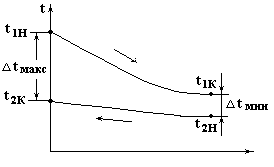
Рис.4.
![]() (1).
(1).
Затем используют те же соотношения (2) и (3), что и для прямотока, для определения средней движущей силы процесса.
Материалы к лекции №7Автоматизация кожухотрубных теплообменников
Схема кожухотрубного теплообменника
с неизменяющимся агрегатным состоянием веществ.
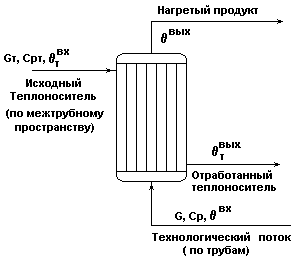
Рис.1.
Технологический процесс: нагревание технологического потока G до температуры θвых с помощью теплоносителя Gт с неизменяющимся агрегатным состоянием.
Показатель эффективности: θвых.
Цель управления: поддержание θвых= θзд.
Математическое описание на основе физики процесса.
Движение теплоносителей осуществляется противотоком при заданных θтвх, θтвых, θвых, θвх.
Движущая сила процесса: ![]() (1),
(1),
где
![]() .
.
Тепловая нагрузка аппарата: ![]() (2).
(2).
Q(дж/с) позволяет определить Gтэфф и Gэфф на основе тепловых балансов:
![]() (3а);
(3а);
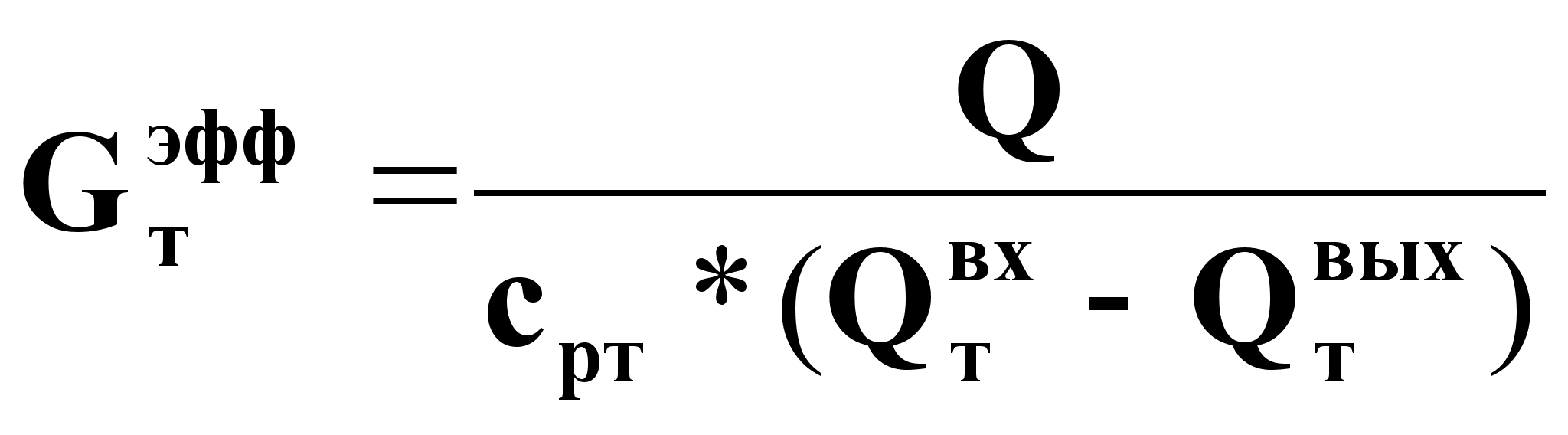 (3б);
(3б);
![]()
![]() (4а);
(4а);
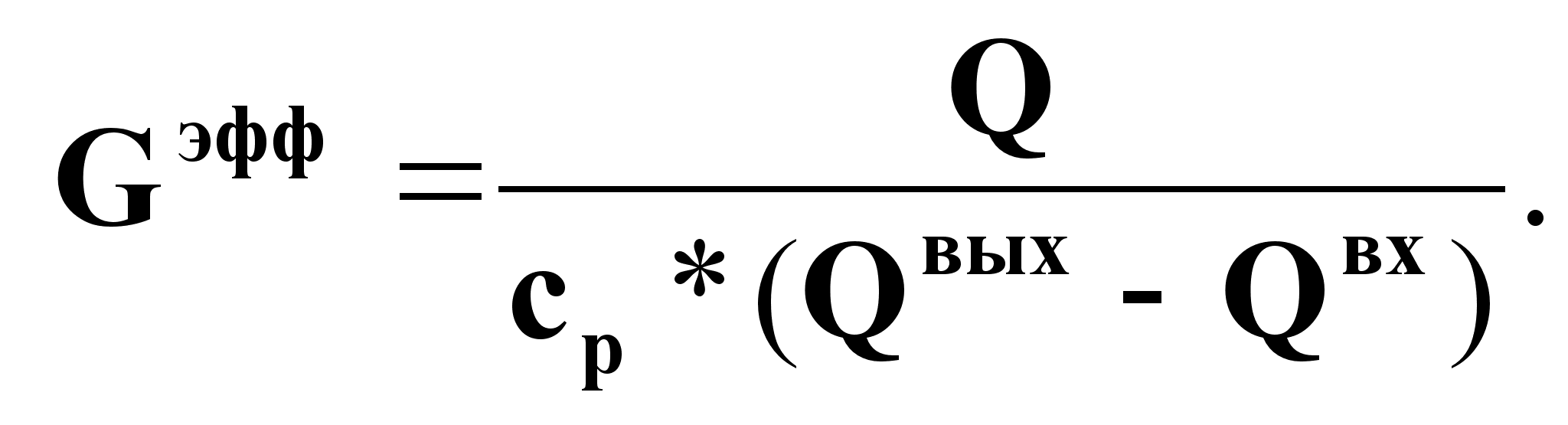 (4б).
(4б).
Эффективное время пребывания:
![]() . (5).
. (5).
Математическое описание на основе теплового баланса.
Уравнение динамики:
![]() (6).
(6).
Уравнение
статики при
![]() :
:
![]() (7)
(7)
На
основании (6) и
(7) можно принять:![]() . (8).
. (8).
Информационная схема объекта.
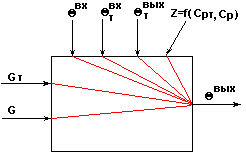
Рис.2.
Возможные управляющие воздействия:![]() .
.
Возможные контролируемые возмущения: ![]() .
.
Возможные неконтролируемые возмущения: ![]() .
.
Возможная управляемая переменная: ![]() .
.
Анализ динамических характеристик объекта.
Уравнение динамики в нормализованном виде.
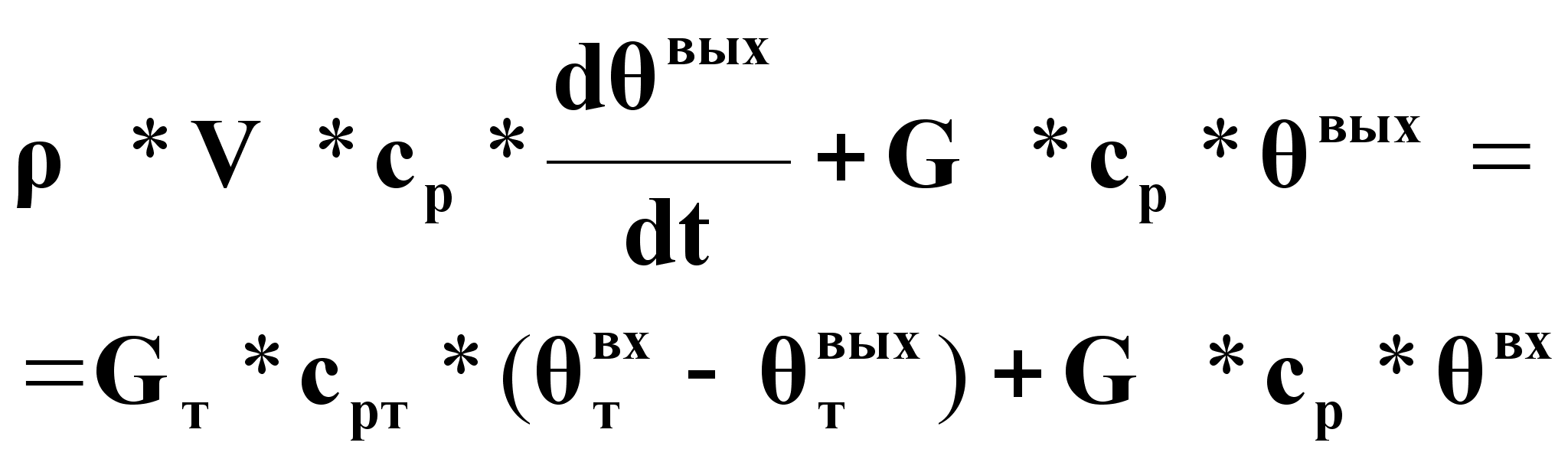 (9).
(9).
На основе
этого уравнения
динамики объект
по каналу ![]() описывается
математической
моделью апериодического
звена 1-го порядка:
описывается
математической
моделью апериодического
звена 1-го порядка:
![]() (10),
(10),
где: ![]() ;
; 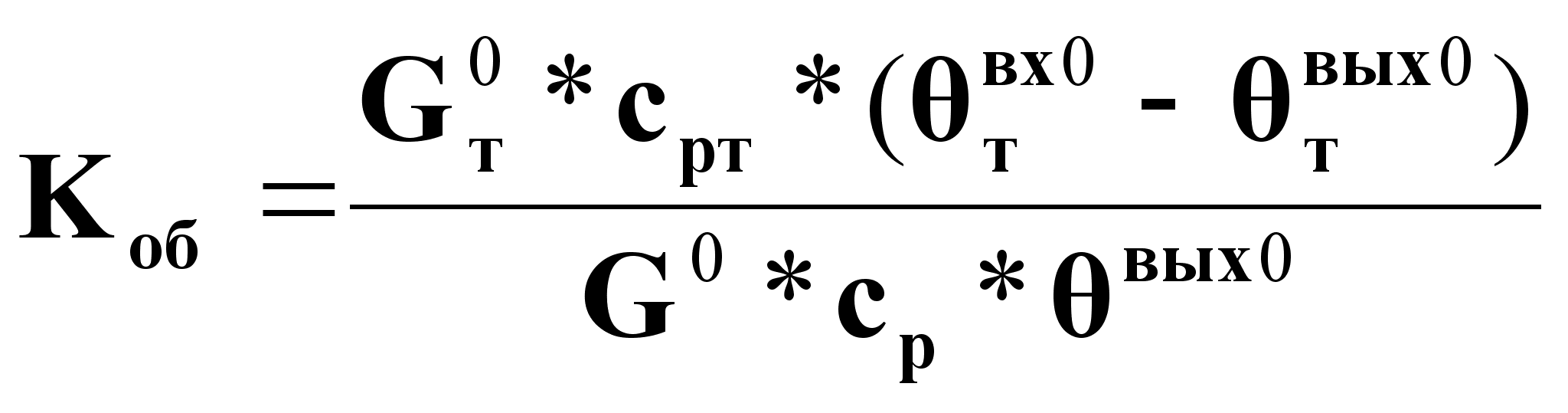 .
.
Объект имеет транспортное запаздывание:
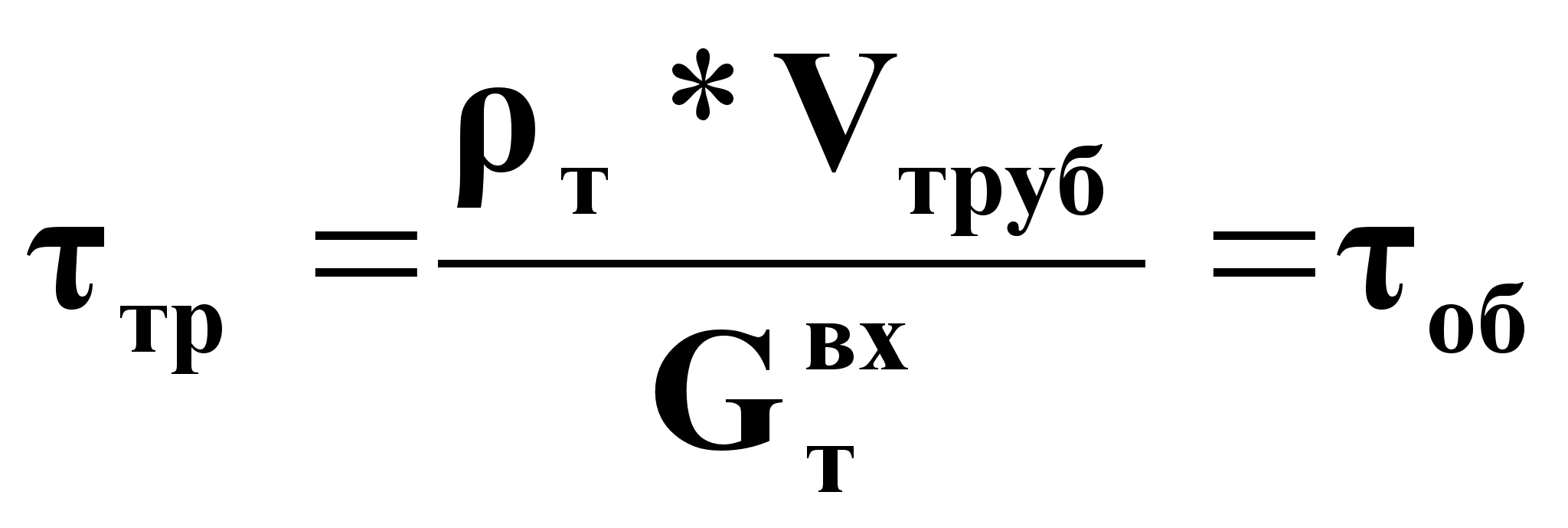 (11),
(11),
где Vтруб - объем трубопровода от Р.О. до входа в аппарат.
Таким образом, в целом динамика объекта по каналу управления описывается математической моделью апериодического звена 1-го порядка с запаздыванием:
![]() (12).
(12).
Анализ статической характеристики объекта.
Из уравнения статики выразим вых в явном виде:
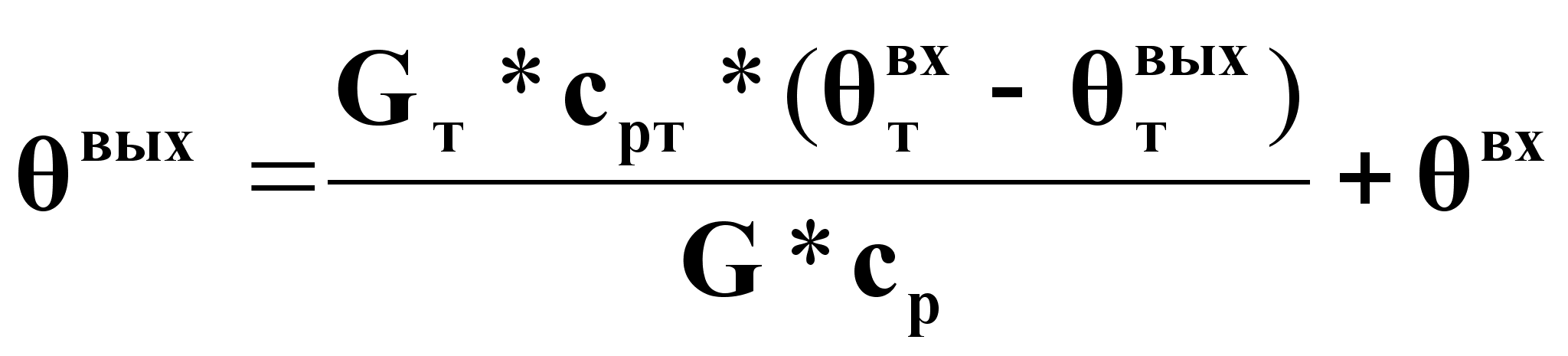 (13).
(13).
Статическая характеристика линейна по каналам: ![]() .
.
Статическая характеристика нелинейна по каналу ![]() .
.
Статическую характеристику можно линеаризовать по отношению к G введением стабилизации соотношения расходов: ![]() , тогда получим:
, тогда получим:
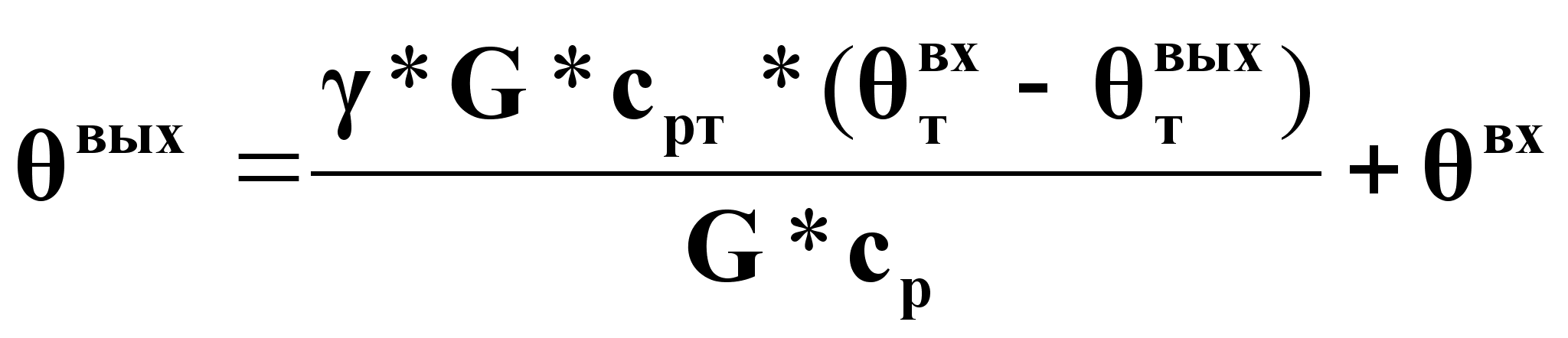 (14).
(14).
Линеаризованное представление статической характеристики через разложение в ряд Тейлора:
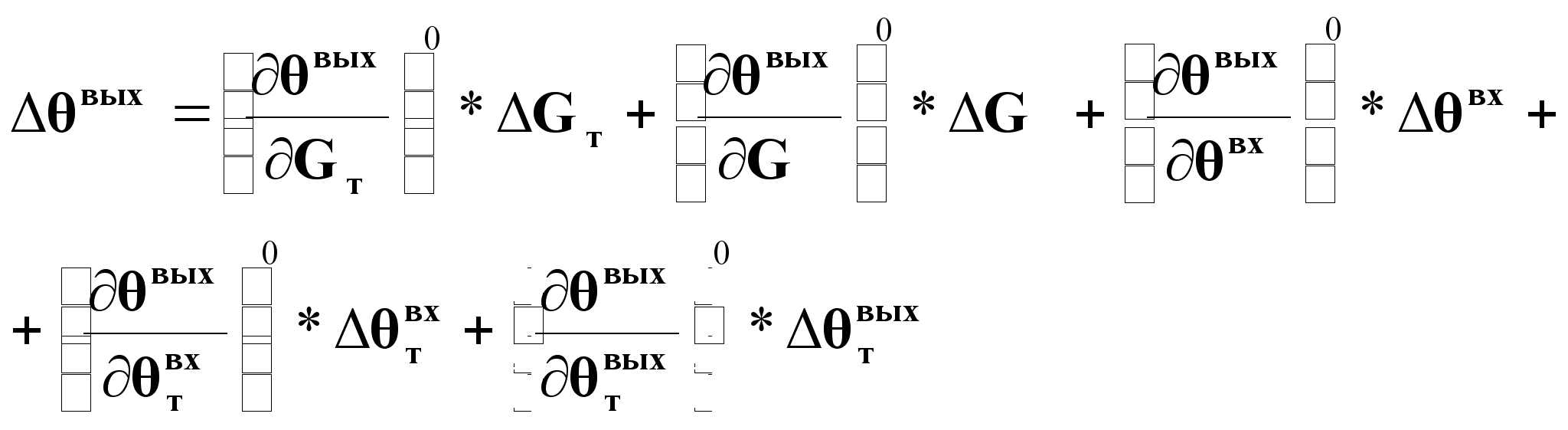 (15).
(15).
Линеаризованное представление приращения выходной переменной через приращения всех возможных входных переменных:
![]() (16).
(16).
Типовая схема автоматизации
кожухотрубного теплообменника.
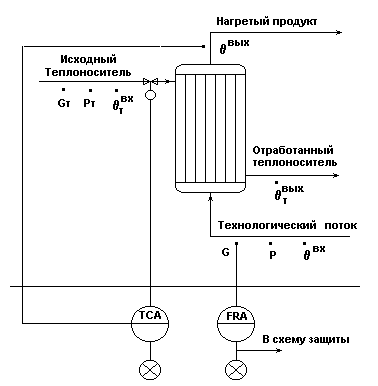
Рис.3.
Типовое решение автоматизации.
Типовое решение автоматизации кожухотрубных теплообменников включает в себя подсистемы регулирования, контроля, сигнализации и защиты.
Регулирование.
Регулирование температуры![]() по подаче теплоносителя Gт - как показателя эффективности процесса нагревания в кожухотрубном теплообменнике.
по подаче теплоносителя Gт - как показателя эффективности процесса нагревания в кожухотрубном теплообменнике.
Контроль.
расходы - Gт, G;
температуры - ![]() ;
;
давление - Рт, Р.
Сигнализация.
существенные отклонения вых от задания;
резкое падение расхода технологического потока G , при этом формируется сигнал «В схему защиты».
Система защиты.
По сигналу «В схему защиты» - отключается магистраль подачи теплоносителя Gт.
Схема парожидкостного теплообменника
(с изменяющимся агрегатным состоянием теплоносителя).
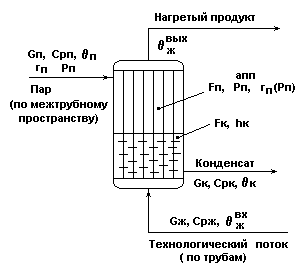
Рис.1.
Технологический поток (нагреваемая жидкость) Gж подается по трубкам теплообменника.
Теплоноситель с изменяющимся агрегатным состоянием (греющий пар) Gп подается по межтрубному пространству.
Показатель эффективности:![]() .
.
Цель управления: поддержание ![]() .
.
Математическое описание на основе физики процесса.
Теплопередача от паровой фазы теплоносителя:
![]() (1),
(1),
Теплопередача от жидкой фазы теплоносителя:
![]() (2),
(2),
где:![]() - количество
тепла, передаваемое
от паровой фазы
и конденсата
теплоносителя
в единицу времени,
дж/с;
- количество
тепла, передаваемое
от паровой фазы
и конденсата
теплоносителя
в единицу времени,
дж/с;
![]() - коэффициенты
теплопередачи
для паровой
фазы и конденсата
теплоносителя,
дж/(м2*К*с);
- коэффициенты
теплопередачи
для паровой
фазы и конденсата
теплоносителя,
дж/(м2*К*с);
![]() - поверхность
теплопередачи
для паровой
фазы и конденсата
теплоносителя,
м2;
- поверхность
теплопередачи
для паровой
фазы и конденсата
теплоносителя,
м2;
![]() - средняя
движущая сила
при теплопередаче
от паровой фазы
к жидкому
технологическому
потоку и от
конденсата
к жидкому
технологическому
потоку.
- средняя
движущая сила
при теплопередаче
от паровой фазы
к жидкому
технологическому
потоку и от
конденсата
к жидкому
технологическому
потоку.
Общая тепловая нагрузка парожидкостного теплообменника:
![]() (3).
(3).
Так как ![]() , то интенсивность теплопередачи от паровой фазы значительно выше, чем от конденсата.
, то интенсивность теплопередачи от паровой фазы значительно выше, чем от конденсата.
Поэтому на величину Q влияет величина соотношения Fп /Fк, которая зависит от уровня конденсата:
![]() (4а).
(4а).
где ![]() и
и ![]() (4б).
(4б).
На основании (4а) общая тепловая нагрузка Q также будет зависеть от уровня конденсата hк:
![]() (4в),
(4в),
Q(дж/с) позволяет определить Gпэффи Gжэфф на основе тепловых балансов:
![]() (5а);
(5а);
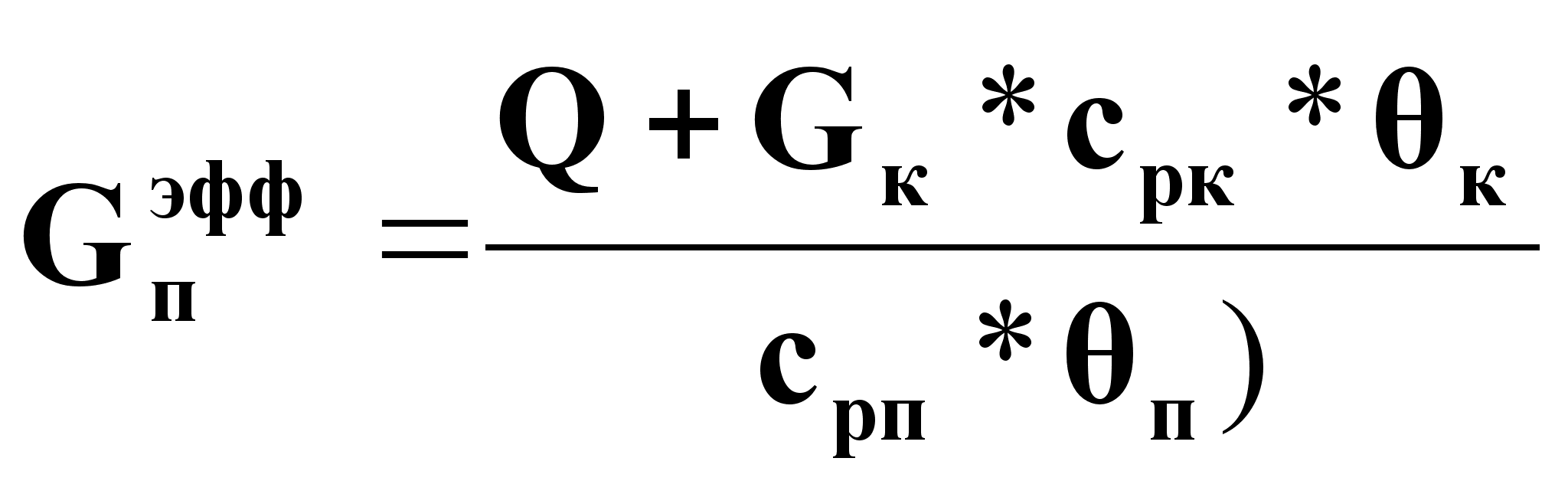 (5б);
(5б);
![]()
![]() (6а);
(6а);
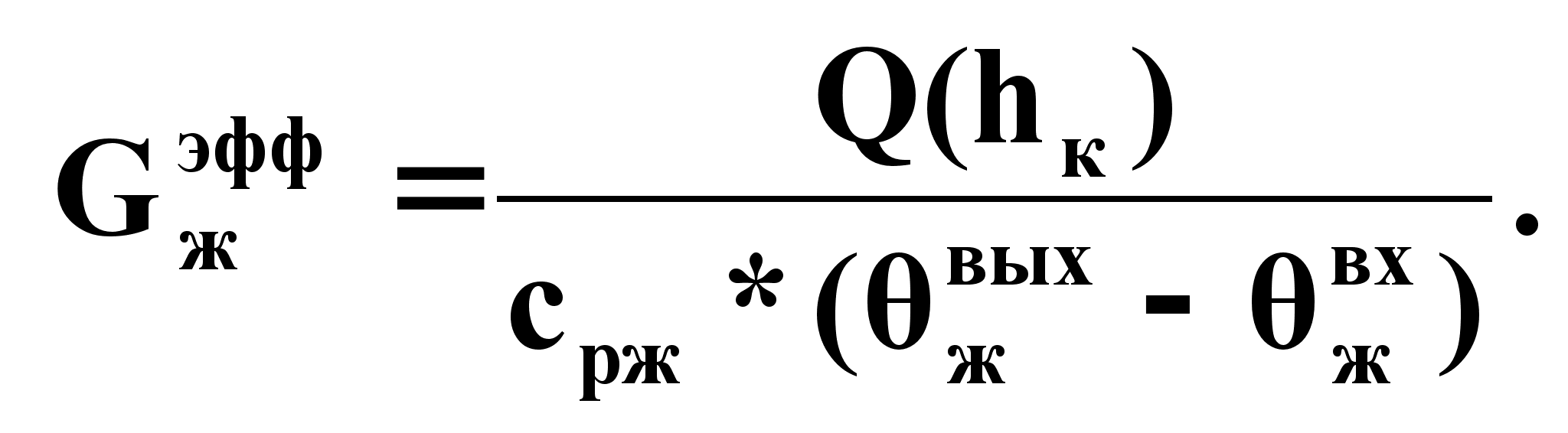 (6б),
(6б),
при hк =hэфф.
Эффективное время пребывания:
![]() . (7).
. (7).
Тепловой баланс парожидкостного теплообменника.
Уравнение динамики:
Полагаем:
пар перегретый
и конденсат
охлаждается
![]() :
:
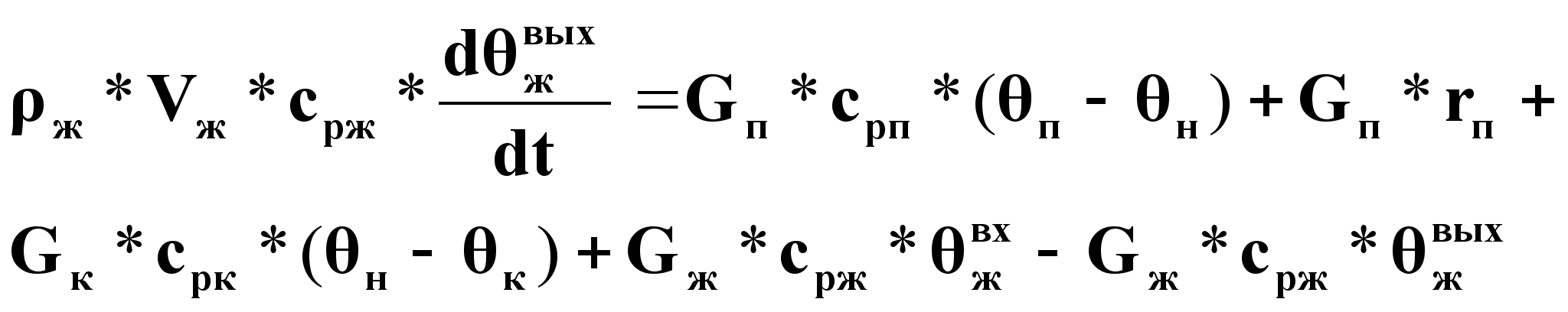 (8).
(8).
Уравнение
статики при
![]() :
:
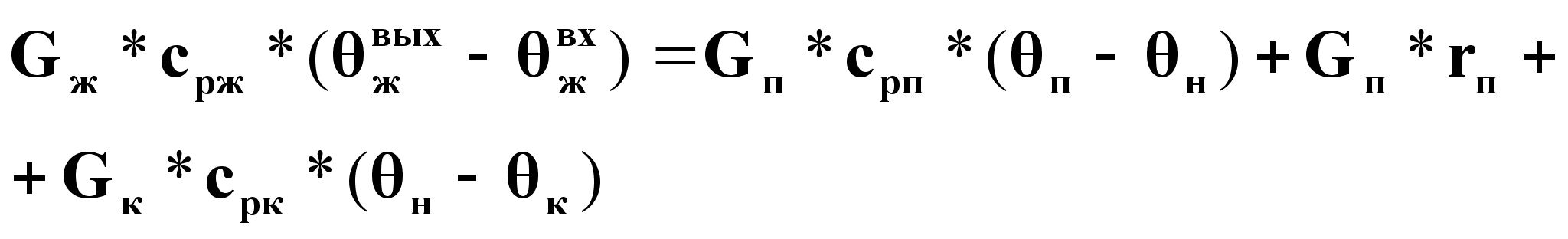 (9).
(9).
На основании (8) и (9) а также (6а) и (4в) можно записать:
![]() . (10),
. (10),
где
![]() ,
так как при Pп
кип
rп
.
,
так как при Pп
кип
rп
.
Материальный баланс по жидкой фазе
для межтрубного пространства.
Уравнение динамики:
![]() , (11),
, (11),
Уравнение
статики при
![]() :
:
![]() (12)
(12)
На
основании (11)
и (12) ![]() и предпочтительное
управляющее
воздействие
– Gк.
и предпочтительное
управляющее
воздействие
– Gк.
Материальный баланс по паровой фазе
для межтрубного пространства.
Уравнение динамики:
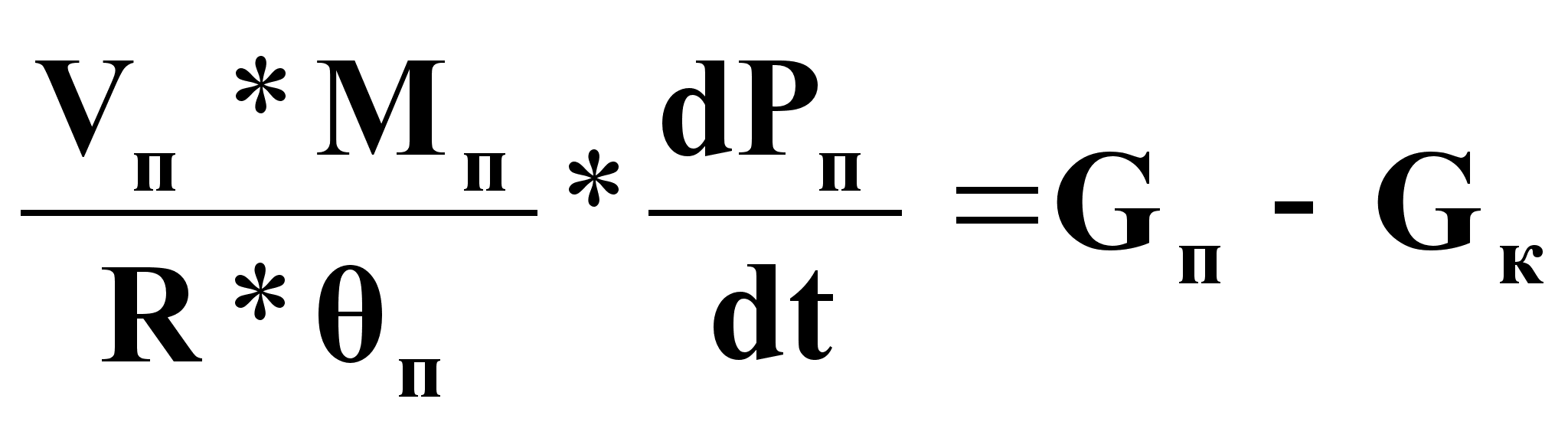 (14),
(14),
где Мп - мольная масса паровой фазы теплоносителя, кг/моль;
Рп - давление паровой фазы теплоносителя, Па;
п - температура паровой фазы теплоносителя, К,
Vп - объем паровой фазы теплоносителя, м3 .
Уравнение
статики при
![]() :
:
![]() (15).
(15).
На
основании (14)
и (15) ![]() и предпочтительное
управляющее
воздействие - Gп.
и предпочтительное
управляющее
воздействие - Gп.
Информационная схема объекта.
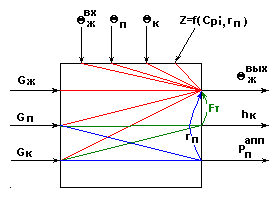
Рис.2.
Возможные управляющие воздействия:![]() .
.
Возможные контролируемые возмущения: ![]() .
.
Возможные неконтролируемые возмущения: ![]() .
.
Возможные управляемые переменные: ![]() .
.
Наиболее эффективные каналы управления:
![]() .
.
Анализ динамических характеристик парожидкостного теплообменника
как объекта управления температурой.
Исходные условия: ![]() .
.
Уравнение динамики в нормализованном виде.
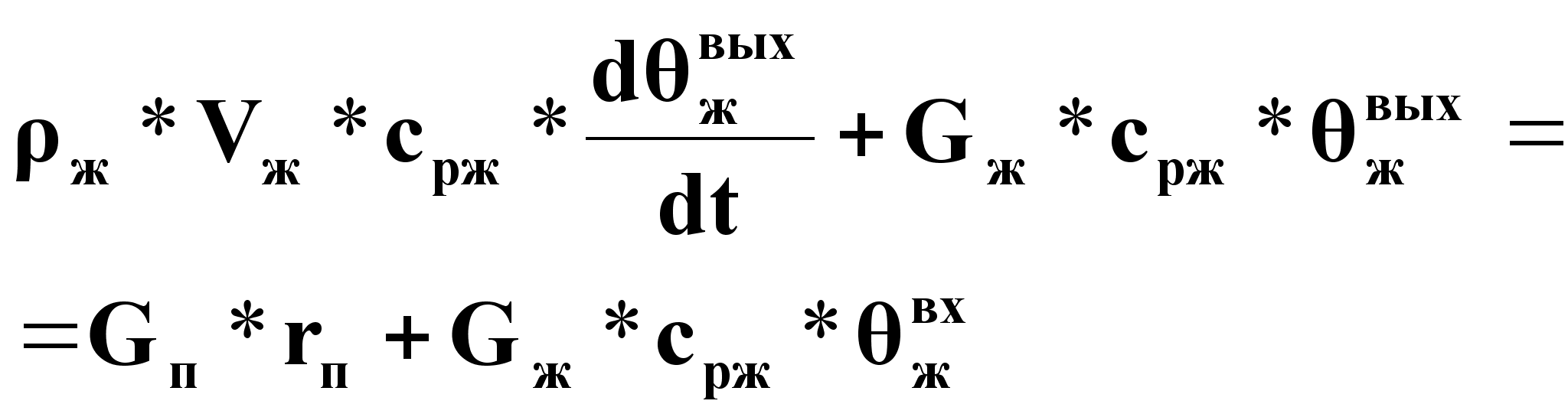 (17)
(17)
На основе этого уравнения динамики объект по каналу ![]() описывается математической моделью апериодического звена 1-го порядка:
описывается математической моделью апериодического звена 1-го порядка:
![]() (18),
(18),
где:
![]() ;
;
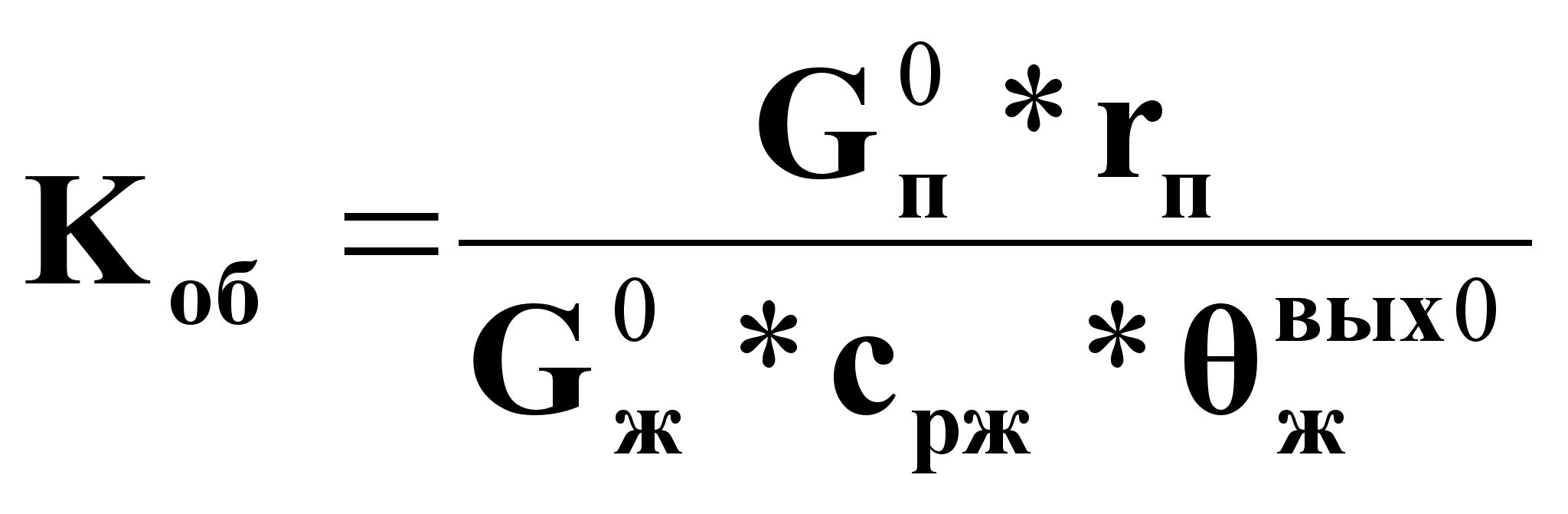 .
.
Объект имеет транспортное запаздывание:
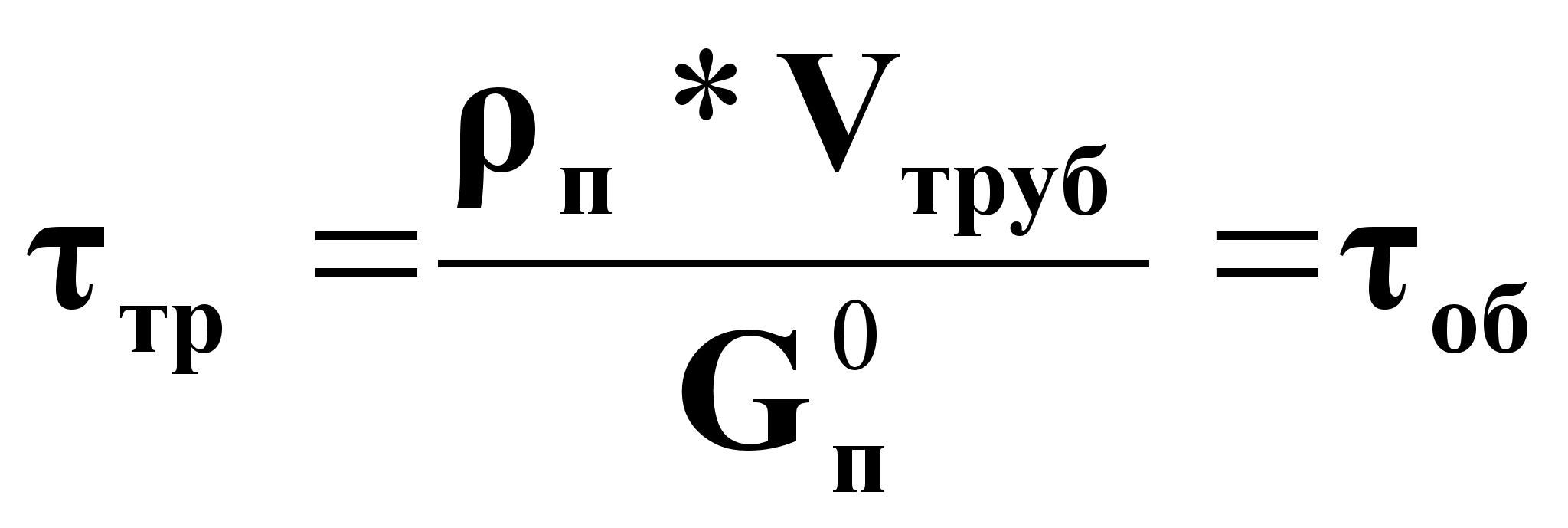 (19),
(19),
где Vтруб - объем трубопровода подачи пара от Р.О. до входа в аппарат.
Таким образом, в целом динамика объекта по каналу управления описывается математической моделью апериодического звена 1-го порядка с запаздыванием:
![]() (20).
(20).
Анализ статической характеристики объекта.
Из уравнения
статики выразим
![]() в явном виде:
в явном виде:
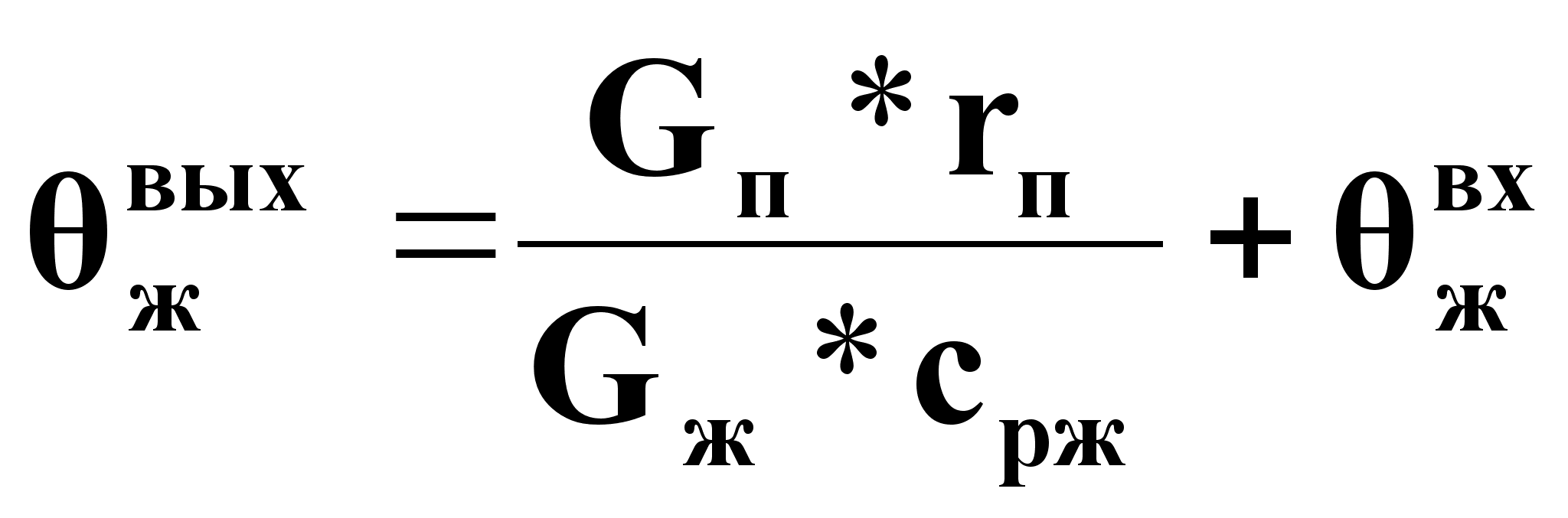 (21).
(21).
Статическая характеристика линейна по отношению к воздействиям по: ![]() .
.
Статическая характеристика нелинейна по отношению к воздействию по Gж.
Статическую характеристику можно линеаризовать по отношению к Gж введением стабилизации соотношения расходов: ![]() , тогда получим:
, тогда получим:
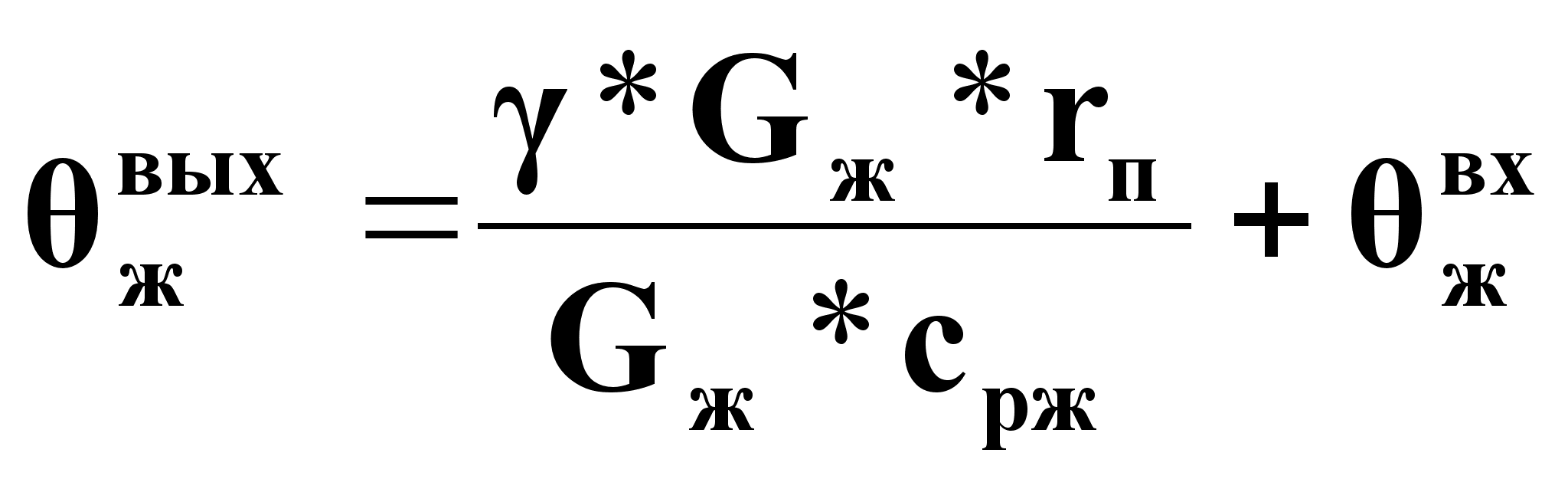 (22).
(22).
Линеаризованное представление статической характеристики через разложение в ряд Тейлора:
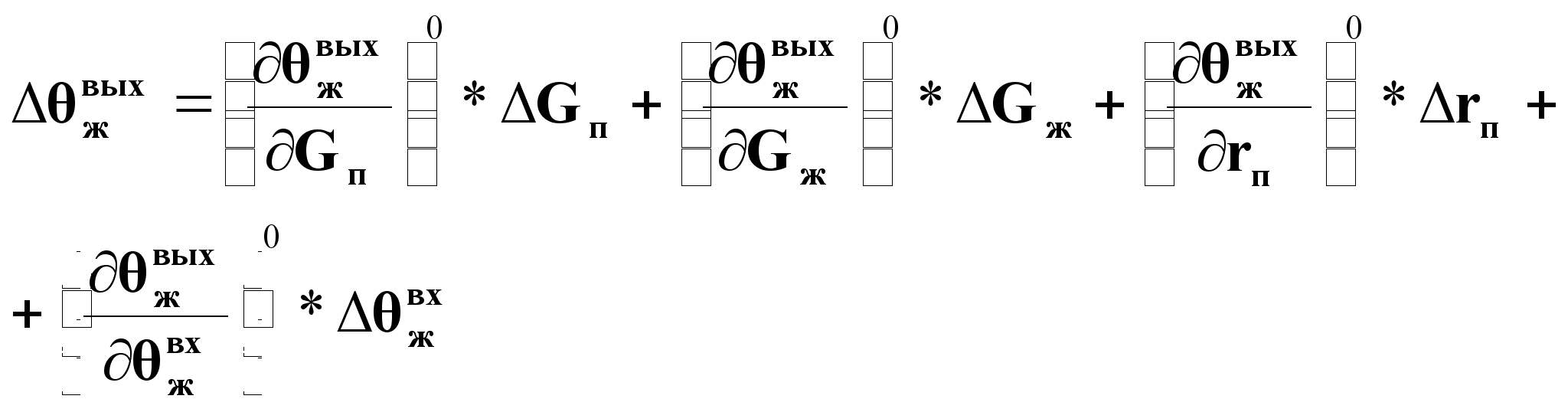 (23).
(23).
На основании (23) можно получить:
![]() (24).
(24).
Схема испарителя
(кожухотрубного теплообменника с изменяющимся агрегатным состоянием
теплоносителя и технологического потока).
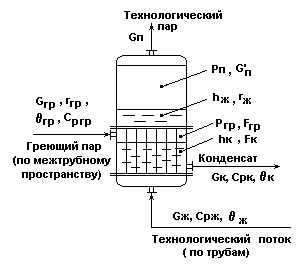
Рис.1.
Показатель эффективности: hж - уровень жидкой фазы в трубках испарителя.
Цель
управления: поддержание
![]() .
.
Математическое описание на основе физики процесса.
Общая тепловая нагрузка испарителя Q:
![]() (1).
(1).
На основании уравнения теплопередачи можно записать:
![]() и
и ![]() (2).
(2).
При теплопередаче от греющего пара и конденсата через трубки справедливы соотношения:
![]() и
и ![]() (3).
(3).
Общая поверхность теплопередачи Fт при конденсации греющего пара определится как:
Fт = Fп + Fк (4а),
и следовательно на основании (3) и (4а) можно записать:
![]() (4б).
(4б).
Определение ![]() на основании теплового баланса по греющему пару:
на основании теплового баланса по греющему пару:
![]() =Gгр
*rгр (5а);
=Gгр
*rгр (5а);
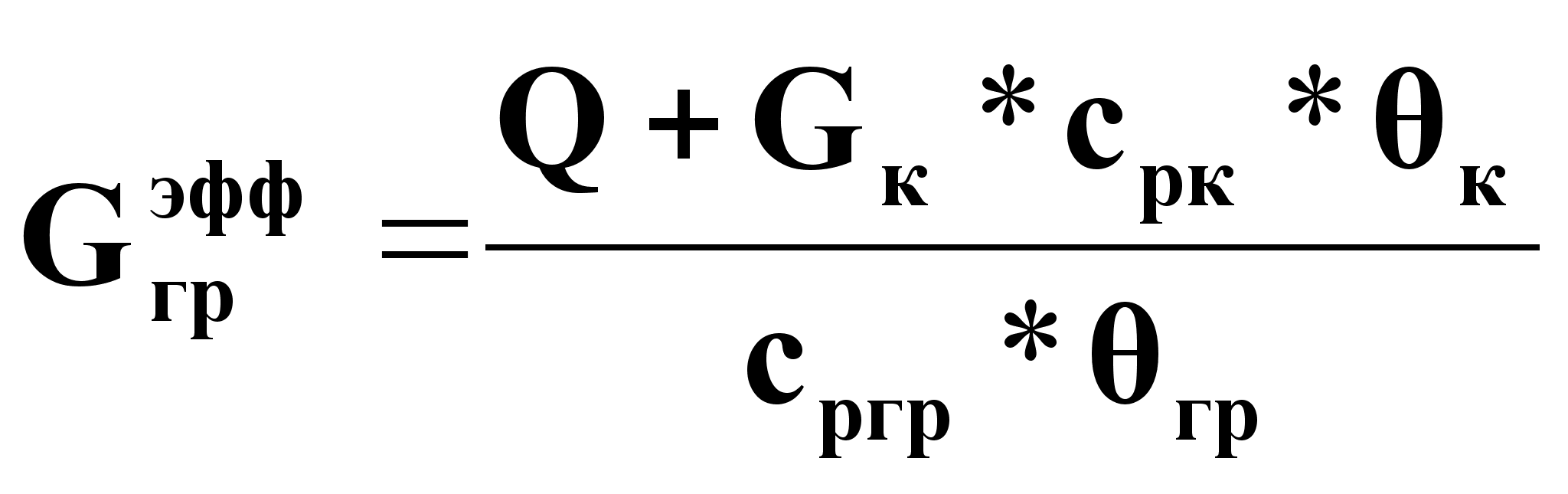 =
= ![]() (5б).
(5б).
Определение ![]() на основании теплового баланса по технологическому потоку:
на основании теплового баланса по технологическому потоку:
![]()
![]()
![]() (6а);
(6а);
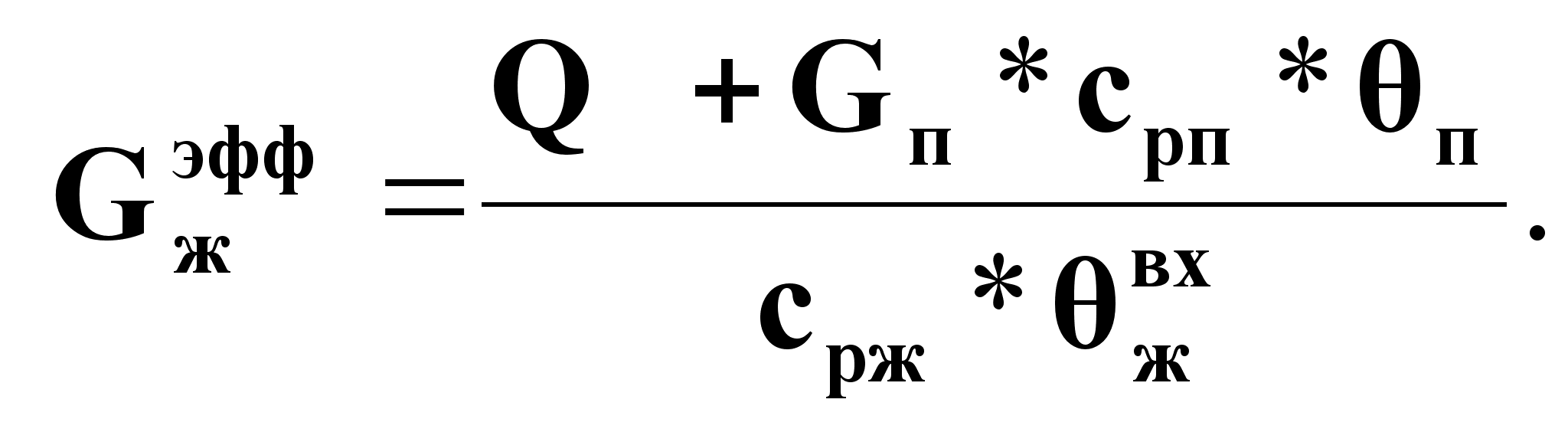 (6б).
(6б).
Выводы из математического описания физики процесса:
Общая тепловая нагрузка, отдаваемая греющим паром зависит следующих его параметров:
![]() (7).
(7).
Общая тепловая нагрузка, получаемая технологическим потоком, определяет следующие его параметры:
![]() и
и
![]() (8);
(8);
![]() (9).
(9).
Математическое описание на основе
теплового и материальных балансов процесса.
Тепловой баланс испарителя.
Уравнение динамики:
В
развернутом
виде при условии
![]() и
и ![]() :
:
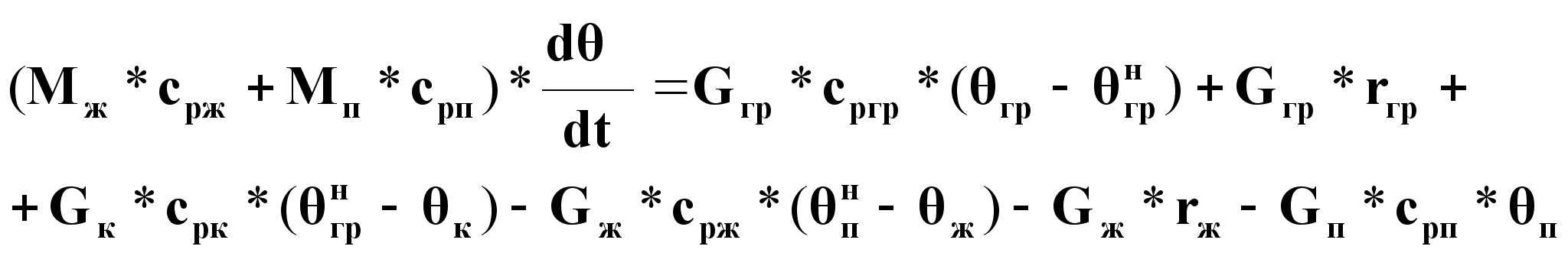 (10а).
(10а).
т.е. тепло выделяется за счет охлаждения Gгр от исходной температуры гр до температуры насыщенного пара ![]() , конденсации пара и последующего охлаждения конденсата до к .
, конденсации пара и последующего охлаждения конденсата до к .
тепло расходуется на нагревание Gж до температуры ![]() , испарение жидкости и отводится с образующейся паровой фазой.
, испарение жидкости и отводится с образующейся паровой фазой.
В свернутом наиболее общем виде выражение (10а) преобразуется к виду:
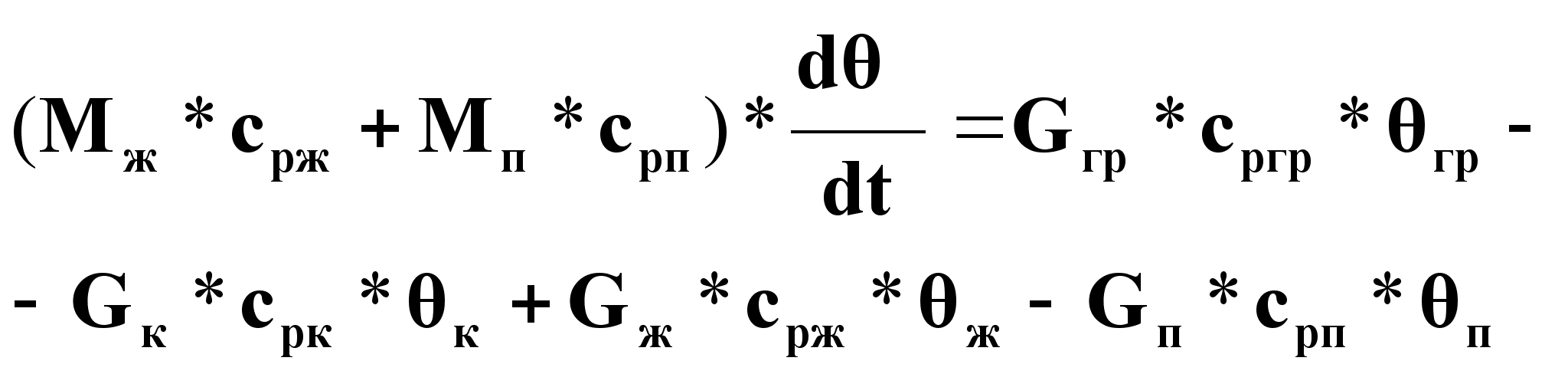 (10б).
(10б).
Уравнение
статики при
![]() :
:
![]() (10в)
(10в)
Выводы по тепловому балансу процесса:
В целом температура в испарителе на основании выражений (8) и (9) зависит от следующих параметров процесса:
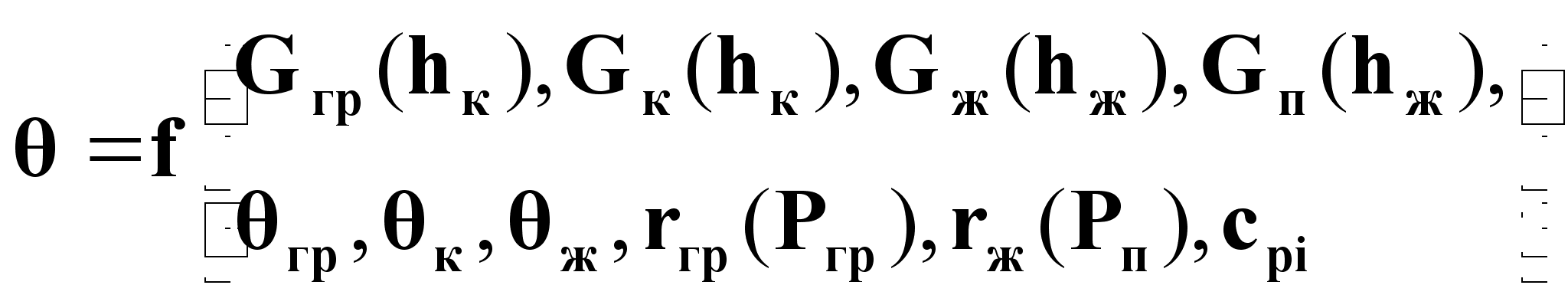 (10г).
(10г).
Так как температура в испарителе у поверхности раздела фаз, т.е. в зоне испарения должна быть равна температуре кипения, то можно полагать:
= ж = п = кип ,
а температура кипения зависит от давления паровой фазы в испарителе, т.е. при Рп кип (при этом rж ).
Поэтому температура не может использоваться как показатель эффективности процесса испарения.
Однако, на основании (6а, 6б) температура важна для обеспечения расчетной общей тепловой нагрузки Q в испарителе, т.е. теплового баланса в аппарате.
Из выражения (10г) следует, что основными параметрами, характеризующими данный процесс, являются:
уровень hж и давление Рп технологического потока в испарителе;
уровень hк и давление Ргр потока греющего пара в кипятильнике;
Материальный баланс по жидкой фазе в испарителе
(для технологического потока)
Уравнение динамики:
![]() , (11),
, (11),
Уравнение статики при ![]() :
:
![]() (12).
(12).
На основании (11) и (12) можно считать:
![]() . (13),
. (13),
Предпочтительное управляющее воздействие Gгр.
Материальный баланс по жидкой фазе в кипятильнике
(для конденсата греющего пара).
Уравнение динамики:
![]() , (14),
, (14),
Уравнение статики при ![]() :
:
![]() (15).
(15).
На основании (14) и (15) можно считать:
![]() . (16).
. (16).
Предпочтительное управляющее воздействие является отбор конденсата Gк.
Материальный баланс по паровой фазе
для технологического потока в испарителе.
Уравнение динамики:
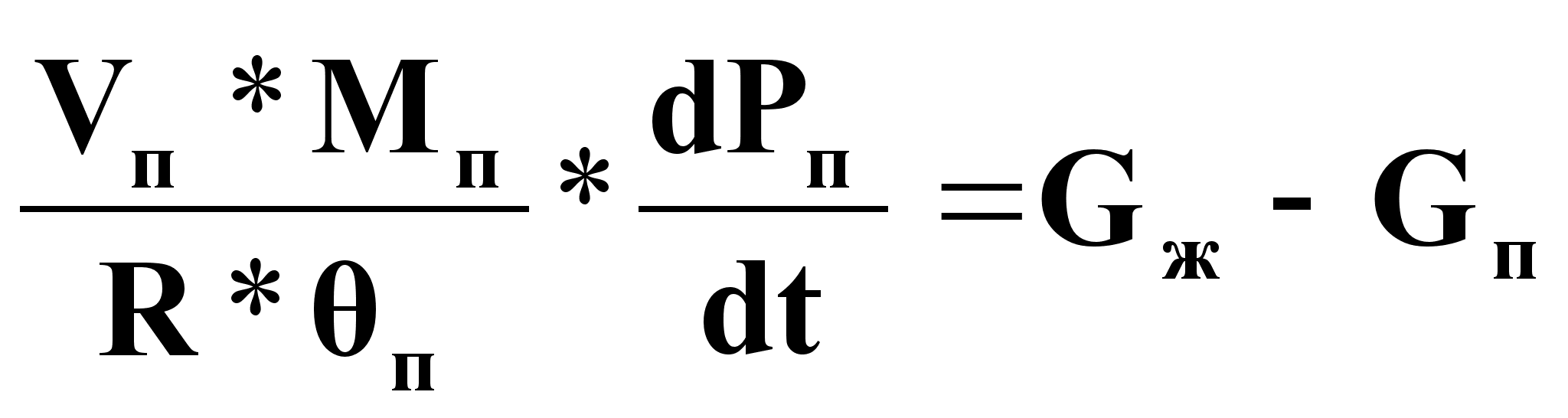 (17),
(17),
где
Мп - мольная масса паровой фазы технологического потока, кг/моль;
Рп - давление паровой фазы технологического
потока, Па;
п - температура паровой фазы технологического
потока, К,
Vп - объем паровой фазы технологического
потока, м3 .
Уравнение статики при ![]() :
:
![]() (18).
(18).
На основании (17) и (18)можно считать:
![]() (19),
(19),
Предпочтительное управляющее воздействие Gп.
Материальный баланс по паровой фазе для кипятильника.
Уравнение динамики:
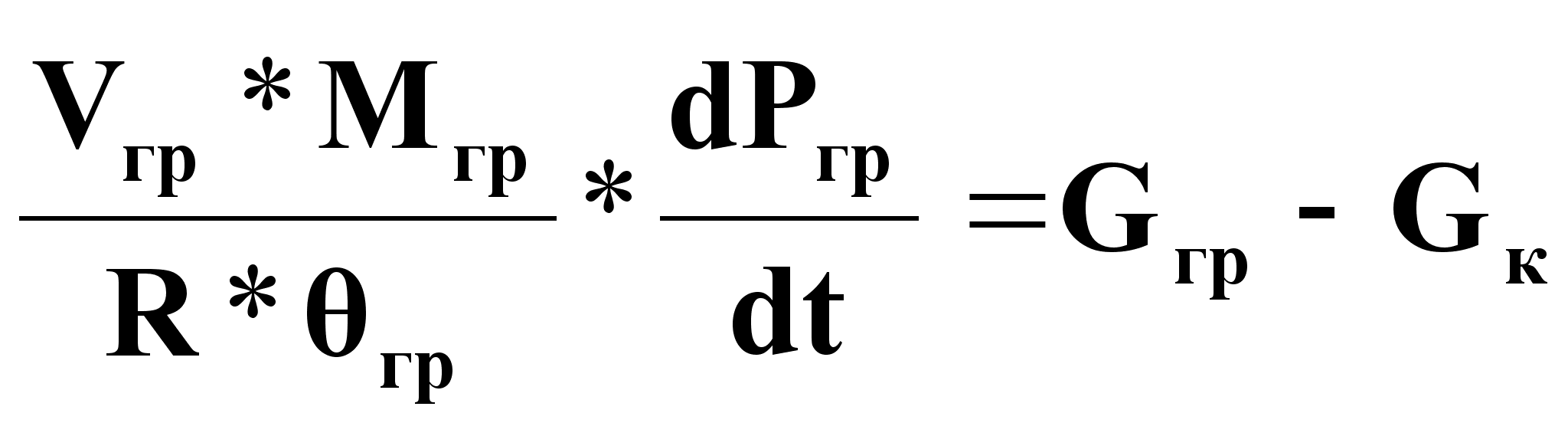 (20),
(20),
где Мгр - мольная масса паровой фазы греющего пара,
кг/моль;
Ргр - давление паровой фазы греющего пара, Па;
гр - температура паровой фазы греющего пара, К,
Vгр - объем паровой фазы греющего пара, м3 .
Уравнение статики при ![]() :
:
![]() (21).
(21).
На основании (20) и (21) можно считать:
![]() (22).
(22).
Предпочтительное управляющее Gгр .
Информационная схема испарителя
на основе материального баланса.
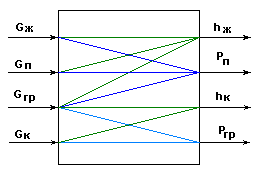
Рис.2.
Возможные управляющие воздействия:
![]() .
.
Возможные управляемые переменные:
![]() .
.
Информационная схема испарителя
для типового решения автоматизации.
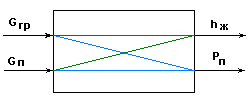
Рис.3.
В типовом решении автоматизации испарителей объект рассматривают как односвязный для основных каналов управления рис.3.
Однако, на основании схемы рис.3. объект можно рассматривать как многосвязный.
Многосвязность объекта с позиций физики процесса можно объяснить следующим образом:
При ![]() ; т.к. при
; т.к. при ![]()
При ![]() ; т.к. при
; т.к. при ![]()
Типовая схема автоматизации испарителей.
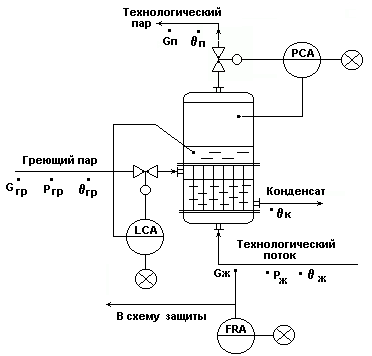
Рис.4.
Типовое решение автоматизации испарителей.
Регулирование.
Регулирование уровня hж по подаче греющего пара Gгр - как показателя эффективности процесса нагревания в испарителе.
Регулирование давления Рп по отбору паровой фазы из испарителя - для обеспечения материального баланса по паровой фазе и стабилизации rж=f(Pп).
Контроль.
расходы - Gгр, Gп , Gж ;
температуры - ![]() ;
;
давление - Ргр, Рж Рп ;
уровень - hж
Сигнализация.
существенные отклонения hж и Рп от заданий;
резкое падение расхода технологического потока Gж , при этом формируется сигнал «В схему защиты».
Система защиты.
По сигналу «В схему защиты» - отключаются магистрали подачи греющего пара Gгр и отбора пара для технологических нужд.
Материалы к лекции №8Автоматизация процесса выпаривания
Движущая сила процесса выпаривания.
Движущей силой процесса выпаривания является полезная разность температур полезн :
полезн = т - р-ракип (1).
Общая разность температур общ в процессе:
общ = т - р-лякип (2).
Общая разность температур общ больше полезной разности температур полезн на величину потерь :
полезн = общ - (3),
Величина потерь в процессе выпаривания:
= г + д + гп (4),
где - г потери за счет гидростатического эффекта; д - температурная депрессия; гп - потери температуры за счет гидравлических потерь в трубопроводе.
На основании выражений (2) и (4) выражение (3) примет вид:
полезн = т - р-лякип -( г + д + гп ) (5).
Температурная депрессия.
Определение д на основании (1) и (5):
д = р-ракип - р-лякип (6).
Определение д по диаграммам «Р - ».
Диаграмма «Р - » для растворов и растворителей.
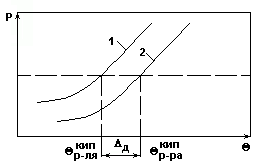
Рис.1.
Из диаграммы следует, что при P=const д = р-ракип - р-лякип
Расчетные соотношения для д:
Для концентрированных растворов недиссоциирующихся веществ:
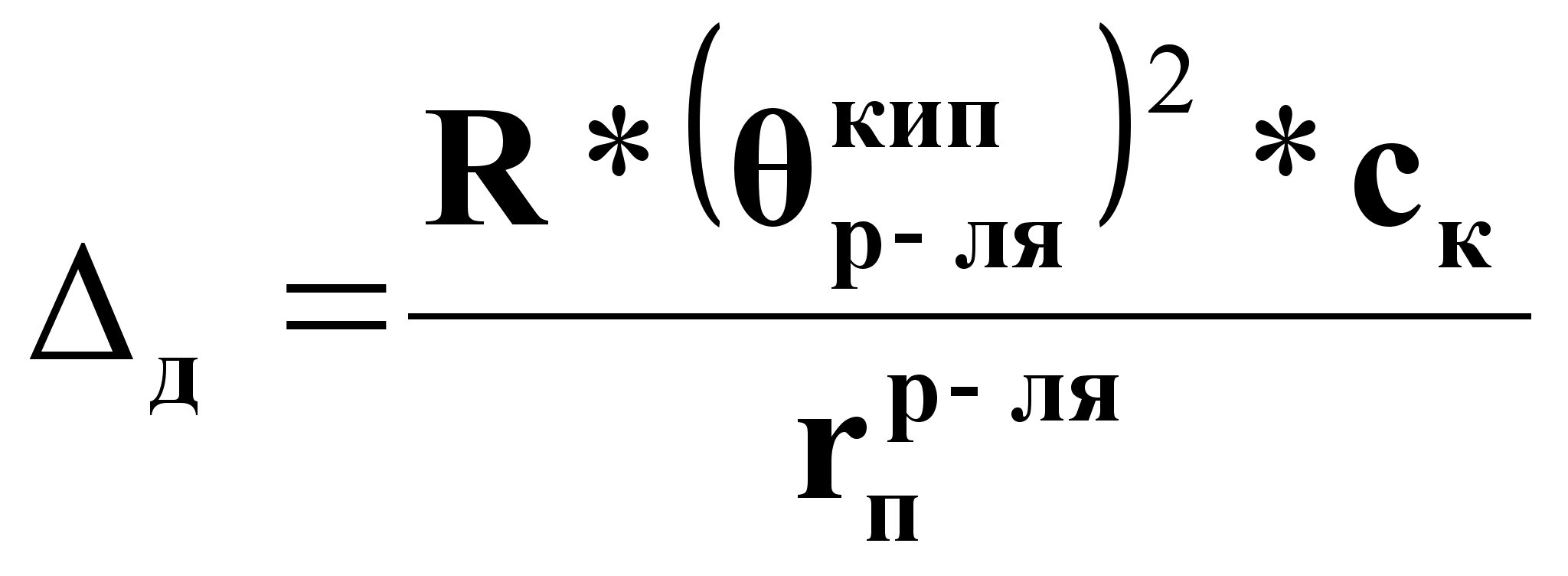 (7),
(7),
Для концентрированных растворов диссоциирующихся веществ:
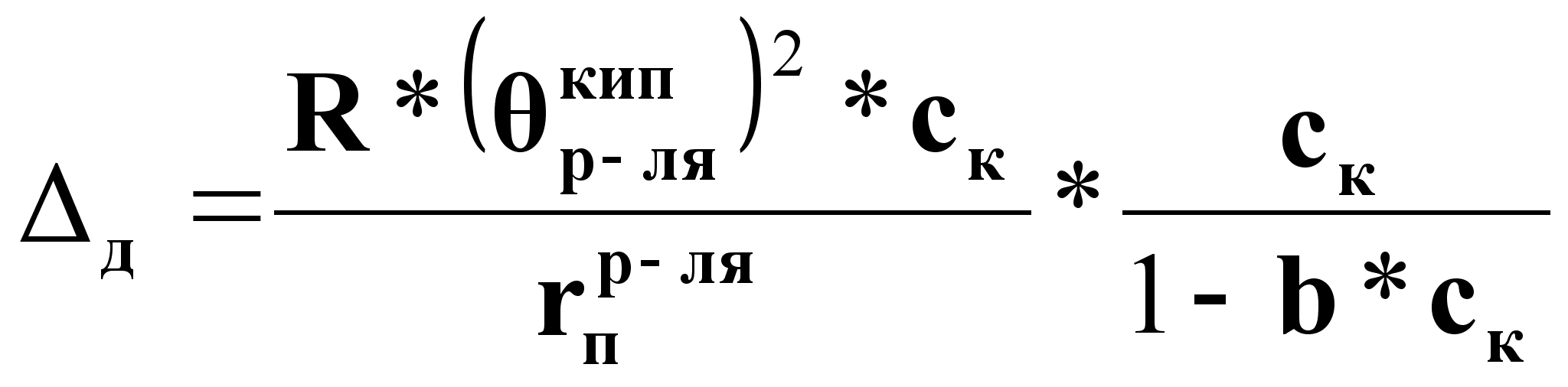 (8),
(8),
где R=8,31, дж/(моль*К);
cк - концентрация растворенного вещества в концентрированном растворе, моль/моль;
rпр-ля - теплота испарения растворителя, дж/моль;
р-лякип - температура кипения растворителя, К;
b - константа, определяемая опытным путем.
Объект управления
Схема выпарной установки естественной циркуляции
с вынесенной греющей камерой.
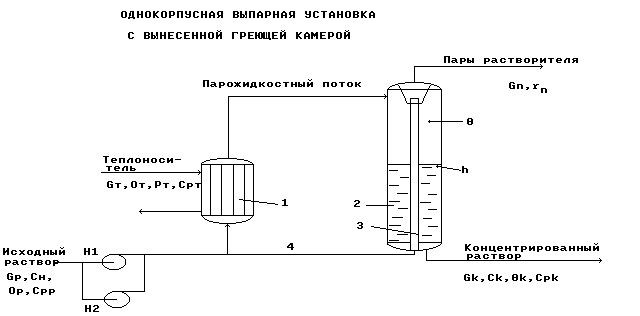
греющая камера;
- выпарной аппарат;
брызгоулавливатель;
циркуляционная труба
Рис.2.
Работа установки.
Исходный раствор подается по трубам кипятильника 1, где нагревается до температуры кипения с образованием парожидкостной смеси, которая далее поступает в выпарной аппарат (сепаратор) 2.
В сепараторе 2 парожидкостная смесь разделяется на паря растворителя и концентрированный раствор.
Пары растворителя проходят через брызгоулавливатель 3 и выводятся из процесса из верха сепаратора в виде парового потока Gп.
Выделенная брызгоулавливателем жидкая фаза из паров растворителя возвращается в кипятильник 1 по циркуляционной трубе 4.
Сконцентрированный раствор в виде потока Gк выводится из низа сепаратора.
Показатель эффективности процесса - концентрация концентрированного раствора ск.
Цель управления - обеспечение ск = скзд (на максимально возможном для данной установки значении).
Материальный баланс по растворенному веществу.
Уравнение динамики:
![]()
![]()
![]() (1),
(1),
Уравнение
статики ![]() :
:
![]() (2)
(2)
Из выражений (1) и (2) следует:
![]() (3),
(3),
Предпочтительное управляющее воздействие: Gр.
Тепловой баланс выпарной установки.
Уравнение динамики процесса выпаривания:
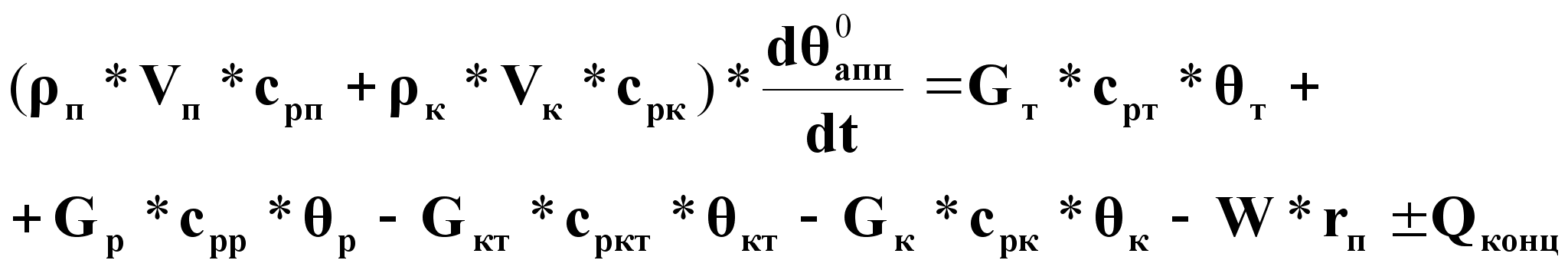 (5).
(5).
Уравнение
статики при
![]() :
:
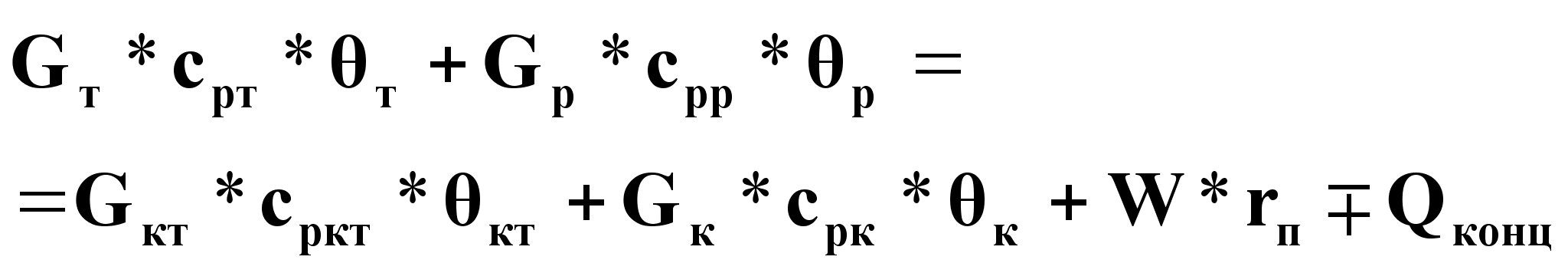 (6).
(6).
В выражениях (5) и (6) принято:
![]() ;
;
![]() ;
;
![]() - количество испаряемого растворителя;
- количество испаряемого растворителя;
![]() - удельные теплоемкости исходного и концентрированного растворов, которые не починяются закону аддитивности;
- удельные теплоемкости исходного и концентрированного растворов, которые не починяются закону аддитивности;
![]() ,
,
где q - тепловой эффект растворения, определяемый на основании закона Гесса:
![]() ,
,
где qн и qк - интегральные теплоты растворения в начале и конце процесса.
На основании (5) и (6):
![]() (7).
(7).
Предпочтительные управляющие воздействия:
для обеспечения теплового баланса процесса - расход теплоносителя Gт;
для косвенного регулирования показателя эффективности процесса ![]() - расход исходного раствора Gр.
- расход исходного раствора Gр.
В типовом решении автоматизации:
для косвенного регулирования показателя эффективности процесса выпаривания используют не температуру в аппарате, а температурную депрессию:
![]() .
.
Материальный баланс по жидкой фазе (для раствора).
Уравнение динамики:
![]() , (8),
, (8),
Уравнение статики:
![]() (9)
(9)
На основании (8) и (9):
![]() . (10).
. (10).
Предпочтительное управляющее воздействие - Gк.
Материальный баланс по паровой фазе (для раствора).
Уравнение динамики:
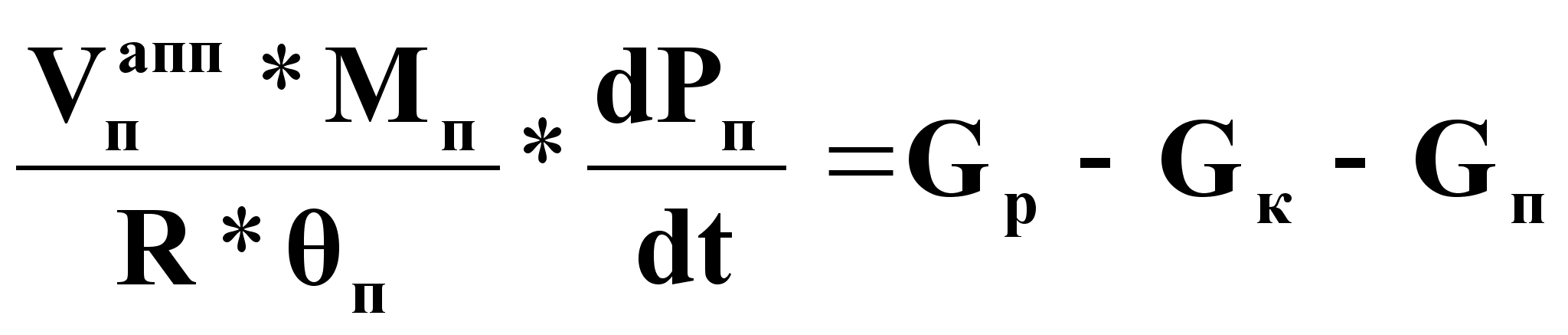 (11),
(11),
где Мп - мольная масса паровой фазы (растворителя),
кг/моль;
Рп - давление в сепараторе, Па;
п = к =апп - температура в сепараторе, К,
Vп - объем паровой фазы в сепараторе, м3 .
Уравнение статики:
![]() (12).
(12).
На
основании (11)
и (12):![]() и предпочтительное
управляющее
воздействие
Gп.
и предпочтительное
управляющее
воздействие
Gп.
Материальный баланс по жидкой фазе (для теплоносителя).
Уравнение динамики:
![]() , (14),
, (14),
Уравнение статики:
![]() (15).
(15).
На основании (14) и (15):
![]() . (16).
. (16).
Предпочтительное управляющее воздействие - Gкт.
Материальный баланс по паровой фазе (для теплоносителя).
Уравнение динамики:
 (17),
(17),
где Мп - мольная масса теплоносителя, кг/моль;
Рт мтр - давление теплоносителя в межтрубном
пространстве кипятильника, Па;
т - температура теплоносителя, К,
Vтмтр - объем паровой фазы теплоносителя в
межтрубном пространстве кипятильника, м3 .
Уравнение статики:
![]() (18).
(18).
На основании (17) и (18):
![]() (19).
(19).
Предпочтительное управляющее воздействие Gт.
Информационная схема процесса выпаривания.
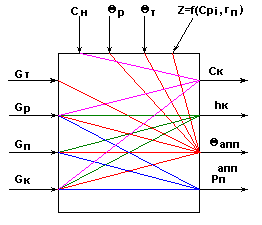
Рис.3
Возможные управляющие воздействия:![]() .
.
Возможные контролируемые возмущения: ![]() .
.
Возможные неконтролируемые возмущения: ![]() - удельные теплоемкости потоков срi и теплота испарения растворителя rп .
- удельные теплоемкости потоков срi и теплота испарения растворителя rп .
Возможные управляемые переменные: ![]() .
.
На основании рис.3 выпарная установка является сложным многосвязным объектом по возможным управляющим воздействиям ![]() .
.
Типовая схема автоматизации процесса выпаривания.
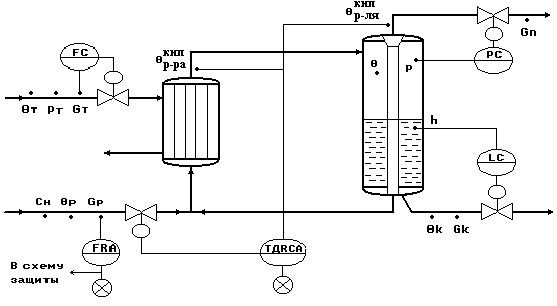
Рис.4.
Типовое решение автоматизации процесса выпаривания.
Регулирование.
Регулирование температурной депрессии Δд по подаче исходного раствора Gр - как параметра, косвенно характеризующего показатель эффективности процесса выпаривания ск .
Регулирование давления в сепараторе Рпапп по отбору паров растворителя Gп - для обеспечения материального баланса по паровой фазе.
Регулирование уровня в сепараторе hк по отбору концентрированного раствора Gк - для обеспечения материального баланса по жидкой фазе.
Стабилизация расхода теплоносителя Gт - для обеспечения теплового баланса установки
Контроль.
расходы - Gт, Gр, Gк, Gп;
температуры - ![]() ;
;
давление - Рп апп, Рт;
уровень концентрированного раствора в аппарате - hк;
Сигнализация.
существенные отклонения ![]() от задания;
от задания;
Прекращение подачи исходного раствора Gр , при этом формируется сигнал «В схему защиты».
Система защиты.
По сигналу «В схему защиты» - открывается магистраль Gп, отключается подача теплоносителя и отбор концентрированного раствора.
СОДЕРЖАНИЕ
Материалы к лекции №1 5
Материалы к лекции №2 12
Материалы к лекции №3 21
Материалы к лекции №4 26
Материалы к лекции №5 35
Материалы к лекции №6 44
Материалы к лекции №7 54
Материалы к лекции №8 70
Министерство образования Российской федерации
Санкт-Петербургский государственный технологический институт
(технический университет)
Кафедра автоматизации процессов химической промышленности
Г.В. Иванова
«Автоматизация технологических процессов
основных химических производств»
Методические материалы по курсу лекций
(в двух частях)
Часть 2.
2003г.
УДК 66-52:66(075)
Иванова Г.В. Автоматизация технологических процессов основных химических производств: Методическое пособие. Часть 2 / СПбГТИ(ТУ).-СПб., 2003.- 70с.
Методическое пособие предназначено для курса лекций по учебной дисциплине «Автоматизация технологических процессов основных химических производств», являющейся дисциплиной специализации 210201 – «Автоматизация технологических процессов химической промышленности» учебного плана по специальности 210200.
Пособие разработано в виде методических материалов, используемых при чтении лекций по дисциплине.
Часть 2 методического пособия включает в себя физико-химические основы технологических процессов, технологические схемы рассматриваемых объектов управления, математические описания объектов управления, постановку задачи автоматизации, типовые схемы автоматизации, типовые решения автоматизации для массообменных и реакторных процессов.
Утверждено на заседании методической комиссии факультета Информатики и управления 23 июня 2003г., протокол № 6.
Материалы к лекции №9Общая характеристика массообменных процессов
Вид диаграммы равновесия
для системы с 3 степенями свободы
c1* =f(c2) при θ=const и P=const;
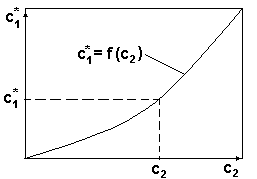
Рис.2.
На диаграмме обозначено:
c1 - концентрация компонента в газовой фазе, cy.
c2 - концентрация компонента в жидкой фазе, cх.
при cх =c2, равновесное значение концентрации в газовой фазе будет cy* = c1*.
Вид диаграммы равновесия
для системы с 2 степенями свободы
c1* =f(c2) при Р=const.
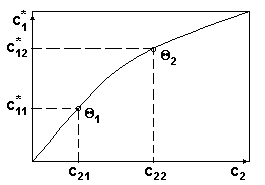
Рис.3.
Каждая точка кривой рис.3 соответствует равновесному состоянию при различных температурах.
Отношение концентраций фаз при равновесии называют коэффициентом распределения:
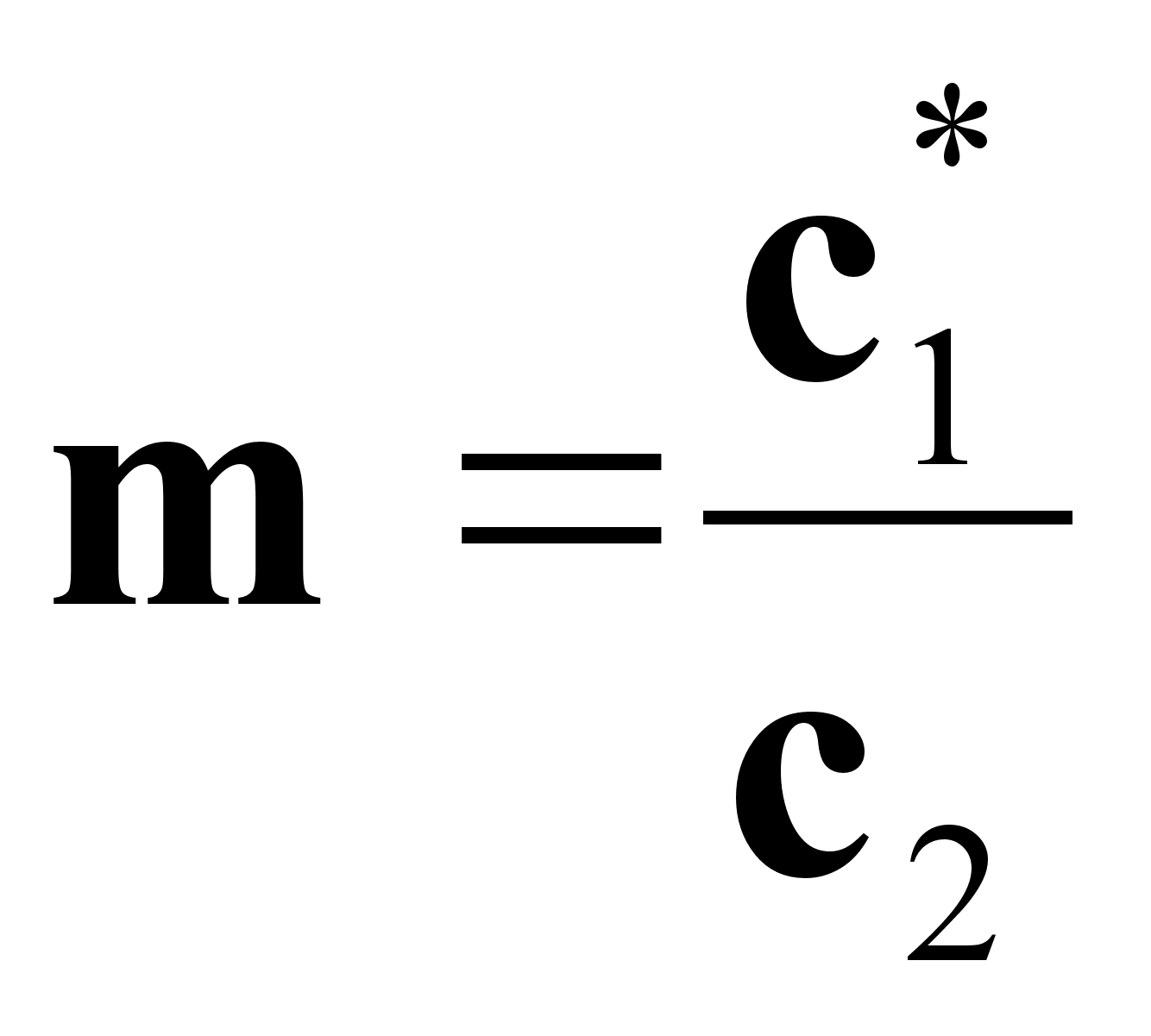 (3).
(3).
Графически m можно определить:![]() ,
,
т. е.как тангенс угла наклона касательной к линии равновесия, если она нелинейна,
или как тангенс угла наклона самой линии равновесия, если она линейна.
Уравнение рабочей линии процесс массопередачи
при противотоке распределяющих веществ.
Схема движения распределяющихся веществ
противотоком:
 G1 c1
G1 c1
с1н с1к
с2к с2н
G2 c2
Рис.1.
Материальный баланс процесса по целевому компоненту можно записать в виде:
![]() (1),
(1),
или
![]() (2).
(2).
Для произвольного сечения аппарата с концентрациями с1 и с2 можно записать:
![]() (3а).
(3а).
или
![]() (3б).
(3б).
Выразим из (3б) зависимость с1 = f(с2):
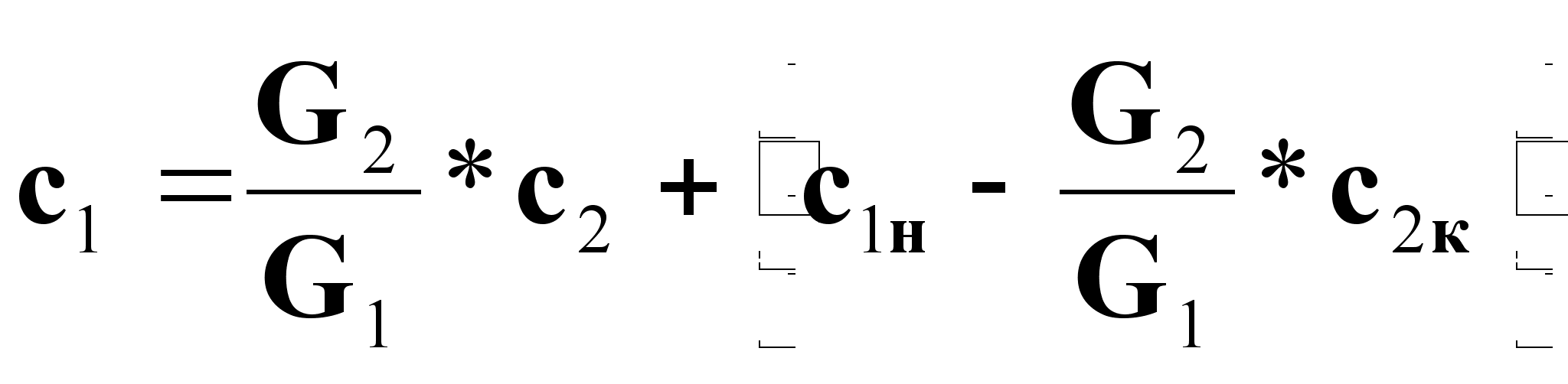 (4).
(4).
Выражение (4) - уравнение рабочей линии (рабочих концентраций) массопередачи.
Это уравнение прямой с ![]() .
.
Рабочая линия всего аппарата ограничена точками с координатами с1н , с1к , с2н , с2н .
Вид рабочей линии
при противотоке распределяющих веществ.
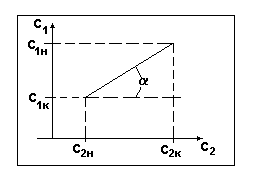
Рис.2.
Уравнение рабочей линии процесса при прямотоке
распределяющих веществ.
Схема движения распределяющихся веществ
прямотоком:
 G1 c1
G1 c1
с1н с1к
с2н с2к
G2 c2
Рис.3.
Материальный баланс процесса по целевому компоненту можно записать в виде:
![]() (5),
(5),
или
![]() (6).
(6).
Для произвольного сечения аппарата с концентрациями с1 и с2 можно записать:
![]() (7а)
(7а)
или
![]() (7б).
(7б).
Выразим из (7б) зависимость с1 = f(с2):
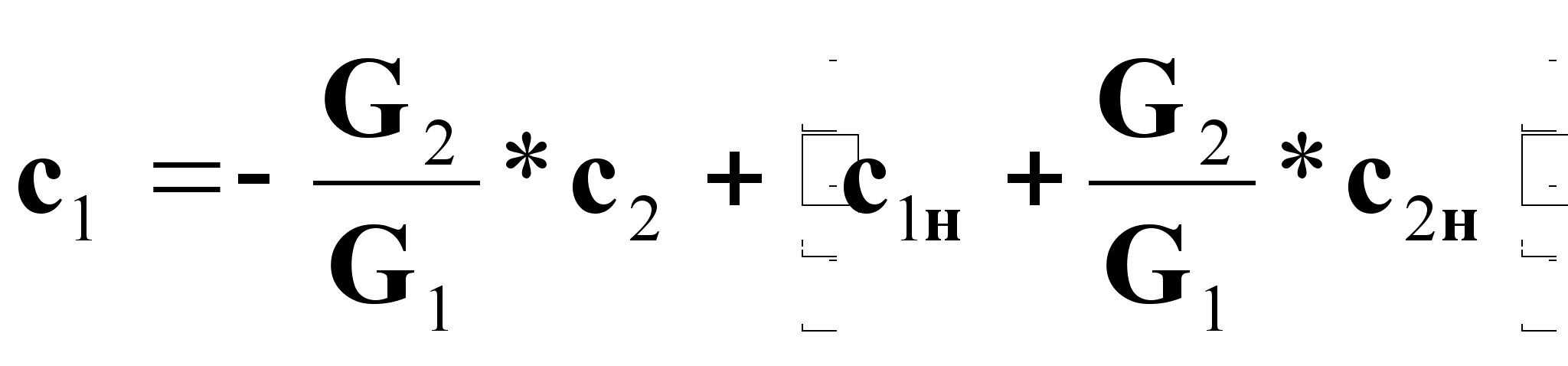 (8).
(8).
Выражение (8) - уравнение рабочей линии (рабочих концентраций массопередачи) при прямотоке распределяющих веществ.
Это уравнение прямой с ![]() .
.
Рабочая линия всего аппарата ограничена точками с координатами с1н , с1к , с2н , с2н .
Вид рабочей линии
при прямотоке распределяющих веществ.
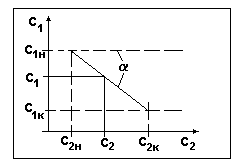
Рис.4.
Диаграмма с1-с2 при расположении рабочей линии
выше равновесной.

Рис.1.
Из диаграммы рис.1 следует:
![]()
Это означает, что целевой компонент будет переходить из фазы G1 в фазу G2.
Диаграмма с1-с2 при расположении рабочей линии
ниже равновесной.
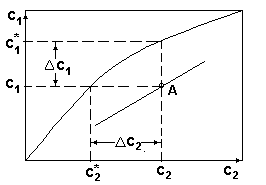
Рис.2
Из диаграммы рис.2. следует:
![]()
Это означает, что целевой компонент будет переходить из фазы G2 в фазу G1.
Средняя движущая сила процессов массопередачи.
при ![]() :
:
![]() (1).
(1).
при ![]() :
:
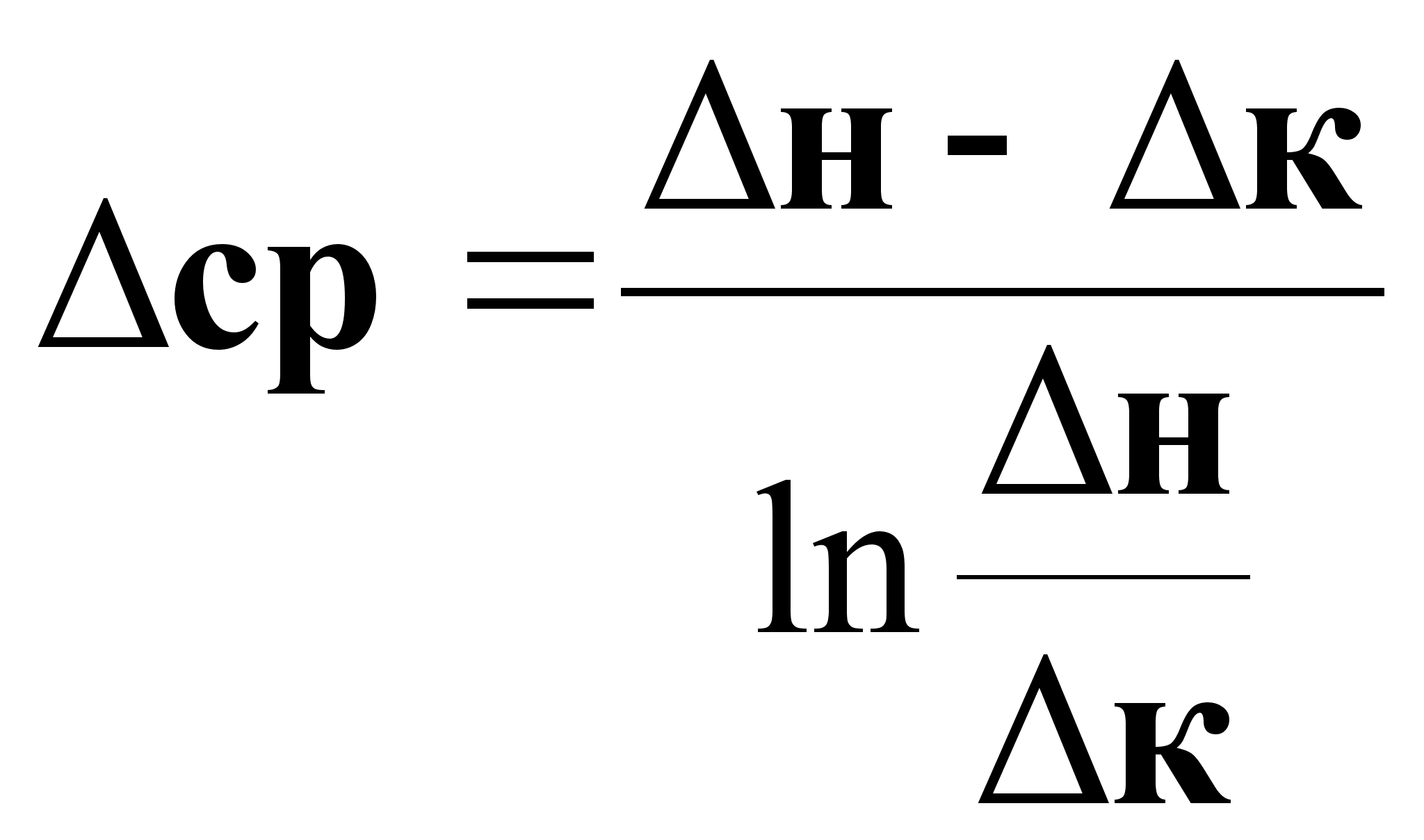 (2).
(2).
Основное уравнение массопередачи.
![]() (1),
(1),
где М - масса переносимого вещества, кг/с;
К - коэффициент
массопередачи,
![]()
∆ср - средняя движущая сила процесса массопередачи.
Определение движущей силы по каждой из фаз:
![]() (2),
(2),
![]() (3),
(3),
где
∆срy и ∆срx - средние движущие силы, в фазах y и x;
Ky и Kx - коэффициенты массопередачи для фаз y и x.
Материалы к лекции №10Автоматизация процесса кристаллизации
Система с резким возрастанием растворимости.
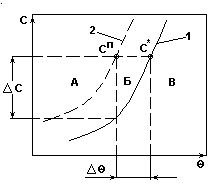
Рис.1.
- c*=f() - кривая растворимости, характеризующая равновесие концентрированного раствора при изменении .
- сп= f() - линия условной границы метастабильной области.
А - неустойчивая, лабильная область массового образования центров кристаллизации;
Б - относительно устойчивая метастабильная область образования и растворения кристаллов;
В - область ненасыщенных растворов.
Система с плавным изменением растворимости.
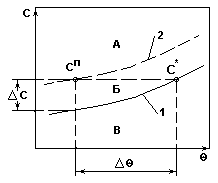
Рис.2.
Переход в область пересыщенных растворов происходит только при значительном охлаждении.
При этом выделяется незначительное количество твердой фазы.
Рекомендуемый способ кристаллизации - получение сп удалением части растворителя из раствора.
Рекомендуемый метод кристаллизации - вакуум-кристаллизация.
Система с незначительным изменением
растворимости.
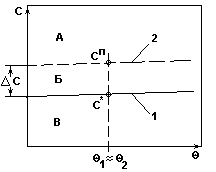
Рис.3.
Рекомендуемый способ кристаллизации - получение сп путем выпаривания растворителя из раствора.
Рекомендуемый метод кристаллизации - изотермическая кристаллизация.
Изотермическая кристаллизация - это кристаллизация с удалением части растворителя испарением или вымораживанием.
Система с незначительным изменением
растворимости.

Рис.3.
Рекомендуемый способ кристаллизации - получение сп путем выпаривания растворителя из раствора.
Рекомендуемый метод кристаллизации - изотермическая кристаллизация.
Изотермическая кристаллизация - это кристаллизация с удалением части растворителя испарением или вымораживанием.
Кинетика процесса кристаллизации.
Скорость образования центров кристаллизации:
![]() ,
,
где
![]() - число
частиц, образующихся
в единице объема
в единицу времени;
- число
частиц, образующихся
в единице объема
в единицу времени;
![]()
КN,
КN0 - константы,
![]() ,
,
EN - энергия активации зародышеобразования, (кдж/кг);
Сп и С* - концентрации пересыщенного и насыщенного растворов, (кг/м3);
m=2 - 4 - кинетический коэффициент, зависящий от типа кристаллизующегося вещества.
Качественная характеристика скорости роста кристаллов.
Зависимости скорости кристаллизации от времени.
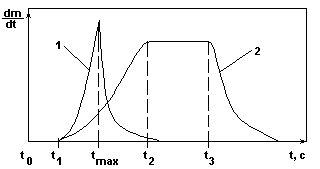
Рис.4.
- ![]() ;
;
- ![]() ;
; ![]() .
.
t0 - t1 - индукционный период, т.е. период подвижного равновесия зародышей с раствором.
Кривая 1 - при большой степени пересыщения имеет резкий максимум скорости процесса в момент tmax.
Кривая 2 - при малой степени пересыщения имеет пологий максимум в течение времени t2 - t3.
Количественные оценки скорости роста кристаллов на основании диффузионной теории.
Процесс встраивания молекул в кристаллы идет с большой скоростью и кинетика процесса определяется скоростью подвода вещества к поверхности кристалла:
![]() (1),
(1),
где
- коэффициент массоотдачи, кг/м2*с;
Сп-С*=, (кг/кг);
F - поверхность кристалла, (м2).
Для аппаратов с мешалками коэффициент массоотдачи зависит от следующих параметров:
![]() ,
,
где
а - характеристический размер кристалла;
n - число оборотов мешалки, об/мин;
dм - диаметр мешалки, м.
Процесс подвода вещества к поверхности кристалла идет с большой скоростью. Кинетика процесса определяется скоростью встраивания молекул в кристалл:
![]() (2),
(2),
где
КB - константа скорости встраивания молекул в кристалл;
n - эмпирическая постоянная.
Оба процесса протекают с соизмеримыми скоростями:
![]() (3),
(3),
где
К - общий коэффициент скорости процесса, определяемый из соотношения:
![]() .
.
Учитывая, что К=f(, KB), а =f(n), в целом можно считать:
![]() .
.
Таким образом, скорость роста кристаллов определяется поверхностью кристалла, движущей силой процесса и скоростью мешалки.
Объект управления
Изогидрический кристаллизатор непрерывного действия с мешалкой.
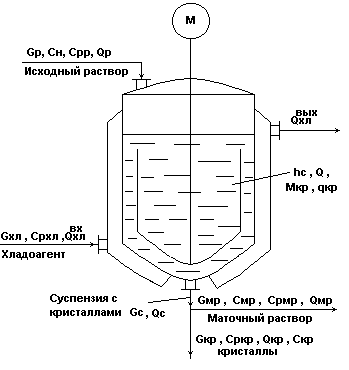
Рис.5.
В схеме принято:
Gс=Gмр+Gкр; мр = кр = с =;
Скр = 1, т.е. кристаллы чистые.
Работа объекта
Исходный горячий насыщенный раствор подается сверху в аппарат, где охлаждается с помощью хладоносителя, подаваемого в рубашку и становится пересыщенным.
В результате пересыщения раствора и при интенсивном перемешивании происходит кристаллизация целевого компонента из раствора с образованием кристаллов (МкрGкр).
При этом концентрация раствора понижается и оставшаяся жидкая фаза Gмр в смеси с Gкр в виде потока суспензии Gc выводится из процесса.
Показатель эффективности процесса - диаметр кристаллов, dкр.
Цель управления процессом - обеспечение dкр = dкрзд.
Материальный баланс по всему веществу
Уравнение динамики:
![]() (1).
(1).
Уравнение
статики при
![]() :
:
![]() (2).
(2).
Материальный баланс по кристаллизуемому веществу.
Уравнение динамики:
![]() (3).
(3).
Уравнение
статики при
![]() :
:
![]() (4).
(4).
В уравнение (4) подставим выражение ![]() из (2) и полагаем Скр=1:
из (2) и полагаем Скр=1:
![]() (5).
(5).
Из (5) выразим Gкр в явном виде:
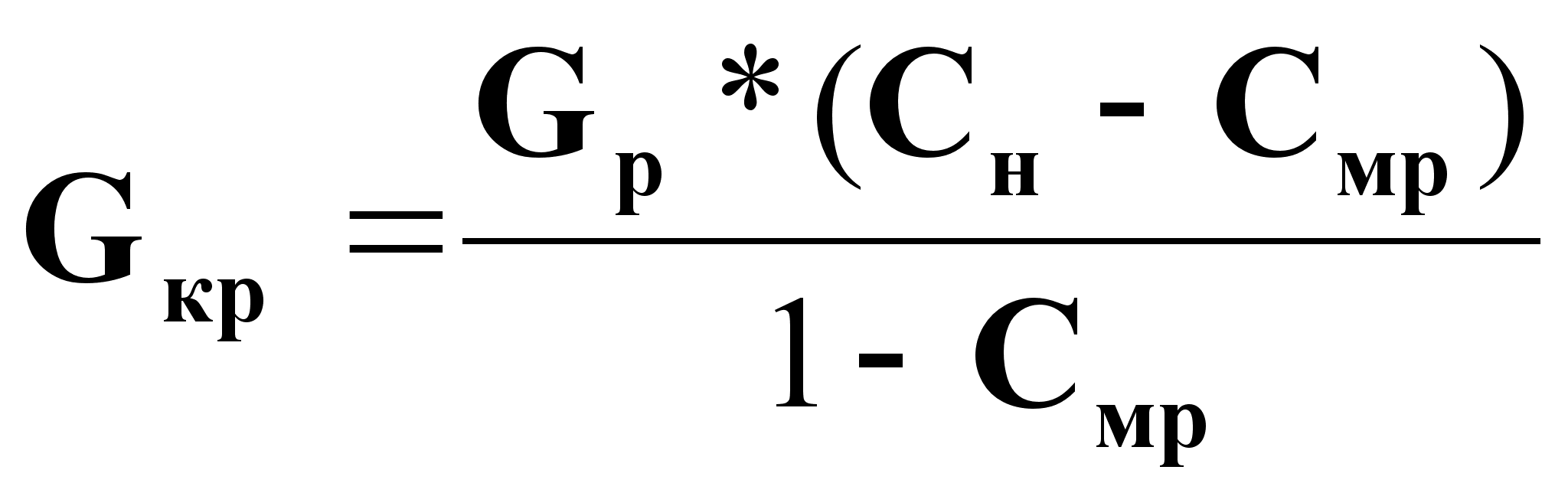 (6).
(6).
Выражение (6) представляет Gкр на основе материального баланса процесса кристаллизации.
Но ![]() , которое определяется на основе физики процесса массопередачи:
, которое определяется на основе физики процесса массопередачи:
![]() (7),
(7),
где
![]() - число
кристаллов,
которое образуется
- число
кристаллов,
которое образуется
за время пр в объеме Vс;
![]() - изменение
массы одного
кристалла в
ед. времени,
кг/с.
- изменение
массы одного
кристалла в
ед. времени,
кг/с.
Так как ![]() и
и ![]() , а также
, а также ![]() , то на основе физики массопередачи можно считать:
, то на основе физики массопередачи можно считать:
![]() .
.
В целом, на основании (6) и (7) можно записать:
![]() .
.
Математическое описание для размера частиц.
На основании диффузионной теории и правила Мак-Бена скорость роста кристаллов можно представить через радиус частиц:
![]() (9),
(9),
где
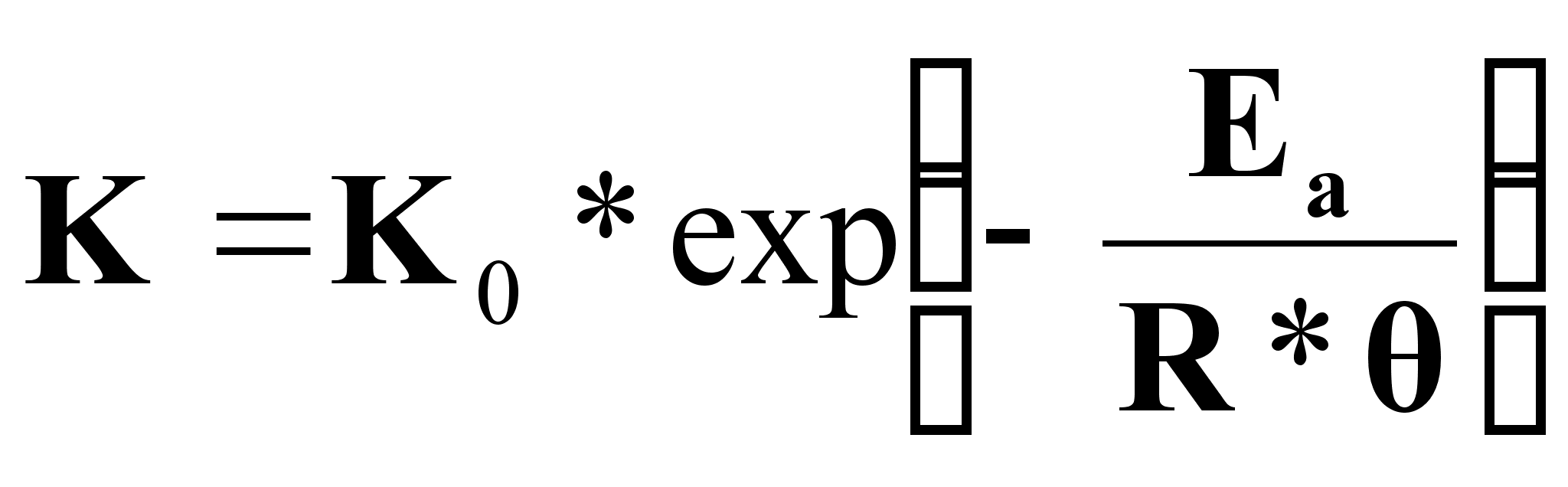 (10);
(10);
r - радиус кристалла, м; t - время, с;
К,
К0 - константы, 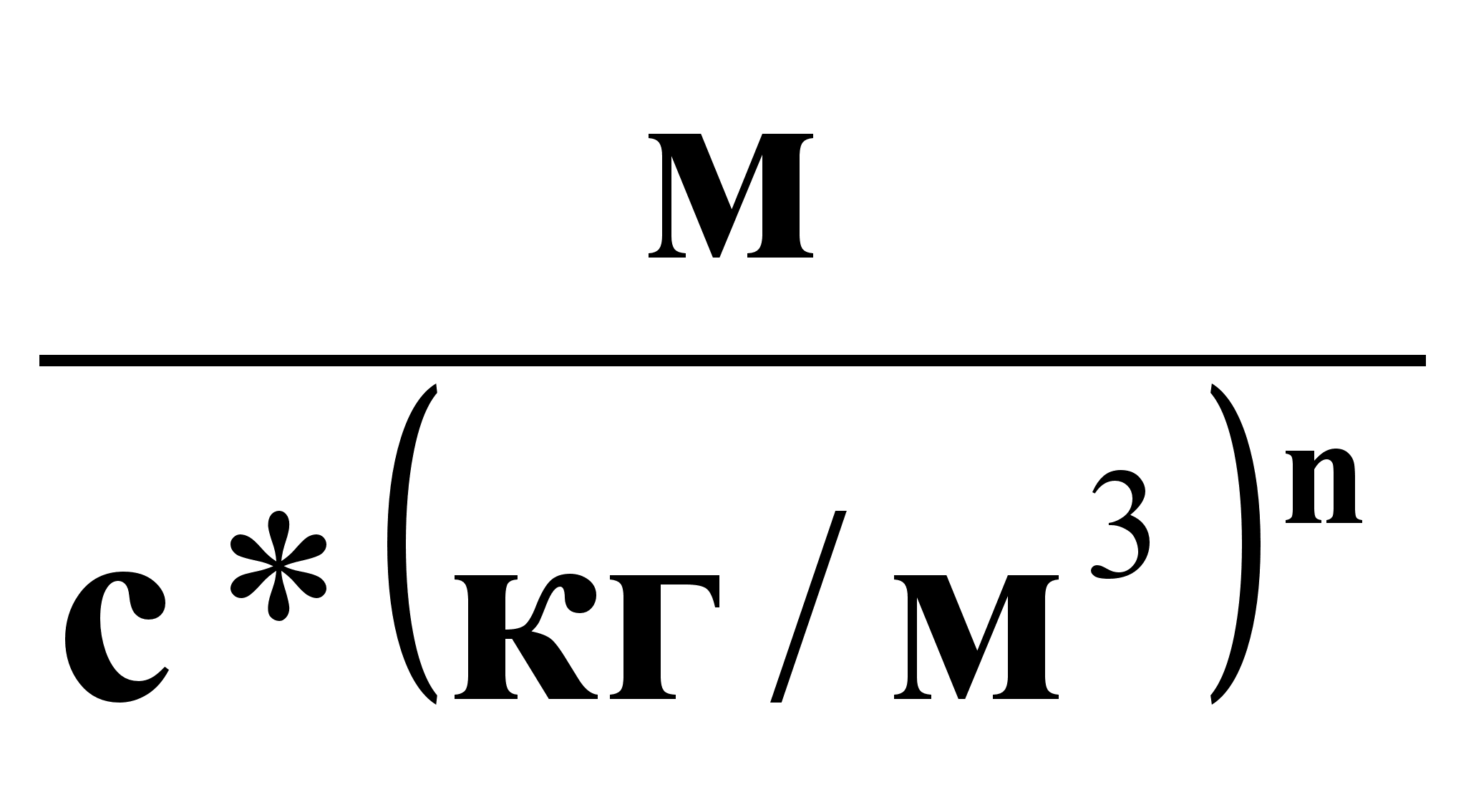 ;
;
Сп, С* - концентрации пересыщенного и насыщенного растворов, кг/м3;
Еа - энергия активации, кдж/кг;
- температура, К;
R - универсальная газовая постоянная, кдж/кг*К.
На основании (9) и (10) - диаметр кристалла можно представить:
![]() .
.
Если процесс кристаллизации вести при = const = зд и обеспечить Сн= const, то Сп и С* будут предопределены, т.к. система имеет 2 степени свободы (s=2).
Таким образом, dкр=dкрзд можно обеспечить стабилизацией при условии Сн= const.
Тепловой баланс процесса кристаллизации.
Уравнение динамики:
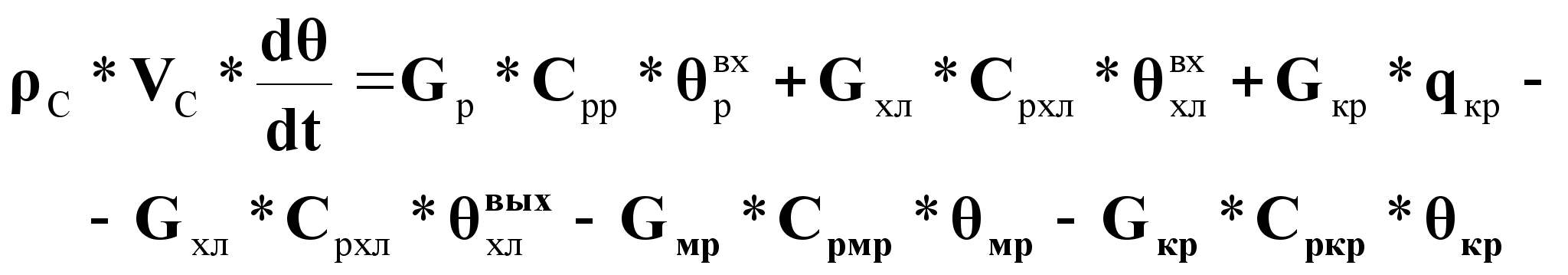 (11).
(11).
Можно принять = мр = кр = с .
Уравнение
статики при
![]() :
:
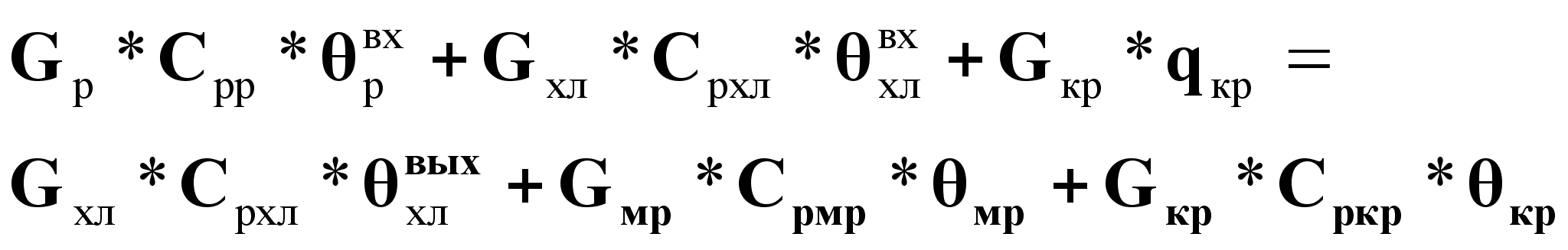 (12).
(12).
На основании (11) и (12) можно считать:
![]()
Предпочтительное управляющее воздействие Gхл .
Информационная схема кристаллизатора
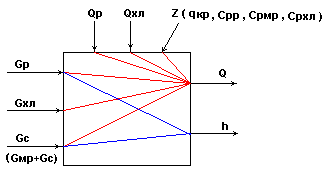
Рис.6.
Основные регулируемые переменные: ![]() ;
;
Возможные регулирующие воздействия: ![]()
Возможные контролируемые возмущения: ![]()
Возможные неконтролируемые возмущения:
![]() .
.
В целом, кристаллизатор является сложным многосвязным объектом.
Типовая схема автоматизации процесса кристаллизации
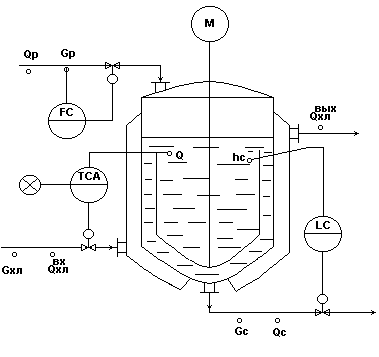
Рис.7.
Регулирование.
Регулирование в аппарате по подаче хладоагента Gхл - обеспечивает косвенное регулирование показателя эффективности процесса: = f (dкр).
Регулирование h по отбору маточного раствора Gмр - для обеспечения материального баланса по жидкой фазе.
Стабилизация расхода исходного раствора Gр - для обеспечения заданной производительности установки.
Контроль.
Расходы: ![]() .
.
Температуры: ![]() .
.
Уровень: h.
Сигнализация.
Значительные отклонения температуры от задания.
3. Материалы к лекции №11Автоматизация процесса абсорбции
Равновесие в процессе абсорбции.
Число степеней свободы для системы бинарный газ+жидкость:
S = k – f + 2=3-2+2=3.
Переменные для данной системы: температура , давление Р; концентрации С.
Равновесие такой системы при постоянных и Р описывается законом Генри:
![]() (1),
(1),
где m - коэффициент распределения:
![]() (2),
(2),
где Е - константа Генри:
![]() (3),
(3),
где q - дифференциальная теплота растворения; R - универсальная газовая постоянная; С - константа.
На основании (2) и (3) коэффициент распределения m зависит от P и следующим образом: при Р, m ; при , Е . m.
Следовательно, растворимость газа в жидкости на основании (1), определяемая как: ![]() , увеличивается с увеличением давления Р и уменьшением температуры .
, увеличивается с увеличением давления Р и уменьшением температуры .
Влияние Р и на среднюю движущую силу процесса абсорбции.
(фазовые диаграммы при противотоке распределяющих веществ)
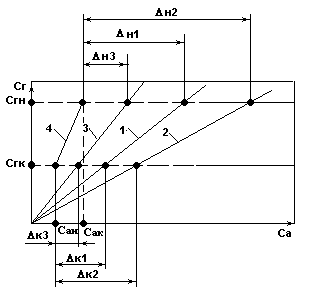
Рис.1.
При Р1 и 1 , Δср1; 2 - При Р2 > Р1 , Δср2 ; 3 - При 3 > 1 , Δср3
Результаты анализа диаграмм:
Δср =f (, Р, сгн , сгк , сан , сак );
Δср2 > Δср1 ; при Р→ Δср ;
Δср3 < Δср1 ; при → Δср
Влияние направления движения потоков
на средние движущие силы процесса абсорбции.
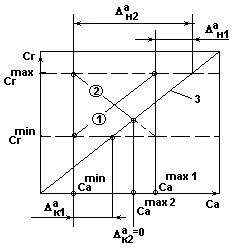
Рис.2а.
- рабочая линия процесса абсорбции при противотоке распределяющих веществ;
- рабочая линия процесса абсорбции при прямотоке распределяющих веществ;
- равновесная линия процесса абсорбции.
Движение распределяющих веществ противотоком.
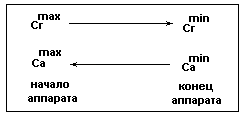
Рис.2б.
Са изменяется от Саmin до Саmax1 , (![]() ).
).
Движущая сила: ![]() .
.
Движение распределяющих веществ прямотоком.
Рис.2в.
Са изменяется от Саmin до Саmax2 , (![]() ).
).
Движущая сила: ![]() .
.
Выводы по характеристикам схем противотока и прямотока:
- ![]() ; 2. -
; 2. - ![]() .
.
Кинетика процесса абсорбции.
Уравнения массопередачи в процессе абсорбции:
![]()
![]() (4а),
(4а),
или
![]() (4б),
(4б),
где
Мга - масса распределяемого компонента, переходящая из газа в абсорбент в единицу времени, кг/ч;
F - поверхность массопередачи м2;
![]() и
и ![]() ;
;
![]() и
и ![]() ;
;
Кг
, Ка - коэффициенты
массопередачи,
![]() ;
;
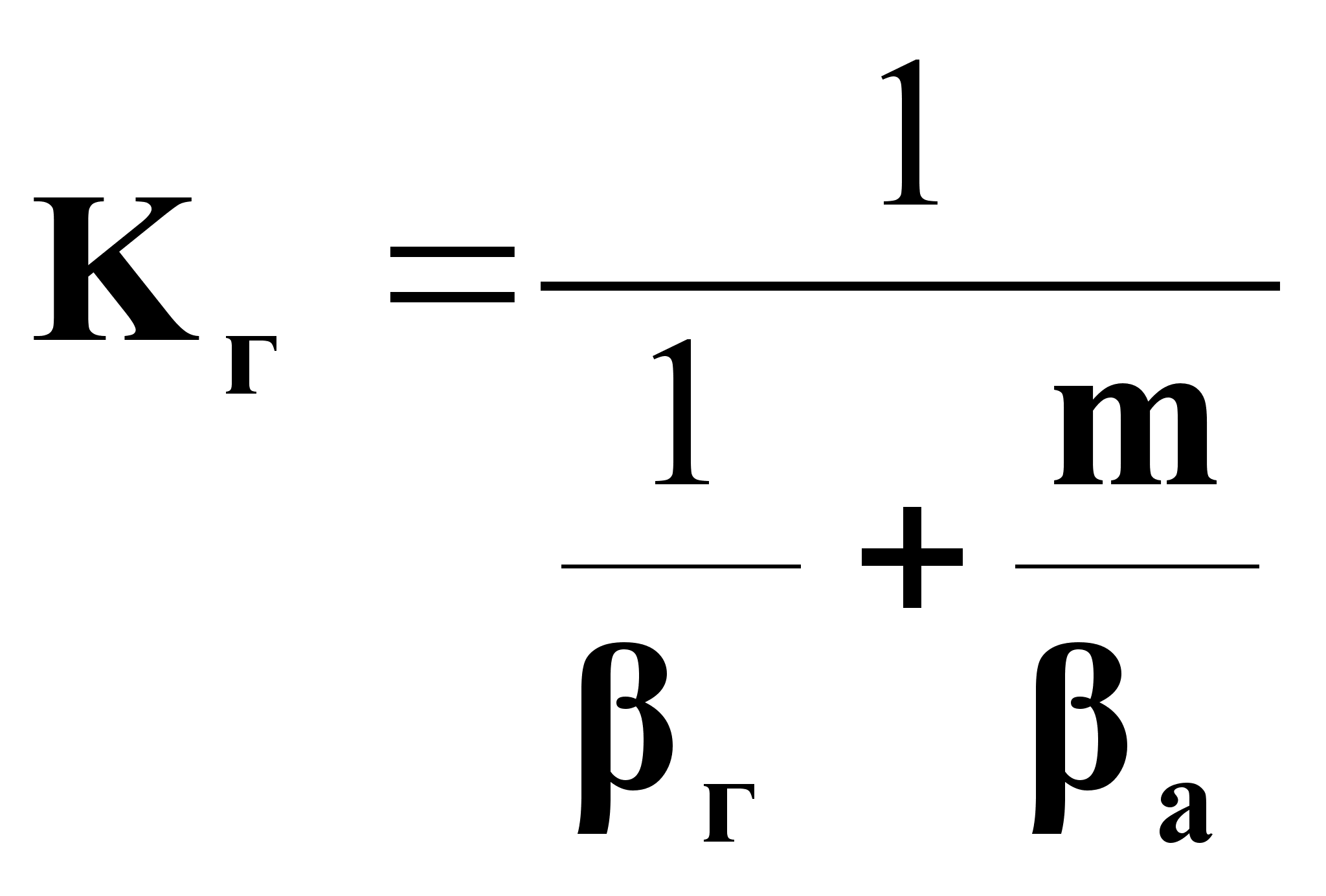 ;
;
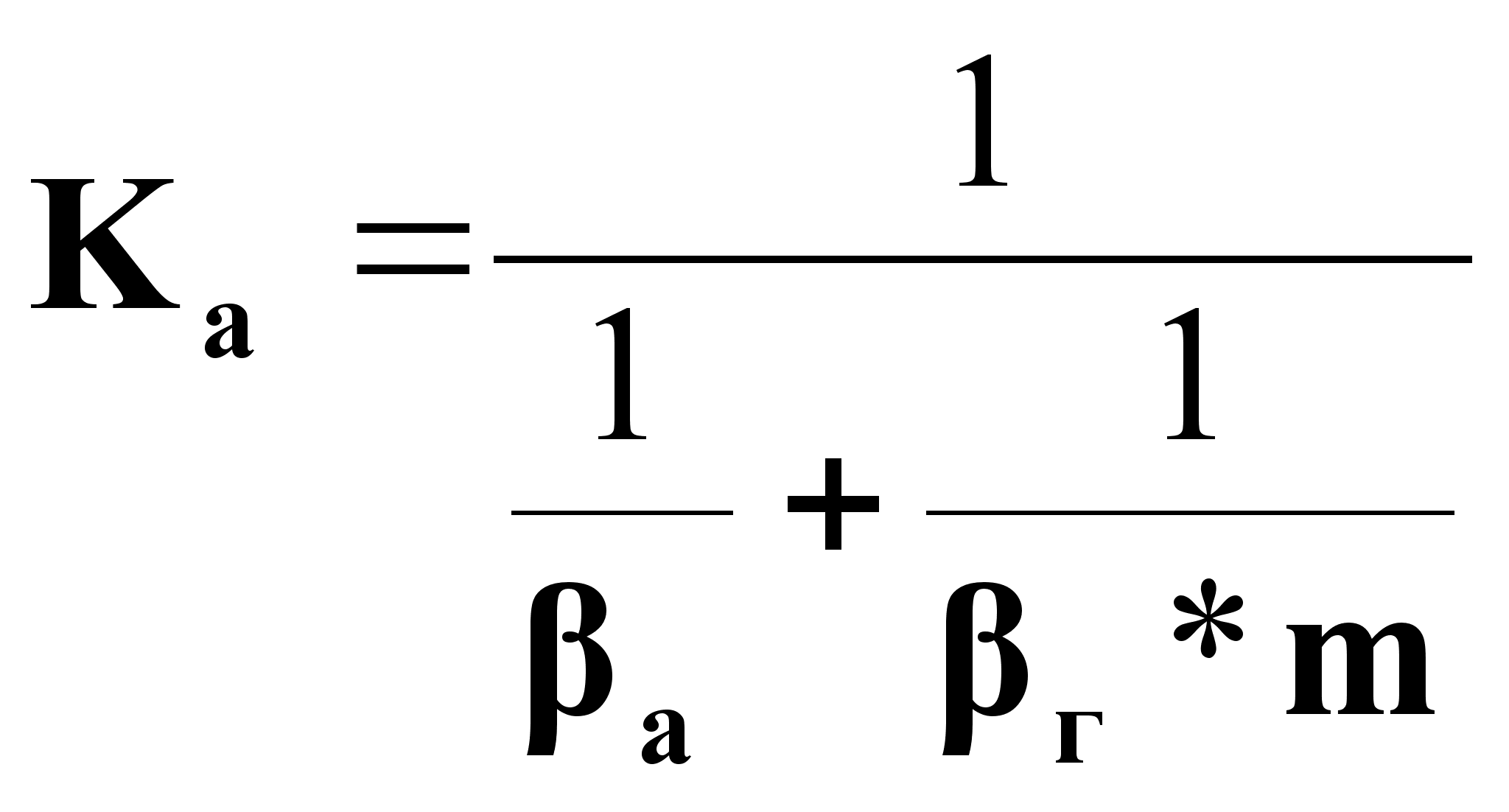 ,
,
где
г - коэффициент массоотдачи от потока газа к поверхности контакта фаз, кг/(м2 *ч);
а - коэффициент массоотдачи от поверхности контакта фаз к потоку абсорбента, кг/(м2 *ч).
Схема насадочного абсорбера.
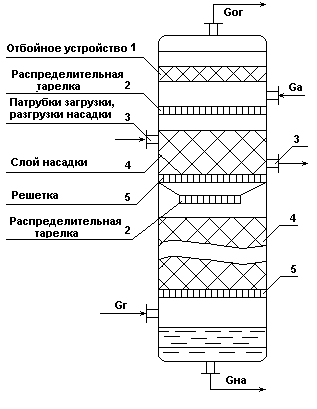
Рис.6.
Объект управления
Схема абсорбционной установки.
1, 2 –
холодильники;
3 – абсорбционная
насадочная
колонна.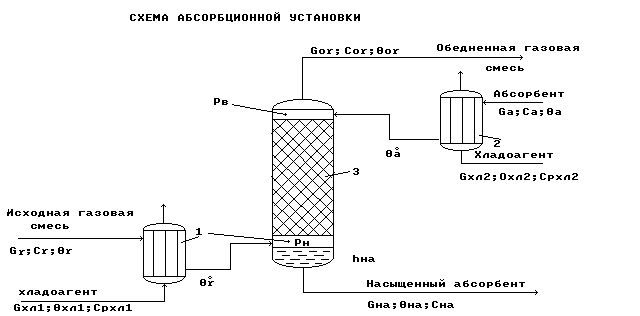
Рис.5.
Работа схемы.
Исходная газовая смесь Gг и абсорбент Gа в холодильниках 1 и 2 охлаждаются до заданных температур г0 и а0 и противотоком подаются в колонну 3.
В колонне 3 происходит извлечение целевого (распределяемого) компонента из исходной газовой смеси с помощью жидкого абсорбента.
В результате массообменного процесса между газовой и жидкой фазами получают:
в низу колонны - насыщенный абсорбент Gна с концентрацией целевого (распределяемого) компонента сна;
в верху колонны - обедненную газовую смесь Gог с концентрацией целевого (распределяемого) компонента сог .
Показатель эффективности процесса - концентрация распределяемого компонента в обедненной газовой смеси сог.
Цель управления - обеспечение сог = согзд на минимально возможном для данной установки значении.
Материальный баланс по целевому компоненту.
Материальный баланс по целевому компоненту в газовой фазе.
Уравнение динамики:
![]()
![]() (1),
(1),
где Мгна - масса целевого компонента, переходящая из газовой фазы в жидкую в единицу времени, кг/ч.
Уравнение
статики ![]() :
:
![]() (2).
(2).
Из
выражений (1) и
(2) следует, что:![]() (3),
(3),
где Мгна - определяется уравнением массопередачи.
Материальный баланс по целевому компоненту в насыщенном абсорбенте.
Уравнение динамики:
![]() (4).
(4).
Уравнение
статики ![]() :
:
![]() (5).
(5).
Из выражений
(4) и (5) следует,
что: ![]() (6),
(6),
где Mгна - определяется уравнением массопередачи.
Материальный баланс по общему количеству целевого компонента в процессе абсорбции.
Уравнение динамики:
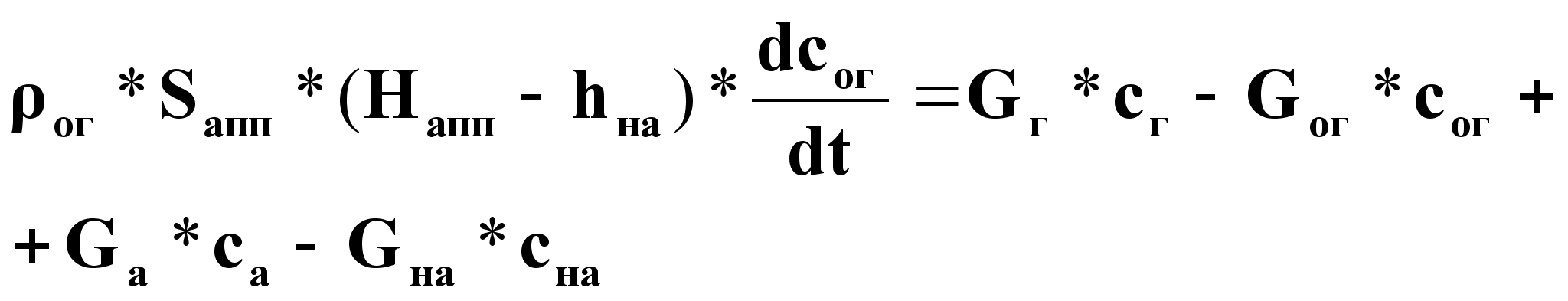 (7),
(7),
Уравнение
статики ![]() :
:
![]() (8).
(8).
На
основании (7) и
(8): ![]() (9).
(9).
Аналогично,
можно получить:
![]() (10).
(10).
Материальный баланс по жидкой фазе.
Уравнение динамики:
![]() , (11),
, (11),
Уравнение статики:
![]() (12)
(12)
На
основании (11)
и (12): ![]() . (13).
. (13).
Материальный баланс по газовой фазе.
Уравнение динамики:
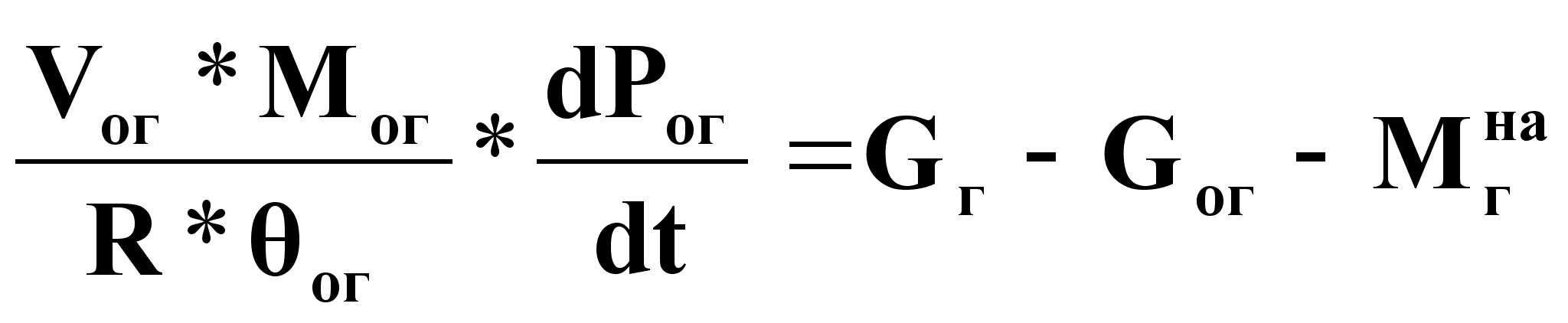 (14),
(14),
где Мог - мольная масса обедненной газовой смеси,
кг/моль;
Рог - давление в колонне, Па;
ог - температура в колонне (по газовой фазе), К,
Vог - объем газовой фазы в колонне, м3 .
Уравнение статики:
![]() (15).
(15).
На основании (14) и (15) можно считать:
![]() (16),
(16),
Предпочтительное управляющее воздействие Gог.
Тепловой баланс в абсорбере.
Уравнение динамики для холодильника1:
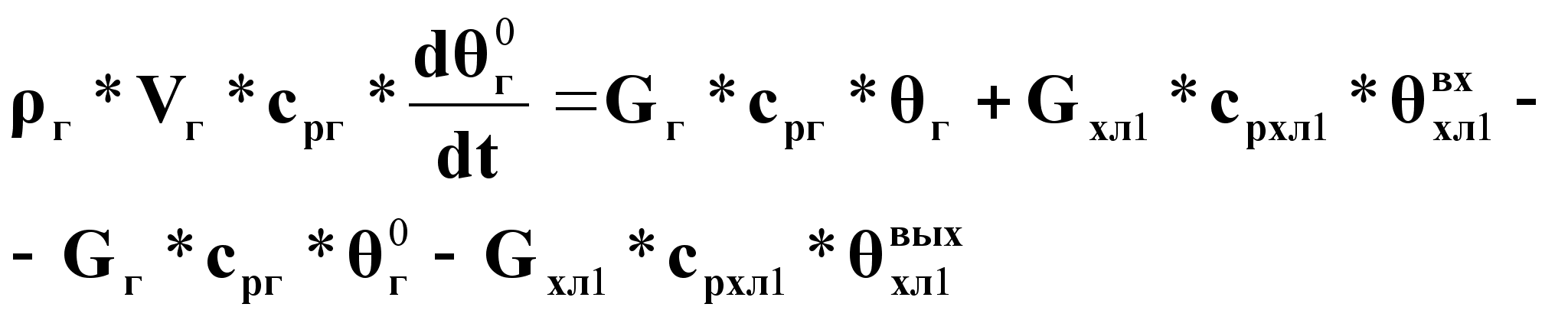 (17).
(17).
Уравнение статики при ![]() :
:
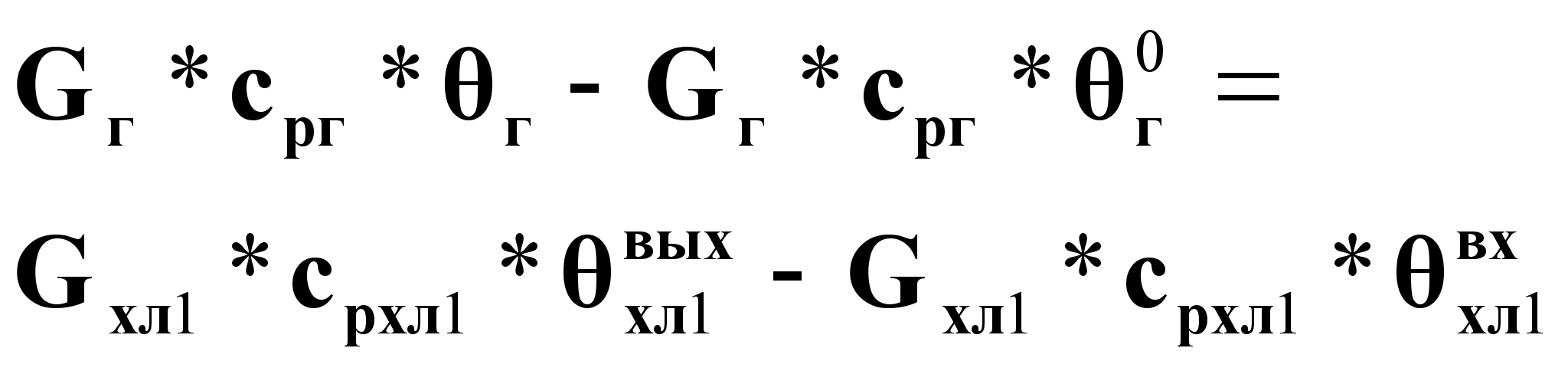 (18).
(18).
На основании (17) и (18) можно считать:
![]() (19).
(19).
Предпочтительное управляющее воздействие Gхл1.
Уравнение динамики для холодильника 2.
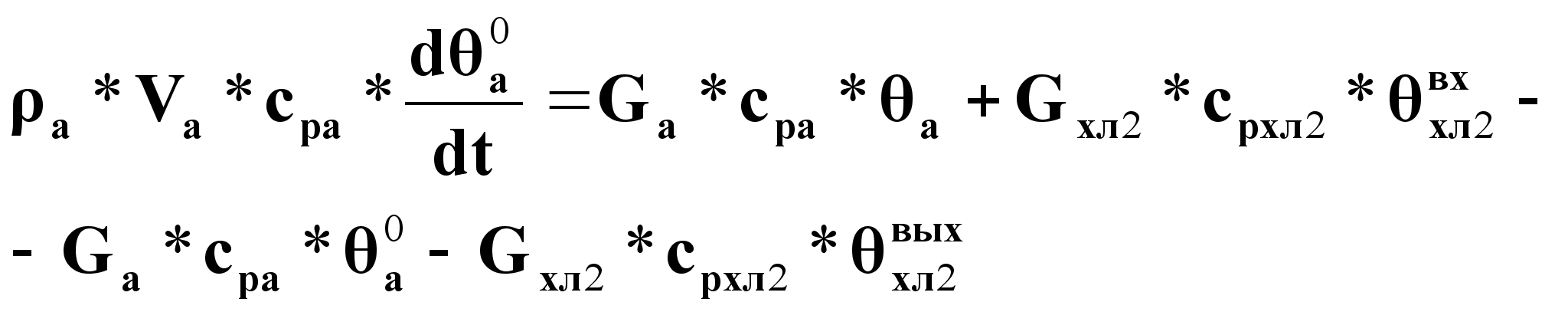 (20).
(20).
На основании (20) можно считать:
![]() (21).
(21).
Предпочтительное управляющее воздействие Gхл2.
Информационная схема для установки с показателем эффективности сог .
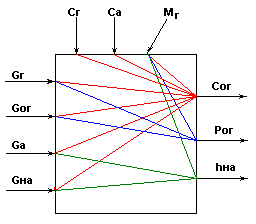
Рис.7
Возможные управляющие воздействия:![]() .
.
Возможные контролируемые возмущения: ![]() .
.
Возможные неконтролируемые возмущения: ![]() .
.
Возможные управляемые переменные: ![]() .
.
Схема абсорбционной колонны как многосвязного
объекта при показателе эффективности сог.
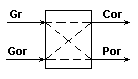
Рис.8
Информационная схема для установки с показателем эффективности сна .
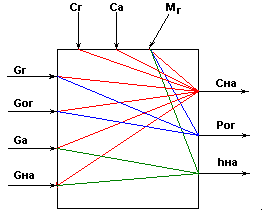
Рис.9
Возможные управляющие воздействия, контролируемые и неконтролируемые возмущения те же, что и в системе с показателем эффективности сог.
Возможные управляемые переменные: ![]() .
.
Схема абсорбционной колонны как многосвязного
объекта при показателе эффективности сна.
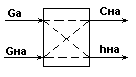
Рис.10.
Типовая схема автоматизации процесса абсорбции.
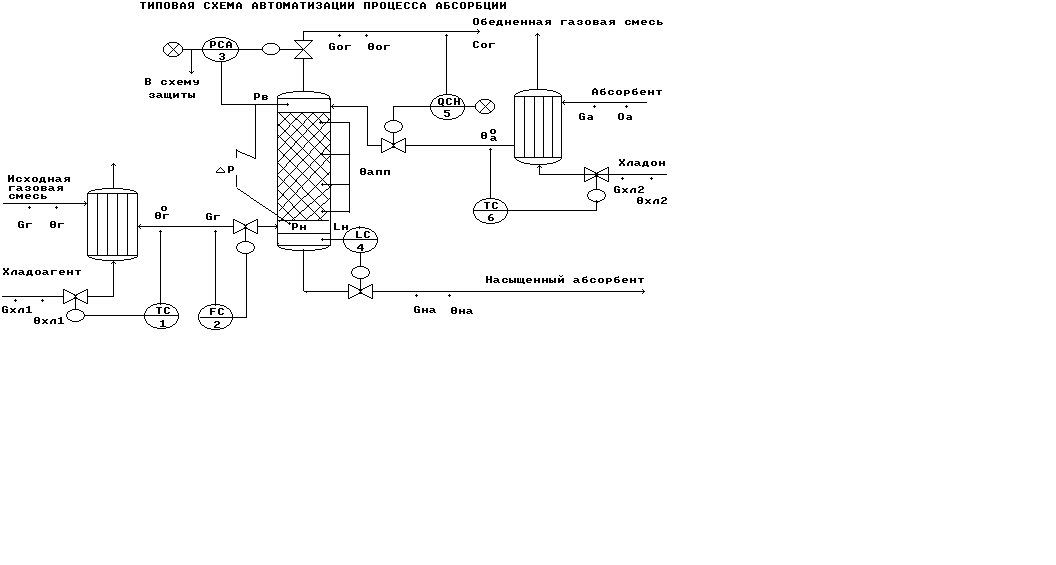
Рис. 11.
Регулирование.
Регулирование сог по подаче абсорбента Gа - как показателя эффективности процесса абсорбции.
Регулирование давления верха колонны Рв = Рог по отбору обедненной газовой смеси Gог - для обеспечения материального баланса по газовой фазе.
Регулирование уровня hна по отбору насыщенного абсорбента Gна - для обеспечения материального баланса по жидкой фазе.
Регулирование температуры исходных материальных потоков газа г0 и абсорбента а0 по подаче хладоагентов Gхл1 и Gхл2 соответственно - для обеспечения теплового баланса установки.
Стабилизация расхода исходной газовой смеси Gг - для обеспечения заданной производительности установки.
Контроль.
расходы - Gг, Gа, Gог, Gна, Gхл1, Gхл2;
температуры - ![]() ;
;
давление - Рв, Рн, Р;
уровень насыщенного абсорбента - hна;
концентрация - сог .
Сигнализация.
существенные отклонения сог от согзд ;
значительное повышение Рв > Рпред , при этом формируется сигнал «В схему защиты».
Система защиты.
По сигналу «В схему защиты» - открывается магистраль Gог, закрываются все остальные магистрали.
4. Материалы к лекции №12Автоматизация процесса сушки
Основные параметры сушильного агента и материала, как влагоносителей.
Относительная влажность сушильного агента :
![]() (1).
(1).
На основании уравнения Менделеева-Клапейрона можно получить :
![]() (3).
(3).
Относительная влажность материала - это
отношение массы влаги Мвл к общей массе влажного материала М=Мсм + Мвл , или к массе абсолютно сухого материала Мсм:
Влажность, отнесенная ко всему веществу:
![]() ,
где М=var
,
где М=var
Влажность, отнесенная к массе абсолютно сухого материала:
![]() , где Мсм=
const
.
, где Мсм=
const
.
Диаграммы равновесия при сушке.
Диаграмма
![]() при
= *.
при
= *.
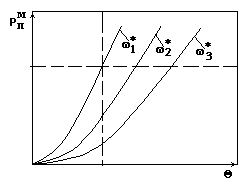
На диаграмме принято 1* >2*>3*.
Рис.1.
Из диаграммы следует:
При ![]() * - эффективность сушки повышается;
* - эффективность сушки повышается;
При * - эффективность сушки повышается.
Диаграмма *= f() при =const.
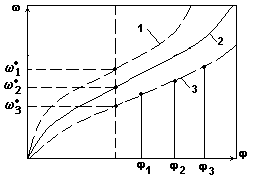
Рис.2.
На рис.2. приведены: 1 - диаграмма при 1; 2- диаграмма при 2;
-диаграмма при 3.
При условии, что 1 < 2 < 3
Из диаграммы следует: При ![]() . При
. При ![]()
Диаграмма - равновесной и рабочей линий
процесса сушки при прямотоке Gм и Gса
(при различных температурах).
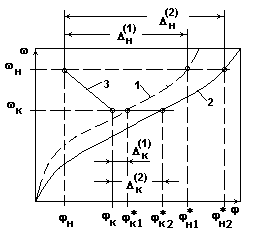
Рис.4.
На диаграмме представлены: 1 - Равновесная линия =f() при 1;
2 - Равновесная линия =f() при 2. 3 - Рабочая линия - .
На диаграмме принято: 2 > 1.
Из диаграммы рис.4 следует:
![]() . При
ср
. При
. При
ср
. При ![]()
Кинетика процесса сушки.
Уравнение массопередачи 1-го периода сушки с постоянной скоростью (Т1 ):
![]() (1),
(1),
где
К=са - коэффициент массоотдачи от поверхности контакта в газовую фазу;
![]() - средняя движущая сила процесса по сушильному агенту, где
- средняя движущая сила процесса по сушильному агенту, где ![]() .
.
Первый период сушки соответствует изменению влажности материала от ![]() .
.
При ![]() наступает 2-ой период сушки.
наступает 2-ой период сушки.
Уравнение массопередачи 2-го периода сушки с уменьшающейся скоростью (Т2 ):
![]()
![]() (2),
(2),
где
К - коэффициент массопередачи от материала к поверхности контакта фаз;
![]() ;
; ![]() .
.
Второй период сушки соответствует изменению влажности материала от ![]() .
.
Кривая скорости сушки.
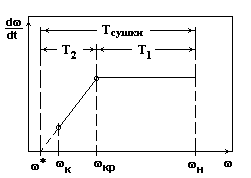
Рис.5.
Возможны следующие соотношения периодов сушки:
Тсушки = Т1
Тсушки = Т2
Тсушки = Т1+ Т2.
При анализе равновесия мы рассмотрели процесс сушки, характеризующийся первым периодом и уравнением массопередачи (1).
Объект управления.
Схема барабанной сушилки прямоточного действия
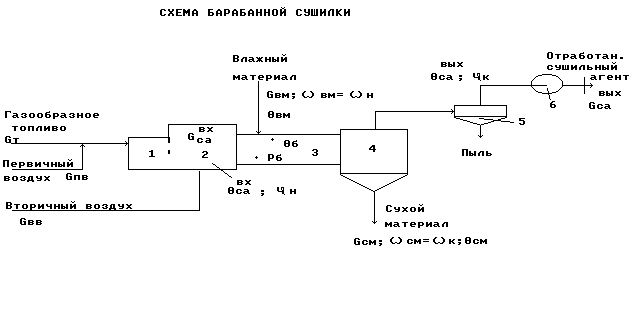
- топка; 2 - смесительная камера; 3 - сушильный барабан;
- циклон; 6 - вентилятор
Рис.6.
Газообразное топливо Gт подается с первичным воздухом Gпв через горелки в топку 1, где сжигается для получения сушильного агента.
Формирование сушильного агента осуществляется в смесительной камере 2, куда подается вторичный воздух Gвв.
Влажный материал подается с помощью автоматического дозатора 7 в сушильный барабан 3. Барабан наклонно расположен и вращается со скоростью 4-5 об/мин, так что материал перемещается вдоль барабана и высушивается к моменту попадания в бункер 4 до определенной влажности см.
Сухой материал Gсм отгружается из бункера 4 автоматическим дозатором 7.
Отработанный сушильный агент Gса в циклоне 5 очищается от пыли и вентилятором 6 выводится из процесса.
Показатель эффективности процесса - влажность сухого материала см .
Цель управления процессом - поддержание см = смзд.
Структурная схема топки и смесительной камеры.
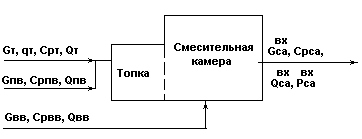
Рис.7.
Материальный баланс по газовой фазе.
Уравнение динамики:
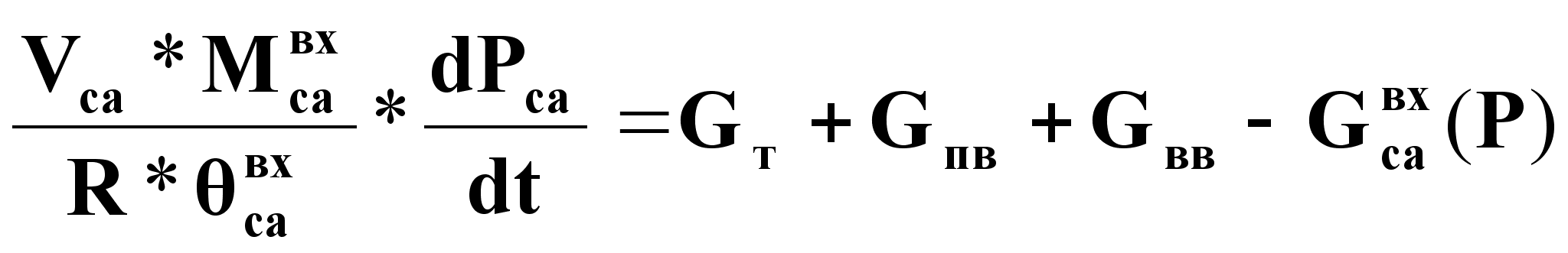 (1),
(1),
Уравнение статики:
![]() . (2)
. (2)
Тепловой баланс.
Уравнение динамики:
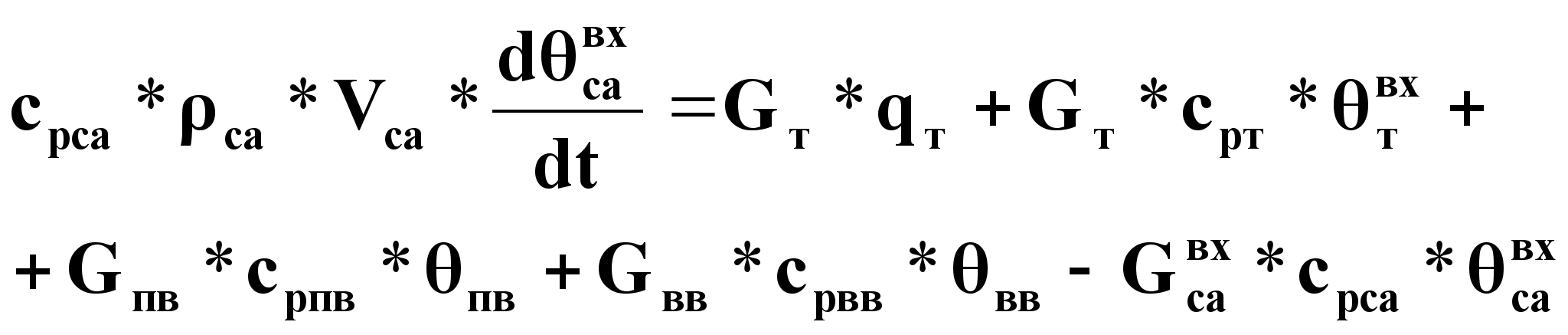 (3).
(3).
Уравнение статики:
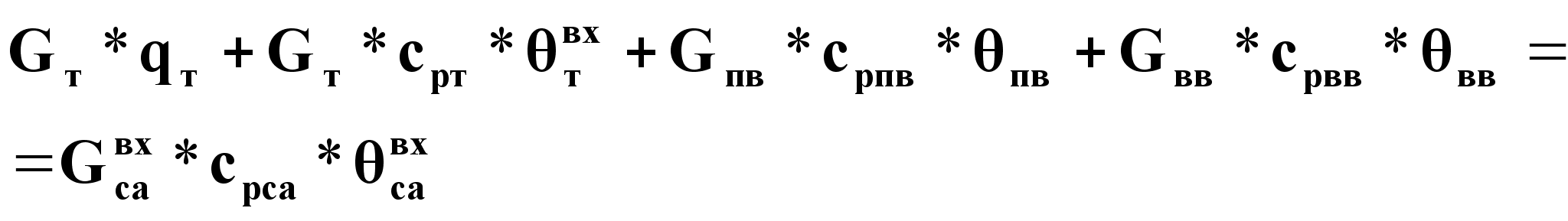 (4)
(4)
Информационная схема топки
и смесительной камеры.
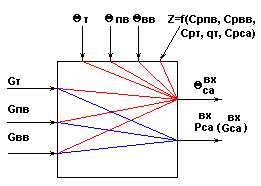
Рис.8.
![]() - возможные неконтролируемые возмущения;
- возможные неконтролируемые возмущения;
![]() - возможные контролируемые возмущения;
- возможные контролируемые возмущения;
![]() - возможные управляющие воздействия.
- возможные управляющие воздействия.
Выводы по анализу топки и смесительной камеры как объекта управления:
![]() ;
;
![]() .
.
Структурная схема сушильного барабана.
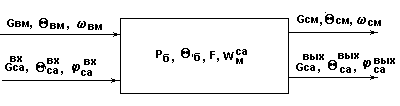
Рис.9.
Материальный баланс по твердой фазе.
Уравнение динамики:
![]() ,
(5),
,
(5),
где hм - высота слоя материала в барабане;
Sапп - сечение аппарата;
м - плотность материала;
Wмса - количество влаги, удаляемой в процессе сушки из материала в единицу времени, кг/с.
Уравнение статики:
![]() (6).
(6).
На основании (5) и (6) можно принять:
![]() .
.
В типовой схеме автоматизации стабилизируют Gвм и Gсм, что обеспечивает также стабилизацию hм
Материальный баланс по газовой фазе.
Уравнение динамики:
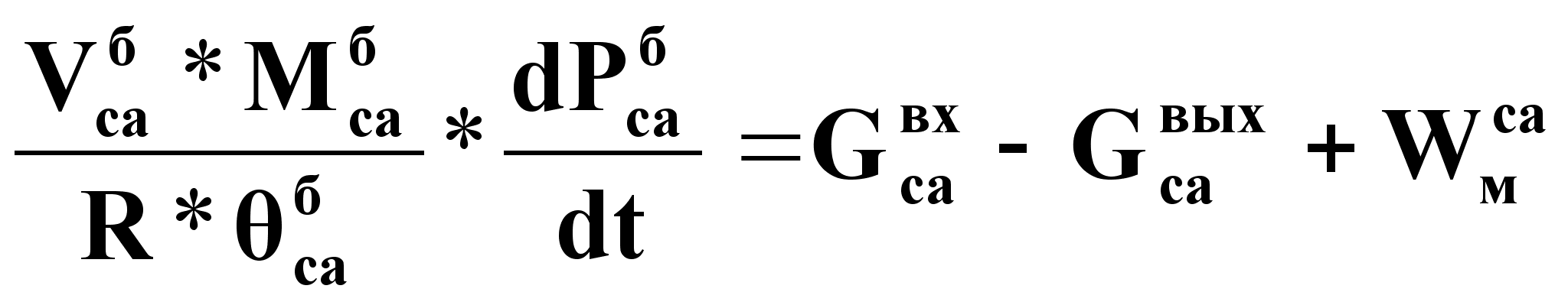 (7),
(7),
где
Мсаб - мольная масса сушильного агента в барабане,
кг/моль;
Рсаб - разрежение в барабане, Па;
саб - температура в барабане (по газовой фазе), К,
Vсаб - объем газовой фазы в барабане, м3.
Уравнение статики:
![]() (8).
(8).
На основании (7) и (8) можно считать:
![]() .
.
Предпочтительным управляющим воздействием является Gсавых.
Тепловой баланс в сушильном барабане.
Уравнение динамики:
 (9).
(9).
Уравнение статики при ![]() :
:
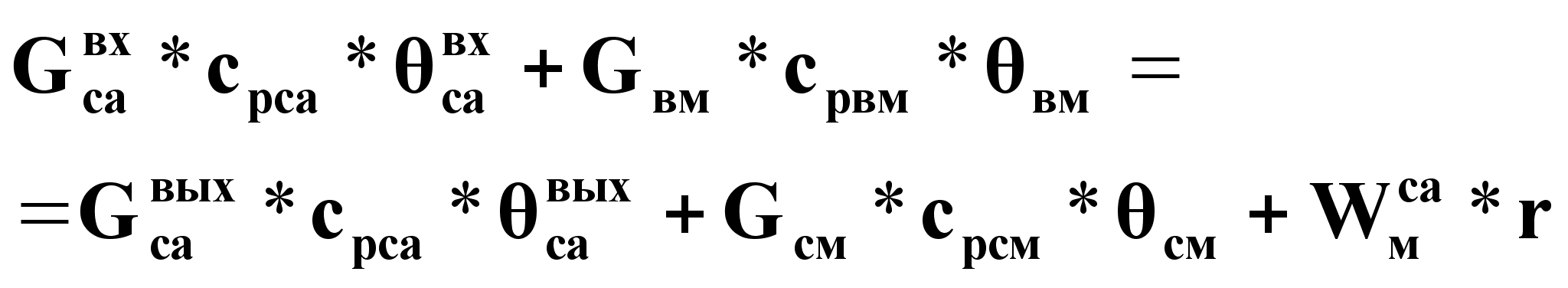 (10).
(10).
В выражениях (9) и (10) принимаем:
![]() ;
;
r - удельная теплота испарения влаги , дж/кг.
На основании (9) и (10) можно принять:
![]() (11),
(11),
где
![]() (12).
(12).
Материальный баланс по количеству влаги в материале.
Уравнение динамики:
![]() (13),
(13),
Уравнение статики ![]() :
:
![]() (14).
(14).
Из выражений (13) и (14) следует, что:
![]() (15),
(15),
где Wмса - определяется уравнением массопередачи.
Материальный баланс по количеству влаги в сушильном агенте.
Уравнение динамики:
![]() (16).
(16).
Уравнение статики ![]() :
:
![]() (17).
(17).
Из выражений (16) и (17) следует, что:
![]() (18).
(18).
Материальный баланс по общему количеству влаги в процессе сушки.
Уравнение динамики:
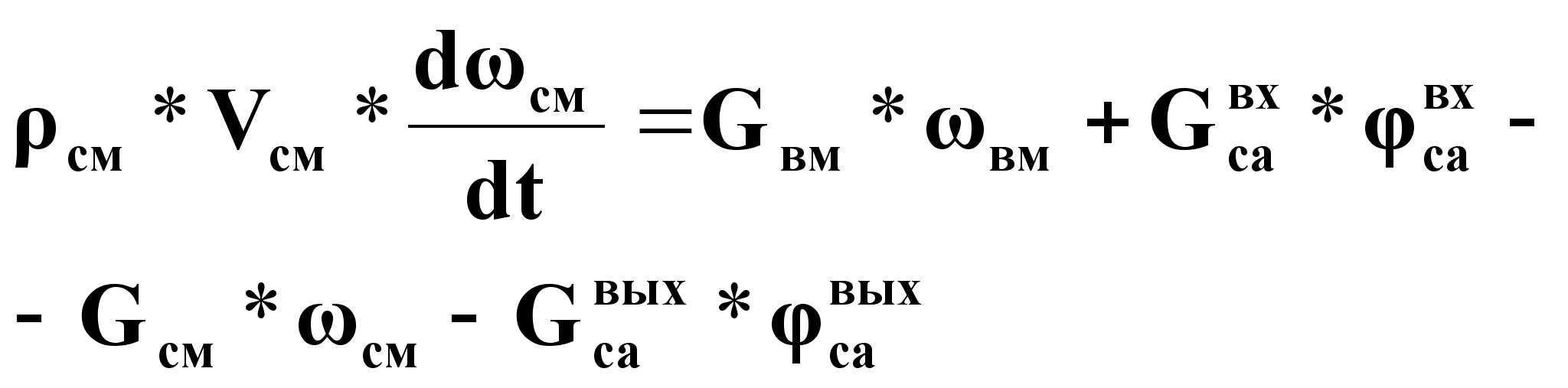 (19),
(19),
где ![]() .
.
Уравнение статики ![]() :
:
![]() (20).
(20).
На основании выражений (19) и (20) можно считать:
![]() (21).
(21).
При анализе топки мы получили:
![]() (22).
(22).
Из всех возможных управляющих воздействий, перечисленных в выражениях (21) и (22), для регулирования конечной влажности материала наиболее информативным является расход топлива Gт.
Информационная схема сушильного барабана.
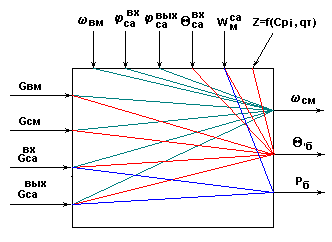
Рис.10.
Возможные управляющие воздействия:
![]() .
.
Возможные контролируемые возмущения:
![]() .
.
Возможные неконтролируемые возмущения:
![]() .
.
Возможные управляемые переменные:
![]() .
.
Сушильный барабан является сложным многосвязным объектом.
Типовая схема автоматизации процесса сушки.
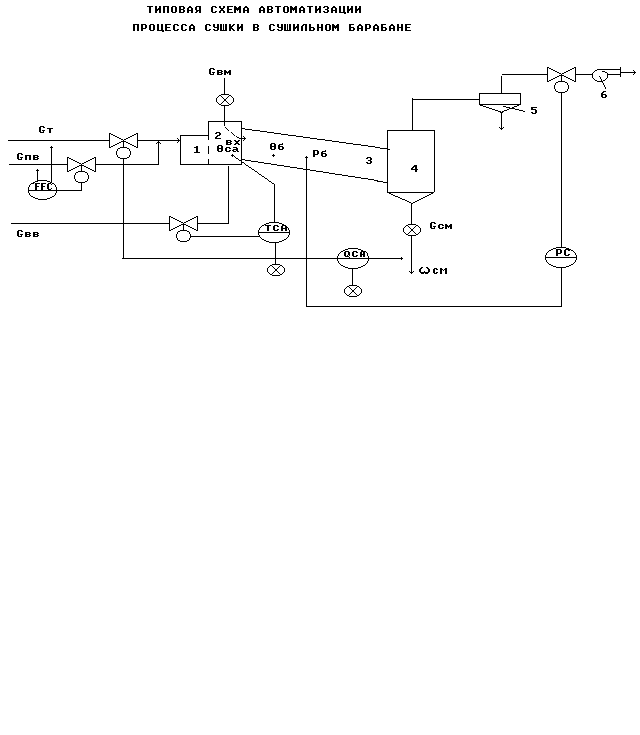
Рис.11.
Регулирование.
Регулирование см по подаче топлива Gт - как показателя эффективности процесса сушки.
Регулирование соотношения расходов топлива Gт и первичного воздуха Gпв по подаче первичного воздуха ![]() - для обеспечения эффективности сгорания топлива.
- для обеспечения эффективности сгорания топлива.
Регулирование температуры сушильного агента на входе в барабан савх по подаче вторичного воздуха Gвв.
Регулирование разрежения в барабане Рсаб по отбору отработанного сушильного агента Gсавых - для для обеспечения материального баланса по газовой фазе.
Стабилизация расходов влажного и сухого материала Gвм и Gсм автоматическими дозаторами - для обеспечения материального баланса по твердой фазе.
Контроль.
расходы - Gт, Gпв, Gвв, Gвм, Gсм;
температуры - ![]() ;
;
разрежение - Рб;
влажность - см (к).
Сигнализация.
существенные отклонения см от зд;
значительное повышение савх;
Незапланированное отключение привода, при этом формируется сигнал «В схему защиты».
Система защиты.
По сигналу «В схему защиты» - прекратить подачу материала и топлива в сушильный агрегат.
5. Материалы к лекции №13Автоматизация процесса ректификации (ч.1)
Диаграмма равновесия «θ – x – y » при Р= const.
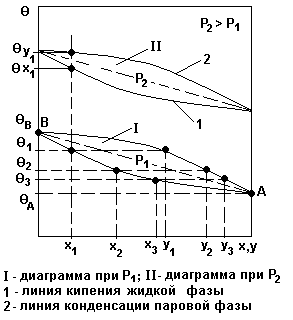
Рис.1.
Смесь двухкомпонентная: компонент А - низкокипящий; компонент В - высококипящий.
Диаграмма позволяет определять:
θx и θy - для любого состояния смеси при заданном Р;
x и y - для любой температуры смеси.
По данным диаграммы «θ – x – y » может быть построена диаграмма равновесия « x – y » при Р= const.
Диаграмма равновесия « x – y » при Р= const.
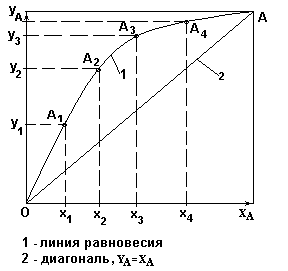
Рис.2.
На осях y и x откладывают значения yА и xА соответствующие 100% содержанию компонента А в паровой и жидкой фазах соответственно;
Диагональ ОА соответствует составам смеси yА = xА.
Расположение равновесной линии выше диагонали означает, что пары обогащены низкокипящим компонентом.
Чем ближе линия равновесия к диагонали, тем меньше разница составов жидкой и паровой фаз и тем труднее разделяется смесь при ректификации.
Схема колонны ректификации для математического
описания рабочих линий процесса.
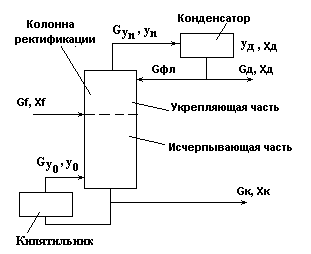
Рис.3.
Обозначения параметров процесса:
Gf, Gфл, Gд, G к - расходы питания, флегмы, дистиллята, куба;
xf, xд, xк - молярные составы соответствующих потоков;
R=Gфл/Gд - флегмовое число.
Расчет рабочего флегмового числа.![]() ,
,
где xf - заданный состав жидкой фазы потока питания;
yf - соответствующий ему равновесный состав паровой фазы потока питания.
Рабочее флегмовое число находят из соотношений:
R=1,3*Rmin+0,3
или
R=σ* Rmin,
где σ=1,2-2,5 - коэффициент избытка флегмы.
Уравнение рабочей линии верхней (укрепляющей) части колонны.
![]() (1),
(1),
где y, x - составы паровой и жидкой фаз верха колонны, молярные доли; xд - состав дистиллята.
Обозначим:
![]() .
.
![]() (2),
(2),
где
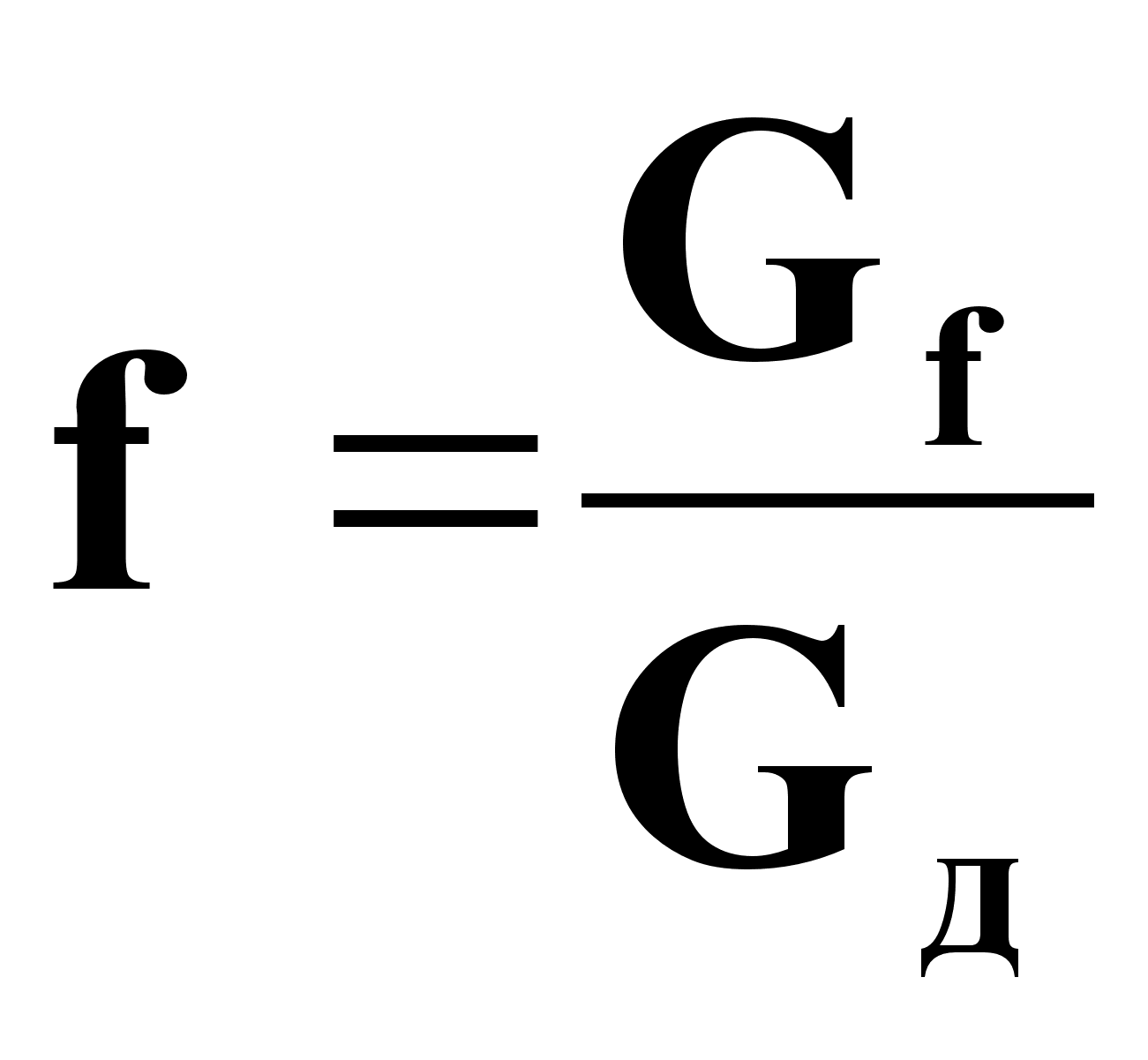 .
.
Обозначим:
![]() ;
; ![]()
Построение рабочих линий процесса ректификации.
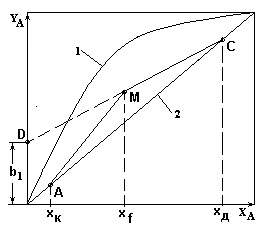
Рис.4.
1 - Равновесная линия процесса ректификации;
2 - Линия равных концентраций паровой и жидкой фаз компонента А в колонне.
Составы паровой и жидкой фаз в верхней и нижней частях колонны равны, т.е соответствуют линии 2.
По xд находят точку С.
По xк находят точку А.
По xf проводят вертикаль.
По оси y откладывают величину ![]() из соотношения (1) и получают точку D.
из соотношения (1) и получают точку D.
Получают точку М на пересечении СD с вертикалью от xf.
Получают СМ - рабочую линию верха колонны.
Проводят МА - рабочую линию низа колонны.
Диаграмма «Рабочая линия-линия равновесия»
процесса ректификации.
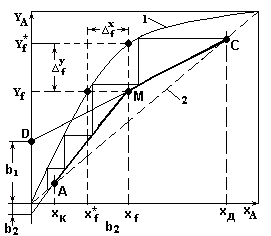
Рис.7.
1 – равновесная линия процесса бинарной ректификации;
2 – Линия равных концентраций в паровой и жидкой фазах
Линия СМ – рабочая линия верха колонны с параметрами: ![]() ;
; 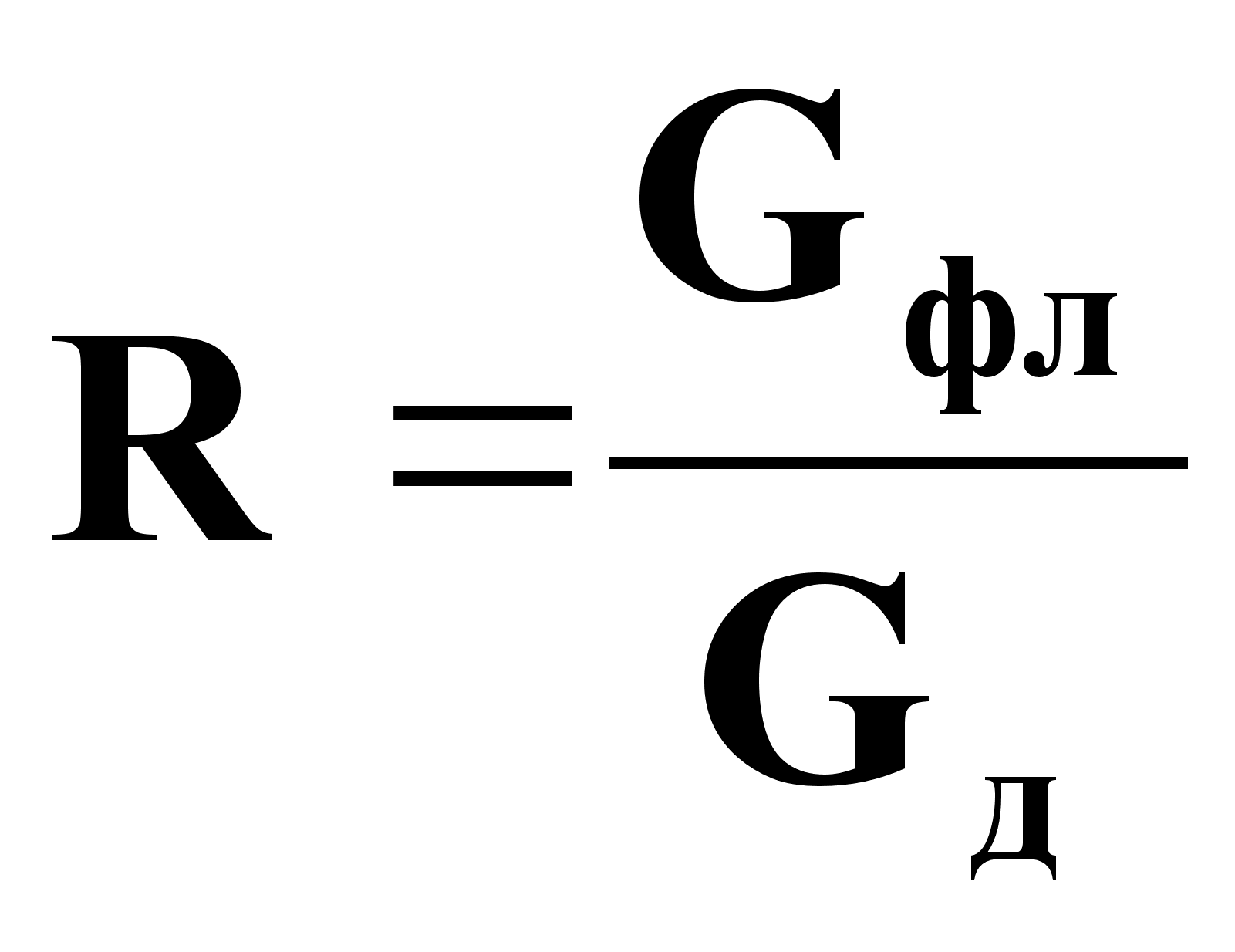
Линия МА – рабочая линия низа колонны с параметрами:
![]() ;
;
![]() ;
; 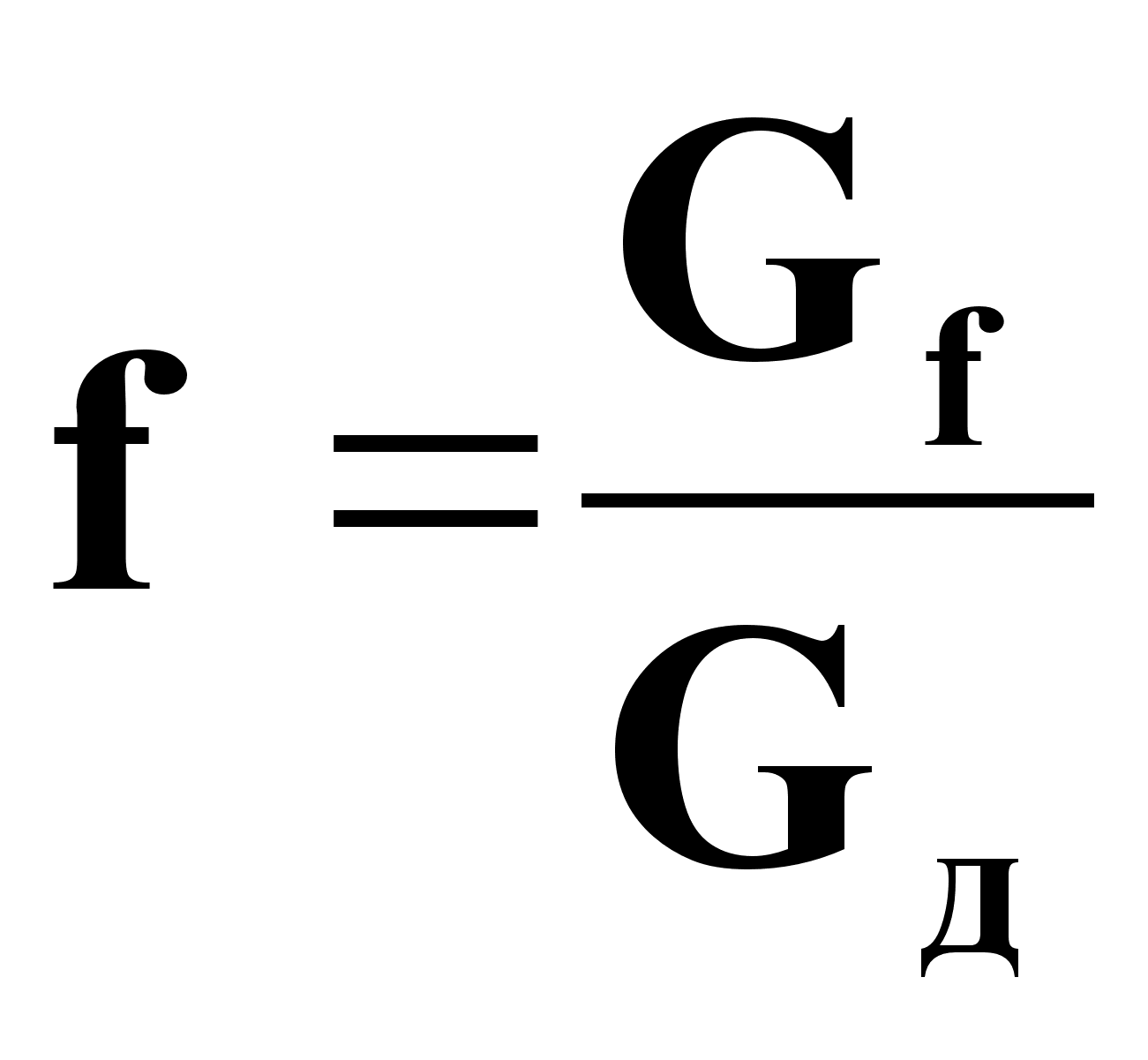 .
.
Анализ диаграммы «Рабочая линия - линия равновесия».
По диаграмме определяют следующие параметры:
Число ступеней разделения, число теоретических тарелок nт и число реальных тарелок ![]() , где η - к.п.д. тарелки.
, где η - к.п.д. тарелки.
Движущую силу процесса в любых точках колонны:
![]() ,
,
![]() ,
что соответствует
направлению
массопередачи
,
что соответствует
направлению
массопередачи
![]() ,
и
,
и ![]() .
.
Движущие силы ![]() зависят:
зависят:
от режимных параметров процесса, определяющих положение равновесной кривой (Р и θ);
от xf , xд, xк - определяющих положение рабочей линии процесса;
от R=Gфл/Gд и 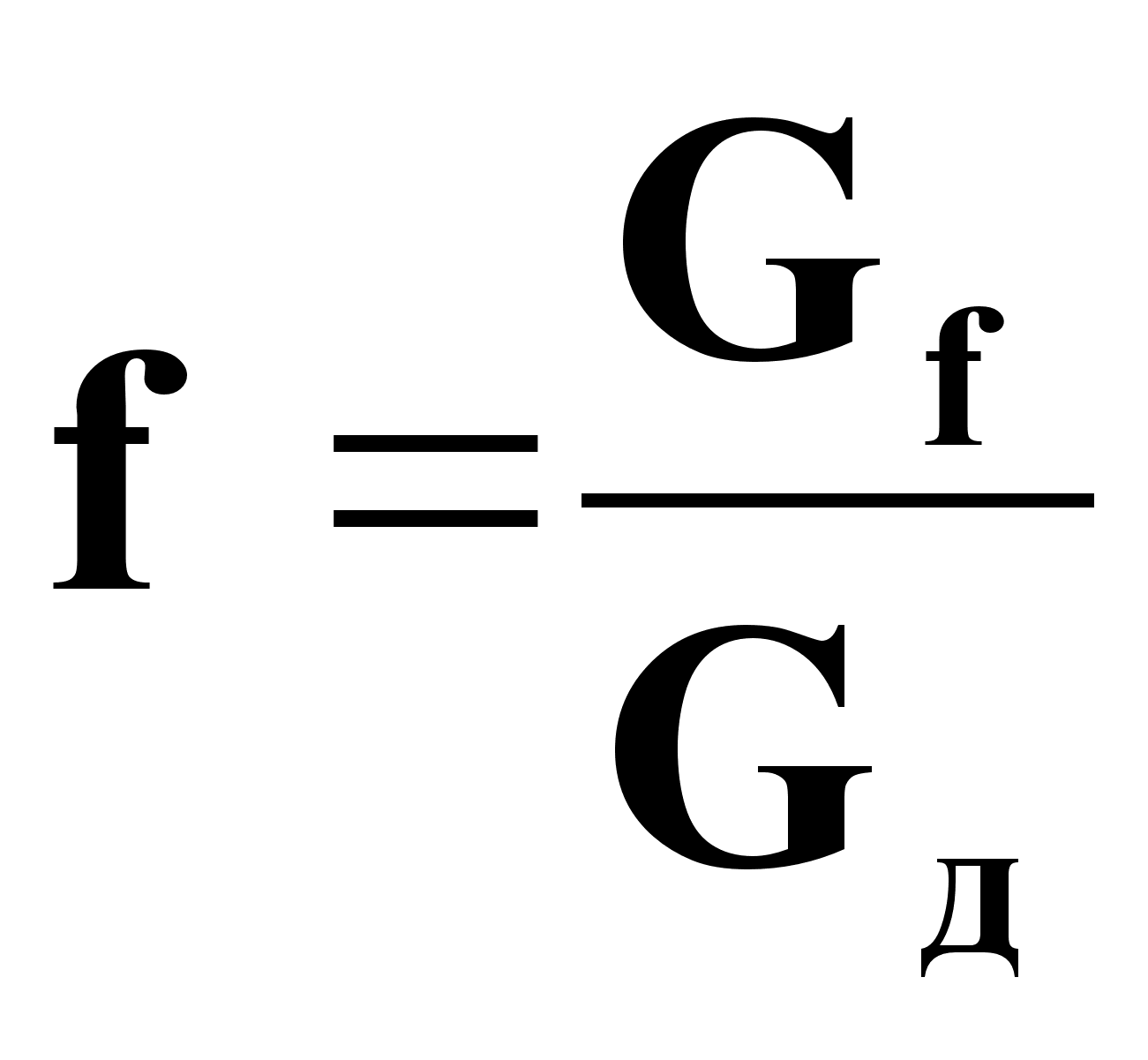 , т.е. от Gфл, Gд, Gf;
, т.е. от Gфл, Gд, Gf;
от тепловых параметров Gf.
Требуемую движущую силу процесса ректификации можно обеспечить:
стабилизацией режимных параметров Р или θ;
стабилизацией параметров потока питания Gf и θ f;
стабилизацией или изменением флегмового числа R=G фл /Gд .
Объект управления
Схема ректификационной установки.
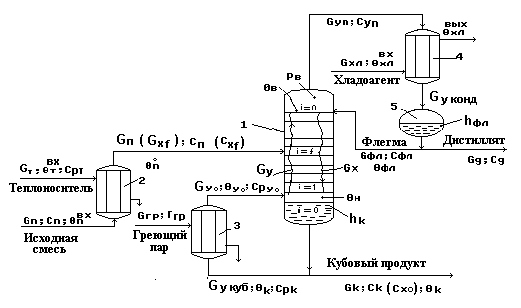
- ректификационная колонна; 2 - подогреватель потока питания;
- кипятильник; 4 - конденсатор (дефлегматор); 5 - флегмовая емкость.
Рис. 8.
Описание установки.
Объект управления - ректификационная установка для выделения из исходной жидкой смеси целевого компонента в составе дистиллята.
Процесс массопередачи происходит на тарелках укрепляющей (верхней) и исчерпывающей (нижней) частей колонны в результате взаимодействия жидкой и паровой фаз, движущихся в колонне противотоком.
Движущая
сила - разность
между равновесной
и рабочей
концентрациями
целевого компонента
в жидкой или
паровой фазе:
![]() и
и ![]() соответственно.
соответственно.
Работа установки.
Исходная смесь Gп (Gxf) нагревается в подогревателе потока питания 2 до температуры кипения θп0 и подается в колонну 1 на тарелку питания (i=f).
Исходная смесь стекает по тарелкам нижней части колонны в виде жидкостного потока Gx в куб колонны, участвуя в массообменном процессе с паровым потоком Gy.
Из куба колонны выводится кубовый продукт Gкуб. Часть кубового продукта подается в кипятильник 3, где испаряется с образованием парового потока Gy0 , который подается в низ колонны.
Паровой поток поднимается вверх колонны, контактируя с жидким потоком и обогащаясь целевым компонентом.
Обогащенный целевым компонентом паровой поток Gyn выводится из верха колонны и подается в дефлегматор 4, где конденсируется.
Конденсат собирается во флегмовой емкости 5. Из сборника флегмы отбирается два потока:
поток дистиллята Gд - целевой продукт;
поток флегмы Gфл - жидкая фаза, используемая для орошения верха колонны.
Показатель эффективности процесса сд - концентрация дистиллята.
Цель управления процессом - обеспечение сд.=сдзд.
6. Материалы к лекции №14
Автоматизация процесса ректификации (ч.2).
Структурная схема ректификационной установки.
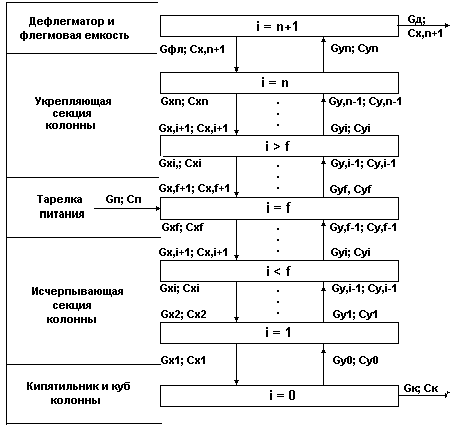
Рис.1.
Математическое описание низа колонны
Структурная схема куба и кипятильника.
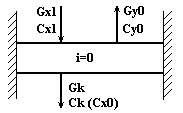
Рис.2.
Тепловой баланс низа колонны ( н = 0 ).
Уравнение динамики:
![]() (5).
(5).
Уравнение статики:
Gгр rгр + Gх1 Cрх1х1 = Gy0 rk + GkCpkн (6).
На основании (5) и (6) можно считать:
н = f (Gгр, Gк ).
Предпочтительное управляющее воздействие Gгр .
Материальный баланс по всему веществу.
Уравнение динамики :
![]() (1).
(1).
Уравнение статики :
G x1 = G k + G y0 (2),
где ρ k - плотность кубовой жидкости , кг/м3;
S k - сечение куба колонны, м2 ;
h k - уровень кубовой жидкости, м;
G x1 , G k , G y0 - массовые расходы потоков в кубе колонны.
На основании (1) и (2) можно считать:
h k = f(G k ,G y0 ).
Предпочтительное управляющее воздействие Gk .
Материальный баланс по легколетучему компоненту.Уравнение динамики:
![]() (3).
(3).
Уравнение статики:
G x1 C x1 = G k C к + G y0 C y0 (4)
Основные допущения:
Кипятильник с полным испарением, т.е. C y0=C x0;
Тепловой баланс кипятильника:
![]()
Обозначения:
М0 - масса жидкости в нижней части колонны, кг;
r гр - удельная теплота конденсации пара, дж/кг;
r k - удельная теплота испарения кубовой жидкости, дж/кг.
На основании (3) и (4) можно записать:
![]() .
.
Предпочтительное управляющее воздействие Gгр .
Информационная схема низа колонны.
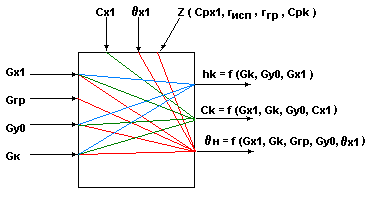
Рис.3.
Информационная схема низа колонны
как многосвязного объекта по hk,
![]() или hk,
Ck
.
или hk,
Ck
.
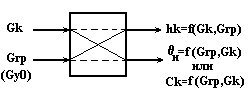
Рис.4
Математическое описание верха колонны.
Структурная схема дефлегматора с флегмовой емкостью.
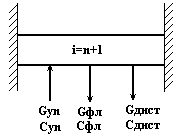
Рис.5.
Материальный баланс по всему веществу.Уравнение динамики:
![]() (7)
(7)
где фл - плотность флегмы , кг/м3 ;
Sфл - сечение флегмовой емкости , м2 ;
hфл - уровень флегмы , м;
Gyn, Gфл, Gдист - массовые расходы, кг/с.
Уравнение статики:
Gyn = Gфл + Gдист (8).
На основании (7) и (8) можно считать:
hфл=f(Gyn, Gфл, Gд )
Предпочтительное управляющее воздействие Gдист .
Материальный баланс по целевому компоненту.
Уравнение динамики:
![]() (9).
(9).
Уравнение статики:
Gyn Cyn = Gдист Cx n+1 + Gфл Cx n+1 (10).
На основании (9) и (10) можно считать:
Cдист=f(Gyn, Gфл, Gд )
Предпочтительное управляющее воздействие Gфл .
Тепловой баланс верха колонны ( в = н ).Структурная схема n–ой тарелки
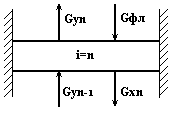
Рис.6.
Уравнение динамики:
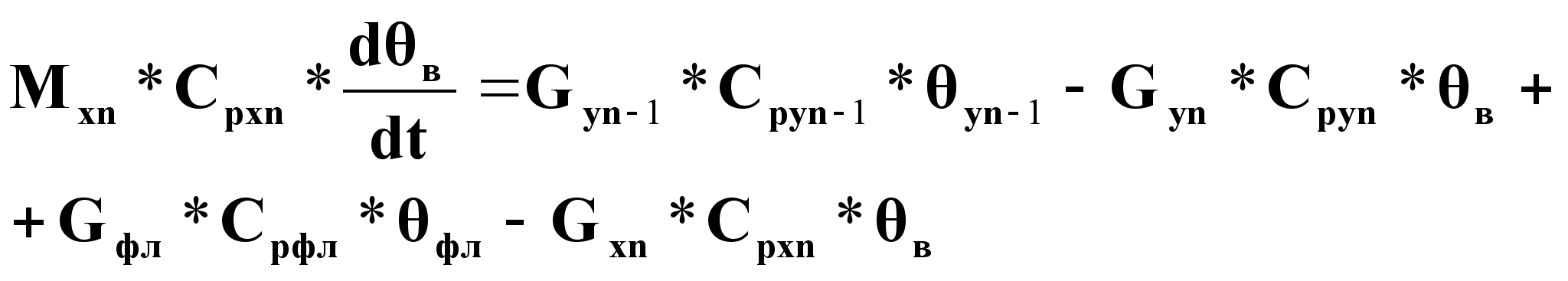 (11).
(11).
Уравнение статики:
Gyn-1*Cpyn-1 *yn-1 + Gфл*Cрфл *фл =
Gyn *Cpyn *в + Gxn *Cpxn *в (12).
Обозначения:
Мxn- масса паровой фазы наверху колонны;
Cpyn, Cpy,n-1, Cрфл, Cpxn - удельные теплоемкости паровой и жидкой фазы на n-ой тарелке;
Gyn-1, Gyn, Gxn - расходы паровой и жидкой фазы на n-ой тарелке.
На основании (11) и (12) можно считать:![]()
Предпочтительное управляющее воздействие Gфл .
Баланс по паровой фазе.Структурная схема конденсатора без флегмовой емкости.
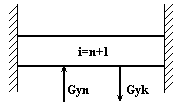
Рис.7
Уравнение динамики:
![]() (13).
(13).
Уравнение статики:
![]() (14).
(14).
Особенности:
Решение уравнения динамики для pв дает выражение для интегрального звена.
Если учесть выражение Gyn = f (pв ), то звено получается апериодическим 1 порядка.
Gyк = f (Gхл ), можно получить на основании теплового баланса конденсатора:
![]() . (15).
. (15).
На основании (13), (14) и (15) можно принять:Pв =f(Gхл).
Информационная схема верха колонны.
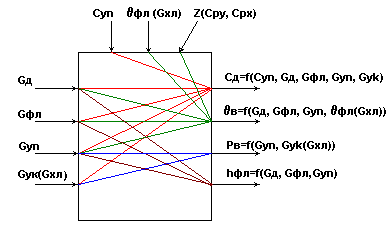
Рис.8.
Информационная схема верха колонны как многосвязного объекта по в и pв
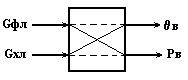
Рис.9а.
Информационная схема верха колонны как многосвязного объекта по hфл и в
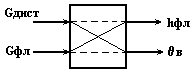
Рис.9б.
Информационная схема колонны как многосвязного объекта по в и н.
Рис.9в.
Математическое описание подогревателя потока питания.
Тепловой баланс
Уравнение динамики.
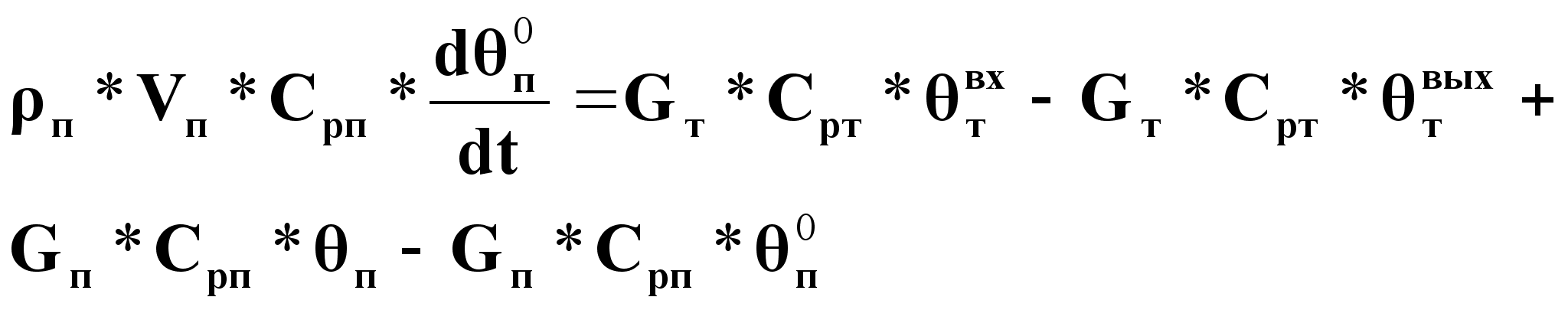 (16).
(16).
Уравнение статики.
Gт Cрт твх - Gт Cрт твых = Gп Cpп n0 - Gп Cpп n , (17)
Обозначения:
твх ,твых , n0 ,n– температуры потоков теплоносителя и питания на входе и выходе из теплообменника;
Vn - объем потока питания в трубах теплообменника;
Cpп, Срт - удельные теплоемкости потоков питания и теплоносителя;
Gт, Gп - массовые расходы теплоносителя и питания, кг/ч.
На основании (16) и (17) можно считать:
![]() .
.
Предпочтительное управляющее воздействие Gт.
Информационная схема подогревателя потока питания
как объекта управления п0
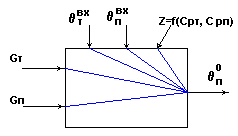
Рис.10.
Типовая схема автоматизации процесса ректификации.
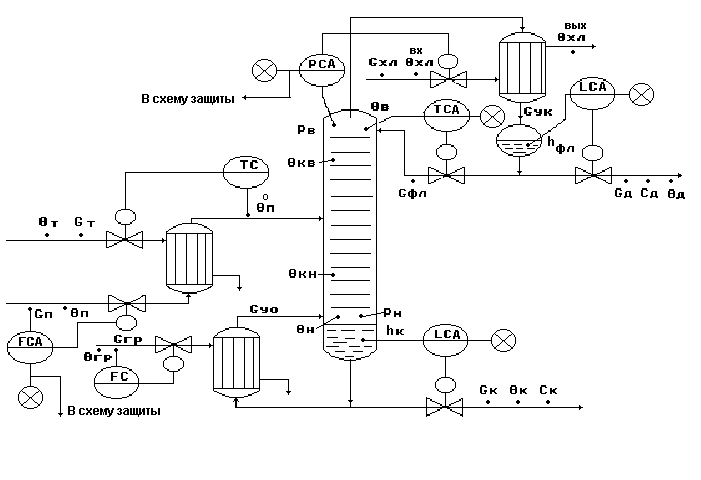
Рис.11.
Типовое решение автоматизации
процесса ректификации.
Регулирование.
Регулирование θв=f(cд) по подаче флегмы - косвенное регулирование показателя эффективности процесса cд.
Регулирование Pв по подаче хладоагента Gхл - обеспечивает материальный баланс по паровой фазе.
Регулирование hфл по отбору флегмы Gфл - обеспечивает материальный баланс по жидкой фазе верха колонны.
Регулирование hк по отбору кубового продукта Gк - обеспечивает материальный баланс по жидкой фазе низа колонны.
Стабилизация расхода питания Gп - обеспечивает:
материальный баланс по всему веществу,
снятие наиболее существенных возмущений,
заданное положение рабочей области колонны;
стабилизацию производительности установки.
Стабилизация расхода греющего пара Gгр - обеспечивает:
тепловой баланс установки;
стабилизацию Gy0 .
Регулирование θп0по подаче Gт обеспечивает:
заданное положение рабочей линии;
эффективность процесса разделения;
тепловой баланс
Контроль.
Температуры и расходы всех исходных потоков.
Температуры - θв, θн, θкв, θкн, θп0.
Давление - Рв, Рн.
Уровень - hфл, hк.
Концентрации - сд или ск .
Сигнализация.
существенные отклонения hфл, hк, θв от заданий:
повышение ![]() ;
;
резкое
снижение или
прекращение
подачи потока
питания ![]() .
.
7. Материалы к лекции №15
Автоматизация реакторных процессов (ч.1)
Упрощенная структурная схема химического реактора.
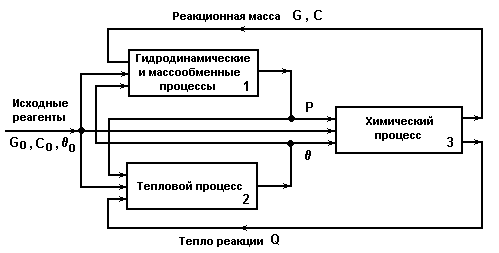
Рис.1.1.
Химический процесс (3) определяется:
уравнениями кинетики
взаимодействием гидродинамических, массообменных и тепловых процессов в аппарате,
от которых зависят концентрации реагентов, температура и давление Р реакторного процесса.
Химические превращения (3) приводят к изменению тепловых (2) и гидродинамических процессов (1) в реакторе.
Определение характера процессов, протекающих в реакторе, на основе анализа соотношения между скоростью химической реакции r и скоростью материального обмена rобм.
При ![]() :
:
процесс идет в кинетической области;
скорость процесса определяет химическое взаимодействие;
массообмен не влияет на скорость химической реакции.
При ![]() :
:
процесс идет в диффузионной области;
процесс характеризуется массообменом;
определяющей стадией является транспорт реагирующих веществ.
При ![]() :
:
процесс идет в переходной области;
скорость процесса является сложной функцией реакционно-кинетических и диффузионных зависимостей.
Показатели эффективности реакторного процесса.
Степень превращения.
Степень превращения Un , представленная через мольные доли:
![]() (1а),
(1а),
где n0 - число молей компонента в исходном потоке;
n - число молей компонента в реакционной смеси.
Степень превращения Um , представленная через массовые доли:
![]() (1б),
(1б),
где m0 - масса компонента в исходном потоке;
m - масса компонента в реакционной смеси.
Факторы, влияющие на степень превращения:
и Р - температура и давление, влияют на смещение химического равновесия в реакции;
tр - продолжительность химической реакции;
С0 - концентрации исходных веществ;
подбор катализатора;
величина потока рециркуляции.
Выход продукта.
Определение выхода продукта Х:
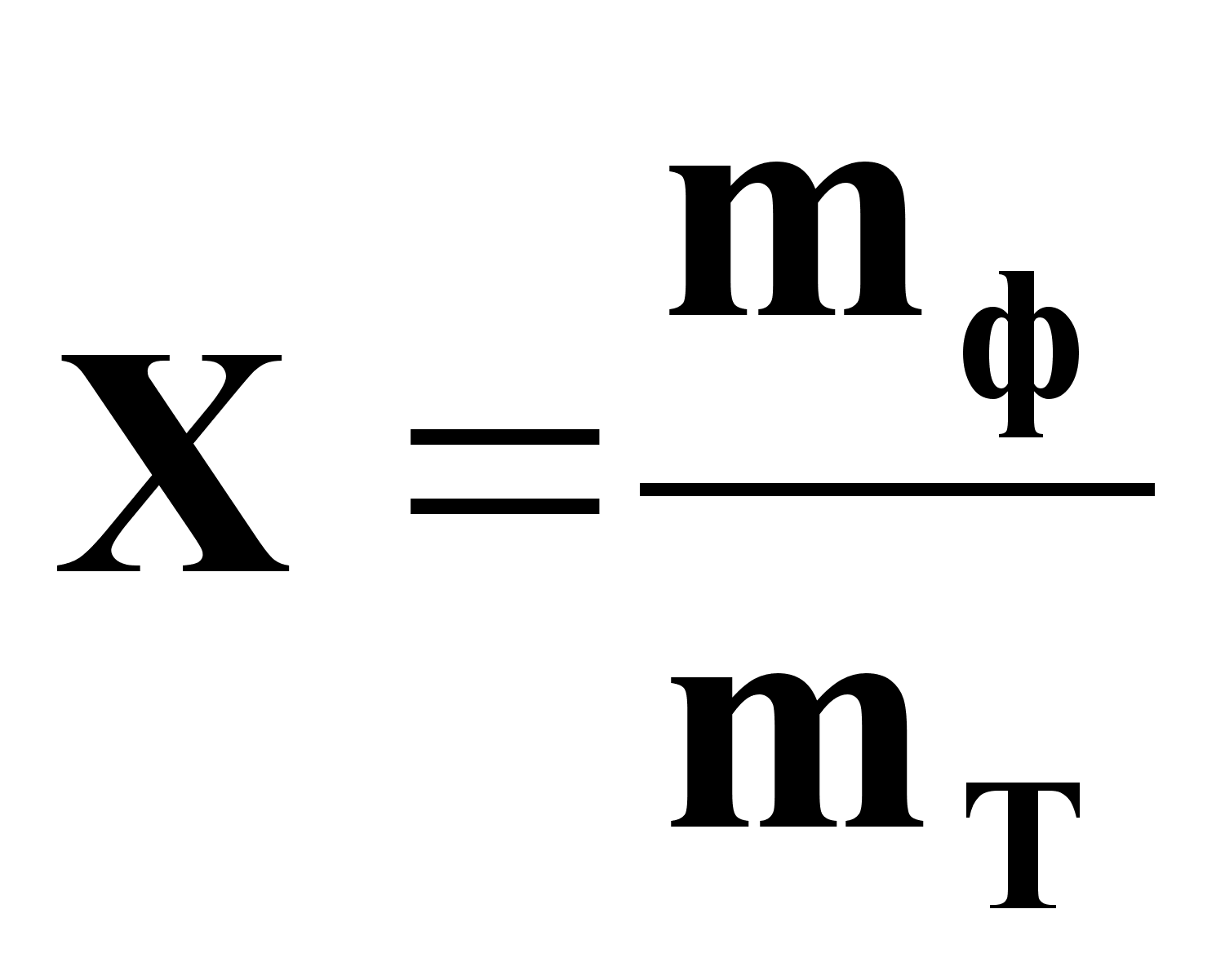 (2),
(2),
где
mф - масса фактически полученного продукта;
mт - масса теоретически возможного количества продукта из данного исходного вещества.
Факторы, влияющие на выход продукта Х:
θ - температура;
Р - давление;
Сi - состав реакционной смеси;
tпр - время пребывания реакционной смеси в аппарате.
Выход продукта характеризует:
степень совершенства технологического процесса: чем ближе Х 1, тем ближе расходные коэффициенты к стехиометрическим;
экономические показатели технологического процесса: чем ближе Х 1, тем лучше экономические показатели реакторного процесса.
Избирательность химического процесса.
Избирательность химического процесса Из характеризует долю исходных веществ, превращенных в целевой продукт, по отношению к общему количеству химически превращенных исходных веществ:
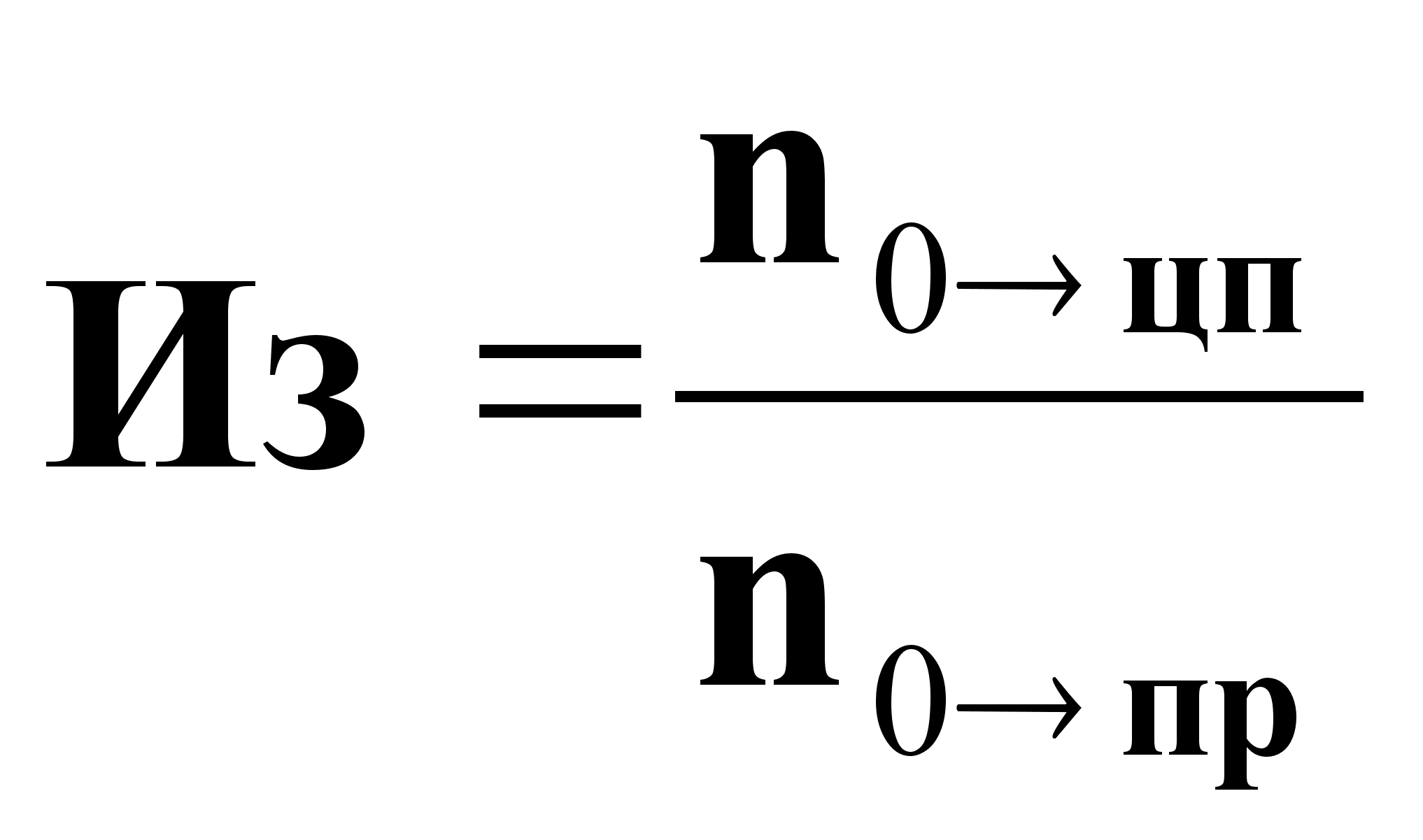 (3).
(3).
где
![]() - количество
молей исходного
продукта,
превращенных
в целевой продукт;
- количество
молей исходного
продукта,
превращенных
в целевой продукт;
![]() - количество
молей химически
превращенных
исходных веществ.
- количество
молей химически
превращенных
исходных веществ.
Избирательность влияет на экономические показатели процесса.
Скорость химического процесса.
Скорость химического процесса - это количество вещества, которое реагирует или образуется в единицу времени в единице объема (или на единице поверхности):
![]() (4),
(4),
где
![]() - движущая
сила процесса,
- движущая
сила процесса,
определяемая для химических реакций как произведение концентраций компонентов в степенях, равных их стехиометрическим коэффициентам;
К - константа скорости реакции,
определяемая на основании уравнения Аррениуса.
Скорость процесса характеризует производительность химического реактора.
Основные факторы, влияющие на скорость реакции:
С0 - состав исходных реагентов;
θ - температура;
Р - давление.
Схема реактора непрерывного действия с мешалкой
с экзотермической реакцией 1-го порядка А В.
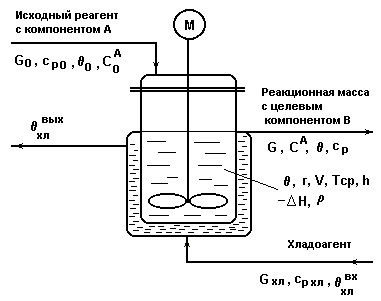
Рис.4.1.
Показатель эффективности реакторного процесса в общем случае - концентрация целевого продукта в реакционной смеси СВ .
Цель управления в общем случае:
обеспечение в реакционной смеси ![]() .
.
Цель управления для данного процесса:
обеспечение в реакционной смеси ![]() .
.
Обозначения на рис.4.1:
G0 , G , Gхл - массовые расходы исходного реагента, реакционной смеси и хладоагента, кг/с;
cp0 , cp , cpхл - удельные теплоемкости соответствующих потоков, дж/(кг*град);
- плотность реакционной смеси, кг/м3 ;
0 , , хл - температуры исходного реагента, реакционной смеси и хладоагента;
![]() - концентрации компонента А в исходном реагенте и реакционной смеси, кг/кг;
- концентрации компонента А в исходном реагенте и реакционной смеси, кг/кг;
V - объем реакционной смеси, м3 ;
h - уровень реакционной смеси, м;
Tср - среднее время пребывания реакционной массы в реакторе; 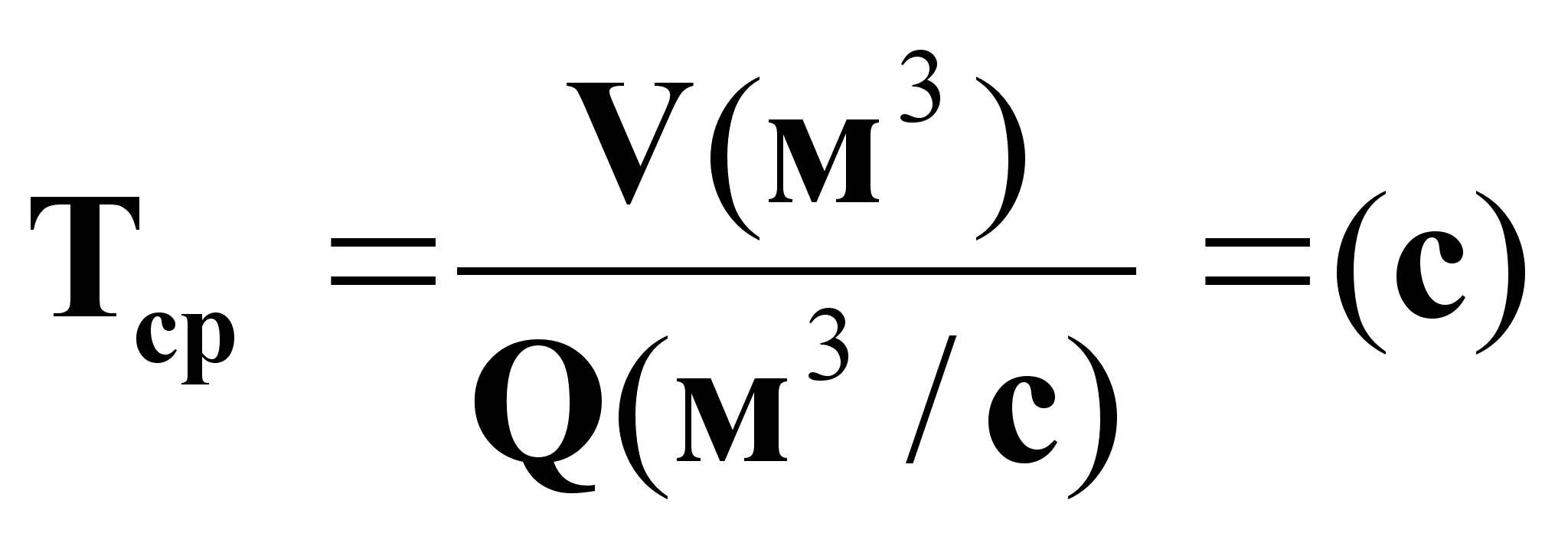
-H - тепловой эффект экзотермической реакции, дж/кг;
r - скорость химической реакции, кг/(м3*с).
Математическое описание реактора
на основе физико-химических особенностей процесса.
Стехиометрическое уравнение химической реакции.
Стехиометрическое уравнение химической реакции, характеризующее ее материальный баланс:
![]() (1а).
(1а).
Стехиометрическое уравнение для данного реактора:
![]() (1б),
(1б),
где i , i , , - стехиометрические коэффициенты, числа реагирующих молей компонентов процесса.
Уравнение кинетики химической реакции.
Результирующая скорость обратимой реакции:
![]() (2),
(2),
где
![]() - общий
порядок реакции;
- общий
порядок реакции;
![]() - скорость
прямой реакции;
- скорость
прямой реакции;
![]() - скорость
обратной реакции;
- скорость
обратной реакции;
![]() ;
;
![]() - константы
скорости,
- константы
скорости,
ZА и ZВ - эмпирические коэффициенты;
ЕА и ЕВ - энергии активации.
Кинетика для реактора типа рис.4.1:
скорость прямого процесса:
![]() (3а);
(3а);
скорость обратного процесса:
![]() (3б).
(3б).
Уравнение гидродинамики процесса.
Уравнение гидродинамики процесса характеризует давление в потоке как сложную функцию:
![]() (4)
(4)
где
x, z - координаты потока;
- ламинарная вязкость, характеризующая силы внутреннего трения;
k - турбулентная вязкость;
- плотность реакционной массы;
V - объем реакционной массы;
t - текущее время.
Материальный баланс реакторного процесса
по всему веществу.
Уравнение динамики:
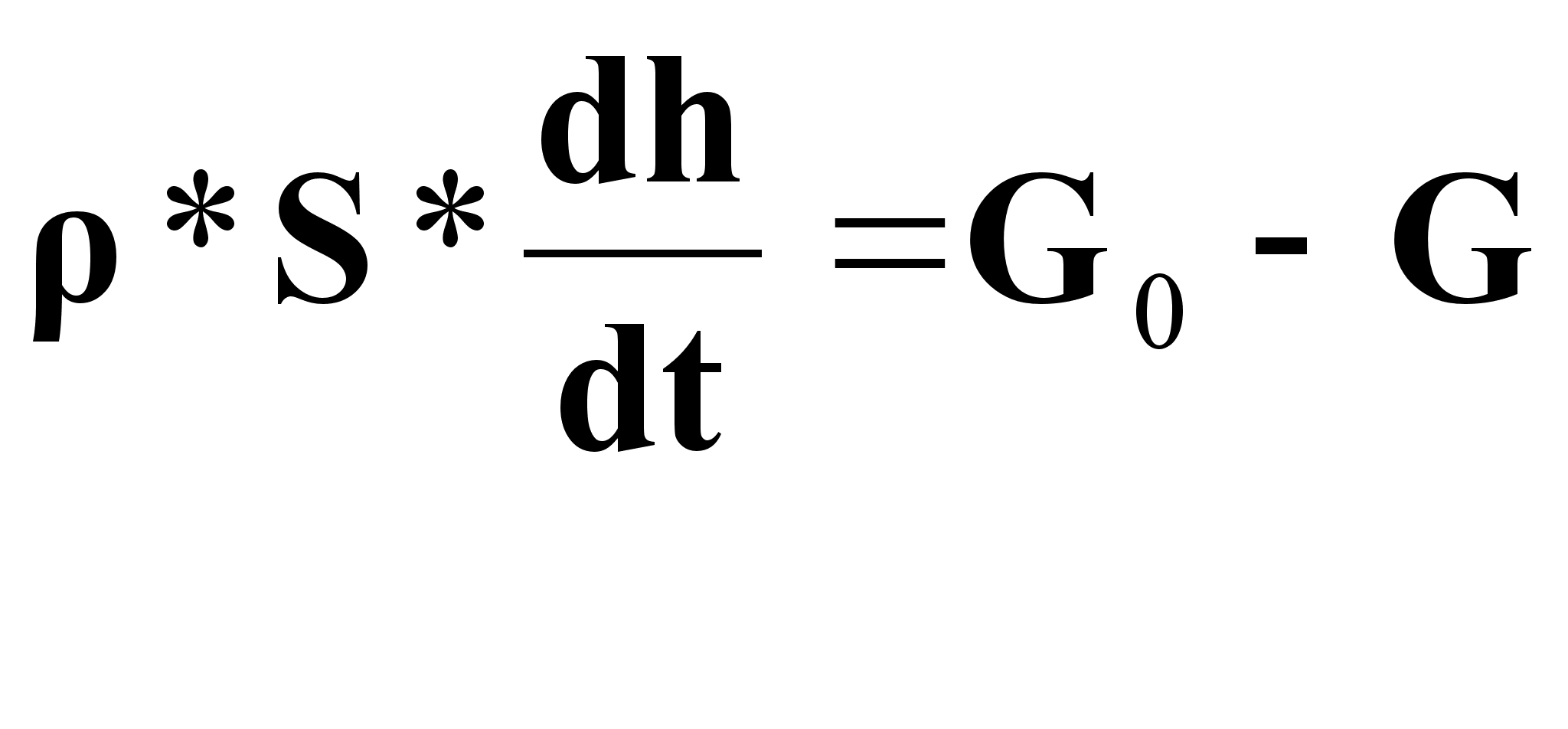 (1),
(1),
где
Уравнение
статики при
![]() :
:
![]() (2).
(2).
На основе(1) и (2):
![]() (3).
(3).
Материальный баланс реакторного процесса
по расходуемому веществу А.
Уравнение динамики:
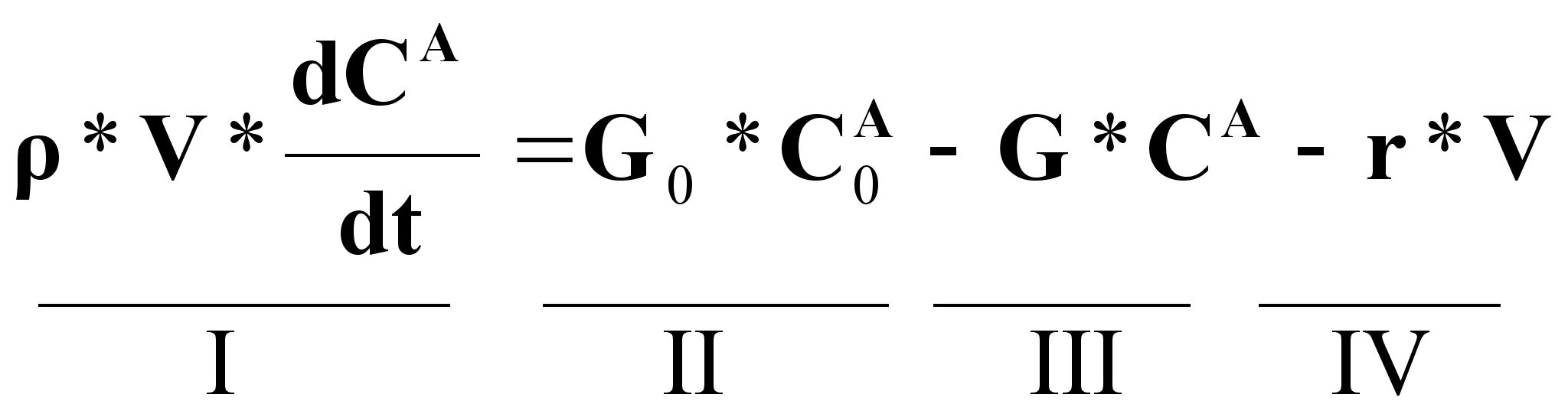 (4),
(4),
где
I - изменение количества вещества А в реакторе в единицу времени;
II - количество вещества А, поступающего в реактор в единицу времени;
III - количество вещества А, отводимого из реактора в единицу времени;
IV - количество вещества А, расходующегося в реакторе на химическую реакцию в единицу времени, где V=S*h.
Уравнение
статики при
![]() :
:
![]() (5).
(5).
На основе (4) и (5):
![]() (6).
(6).
Тепловой баланс реакторного процесса.
Уравнение динамики:
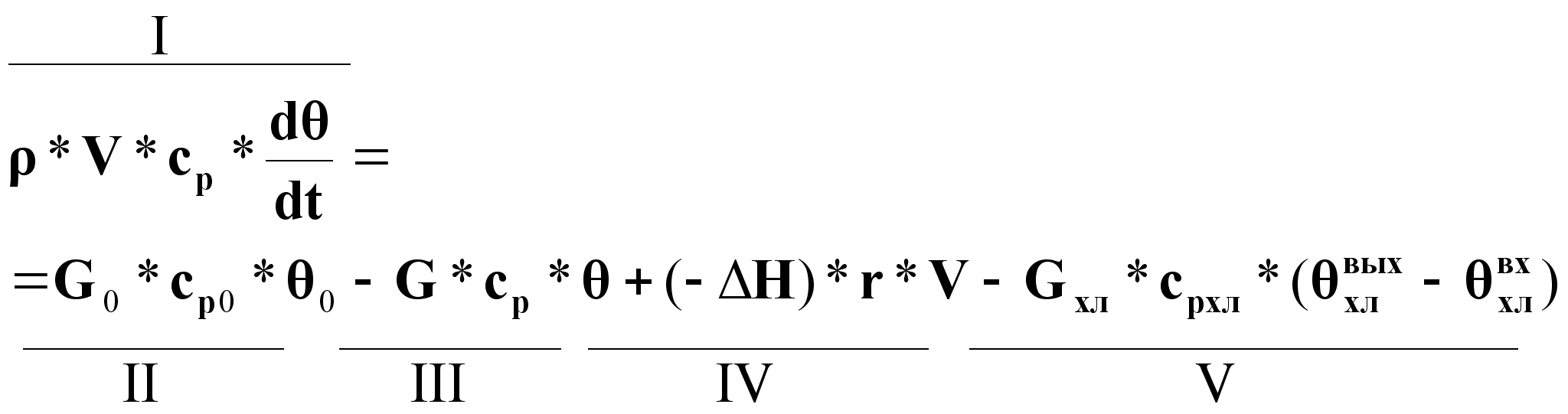 (7),
(7),
где
I - изменение количества тепла в реакторе в единицу времени;
II - количество тепла, поступающего в реактор с исходным реагентом в единицу времени;
III - количество тепла, отводимого из реактора с реакционной массой в единицу времени;
IV - количество тепла, выделяющегося в реакторе в результате химической реакции в единицу времени;
V - количество тепла, отводимого из реактора с хладоагентом в единицу времени.
Уравнение
статики при
![]() :
:
![]() (8).
(8).
На основании (7) и (8):
![]() (9).
(9).
Информационная схема реактора на основе балансовой модели.
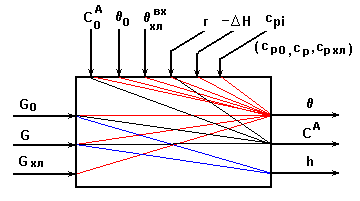
Рис.6.1.
Возможные управляемые переменные: ![]() .
.
Возможные управляющие воздействия: ![]() .
.
Возможные контролируемые возмущения: ![]() .
.
Возможные неконтролируемые возмущения: ![]() .
.
Автоматизация реакторных процессов (ч.2)
Диаграмма
![]()
реакторного процесса в адиабатическом режиме.
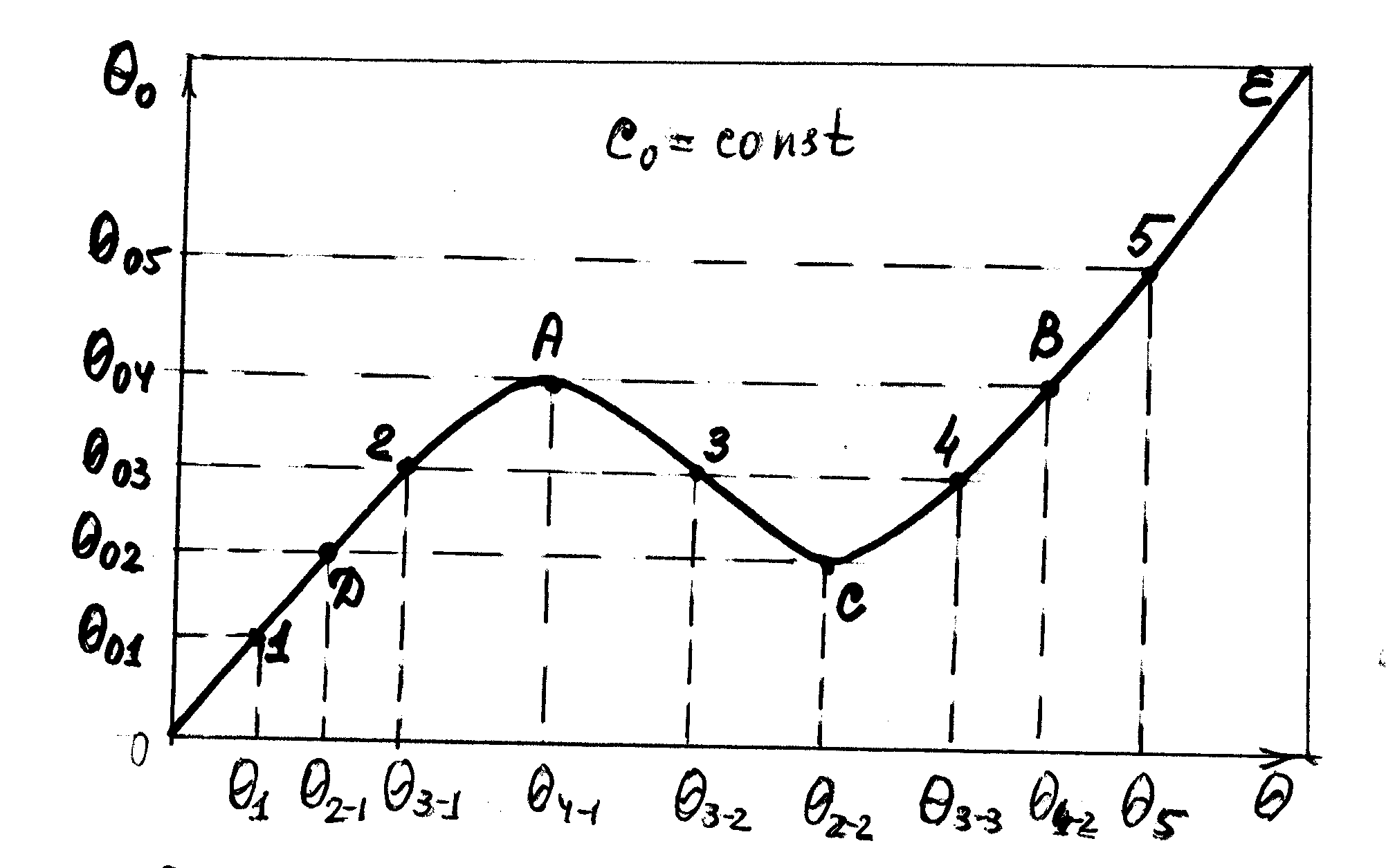
Рис.1.1.
Влияние изменения температуры 0 на температуру реакторного процесса .При изменении входной температуры 0 в пределах от 02 до 04 работа реактора осуществляется по петле гистерезиса D-A-B-C-D.
Участок статической характеристики А-3-С - путем изменения входной температуры не реализуется.
Возможные стационарные состояния реактора.
При 01 - одно устойчивое состояние в ()1, но температура в реакторе низкая и реакция идет слабо.
При 02 - два стационарных состояния в ()D и ()С:
()D - устойчивое состояние, но при низкой температуре;
()С - неустойчивое состояние с возвратом в ()D при уменьшении начальной температуры.
При 03-три стационарных состояния в ()2, ()3, ()4:
()2 - устойчивое состояние, но с низкой скоростью реакции;
()4 - устойчивое состояние, почти полное превращение реагентов, но реакция идет с высокой температурой – вне рабочего диапазона;
()3 - изменением начальной температуры не реализуется.
При 04 - два стационарных состояния в ()А и ()В:
()А - неустойчивое состояние, с проскоком в ()В при увеличении начальной температуры;
()В - устойчивое состояние, почти полное превращение реагентов, но реакция идет с высокой температурой – вне рабочего диапазона.
При 05 - одно устойчивое состояние в ()5, но температура в реакторе вне рабочего диапазона.
Зависимость
статической
характеристики
![]()
от концентрации С0 исходного реагента.
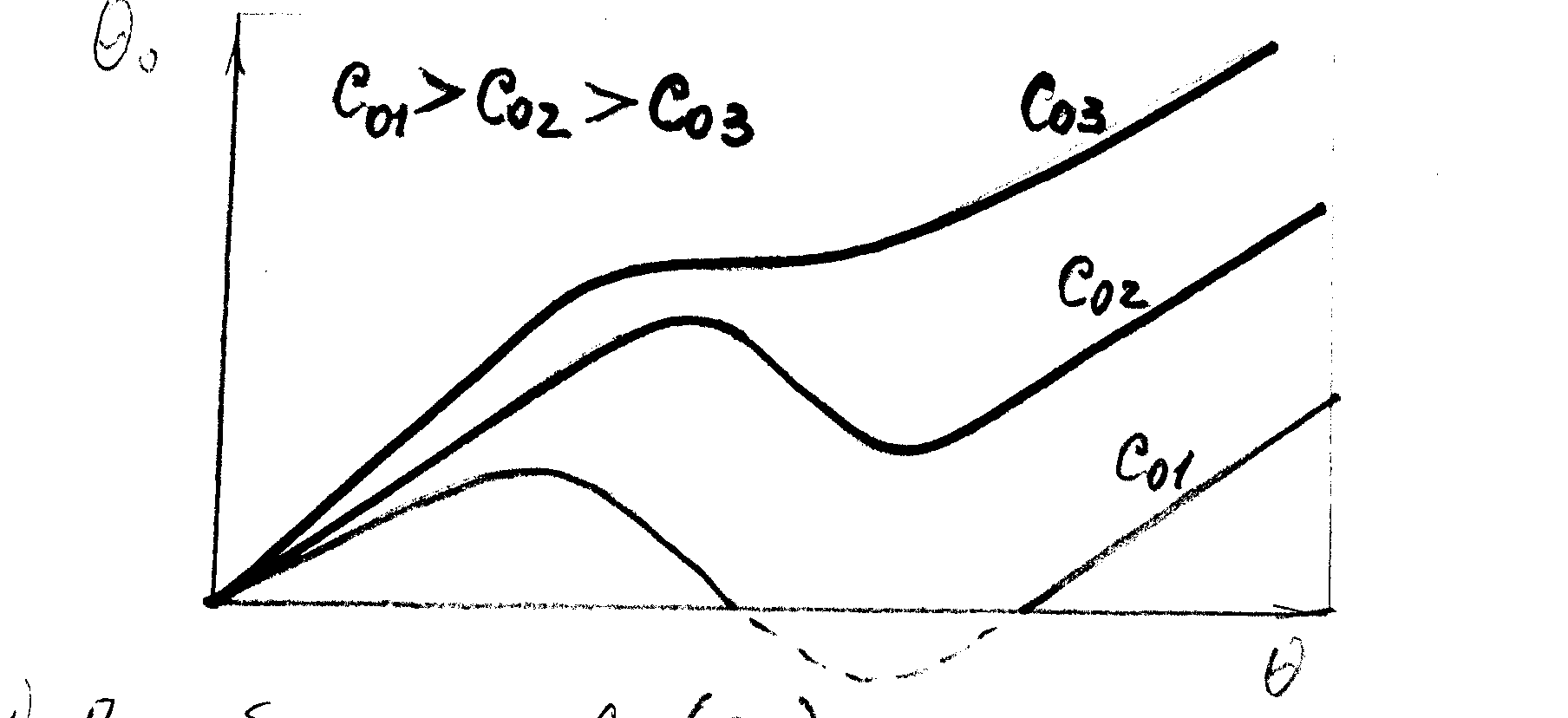
Рис.1.2.
При больших значениях С0 (С01 ) - статическая характеристика неоднозначна даже при низких температурах.
Единственность стационарного состояния возможна только при высоких значениях 0 .
Область отрицательных значений 0 практического смысла не имеет, поэтому показана пунктиром.
Уменьшение входных концентраций (С02 и С03) вызывает смещение неоднозначности статической характеристики в область более высоких температур.
Зависимость статической характеристики

Рис.1.2.
При больших значениях С0 (С01) - статическая характеристика неоднозначна даже при низких температурах.
Единственность стационарного состояния возможна только при высоких значениях 0 .
Область отрицательных значений 0 практического смысла не имеет, поэтому показана пунктиром.
Уменьшение входных концентраций (С02 и С03) вызывает смещение неоднозначности статической характеристики в область более высоких температур.
Определение стационарных состояний
по диаграмме «выделения – отвода тепла».
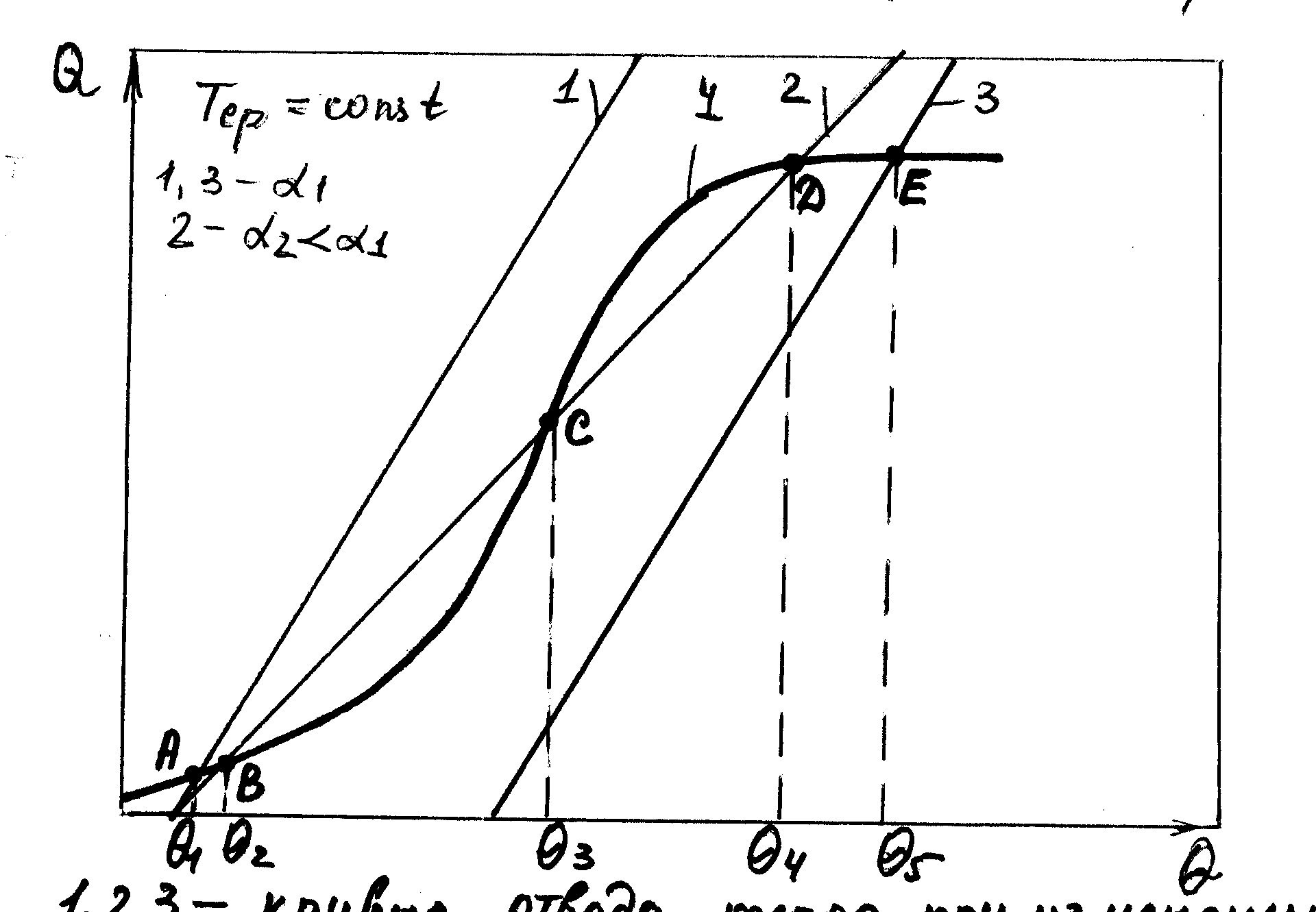
Рис.2.1.
1, 2, 3 - кривые отвода тепла Q при изменении температуры в реакторе c различными значениями коэффициента теплопередачи : 1 = 3 и 2 < 1,3.
4 - кривая выделения тепла ![]() .
.
Система 1-4:
одно стационарное состояние в ()А;
очень низкая температура в реакторе 1 ;
низкая скорость реакции.
Система 3-4:
одно стационарное состояние в ()Е;
практически полное превращение реагента;
очень высокая температура 5 , которая может быть вне рабочей зоны реактора.
Система 2-4:
три стационарных состояния в ()В, С, D;
()В - очень низкая температура в реакторе 2; низкая скорость реакции; стационарное состояние устойчивое;
()D - практически полное превращение реагента; но очень высокая температура 4 , которая может быть вне рабочей зоны реактора; стационарное состояние устойчивое;
()С - температура в рабочей зоне реактора 3; но стационарное состояние - неустойчивое.
Зависимость характеристики выделения тепла
от времени пребывания реакционной массы в реакторе.
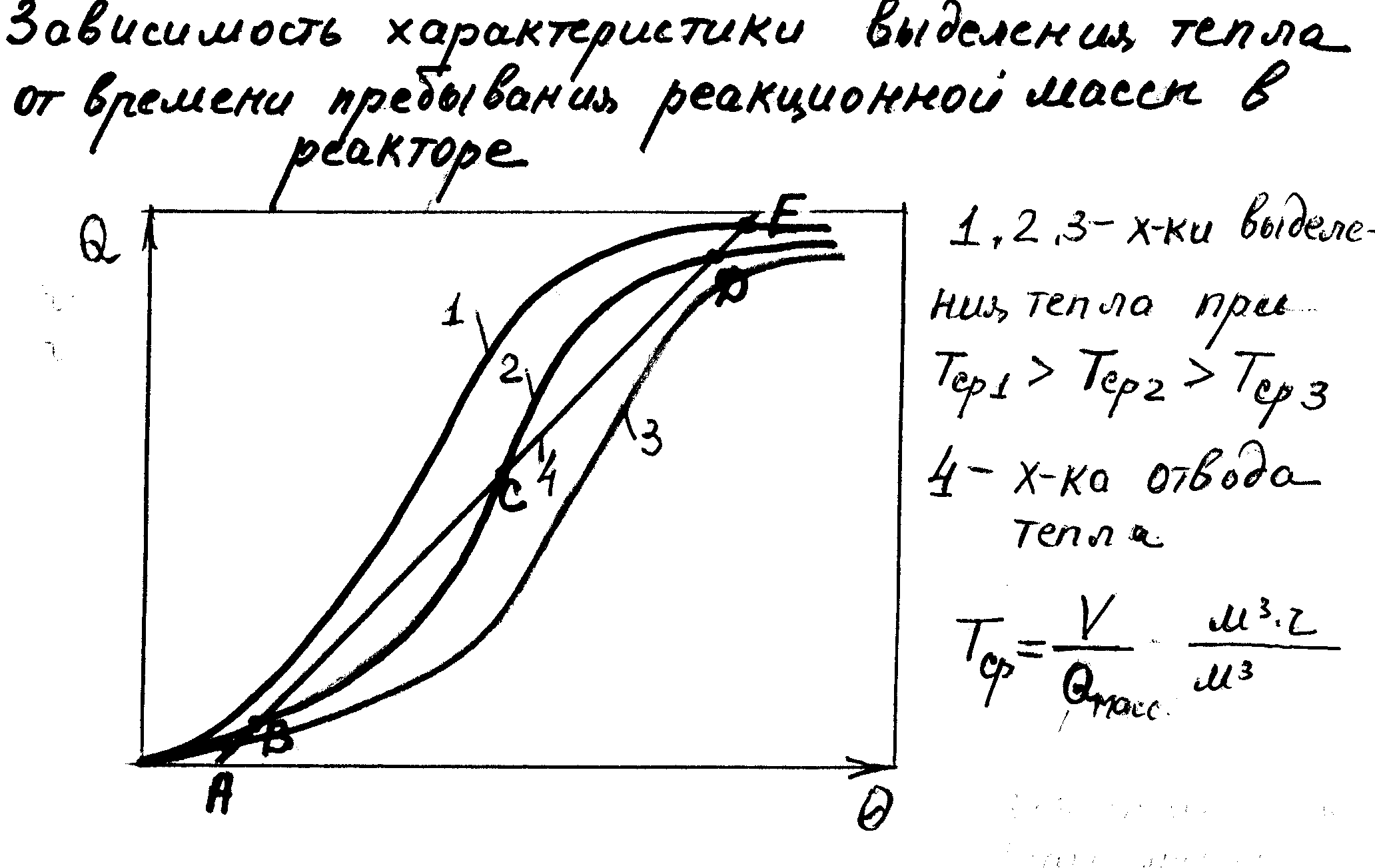
Рис.2.2.
1, 2, 3 - характеристики выделения тепла при Тср1 > Тср2 > Тср3 .
4 - характеристика отвода тепла.
Среднее время пребывания определяется по соотношению: 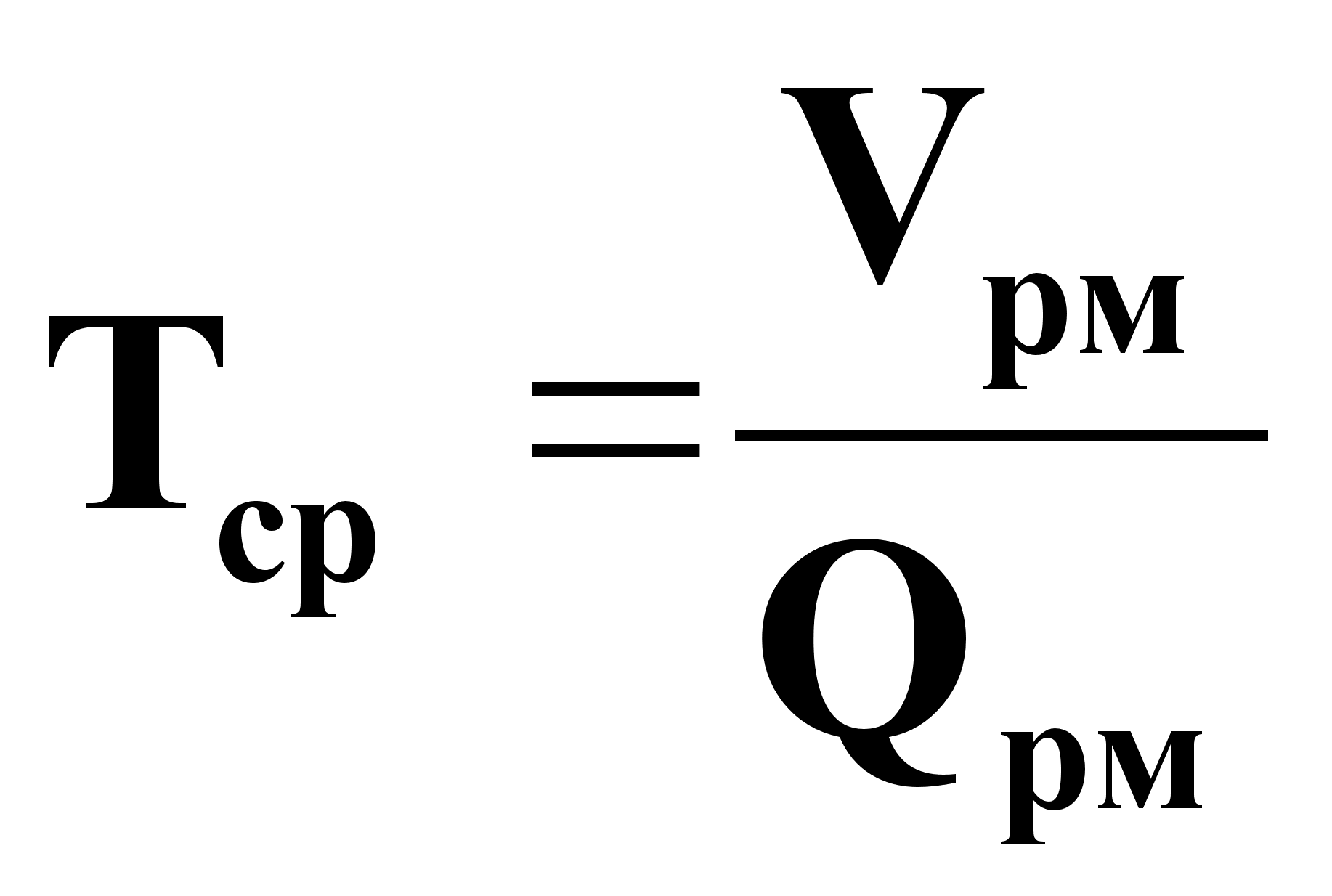 , где Vрм и Qрм - объем и объемный расход реакционной массы.
, где Vрм и Qрм - объем и объемный расход реакционной массы.
При увеличении времени пребывания характеристика выделения тепла смещается влево.
Система 1-4:
одно устойчивое стационарное состояние в ()Е;
практически полное превращение реагента;
но очень высокая температура, которая может быть вне рабочей зоны реактора;
Система 3-4.
одно устойчивое стационарное состояние в ()А;
очень низкая температура в реакторе;
низкая скорость реакции.
Система 2-4.
три стационарных состояния в ()В , D и С;
()В - очень низкая температура в реакторе; низкая скорость реакции, стационарное состояние устойчивое;
()D - практически полное превращение реагента; но очень высокая температура, которая может быть вне рабочей зоны реактора; стационарное состояние устойчивое;
()С - температура в рабочей зоне реактора; но стационарное состояние - неустойчивое.
Оценка устойчивости стационарных состояний
по диаграмме «выделения – отвода тепла».
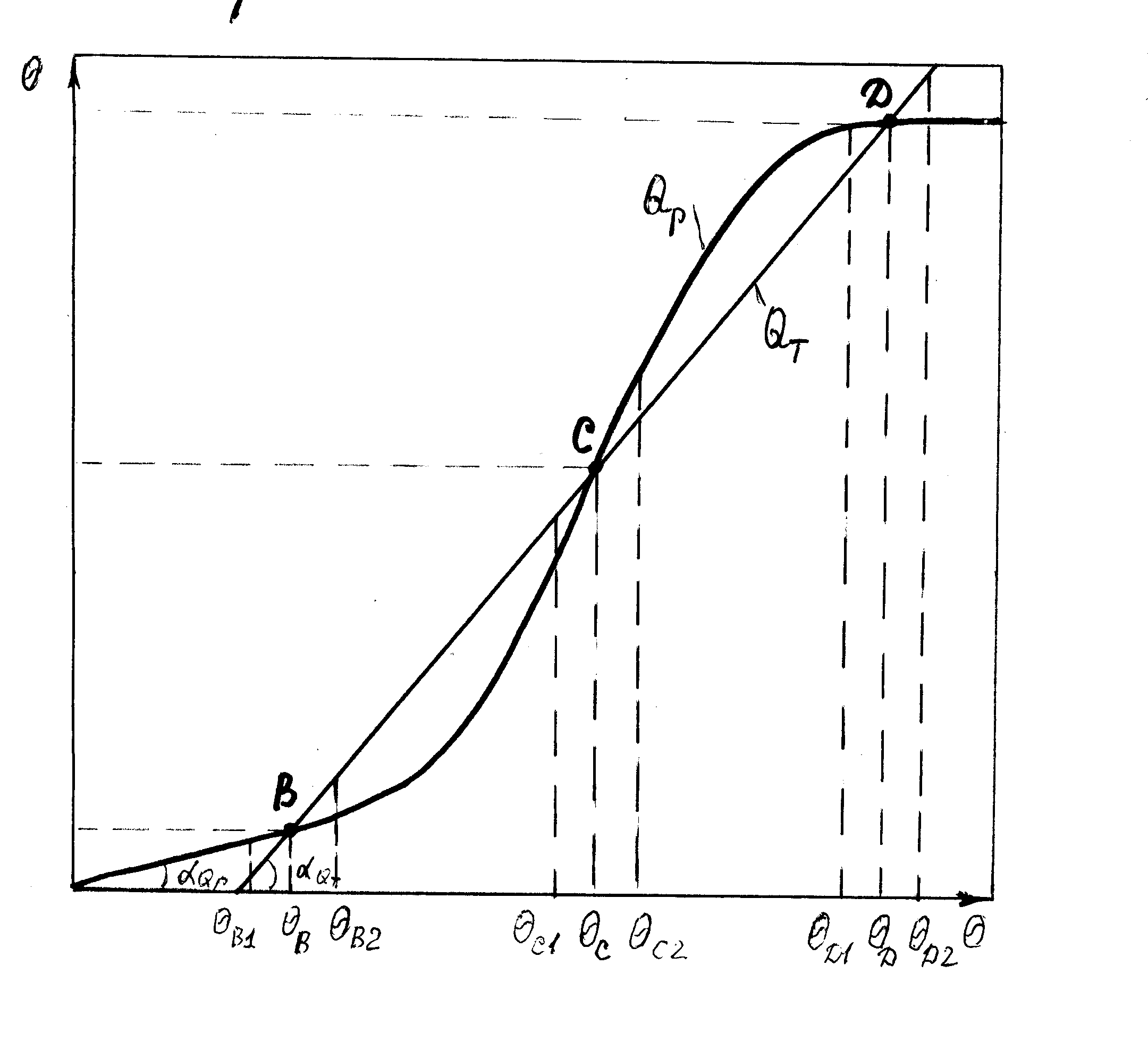
Qр = f() - характеристика выделения тепла реакции;
Qт = f() - характеристика отвода тепла.
Рис.2.3.
Устойчивость реактора в стационарном состоянии В:
при ![]() ;
;
при ![]() ;
;
стационарное состояние в ()В - устойчивое.
Устойчивость реактора в стационарном состоянии D:
при ![]() ;
;
при ![]() ;
;
стационарное состояние в ()D - устойчивое.
Устойчивость реактора в стационарном состоянии C:
при ![]() переход в()D;
переход в()D;
при ![]() переход в ()В;
переход в ()В;
стационарное состояние в ()С - неустойчивое.
9. Материалы к лекции №17Автоматизация реакторных процессов (ч.3).
Схема для реакции типа А(ж) + В (г) D (г-ц.пр)+С (ж).
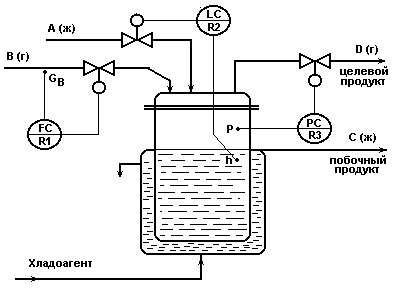
Рис.1.1.
Схема для реакции типа А(ж) + В (г) D (г)+С (ж-ц.пр).
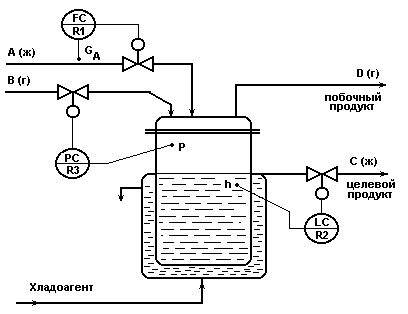
Рис.1.2.
Схема автоматизации для реакции типа
А(ж) + В{Всв(ж) + Врец(ж)} С(ж- ц.пр)+В(ж).
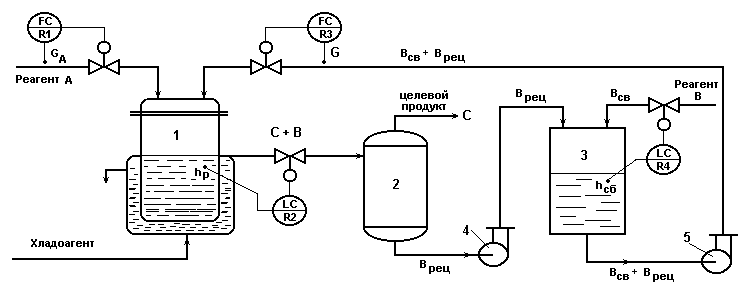
1- реактор; 2 - сепаратор; 3 - сборник; 4, 5 - насосы;
А, В - исходные реагенты; С - целевой продукт; Врц - возвратный (рецикловый) поток реагента В; Всв - свежий поток реагента В.
Рис.1.3.
Система регулирования концентрации
из двух одноконтурных АСР.
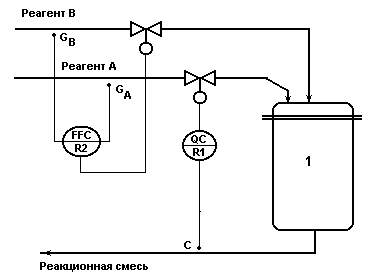
Рис.1.5.
Каскадная АСР концентрации со вспомогательным контуром
стабилизации соотношения расходов исходных реагентов.
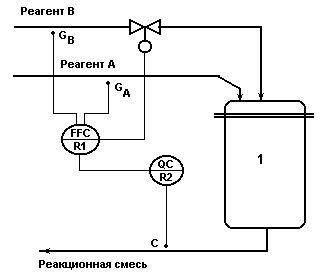
Рис.1.6.
Каскадная АСР концентрации со вспомогательным контуром
стабилизации температуры исходного реагента.
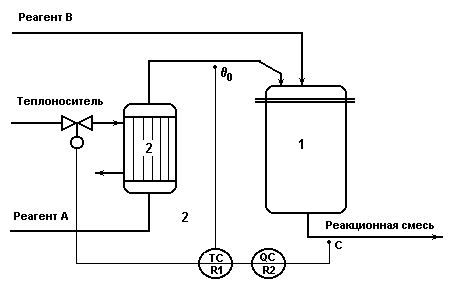
Рис.1.7.
Каскадная АСР концентрации со вспомогательным контуром
стабилизации температуры хладоагента.
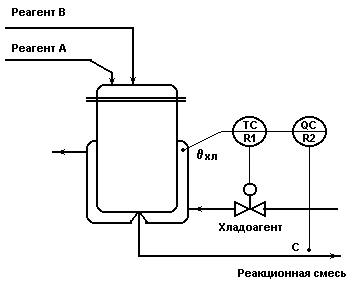
Рис.1.8.
Одноконтурная АСР температуры в реакторе
по подаче исходного реагента.
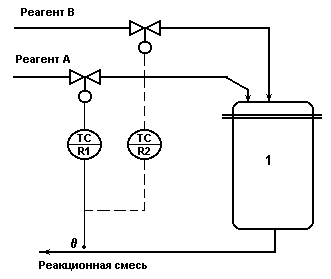
Рис.2.1.
Каскадная АСР температуры в реакторе со вспомогательным контуром
стабилизации температуры исходного реагента.
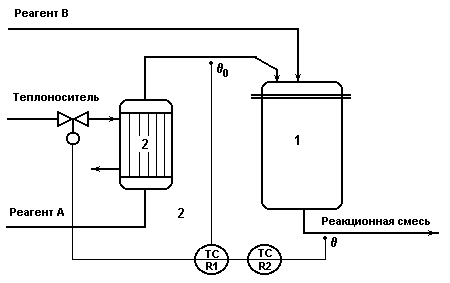
Рис.2.2.
Каскадная АСР температуры в реакторе со вспомогательным контуром
стабилизации температуры хладоагента.
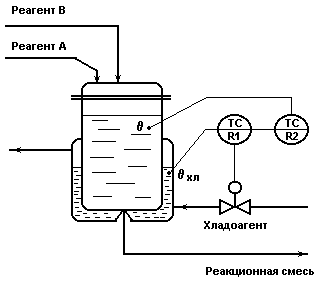
Рис.2.3.
Каскадная АСР температуры в реакторе со вспомогательным контуром
стабилизации давления хладоагента.
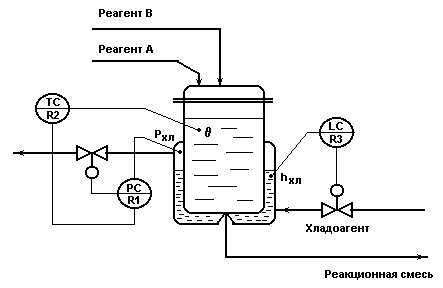
Рис.2.4.
10. Рекомендуемая литератураОсновная литература
1. Дудников Е.Г. Автоматическое управление в химической промышленности. - М.: Химия, 1987.- 368 с.
2. Полоцкий Л.М., Лапшенков Г.И. Автоматизация химических производств. - М.: Химия, 1982.- 295 с.
3. Автоматизация технологических процессов легкой промышленности: Учеб пособие для вузов по спец. «Автоматизация технологических процессов и производств» / Под ред. Л.Н. Плужникова. - 2-е изд., перераб. и доп. - М.: Легпромбытиздат, 1984.- 366с.
4. Мамиконов А.Г. Проектирование АСУ.- М.: Высшая школа, 1987.- 303 с.
5. Стефани Е.П. Основы построения АСУ ТП.- М.: Энергоиздат, 1982.- 352с.
6. Пиггот С.Г. Интегрированные АСУ химических производств. - М.: Химия, 1985.- 410 с.
7. Кафаров В.В., Макаров В.В. Гибкие автоматизированные системы в химической промышленности: Учебник для вузов. - М.: Химия, 1990.- 320с.
8. Плютто В.П. Управление химико-технологическими процессами. Процессы массообмена: [Учеб. пособие].- М.: МХТИ, 1984.-48с.
9. Плютто В.П. и др. Автоматизированные системы управления периодическими пролцессами химической технологии. – М.: МХТИ, 1985.-48с.
10. Ицкович Э.Л., Сорокин Л.Р. Оперативное управление непрерывным производством. – М..: Наука, 1989.-155с.
Дополнительная литература
11. Автоматизация технологических процессов легкой промышленности: Учеб пособие для вузов по спец. «Автоматизация технологических процессов и производств» / Под ред. Л.Н. Плужникова. - 2-е изд., перераб. и доп. - М.: Легпромбытиздат, 1993 .
12. Уланов Г.М. и др. Методы разработки интегрированных АСУ промышленными предприятиями. - М.: Энергоатомиздат, 1983.- 320 с.
13. Практикум по автоматике и системам управления производственными процессами: Учеб. пособие для вузов / Под ред. И.М. Масленникова - М.: Химия,1986.- 336 с.
14. Плютто В.П., Путинцев В.А., Глумов В.М. Практикум по теории автоматического управления химико-технологическими процессами: Цифровые системы - М.: Химия,1989.- 168 с.
15. Голубятников В.А., Шувалов В.В. Автоматизация производственных процессов в химической промышленности. - М.: Химия, 1985.-352с.
16. Шувалов В.В. Огаджанов Г.А., Голубятников В.А. Автоматизация производственных процессов в химической промышленности. - М.: Химия, 1991.-480с.
17. Процессы и аппараты химической технологии. Учебник для вузов./ Н.Н. Смирнов, М.И. Курочкина, А.И. Волжинский, В.А. Плессовских. - СПб.: Химия, 1996.-400с.
18. Математическое моделирование основных процессов химических производств. Учеб. пособие для вузов. / В.В. Кафаров, М.Б. Глебов. - М.:Высш.шк., 1991.-399с.
19. Математическое моделирование химико-технологических систем: Учеб. пособие в 3ч./ под ред Л.С. Гордеева. - М.:РХТУ, 1999- 48с.( ч1); 47с.( ч2), 67с.( ч3)
.
СОДЕРЖАНИЕ
1. Материалы к лекции №9 3
2. Материалы к лекции №10 8
3. Материалы к лекции №11 17
4. Материалы к лекции №12 25
5. Материалы к лекции №13 34
6. Материалы к лекции №14 41
7. Материалы к лекции №15 51
8. Материалы к лекции №16 59
9. Материалы к лекции №17 65
10. Рекомендуемая литература 71
Похожие работы
... решить только на основе широкого внедрения автоматики в производственные процессы и внедрить автоматизированные системы в различные сферы хозяйственной деятельности, и в первую очередь в проектирование, управление оборудованием и технологическими процессами. Поднять уровень автоматизации производства примерно в 2 раза. Создавать комплексно-автоматизированные производства, которые можно быстро и ...
... не только уменьшаться, например, за счет улучшения культуры производства и использования экологически более совершенного оборудования и технологий, но и увеличиваться, например, при введении новых технологических процессов, таких, как десульфуризация и денитрификация дымовых газов. Сточная вода - это вода, свойства которой изменены в результате бытовых, промышленных, сельскохозяйственных или ...
... функций можно классифицировать по следующим признакам: v по влиянию на работу объекта управления (вызвавшие аварию с повреждением оборудования, останов технологического процесса, ухудшение качества протекания технологического процесса); v по причинам возникновения (из-за отказов технических средств, ошибок программного обеспечения, неправильных действий персонала); v по степени нарушения ...
... определяется сложностью схемы и конструктивными особенностями системы управления и обычно задается в паспортных данных на систему в виде среднего времени наработки на отказ. 3. Требования безопасности к производственному оборудованию Основными требованиями безопасности, предъявляемыми к конструкции машин и механизмов, являются: безопасность для здоровья и жизни человека, надежность, ...
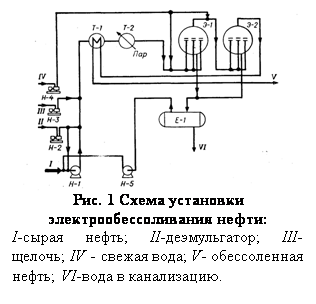
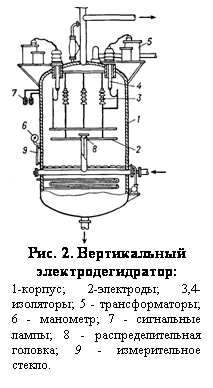
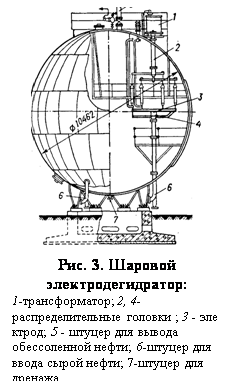
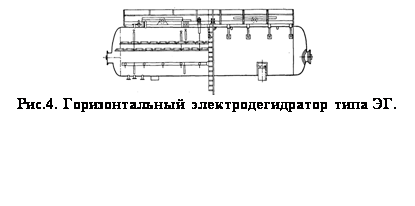

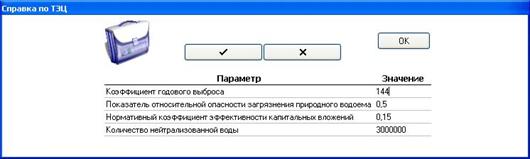
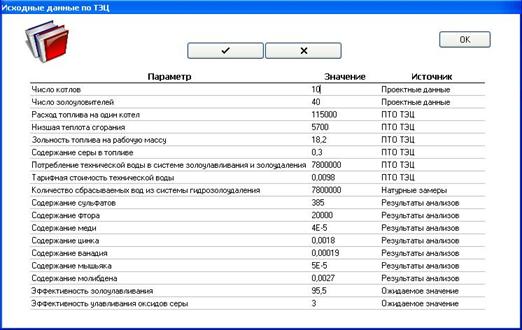
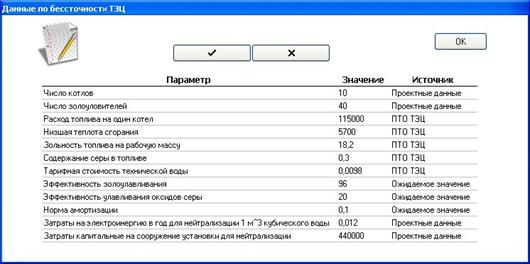




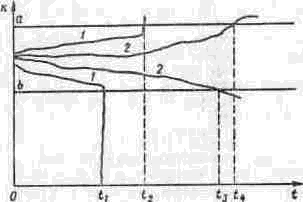
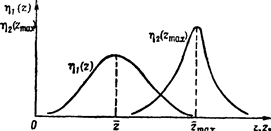

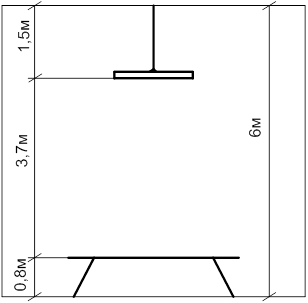
0 комментариев