Навигация
Конструкционное применение магния
2. Конструкционное применение магния.
Основное преимущество металлического магния – его легкость (магний – самый легкий из конструкционных металлов). Технически чистый магний обладает невысокой механической прочностью, однако введение в него в небольшом количестве других элементов (алюминия, цинка, марганца) может значительно улучшить его механические свойства почти без увеличения удельного веса. На основе этих свойств магния был создан знаменитый сплав “Электрон”, содержащий, помимо магния, 6% алюминия, 1% цинка и 0,5% марганца. (В настоящее время под техническим названием “электрон” понимаются вообще все сплавы, в которых магний является главной составной частью). Плотность этого сплава – 1,8 г/см3; прочность на разрыв – до 32 кГ/мм2; твердость по Бринелю – 40–55 кГ/мм2. Этот, а также многие другие сплавы на основе магния широко применялись в авиа- и автостроении. В последнее время, однако, оказалось, что эти сплавы резко изменяют свои механические свойства при повышении температуры, и они были признаны непригодными. В результате было создано множество новых сплавов, отличавшихся значительно лучшими механическими и антикоррозийными свойствами, а также повышенной жаропрочностью и способностью сохранять свои прочностные характеристики при повышении температуры. В эти сплавы вводились небольшие добавки различных элементов – циркония, тория, цинка, серебра, меди, бериллия, титана и других. Подобного рода сплавы нашли широкое применение в авиации и ракетостроении.
Кроме того, было создано большое количество разнообразных сплавов, в которых магний не является главной составной частью. Важнейшим из таких сплавов является “магналий” – сплав алюминия с 5-30% магния. Магналий тверже и прочнее чистого алюминия, легче последнего обрабатывается и полируется.
Как “магналий”, так и “электрон” на воздухе покрываются защитной окисной пленкой, предохраняющей их от дальнейшего окисления.
Введение 0,05% Mg в чугун резко повышает его ковкость и сопротивление разрыву.
Многие магниевые детали применяются в настоящее время в самых разных областях электротехники. Небольшой вес изделий, выполненных из магниевых сплавов, явился также важной причиной применения их для изготовления различных бытовых предметов и аппаратуры.
Магниевые детали очень хорошо поглощают вибрацию. Их удельная вибрационная прочность почти в 100 раз больше, чем у лучших алюминиевых сплавов, и в 20 раз больше, чем у легированной стали. Это очень важное свойство при создании разнообразных транспортных средств.
Магниевые сплавы превосходят сталь и алюминий по удельной жесткости и поэтому применяются для изготовления деталей, подвергающихся изгибающим нагрузкам (продольным и поперечным). Магниевые сплавы немагнитны, совершенно не дают искры при ударах и трении, легко обрабатываются резанием (в 6-7 раз легче, чем сталь, в 2-2,5 раза – чем алюминий).
Магний и его сплавы обладают очень высокой хладостойкостью.
Долгое время считалось, что область возможного применения магния ограничивается его легкой воспламеняемостью. Действительно, небольшие кусочки магния воспламеняются на воздухе при температуре 550оС. Однако изделия из магния и магний в слитках неогнеопасны, так как магний имеет очень высокую теплопроводность и нагреваемый участок детали быстро распространяет тепло по всей детали. Были даже попытки применения магния для изготовления двигателей внутреннего сгорания; в испытаниях он хорошо выдерживал тепло, но оказался недостаточно стоек к агрессивному воздействию продуктов сгорания. Поэтому магниевые поршни используются редко, в основном в гоночных машинах и в технике специального назначения.
Основной недостаток магния – пониженная стойкость против коррозии. Магний сравнительно устойчив в сухом атмосферном воздухе в дистиллированной воде, но быстро разрушается в воздухе, насыщенном водными парами и загрязненном примесями, в особенности сернистым газом.
Магний нестоек в очень многих веществах, так как является самым активны из конструкционных металлов. Его поверхностная активная пленка имеет пористую структуру и поэтому слабо защищает от коррозии.
Магний совершенно устойчив к плавиковой кислоте и другим соединениям фтора, так как при контакте с ним образуется слой MgF2 – прочная сплошная пленка. На этом основано применение магния для изготовления тары и насосов для перекачки плавиковой кислоты.
Магний стоек и при контакте с другими галогенами, причем, в отличие от алюминия, он спокойно переносит сухой хлор и стремительно разрушается во влажном.
На стойкости магния в броме и иоде основано применение его для изготовления резервуаров для их хранения. Кроме того, он устойчив в бензине, керосине, смазочных маслах, жирах и т.п. и из него делают емкости для хранения нефти и нефтепродуктов и бензобаки.
Поверхность магниевых сплавов защищают от коррозии нанесением слоев лака, пленкой более стойкого металла, либо электрохимической и химической обработкой, а иногда – нанесением слоев эмали.
Чем чище магний, тем он устойчивее к коррозии. Это связано с тем, что он вступает в электрохимическую реакцию с крупицами практически любых других элементов, которая разрушает из двух веществ более активное. Особенно вредоносными являются примеси железа, никеля, меди, хрома, свинца, кобальта – они способствуют коррозии магния даже в очень небольших количествах: например, предельно допустимая концентрация железа в промышленно выпускаемом магнии составляет 0,01%, никеля – 0,0005%.
С другой стороны, такие элементы, как марганец, цирконий, цинк, титан улучшают коррозионную стойкость магния: при добавлении к магниевому сплаву нескольких девятых процентов титана коррозионная стойкость увеличивается в 3 раза.
Возможности применения магния еще далеко не исчерпаны, а если учитывать широкое распространение магния в природе, относительную простоту способов его производства и ряд благоприятных свойств этого металла, можно полагать, что дальнейшее развитие металлургии магния будет в первую очередь определяться его общетехническим значением.
Биологическая роль магния
В человеческом организме количество магния составляет всего несколько десятых или сотых долей процента, однако он играет немаловажную роль в процессах жизнедеятельности. Доказано, что недостаток магния в организме способствует заболеванию инфарктом миокарда. Недостаточное количество магния в крови – признак переутомления или стрессового состояния.
Основные продукты, содержащие магний – это абрикосы, персики, цветная и белокочанная капуста, помидоры, картофель.
Потребность взрослого организма в магнии составляет 300–500 мг/день. Обычно магний в достаточном количестве поступает с пищей, в случае нехватки его недостаток проще всего восполнить, потребляя минеральную воду. В организме усваивается менее 40% поступающего в него магния, так как его соединения плохо всасываются кишечником. Магний усиливает процессы обмена углеводов в мышцах, укрепляет кости; если в организме нарушено магние-кальциевое равновесие, то почти весь магний включается в состав костных тканей, вытесняя оттуда кальций. Это ведет к заболеванию рахитом.
В нервной системе также содержатся большие количества магния, особенно в спинном мозге. Большое значения магния для деятельности нервной системы подтверждается тем, что при инъекции магния в кровь человек или животное впадает в состояние, близкое к наркотическому. Это свойство магния используется в медицине.
В организмах некоторых животных содержание магния сравнительно высоко. Так, например, в организме известковой губки содержится 4% магния, в талломе некоторых водорослей – больше 3%.
Магний входит в состав хлорофилла и, следовательно, играет незаменимую роль в фотосинтезе и в газообмене планеты; общее содержание магния в тканях растений на Земле по некоторым оценкам составляет порядка 1011 тонн.
Кроме хлорофилла, магний во всех тканях растений участвует также в образовании жиров, в превращении фосфорных соединений. Особенно много магния в соке каучуконосных растений. Нехватка магния приводит к уменьшению количества хлорофилла и к побледнению и смене окраски листьев на красную и желтую.
Магний как лекарственное средство
Английская соль (MgSO4Ч7H2O) используется как слабительное и желчегонное средство. При инъекциях она вызывает состояние, близкое к наркотическому, и используется для борьбы с судорогами, для лечения гипертонии, психического возбуждения; в сочетании с другими препаратами – для обезболивания при родах.
Водные растворы тиосульфата магния используются для лечения ожогов и других заболеваний кожи.
Белая магнезия (MgCO3) входит в состав зубных порошков и присыпок; кроме того, она уменьшает кислотность желудочного сока.
Жженая магнезия (MgO) тоже нейтрализует желудочный сок. Кроме того, она применяется внутрь при кислотных отравлениях.
Приложение. Практическая часть.
2Mg+O2=2MgO (магний горит в кислороде воздуха ослепительно-белым пламенем).
Mg+2HCl=MgCl2+H2 (выделяемый кислород можно определить по пузырькам на поверхности металла и по взрыву при поджигании).
Mg+H2O=Mg(OH)2+H2 (реакция идет очень медленно при кипячении).
Mg+2H2O+2NH4Cl=MgCl2+2NH4OH+H2 (при проведении реакции ощущается характерный запах аммиака). В этой и предыдущей реакции образующийся MgCl2 можно определить с помощью реакции
MgCl2+2AgNO3=2AgClЇ+Mg(NO3)2.
MgO+MgCl2+H2O=2MgOHCl (образование магнезиального цемента). Через некоторое время цемент затвердевает.
MgO+H2O=Mg(OH)2 (реакция идет при нагревании). Образующийся Mg(OH)2 в этой и следующей реакции можно определить по фиолетовому окрашиванию добавляемого раствора фенолфталеина.
MgSO4+2NaOH=Mg(OH)2Ї+Na2SO4 (выпадает желтоватый осадок Mg(OH)2).
MgCl2+Na2CO3=MgCO3Ї+2NaCl (выпадает белый осадок MgCO3).
MgCO3+2HCl=MgCl2+CO2+H2
MgCl2+2AgNO3=2AgClЇ+Mg(NO3)2
Ca(OH)2+CO2=CaCO3+H2O.
MgCl2+NaOH=Mg(OH)2+2NaCl
Использованная литература
1. Беляев А.И. История магния. М.: Наука, 1974.
2. Некрасов Б.В. Основы общей химии. М.: Химия, 1967.
3. Николаев Г.И. Магний служит человеку. М.: Металлургия, 1978.
4. Самсонов Г.В., Перминов В.П. Магниды. Киев: Наукова думка, 1971.
5. Тихонов В.Н. Аналитическая химия магния. М.: Наука,
Похожие работы
... його, якщо необхідно, і виводять будь-які надлишки, тому і нестача, і надлишок магнію в організмі - явище достатньо рідкісне, але коли таке трапляється, виникають дуже небезпечні захворювання. III. Схема біогеохімічного циклу магнію. Кругообіг макроелементів. Калій, кальцій, натрій і магній не зв'язані з органічними сполуками хімічно, хоча вони містяться у великих кількостях у клітинних і позакл ...
... тного поля в точці на осі колового провідника радіусом R на відстані d від центра колового провідника дорівнює: . Аналогічно обчислюється індукція магнітного поля, створена іншими провідниками з струмом. 2. ЗАКОН ПОВНОГО СТРУМУ ТА ЙОГО ВИКОРИСТАННЯ ДЛЯ РОЗРАХУНКУ МАГНІТНИХ ПОЛІВ. ВИХРОВИЙ ХАРАКТЕР МАГНІТНОГО ПОЛЯ У електростатиці було встановлено, що робота при переміщенні одиничного ...
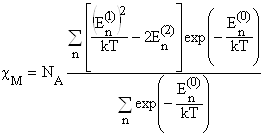
... вираз для макроскопічної магнітної сприйнятливості з урахуванням больцманівського розподілу ансамблю магнітних моментів по енергетичних рівнях приймає вигляд: Це і є рівняння Ван-Флека – основне в магнетохімії, пов’язуюче магнітні властивості з будовою молекул. Тут NA – число Авогадро, k – постійна Больцмана. З деякими крайніми випадками його ми вже зустрічалися вище. Якщо Е(0) = 0, а Е(2) ...
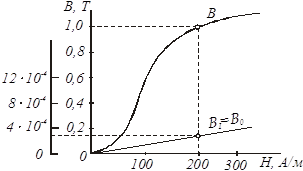
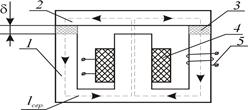
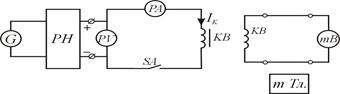
... І = const при вимірюванні. 5.3 Програма роботи 1. Вивчити будову та принципи дії мілівеберметра і мілітесламетра. 2. Вивчити лабораторну установку дослідження характеристик Ш-подібного електромагніта. 3. Експериментальним шляхом зняти вебер-амперну характеристику електромагніта . На підставі експериментальних даних провести необхідні розрахунки і побудувати криву намагнічування B = f(H) і ...
0 комментариев