Навигация
Фазовые превращения в твердом состоянии
2.3. Фазовые превращения в твердом состоянии.
При последовательном построении теории фазовых превращений [10] рассматриваются причины изменения фазового состояния и механизм превращения. Причиной фазовых превращений является изменение стабильности фаз в зависимости от внешних воздействий. Например, стабильная в определенной температурной области фаза становится нестабильной при понижении или повышении температуры.
При любом фазовом превращении в твердом состоянии происходит перестройка атомной структуры системы. В твердом состоянии перестройка структуры имеет место, кроме того, при процессах, не являющимися фазовыми превращениями, например, при рекристаллизации, пластической деформации скольжением и двойникованием. Такие процессы отличаются от фазовых превращений причиной перестройки кристаллической решетки: атомы занимают новые положения под действием поверхностных или упругих сил, внешнего напряжения, а не вследствие того, что термодинамический потенциал одной конфигурации атомов ниже, чем другой.
Классификация фазовых превращений может быть проведена на основе сравнения фазового состава системы в начальном и конечном состояниях. Продукт фазового превращения может отличаться от исходной (матричной) фазы:
1. составом при сохранении координации атомов в решетке (изоструктурный распад твердого раствора);
2. структурой и фазовым составом (эвтектоидный распад, выделение избыточной фазы);
3.кристаллической структурой, т.е. координацией атомов в решетке (мартенситное и массивное превращения, упорядочения атомно-кристаллической структуры).
Другая классификация фазовых превращений в твердом теле может быть основана на механизме протекающих процессов.
Диффузионные процессы. К ним относятся как процессы, протекающие через стадии образования и роста зародышей новой фазы, так и процессы, связанные с расслаиванием твердого раствора на участки с большей и меньшей концентрацией компонента (спинодальный распад, образование зон Гинье - Престона).
Бездиффузионные процессы. Это процессы, происходящие за счет коллективных перегруппировок атомов на расстояния порядка межатомных (например мартенситное и массивное превращения).
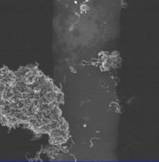
Вывод о протекании процесса по тому или иному механизму можно сделать исходя из морфологии полученного продукта по данным электронной или оптической микроскопии.
3. Экспериментальная часть.
3.1. Синтез твердых растворов Bi2O3-CaO.
Для первой стадии эксперимента в качестве исходных веществ были взяты оксид висмута (Bi2O3) и карбонат кальция (CaCO3) в мольных соотношениях Bi2O3/CaCO3 - 0.96:0.04, 0.9:0.1, 0.8:0.2, 0.76:0.24, 0.7:0.3, 0.6:0.4, 0.5:0.5. Квалификация всех исходных препаратов была не ниже “ч.д.а.”. Реагенты смешивались для получения как можно более однородной смеси, после чего прокаливались на воздухе при температуре 750С в течение 24 часов в трубчатой печи с последующим рентгенофазовым анализом полученных образцов. В ходе реакции
0.5(1-х) Bi2O3 + х CaCO3== Bi1-хСахО1.5-0.5x+ х CO2 (спекание при 750С, 24 часа)
выделялся углекислый газ (CO2) и образовывался желтый порошок. Для неоднофазных, по данным РФА , образцов цикл “помол-отжиг” был повторен при тех же условиях.
Полученный в результате предыдущей стадии эксперимента порошок состава Bi1-xCaxOy (х = 0.02, 0.05) был растворен в разбавленном растворе азотной кислоты (30%) и упарен на горелке до начала выделения BiONO3 в виде тонкой пленки на поверхности раствора:
Bi(NO3)3 = BiONO3 + 2 NO2 + 0.5 O2
После этого был произведен так называемый “бумажный синтез” [11] : образовавшимся раствором пропитали несколько листов бумажного фильтра (для предотвращения расслоения компонентов раствора при разложении) и производили разложение на горелке до окончания реакции восстановления избыточной азотной кислоты глюкозой, образовавшейся при гидролизе целлюлозы бумаги (признаком окончания реакции было прекращение выделения бурого газа NO2), нитрат висмута при этом полностью разложился до оксинитрата. Затем продукт реакции в течении 30 минут отжигали в муфельной печи при температуре 750С, а после произвели закалку на воздухе. При этом происходило разложение нитратов с одновременным образованием твердого раствора:
(1-х) BiONO3 + x Ca(NO3)2 = Bi1-xCaxO1.5-0.5x + (1+2x) NO2 + 0.25(1+2x) O2
Следующей стадией эксперимента был помол полученного вещества с последующей обработкой в трубчатой печи в течение 24 часов при температуре 750С, с последующей закалкой на воздухе и снятием рентгенограмм полученного вещества.
Похожие работы
... это соответственно жидкие и студнеобразные коллоидные системы, а коллоидные системы — это дисперсные системы, промежуточные между истинными растворами и грубодисперсными системами — суспензиями и эмульсиями). Золь-гель-метод — удобный путь получения дисперсных материалов, он позволяет исключить многочисленные стадии промывки, так как в качестве исходных веществ используют соединения, не вносящие ...
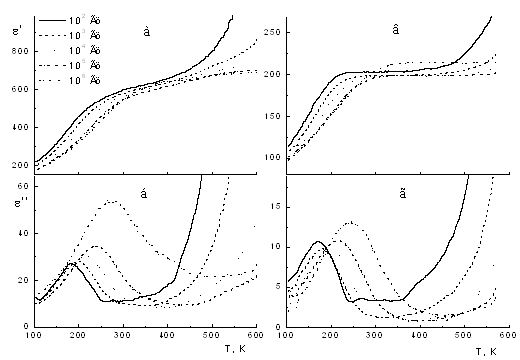
... диэлектрического отклика для составов 0.1<х£0.4 в области низких температур проявляются особенности, которые выражаются в частотной дисперсии ε¢ и ε¢¢, характерной для релаксорных сегнетоэлектриков (рис. 1): Рисунок 1 – Температурные зависимости ε¢ и ε¢¢ для составов х=0.2 (а, б) и х=0.4 (в, г) Наблюдаемое низкотемпературное плечо на ...
... при изучении синтеза новых материалов и процессов ионного транспорта в них. В чистом виде такие закономерности наиболее четко прослеживаются при исследовании монокристаллических твердых электролитов. В то же время при использовании твердых электролитов в качестве рабочих сред функциональных элементов необходимо учитывать, что нужны материалы заданного вида и формы, например в виде плотной керамики ...
... пластмасс различного назначения. Приводимый ниже материал предназначен для студентов химического отделения, специализирующихся по органической химии и химии и физике высокомолекулярных соединений, а также может быть полезен аспирантам, инженерам и научным работникам. 2.1 Метод изучения релаксации напряжения Явление релаксации - это процесс перехода из неравновесного в равновесное состояние ...





0 комментариев