Навигация
8 NO3 + 2H ----- NO2 +H2O
PbS + 4H2O + 8NO3 + 16H ----- PbSO4 + 8H + 8NO2 +8H2O
Записываем в молекулярном виде, сокращая молекулы воды и стягивая ионы NO3 и H :
PbS + 8HNO3 + 8H ----- PbSO4 + 8H + 8NO2 + 4H2O
Конечный вид уравнения :
PbS + 8HNO3 == PbSO4 + 8NO2 + 4H2O
РЕАКЦИИ ОКИСЛЕНИЯ-ВОССТАНОВЛЕНИЯ В НЕЙТРАЛЬНОЙ СРЕДЕПример 1. Рассмотрим реакции окисления-восстановления, протекающие в нейтральной среде по схеме
Na2SO3 + KMnO4 + H2O ----- MnO2 + Na2SO4 +
SO3 + H2O – 2e ----- SO4 + 2H
MnO4 + 2H2O + 3e ----- MnO2 + 4OH
3SO3 + 3H2O + 2MnO4 + 4H2O ----- 3SO4 + 6H + 2MnO2 + 3OH .
Ионы H и ОН стягиваются с образованием слабо диссоциированных молекул воды:
3Na2SO3 + H2O + 2KMnO4 ----- Na2SO4 + 6H2O + 2MnO2 + 2OH
3Na2SO3 + H2O + 2KMnO4 == Na2SO4 + 2MnO2 + KOH
СОСТАВЛЕНИЕ УРАВНЕНИЙ РЕАКЦИЙ ОКИСЛЕНИЯ – ВОССТАНОВЛЕНИЯ С УЧАСТИЕМ СОЕДИНЕНИЙ ПЕРЕКИСНОГО ТИПА (H2O, BaO2, H2S2, FeS2 и т. д. )
Все эти соединения содержат двухвалентные ионы ( S –S ) и (О – О),
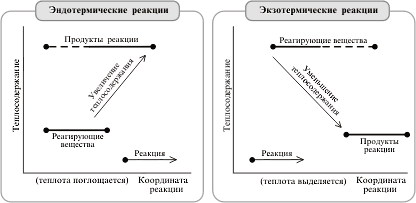
поэтому состояние окисления каждого из атомов кислорода и серы, образующих данные цепи, равно I. При разложении H2O2 переходит в более стабильное состояние: в H2O и О2, в которых соответственно равны степени окисления кислорода (-2 ) и 0.
В окислительно-восстановительных реакциях пероксид водорода в зависимости от партнёров и условий реакции может выступать и как окислитель, и как восстановитель.
Рассмотрим реакции этих соединений на примерах пероксида водорода:
Пример 1. Н2О2 - окислитель:а) в кислой среде молекула пероксида водорода, принимая
два электрона, переходит в две молекулы воды по схеме
H2O2 +2e + 2H ----- 2H2O; H2O2 +H2 S ----- H2SO4 + …
H2O2 + 2e + 2H ----- 2H2O2 HS + 4H2O – 8e ------ SO4 + 9H4H2O2 + 8H + HS + 4H2O ----- 8H2O + SO4 + 9H
4H2O2 + H2S + 7H ----- 4H2O + H2SO4 + 7H
4H2O2 + H2S == 4H2O + H2SO4
б) в нейтральной среде Н2О2 + 2е ----- 2ОН
ОСОБЫЕ СЛУЧАИ СОСТАВЛЕНИЯ УРАВНЕНИЙ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
Если в реакции участвуют вещества, для которых сложно подсчитать степень окисления (например, В5Н11, FeAsS, органические вещества ) можно использовать метод схематического (формального) электронного баланса, суть которого заключается в том, что алгебраическая сумма зарядов в левой части уравнения реакции окисления или восстановления должна быть равна сумме зарядов в правой части этого же уравнения.
Пример 1. Дана схема реакции
В2Н6 + KclO3 ----- KCl + H3BO3
Определяем восстановитель и окислитель, составляем уравнение для процессов окисления и восстановления:
В2Н6 – 12е + 6Н2О ----- 2Н3ВО3 + 12Н
Восстановителем в этой реакции являются молекулы В2Н6, которые окисляются до борной кислоты :
В2Н6 + 6Н2О ----- 2Н3ВО3 + 12Н
Недостающие ионы кислорода для образования борной кислоты можно получить из молекул воды, при этом образуются ионы Н . Как нетрудно видеть, в левой части данной схемы процесса окисления имеется 0 зарядов, а в правой части – 12 положительных зарядов. Для уравнивания зарядов в обеих частях необходимо в левой части схемы отнять 12 электронов.
Окислителем являются анионы ClO3 , которые превращаются в ионы Cl , принимая 6 электронов :ClO3 + 6e + 3H2O ----- Cl + 6OH .
При этом освобождающиеся ионы кислорода соединяются с молекулами воды ( реакция происходит в водной среде ) , образуя ионы ОН . Затем производим балансирование уравнений процессов окисления и восстановления :
1 В2Н6 – 12е + 6Н2О ----- 2Н3ВО3 + 12Н
2 ClO3 + 6e + 3H2O ----- Cl + 6OH
B2H6 + 6H2O + 2ClO3 + 6H2O ----- 2H3BO3 + 12H + 12OH + 2Cl
B2H6 + 2KClO3 == 2H3BO3 + 2KCl 12H2O
Цифры таблицы получены при температуре 25 С. С изменением температуры они мало изменяются, поэтому ими можно пользоваться для определения направления реакции в обычных условиях. Цифры таблицы действительны для случаев, когда концентрация ( или, точнее активность ) растворов в гальванической цепи равна единице ( т. е. 1 моль/л ).
Необходимо иметь в виду следующее :
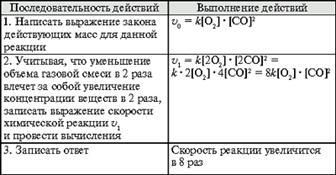
1. Увеличение концентрации ионов, в которые переходит окисляющийся атом или ион, понижает э. д. с. реакции, а уменьшение – повышает.
2. Увеличение концентрации окисляющихся атомов или ионов повышает э. д. с. реакции, а уменьшение понижает.
3. Правила пользования таблицами для определения направления окисления – восстановления.
В таблицах реакций представлены величины нормальных потенциалов окисления ( Еокисл ) и восстановления ( Евосст ) важнейших процессов. Таблицы соответственно разделены на две группы : “ Окисление “ и “ Восстановление “ .
Знак “ + “ у Еокисл (или Евосст ) и у соответствующего lgKокисл (или lgKвосст) показывает, что процесс идёт преимущественно слева направо, а знак “ – “ у этих же величин – справа налево.
Для определения направления той или иной реакции окисления-восстановления берут данные разделов “ Окисление “ и “ Восстановление “, распологая в одну строку уравнение рассматриваемого процесса окисления с уравнением заданного процесса восстановления. При этом получают несбалансированное общее ионное уравнение возможной окислительно-восстановительной реакции.
Алгебраическая сумма Еокисл + Евосст рассматриваемых процессов может быть величиной положительной, и тогда данная реакция ( при условии аокисл = авосст = 1 и определённом значении рН ) идёт, а если эта величина окажется отрицательной, то реаакция ( при тех же условиях ) невозможна.
Пример. Пойдёт ли реакция между I - ионами и Fe ионами с образованием свободного йода ?
![]()
![]() Решение. На таблице “Окисление “ ( в группе реакций “Йод“ ) находят уравнение 2I – 2e I2, по таблице “Восстановление “ ( в группе реакций “Железо” ) находят уравнение Fe + e Fe и записывают их в одну строчку, складывая величины Еокисл + Евосст;
Решение. На таблице “Окисление “ ( в группе реакций “Йод“ ) находят уравнение 2I – 2e I2, по таблице “Восстановление “ ( в группе реакций “Железо” ) находят уравнение Fe + e Fe и записывают их в одну строчку, складывая величины Еокисл + Евосст;
![]()
![]() :lgKокисл :Еокисл :Евосст :lgKвосст:
:lgKокисл :Еокисл :Евосст :lgKвосст:
![]() 2I - 2e = I2
-18,07 -0,5345 +0,771 +13,04 Fe +e Fe
2I - 2e = I2
-18,07 -0,5345 +0,771 +13,04 Fe +e Fe
Алгебраическая сумма ( - 0,5345 ) + ( +0,771 ) = + 0,2365 –величина положительная : следовательно, реакция 2 I + 2 Fe ----- I2 + 2Fe будет протекать при определённых условиях.
С помощью указанных в этих же монограммах логарифмов констант равновесия можно также вычислить константы равновесия разнообразных реакций окисления-восстановления.
Анализируя таблицу определения направления реакции окисления-восстановления, можно сделать следующие выводы :
1. Ионы “ благородных “ металлов – сильные окислители.
Например : Cr + Ag----- Cr + Ag э. д. с. = + 0,7995- - 0,4 = 1,209 в.
Fe + Au---- Fe + Au э. д. с. = + 1,68- + 0,77 = 0,91 в.
2. Наиболее сильные восстановители – атомы щелочных и щелочно –земельных металлов. Наиболее слабые восстановители – “благородные” металлы и ионы галогенов ( за исключением иона йода ).
3. Наиболее сильные окислители – нейтральные атомы галогенов, высокоположительные ионы металлов, а также ионы “благородных” металлов. Наиболее слабые окислители – ионы щелочных и щелочноземельных металлов.
![]()
Похожие работы
... Для составления уравнений окислительно-восстановительных реакций обычно используют два метода: 1) метод электронного баланса, 2) электронно-ионный метод. При расчете коэффициентов в окислительно-восстановительных реакциях пользуются правилом электронного баланса: суммарное число электронов, теряемых восстановителем, должно быть равно суммарному числу электронов, приобретаемых окислителем. ...
... раствора; · присутствие катализатора. В большинстве случаев скорость реакции находится в прямой зависимости от температуры и рН раствора. Поэтому многие определения методом окислительно-восстановительного титрования следует проводить при определенном значении рН и при нагревании. Индикаторы окислительно-восстановительного титрования окислительный восстановительный титрование При анализе ...
... : 2Cu0 + O0 = 2Cu2+O2-, Cu2+O2- + H0 = Cu0 + H1+O2-, Cl0 + 2Na1+O2-H1+ = Na1+Cl1- + Na1+Cl1+O2- + H1+O2-. 2. Окислительно-восстановительные реакции Окислительно-восстановительные реакции – это химические реакции, протекающие с изменением степени окисления элементов, входящих в состав реагирующих веществ. Окисление – это процесс отдачи электронов атомом, молекулой или ионом. Если ...
... условия сдвига равновесия вправо .... Глава 2. Прикладные аспекты преподавания темы «Закономерности течения химических реакций» Прикладные аспекты преподавания темы «Закономерности течения химических реакций» на мой взгляд удобнее всего рассматривать на уроках, которые следуют сразу за рассмотрением скорости реакции и химического равновесия, - это производство серной кислоты. 2.1 ...



0 комментариев