Содержание
Введение. 2
Вода. 3
Спички. 9
Бумага и карандаши. 11
Стекло. 13
Мыла и моющие средства. 17
Химические средства гигиены и косметики. 20
Химия в земледелии. 24
Свеча и электрическая лампочка. 26
Химические элементы в организме человека. 29
Использованная литература. 33
Введение
Повсюду, куда бы ни обратил свой взор, нас окружают предметы и изделия, изготовленные из веществ и материалов, которые получены на химических заводах и фабриках. Кроме того, в повседневной жизни, сам того не подозревая, каждый человек осуществляет химические реакции. Например, умывание с мылом, стирка с использованием моющих средств и др. При опускании кусочка лимона в стакан горячего чая происходит ослабление окраски — чай здесь выступает в роли кислотного индикатора, подобного лакмусу. Аналогичное кислотно-основное взаимодействие проявляется при смачивании уксусом нарезанной синей капусты. Хозяйки знают, что капуста при этом розовеет. Зажигая спичку, замешивая песок и цемент с водой или гася водой известь, обжигая кирпич, мы осуществляем настоящие, а иногда и довольно сложные химические реакции. Объяснение этих и других широко распространенных в жизни человека химических процессов — удел специалистов.
Приготовление пищи — это тоже химические процессы. Не зря говорят, что женщины-химики часто очень хорошие кулинары. Действительно, приготовление пищи на кухне иногда напоминает выполнение органического синтеза в лаборатории. Только вместо колб и реторт на кухне используют кастрюли и сковородки, но иногда и автоклавы в виде скороварок. Не стоит далее перечислять химические процессы, которые проводит человек в повседневной жизни. Необходимо лишь отметить, что в любом живом организме в огромных количествах осуществляются различные химические реакции. Процессы усвоения пищи, дыхания животного и человека основаны на химических реакциях. В основе роста маленькой травинки и могучего дерева также лежат химические реакции.
Химия - это наука, важная часть естествознания. Строго говоря, наука не может окружать человека. Его могут окружать результаты практического приложения науки. Это уточнение весьма существенное. В настоящее время часто можно слышать слова: «химия испортила природу», «химия загрязнила водоем и сделала его непригодным для использования» и т. д. На самом же деле наука химия здесь вовсе непричем. Люди, используя результаты науки, плохо оформили их в технологический процесс, безответственно отнеслись к требованиям правил безопасности и к экологически допустимым нормам промышленных сбросов, неумело и не в меру использовали удобрения на сельскохозяйственных угодьях и средства защиты растений от сорняков и вредителей растений. Любая наука, особенно естествознание, не может быть хорошей или плохой. Наука — накопление и систематизация знаний. Другое дело, как и в каких целях используются эти знания. Однако это уже зависит от культуры, квалификации, моральной ответственности и нравственности людей, не добывающих, а использующих знания.
Без продуктов химической промышленности современному человеку не обойтись, так же как нельзя обойтись без электричества. Такая же ситуация и с продуктами химической промышленности. Нужно протестовать не против некоторых химических производств, а против их низкой культуры.
Культура человека — сложное и разноплановое понятие, при котором возникают такие категории, как умение человека вести себя в обществе, правильно владеть родным языком, следить за опрятностью своей одежды и внешним видом и т. д. Однако мы часто говорим и слышим о культуре строительства, культуре производства культуре ведения сельского хозяйства и т. д. Действительно, когда речь заходит о культуре Древней Греции или еще более ранних цивилизациях, то прежде всего вспоминают о ремеслах, которыми владели люди той эпохи, какие орудия труда они использовали, что умели строить, как умели украшать строения и отдельные предметы.
Многие важные для человека химические процессы были открыты задолго до того, как химия оформилась в науку. Значительное количество химических открытий было сделано наблюдательными и любознательными ремесленниками. Эти открытия переходили в семейные или клановые секреты и далеко не все дошли до нас. Часть из них была утеряна для человечества. Приходилось и приходится затрачивать огромный труд, создавать лаборатории, а иногда и институты для раскрытия секретов древних мастеров и их научного толкования.
Многие не знают, как устроен телевизор, но успешно пользуются им. Однако знание устройства телевизора никогда и никому не помешает в правильной его эксплуатации. Так и с химией. Понимание сущности химических процессов, с которыми мы встречаемся в повседневной жизни, может принести человеку только пользу.
Вода
Вода в масштабе планеты. Человечество издавна уделяло большое внимание воде, поскольку было хорошо известно, что там, где нет воды, нет и жизни. В сухой земле зерно может лежать многие годы и прорастает лишь в присутствии влаги. Несмотря на то, что вода — самое распространенное вещество, на Земле она распределена весьма неравномерно. На африканском континенте и в Азии имеются огромные пространства, лишенные воды, — пустыни. Целая страна — Алжир — живет на привозной воде. Воду доставляют на судах в некоторые прибрежные районы и на острова Греции. Иногда там вода стоит дороже вина. По данным Организации Объединенных Наций, в 1985 г. 2,5 млрд. населения земного шара испытывали недостаток в чистой питьевой воде.
Поверхность земного шара на 3/4 покрыта водой — это океаны, моря; озера, ледники. В довольно больших количествах вода находится в атмосфере, а также в земной коре. Общие запасы свободной воды на Земле составляют 1,4 млрд. км3. Основное количество воды содержится в океанах (около 97,6%), в виде льда на нашей планете воды имеется 2,14 %. Вода рек и озер составляет всего лишь 0,29 % и атмосферная вода — 0,0005 %.
Таким образом, вода находится на Земле в постоянном движении. Среднее время ее пребывания в атмосфере оценивается 10 сутками, хотя и меняется с широтой местности. Для полярных широт оно может достигать 15, а в средних — 7 суток. Смена воды в реках происходит в среднем 30 раз в год, т. е. каждые 12 дней. Влага, содержащаяся в почве, обновляется за 1 год. Воды проточных озер обмениваются за десятки лет, а непроточных за 200—300 лет. Воды Мирового океана обновляются в среднем за 3000 лет. Из этих цифр можно получить представление о том, сколько времени необходимо для самоочистки водоемов. Нужно лишь иметь в виду, что если река вытекает из загрязненного озера, то время ее самоочистки определяется временем самоочистки озера.
Вода в организме человека. Не очень легко представить, что человек примерно на 65 % состоит из воды. С возрастом содержание воды в организме человека уменьшается. Эмбрион состоит из воды на 97 %, в теле новорожденного содержится 75 %, а у взрослого человека — около 60 %.
В здоровом организме взрослого человека наблюдается состояние водного равновесия или водного баланса. Оно заключается в том, что количество воды, потребляемое человеком, равно количеству воды, выводимой из организма. Водный обмен является важной составной частью общего обмена веществ живых организмов, в том числе и человека. Водный обмен включает процессы всасывания воды, которая поступает в желудок при питье и с пищевыми продуктами, распределение ее в организме, выделения через почки, мочевыводящие пути, легкие, кожу и кишечник. Следует отметить, что вода также образуется в организме вследствие окисления жиров, углеводов и белков, принятых с пищей. Такую воду называют метаболической. Слово метаболизм происходит от греческого, что означает перемена, превращение. В медицине и биологической науке метаболизмом называют процессы превращения веществ и энергии, лежащие в основе жизнедеятельности организмов. Белки, жиры и углеводы окисляются в организме с образованием воды Н2О и углекислого газа (диоксида углерода) СО2. При окислении 100 г жиров образуется 107 г воды, а при окислении 100 г углеводов — 55,5 г воды. Некоторые организмы обходятся лишь метаболической водой и не потребляют ее извне. Примером является ковровая моль. Не нуждаются в воде в природных условиях тушканчики, которые водятся в Европе и Азии, и американская кенгуровая крыса. Многие знают, что в условиях исключительно жаркого и сухого климата верблюд обладает феноменальной способностью долгое время обходиться без пищи и воды. Например, при массе 450 кг за восьмидневный переход по пустыне верблюд может потерять 100 кг в массе, а потом восстановить их без последствий для организма. Установлено, что его организм использует воду, содержащуюся в жидкостях тканей и связок, а не крови, как это происходит с человеком. Кроме того, в горбах верблюда содержится жир, который служит одновременно запасом пищи и источником метаболической воды.
Общий объем воды, потребляемый человеком в сутки при питье и с пищей, составляет 2—2,5 л. Благодаря водному балансу столько же воды и выводится из организма. Через почки и мочевыводящие пути удаляется около 50—60 % воды. При потере организмом человека 6—8 % влаги сверх обычной нормы повышается температура тела, краснеет кожа, учащается сердцебиение и дыхание, появляется мышечная слабость и головокружение, начинается головная боль. Потеря 10 % воды может привести к необратимым изменениям в организме, а потеря 15—20 % приводит к смерти, поскольку кровь настолько густеет, что с ее перекачкой не справляется сердце. В сутки сердцу приходится перекачивать около 10 000 л крови. Без пищи человек может прожить около месяца, а без воды — всего лишь несколько суток. Реакцией организма на нехватку воды является жажда. В этом случае ощущение жажды объясняют раздражением слизистой оболочки рта и глотки из-за большого понижения влажности. Существует и другая точка зрения на механизм формирования этого ощущения. В соответствии с ней сигнал о понижении концентрации воды в крови на клетки коры головного мозга подают нервные центры, заложенные в кровеносных сосудах.
Водный обмен в организме человека регулируется центральной нервной системой и гормонами. Нарушение функции этих регуляторных систем вызывает нарушение водного обмена, что может приводить к отекам тела. Конечно, различные ткани человеческого организма содержат различное количество воды. Самая богатая водой ткань — стекловидное тело глаза, содержащее 99%. Самая же бедная — эмаль зуба. В ней воды всего лишь 0,2%. Много воды содержится в веществе мозга.
Важной функцией океанов и морей является регулирование содержания в атмосфере углекислого газа (диоксида углерода). Его относительное содержание в атмосфере невелико и составляет всего лишь 0,03— 0,04 %, Однако общая масса, заключающаяся в атмосфере, очень большая — 2000—2500 млрд. т. В связи с развитием энергетики, промышленности и транспорта сжигается огромное количество угля и нефтепродуктов. Основным продуктом их окисления является СО2. Учеными установлено, что атмосферный СО2 обладает способностью задерживать, т. е. не пропускать в космическое пространство, тепловое излучение Земли («парниковый эффект»). Чем больше СО2 в атмосфере, тем теплее климат Земли. Общее потепление климата может привести к катастрофическим последствиям. В результате потепления усилится таяние льдов на полюсах планеты и в горных районах, что приведет к повышению уровня Мирового океана и к затоплению огромных площадей суши. Подсчитано, что если расплавить все ледники Гренландии и Антарктиды, то уровень океана поднимется почти на 60 м. Нетрудно догадаться, что тогда Санкт-Петербург и многие приморские города окажутся под водой. Важным регулятором содержания СО2 в атмосфере является растительный покров Земли. В результате фотосинтеза растения превращают СО2 в клетчатку и освобождают кислород:
CO2 + 6H2O-> C6H12O6 + 6O2
Уместно отметить, что растения — основные поставщики атмосферного кислорода, а его источником прямо или косвенно является вода. Ежегодное продуцирование кислорода земной растительностью планеты составляет 300 млрд. т.
Основную роль в регулировании содержания СО2 в атмосфере играют океаны. Между Мировым океаном и атмосферой Земли устанавливается равновесие: углекислый газ СО2 растворяется в воде, превращаясь в угольную кислоту Н2СО3, и далее превращается в донные карбонатные осадки. Дело в том, что в морской воде содержатся ионы кальция и магния, которые с карбонатным ионом могут превращаться в малорастворимый карбонат кальция СаСО3 и магния MgCO3. Многие морские организмы извлекают первую соль из морской воды и строят из нее панцири. При отмирании этих организмов за большие периоды времени на дне образуются огромные скопления панцирей. Так формируются залежи мела, а в результате вторичных геологических превращений — залежи известняков, часто в виде бутовых плит. Как мел, так и бутовый камень широко используют в строительном деле.
Зеленому покрову Земли невозможно справиться с задачей удержания примерно на одном и том же уровне содержания СО2 в атмосфере. Подсчитано, что наземные растения для построения своего тела ежегодно потребляют из атмосферы 20 млрд. т СО2, а обитатели океанов и морей извлекают из воды 155 млрд. т в пересчете на СО2.
Не менее важным веществом в создании «парникового эффекта», чем СО2, является атмосферная вода. Она также перехватывает и поглощает тепловое излучение Земли. Однако в атмосфере ее гораздо больше, чем углекислого газа. Атмосферную влагу, особенно в виде облаков, иногда сравнивают с «одеялом» планеты. Многие замечали, при ясном и безоблачном небе ночи бывают холоднее, чем в облачную погоду.
К основным потребителям пресной воды относятся: сельское хозяйство (70%), промышленность, включая энергетику (20 %) и коммунальное хозяйство (~ 10 %). В промышленном производстве наиболее водоемкими являются химическая, целлюлозно-бумажная и металлургическая промышленность. Так, на изготовление I т синтетического волокна расходуется 2500—5000, пластмассы — 500—1000, бумаги — 400—800, стали и чугуна — 160—200 м3 воды. Опыт показывает, что на бытовые нужды житель благоустроенного города расходует 200—300 л воды в день. Распределение потребления воды в среднем следующее: на приготовление пищи и питье расходуется всего лишь 5 %, в смывном бачке туалета — 43, для ванны и душа — 34, на мытье посуды — 6, на стирку — 4, на уборку помещения — 3 %.
Для приготовления пищи и в качестве питьевой может быть использована природная вода, если она не содержит вредных микроорганизмов, а также вредных минеральных и органических примесей, если она прозрачна, бесцветна и не имеет привкуса и запаха. В соответствии с Государственным стандартом содержание минеральных примесей не должно превышать 1 г/л. Кислотность воды в единицах рН должна быть в пределах 6,5—9,5. Концентрация нитратного иона не должна превышать 50 мг/л. Естественно, что она должна также отвечать бактериологическим требованиям и иметь допустимые показатели на токсичные химические соединения. Этим требованиям наиболее часто удовлетворяет колодезная и родниковая вода. Однако в больших количествах найти воду, отвечающую Государственному стандарту, трудно. Поэтому ее приходится очищать на специальных станциях. Основными стадиями очистки являются фильтрование (через слой песка) и обработка окислителями (хлором или озоном). В некоторых случаях приходится применять коагуляцию. Для этого используют сульфат алюминия A12{SO4)3. В слабощелочной среде, создаваемой карбонатами кальция, под действием воды эта соль гидролизуется и из нее получается хлопьевидный осадок гидроксида алюминия Аl(ОН)3, а также сульфат кальция CaSO4 в соответствии с уравнением
Al2 (SO4)3 + ЗСа (НСО3)2 = 2AI (ОН) 3 ↓ + 3CaSO4↓ + 6СО2
Гидроксид алюминия А1(ОН)3 вначале образуется в виде мелких коллоидных частиц, которые со временем объединяются в более крупные. Этот процесс называют коагуляцией. При коагуляции хлопья А1(ОН)3 захватывают взвешенные примеси и сорбируют на своей развитой поверхности органические и минеральные вещества.
С давних пор для стерилизации питьевой воды использовалось простое кипячение, а древние греки добавляли в воду сухое вино, что создавало кислую среду, в которой погибали многие болезнетворные микробы.
Питьевая вода должна содержать небольшие количества растворенных солей и газов. В зависимости от них в различных местах вода отличается по вкусу. Макрокомпонентами химического состава поверхностных и некоторых подземных вод считают ионы Na+, K+, Mg2+, Са2+, SO4, Сl, NO3. Ионы Fe2+, Fe3+, Al3+в заметных количествах содержатся только в локальных подземных водах, характеризующихся кислой средой. Кремниевая кислота H2SiO3 является преобладающим компонентом в некоторых типах грунтовых и поверхностных вод с очень малой минерализацией, а также в термальных водах. Границей между пресной и минеральной водой считается содержание минеральных химических соединений в количестве 1 г/л.
Природные воды, содержащие соли, растворенные газы, органические вещества в более высоких концентрациях, чем питьевая, называют минеральными. Некоторые из минеральных вод содержат биологически активные компоненты: СО2, H2S, некоторые соли (например, сульфаты натрия и магния), соединения мышьяка, радиоактивные элементы (например, радон) и др. Поэтому минеральные воды с давних пор использовали в качестве лечебного средства. В настоящее время минеральные воды делят на лечебные, лечебно-столовые и столовые.
Лечебные минеральные воды проявляют свое действие в одних случаях при наружном, а в других — при внутреннем применении. Конечно, воды, пригодные для внутреннего применения, иногда оказываются полезными и при наружном использовании. В качестве лечебных вод широко известны сероводородные (например, воды в районе курорта Мацеста), в качестве лечебно-столовой воды наиболее известна «Боржоми», а в качестве столовых вод — «Нарзан» и «Ессентуки № 20». В различных районах нашей страны как столовые широко используют разные местные минеральные воды, например, в Санкт-Петербурге известна вода «Полюстрово». Перед разливом в бутылки столовые минеральные воды обычно дополнительно насыщают углекислым газом до концентрации 3—4 %.
Дистиллированная вода, полученная конденсацией пара, практически не содержит солей и растворенных газов и потому неприятна на вкус. Кроме того, при продолжительном употреблении она даже вредна для организма. Это связано с вымыванием из клеток тканей желудка и кишечника содержащихся в них солей и микроэлементов, которые необходимы для нормального функционирования организма.
Поскольку вода является очень хорошим растворителем, в природе она всегда содержит растворенные вещества, так как не существует абсолютно нерастворимых веществ. Их количество и характер зависят от состава пород, с которыми вода находилась в контакте.
Наименьшее количество примесей и растворенных веществ содержится в дождевой воде. Однако даже она содержит растворенные газы, соли и твердые частицы. Соли, содержащиеся в дождевой воде, имеют свое происхождение из океанов и морей. Лопающиеся пузырьки на поверхности океанов выбрасывают в атмосферу довольно большое количество солей. Они захватываются потоками воздуха {особенно в штормовую погоду) и распределяются в атмосфере. Твердый остаток, который образуется при испарении дождевой воды,— это частички пыли, захваченные капельками дождя. Из 30 л дождевой воды при испарении остается примерно 1 г сухого остатка. Растворенными газами являются как основные компоненты воздуха, так и загрязнения, встречающиеся в данном районе. Состав дождевых осадков над морем согласуется с правилом, согласно которому он идентичен тому, что получается при добавлении к 1 л дистиллированной воды 1,5 мл морской воды.
Получение высокочистой воды — весьма сложная задача. Поскольку она хранится в каком-то сосуде, в ней должны быть примеси материала этого сосуда (будь то стекло или металл). Для прецизионных научных исследований наиболее чистую воду получают методом ректификации (перегонкой) дистиллированной воды во фторопластовых колоннах.
Основные запасы пресной воды на Земле сосредоточены в ледниках.
Влажность воздуха.
Важной характеристикой состояния атмосферы является влажность воздуха или, что то же самое, степень насыщения воздуха водяными парами. Она выражается отношением содержания водяных паров в воздухе к их содержанию при насыщении воздуха при данной температуре. Поэтому правильнее говорить не просто о влажности, а об относительной влажности. При насыщений воздуха водяными парами вода в нем больше не испаряется. Для человека наиболее благоприятная влажность воздуха 50 %. На влажность, как и на многое другое, распространяется правило: слишком много и слишком мало — одинаково нехорошо. Действительно, при повышенной влажности человек острее ощущает низкие температуры. Многие могли убедиться, что сильные морозы при низкой влажности воздуха переносятся легче, чем не столь сильные, но при высокой влажности. Дело в том, что пары воды, так же как и жидкая вода, обладают гораздо большей теплоемкостью, чем воздух. Поэтому во влажном воздухе тело отдает в окружающее пространство больше теплоты, чем в сухом. В жаркую погоду высокая влажность опять же вызывает дискомфорт. В этих условиях уменьшается испарение влаги с поверхности тела (человек потеет), а значит, тело хуже охлаждается и, следовательно, перегревается. В очень сухом воздухе тело теряет слишком много влаги и, если не удается ее восполнить, это сказывается на самочувствии человека.
Абсолютно сухого воздуха практически не бывает.
В 1913 г. английским химиком Бейкером было установлено, что жидкости, осушенные в течение девяти лет в запаянных ампулах, кипят при гораздо более высоких температурах, чем указано в справочниках. Например, бензол начинает кипеть при температуре на 26° выше обычной, а этиловый спирт — на 60, бром — на 59, а ртуть — без малого на 100°. Температура замерзания этих жидкостей повысилась. Влияние следов воды на эти физические характеристики до сих пор не нашли удовлетворительного объяснения. В настоящее время известно, что тщательно высушенные газы NH3 и HG1 не образуют хлорида аммония, а сухой NH4C1 в газовой фазе не диссоциирует на NH3 и НС1 при нагревании. Кислотный триоксид серы в сухих условиях не взаимодействует с основными оксидами СаО, BaO, CuO, а щелочные металлы не реагируют ни с безводной серной кислотой, ни с безводными галогенами.
В хорошо высушенном кислороде уголь, сера, фосфор горят при температуре, на много превышающей температуру их горения в неосушенном воздухе. Считают, что влага играет каталитическую роль в этих химических реакциях.
Весьма редкое свойство воды проявляется при ее превращении из жидкого состояния в твердое. Этот переход связан с увеличением объема, а следовательно, с уменьшением плотности.
Ученые доказали, что вода в твердом состоянии имеет ажурное строение с полостями и пустотами. При плавлении они заполняются молекулами воды, поэтому плотность жидкой воды оказывается выше плотности твердой. Поскольку лед легче воды, то он плавает на ней, а не опускается на дно. Это играет в природе очень важную роль. Если бы плотность льда была выше, чем воды, то, появившись на поверхности вследствие охлаждения воды холодным воздухом, он погружался бы на дно и в результате весь водоем должен был бы промерзнуть. Это катастрофически сказалось бы на жизни многих организмов водоемов.
Интересно, что если над водой создать высокое давление и затем ее охладить до замерзания, то образующийся лед в условиях повышенного деления плавиться не при 00С, а при более высокой температуре. Так, лед, полученный при замерзании воды, который находиться под давлением 20 000 атм., в обычных условиях плавиться только при 800С.
Поваренная соль
Солевое голодание может привести к гибели организма. Суточная потребность в поваренной соли взрослого человека составляет 10-15 г. В условиях жаркого климата потребность в соли взрастает до 25-30 г.
Хлорид натрия нужен организму человека или животного не только для образования соляной кислоты в желудочном соке. Эта соль входит в тканевые жидкости и в состав крови. В последней ее концентрация равна 0,5—0,6 %.
Водные растворы NaCI в медицине используют в качестве кровезамещающих жидкостей после кровотечений и при явлениях шока. Уменьшение содержания NaCI в плазме крови приводит к нарушению обмена веществ в организме.
Не получая NaCI извне, организм отдает его из крови и тканей.
Хлорид натрия способствует задерживанию воды в организме, что, в свою очередь, приводит к повышению артериального давления. Поэтому при гипертонической болезни, ожирении, отеках врачи рекомендуют снижать суточное потребление поваренной соли. Избыток в организме NaCI может вызвать острое отравление и привести к параличу нервной системы.
Организм человека быстро реагирует на нарушение солевого баланса появлением мышечной слабости, быстрой утомляемостью, потерей аппетита, возникновением неутолимой жажды.
Поваренная соль обладает хотя и слабыми, но антисептическими свойствами. Развитие гнилостных бактерий прекращается лишь при ее содержании в 10—45 %. Это свойство широко используют в пищевой промышленности и при сохранении пищевых продуктов в домашних условиях.
При испарении морской воды при температурах 20— 35 °С вначале выделяются наименее растворимые соли — карбонаты кальция, магния и сульфат кальция. Затем выпадают более растворимые соли — сульфаты натрия и магния, хлориды натрия, калия, магния и после них сульфаты калия и магния. Порядок кристаллизации солей и состав образующихся осадков может несколько изменяться в зависимости от температуры, скорости испарения и других условий.
Поваренная соль, находящаяся на влажном воздухе, отсыревает. Чистый хлорид натрия — негигроскопичное вещество, т. е. не притягивает влагу. Гигроскопичны хлориды магния и кальция. Их примеси почти всегда содержатся в поваренной соли и благодаря им происходит поглощение влаги.
В земной коре довольно часто встречаются пласты каменной соли. Поваренная соль является важнейшим сырьем химической промышленности. Из нее получают соду, хлор, хлороводородную кислоту, гидроксид натрия, металлический натрий.
При изучении свойств почв ученые установили, что, будучи пропитанными хлоридом натрия, они не пропускают воду. Это открытие было использовано при строительстве оросительных каналов и водоемов. Если дно водоема покрыть слоем земли, пропитанной NaCl, то утечки воды не происходит. Для этой цели, конечно, применяют техническую соль. Строители используют хлорид натрия для устранения смерзания зимой земли и превращения ее в твердый камень. Для этого участки грунта, которые планируется вынимать, осенью густо посыпают NaCl. В этом случае в сильные морозы данные участки земли остаются мягкими.
Химики хорошо знают, что смешением мелкоизмельченного льда с поваренной солью можно получить эффективную охлаждающую смесь. Например, смесь состава 30 г NaCl на 100 г льда охлаждается до температуры -20 С0 происходит потому, что водный раствор соли замерзает при отрицательных температурах. Следовательно, лед, имеющий температуру около 0°С, будет плавиться в таком растворе, отнимая теплоту от окружающей среды. Это свойство смеси льда и поваренной соли могут с успехом использовать также и домохозяйки.
Спички
Высекание искр при ударе камня о кусок пирита FeS2 и поджигание ими обуглившихся кусков дерева или растительных волокон было способом получения огня человеком.
Поскольку способы получения огня были несовершенны и трудоемки, человеку приходилось постоянно поддерживать горящий источник огня. Для перенесения огня в Древнем Риме использовали деревянные палочки, обмакнутые в расплав серы.
Приспособления для получения огня, основанные на химических реакциях, начали делать в конце XVIII в. Вначале это были древесные лучинки, на кончике которых в виде головки закреплялись хлорат калия (бертолетова соль КС1Оз) и сера. Головка погружалась в серную кислоту, происходила вспышка и лучинка загоралась. Человек был вынужден хранить и обращаться с небезопасной серной кислотой, что было крайне неудобно. Тем не менее это химическое «огниво» можно рассматривать как прародитель современных спичек.
В начале XIX в. немецкий химик Деберейнер изобрел более совершенное, но и более сложное огниво. Им было установлено, что струя водорода, направленная на губчатую платину, воспламеняется на воздухе.
Губчатая платина играет роль катализатора. Для использования этого средства при получении огня в быту им был создан небольшой стеклянный прибор (по типу ранее изобретенного Киппом аппарата, носящего его имя). Водород получался приведением в контакт металлического цинка и серной кислоты. Таким образом, получение пламени и его тушение обеспечивалось поворотом крана, приводящего в контакт (или разделяющего) серную кислоту и цинк. Огниво Деберейнера можно считать прародителем современной газовой или бензиновой зажигалки.
В современной зажигалке воспламенение горючего производится под действием искры, получающейся от сгорания мельчайшей частицы «кремня», срезанной зубчатым колесиком. «Кремень» представляет собой смесь редкоземельных металлов (лантаноидов). В мелкораздробленном состоянии эта смесь пирофорна, т. е. самовоспламеняется на воздухе, образуя искру.
Однако более ранний пирофор изготавливали из смеси поташа К2СО3 и высушенных квасцов K2SO4 ∙ Al2(SO4)3.К нему добавляли мелкодисперсный уголь или сажу и нагревали до каления без доступа воздуха. Порошок охлаждали и помещали в герметически закрытый сосуд, откуда он мог извлекаться по мере необходимости, Для добывания огня порошок высыпался на трут, вату или тряпки и уже в воздухе воспламенялся. Считают, что при прокаливании на оставшихся частичках угля образуется мелкодисперсный металлический калий, который, окисляясь на воздухе, и служит инициатором воспламенения.
Важнейшим этапом на пути к современным спичкам было введение в состав массы спичечной головки белого фосфора (1833). Такие спички легко зажигались от трения о шероховатую поверхность. Однако при горении они создавали неприятный запах и главное, их производство было весьма вредно для рабочих. Пары белого фосфора приводили к тяжелейшему заболеванию — фосфорному некрозу костей. Прежде всего некрозу подвергались кости челюстей людей, так как фосфор проникал через кариозные зубы.
В 1847 г. было установлено, что белый фосфор при нагревании в закрытом сосуде без доступа воздуха превращается в другую модификацию — красный фосфор. Он гораздо менее летуч и практически не ядовит. Вскоре белый фосфор в головках спичек был заменен на красный. Такие спички зажигались лишь при трении о специальную поверхность из красного фосфора, клея и других веществ. Эти спички называли безопасными или шведскими, так как фабричным способом их впервые начади, изготавливать в Швеции в 1867—1869 гг.
Существует несколько разновидностей современных спичек. По назначению различают спички, зажигающиеся в обычных условиях, влагоупорные (рассчитанные на зажигание после хранения во влажных условиях, например в тропиках), ветровые (зажигающиеся на ветру) и др.
В качестве основного сырья для изготовления спичечной соломки с прошлого столетия используют главным образом осину и реже липу. Для этого с круглого очищенного от коры чурака специальным ножом по спирали снимается лента, которая затем рубится на спичечную соломку. При сгорании спички необходимо получить нетлеющий уголек от соломки и удержать на нем раскаленный шлак от сгоревшей головки. Необходимость последнего обусловливается стремлением обезопасить потребителя от прожогов одежды при попадании раскаленного шлака. Тлеющий уголек от соломки, естественно, представляет пожарную опасность. Для устранения тления соломки и закрепления шлака от головки соломку пропитывают веществами, образующими на ее поверхности при горении пленку. Благодаря этой пленке прекращается сгорание угля. Она же закрепляет шлак от головки. В качестве противотлеющих веществ используют фосфорную кислоту и ее соль (NH4)2HPO4.
За период более чем 150 лет было использовано большое количество рецептур зажигательных масс, из которых изготавливают головки спичек. Они являются сложными многокомпонентными системами. В них входят: окислители (КС1О3, КгСг2О7, МпО2), дающие кислород, необходимый для горения; горючие вещества (сера, животные и растительные клеи, сульфид фосфора P4S3); наполнители — вещества, предотвращающие взрывной характер горения головки (измельченное стекло, Fe2Оз); склеивающие вещества (клеи), которые одновременно являются и горючими; стабилизаторы кислотности (ZnO, СаСОз и др.); вещества, окрашивающие спичечную массу в определенный цвет (органические и неорганические красители).
По количеству кислорода, выделяемого на одну массовую часть, хромпик К2Сr2О7 уступает бертолетовой соли КСlO3, но зажигательные составы, содержащие первый окислитель, воспламеняются значительно легче. Кроме того, хромпик улучшает качество шлака.
Пиролюзит MnO2 играет двойную роль: катализатора разложения бертолетовой соли и источника кислорода. Оксид железа (III) Fe2O3 также выполняет две функции. Он является минеральной краской (цвет ржавчины) и существенно уменьшает скорость горения массы, делая горение более спокойным.
Температура горения спичечных головок достигает 1500 0C, а температура их воспламенения лежит в пределах 180 – 200 0С.
Фосфорная (терочная) масса также является
Бумага и карандаши
Сохранились документы, указывающие на то, что в 105 г. н. э. министр китайского императора организовал производство бумаги из растений с добавками тряпья. Около 800.г. такая бумага получила широкое распространение в Китае, а также на Ближнем Востоке. Знакомство с бумагой европейцев связано с крестовыми походами на Ближний Восток — в Сирию, Палестину, Северную Африку, организованными западно-европейскими феодалами и католической церковью (первый поход состоялся в 1096—1099 гг.). В эпоху раннего средневековья (до начала крестовых походов) для письма в Европе использовался главным образом папирус. В Италии им пользовались еще в XII в.
Письменность же была известна в Египте и Месопотамии с конца IV и начала III тысячелетия до н. э., т. е. задолго до изобретения бумаги. Как уже было отмечено, основными предшественниками бумаги как материала, на которое наносилось письмо, были папирус и пергамент.
Растение папирус (Cyperus papyrus) произрастает в Египте в болотистой местности около реки Нила. Стебель растения очищали от коры и луба и из белоснежного материала нарезали тонкие полосы. Их укладывали слоями вдоль и поперек, а затем механическим давлением выжимали из них растительный сок. Этот сок сам обладает способностью склеивать полосы папируса. Позднее для скрепления полос стали применять клей, приготовленный из невыделанных шкур или муки. После высушивания на солнце получающиеся листы шлифовали камнем или кожей. Папирус для письма стали изготовлять около 4000 лет назад. Считают, что и название бумаги (papiera) происходит от слова папирус.
Пергамент — это невыделанная, но освобожденная от волос и обработанная известью звериная, овечья или козлиная кожа. Так же, как и папирус, пергамент — прочный и долговечный материал. Хотя бумага менее прочна и долговечна, она более дешева и потому более доступна для широкого использования.
Волокна целлюлозы в древесине связаны между собой лигнином. Для удаления лигнина и освобождения от него целлюлозы проводят варку древесины. Распространенным способом варки является сульфитный. Он был разработан в США в 1866 г., а первый завод по данной технологии был построен в Швеции в 1874 г. Широкое промышленное значение способ получил с 1890 г По этому способу для отделения лигнина и некоторых других веществ, содержащихся в древесине, последняя варится в сульфитном щелоке, который состоит из Са(НSОз)2, H2SO3 и SO2.
Для обеспечения прочности соединения частиц пигментов с бумагой-основой требуются связующие. Часто их роль выполняют вещества, обеспечивающие проклейку бумаги. В качестве минеральных пигментов широко используют каолин — землистую массу, близкую по составу к глинам, но по сравнению с последними характеризующуюся пониженной пластичностью и повышенной белизной. Одним из старейших наполнителей является карбонат кальция (мел), потому такие бумаги и назвали мелованными. К известным пигментам также относятся диоксид титана ТiO2 и смесь гидроксида кальция Са(ОН)2 (гашеной извести) и сульфата алюминия A12(SO4)3. Последний, по существу, является смесью сульфата кальция CaSO4 и гидроксида алюминия А1(ОН)з, которые получаются в результате обменной реакции.
Для изготовления рабочей части графитового карандаша готовят смесь графита и глины с добавкой небольшого количества гидрированного подсолнечного масла. В зависимости от соотношения графита и глины получают грифель различной мягкости — чем больше графита, тем более мягкий грифель. Смесь перемешивают в шаровой мельнице в присутствии воды в течение 100 ч. Приготовленную массу пропускают через фильтр-прессы и получают плиты. Их подсушивают, а затем из них выдавливают на шприц-прессе стержень, который режут на части определенной длины. Стержни в специальных приспособлениях высушивают и исправляют возникшую кривизну. Затем их обжигают при температуре 1000—1100°С в шахтных тиглях.
В состав грифелей цветных карандашей входят каолин, тальк, стеарин (широкому кругу людей он известен как материал для изготовления свечей) и стеарат кальция (кальциевое мыло). Стеарин и стеарат кальция являются пластификаторами. В качестве связывающего материала используют карбоксиметилцеллюлозу. Это клей, используемый для наклейки обоев. Здесь его также предварительно заливают водой для набухания. Кроме того, в грифели вводят соответствующие красители, как правило, это органические вещества. Такую смесь перемешивают (вальцуют на специальных машинах) и получают в виде тонкой фольги. Ее измельчают и полученным порошком набивают пистолет, из которого и шприцуют смесь в виде стержней, которые режут на куски определенной длины и затем сушат. Для окраски поверхности цветных карандашей используют те же пигменты и лаки, которыми обычно окрашивают детские игрушки. Подготовку деревянной оснастки и ее обработку проводят так же, как и для графитовых карандашей.
Стекло
История стекла уходит в глубокую древность. Известно, что в Египте и Месопотамии его умели делать уже 6000 лет назад. Вероятно, стекло начали изготавливать все же позже, чем первые керамические изделия, так как для его производства требовались более высокие температуры, чем для обжига глины. Если для простейших керамических изделий было достаточно только глины, то в состав стекла необходимо минимум три компонента.
В стекловарении используют только самые чистые разновидности кварцевого песка, в которых общее количество загрязнений не превышает 2—3 %. Особенно нежелательно присутствие железа, которое даже в ничтожных количествах (десятые доли %) окрашивает стекло в зеленоватый цвет. Если к песку добавить соду Na2CO3, то удается сварить стекло при более низкой температуре.(на 200—300°). Такой расплав будет иметь менее вязкий (пузырьки легче удаляются при варке, а изделия легче формуются). Но! Такое стекло растворимо в воде, а изделия из него подвергаются разрушению под влиянием атмосферных воздействий. Для придания стеклу нерастворимости в воде в него вводят третий компонент — известь, известняк, мел. Все они характеризуются одной и той же химической формулой — СаСО3.
Стекло, исходными компонентами шихты которого является кварцевый песок, сода и известь, называют натрий-кальциевым. Оно составляет около 90 % получаемого в мире стекла. При варке карбонат натрия и карбонат кальция разлагаются в соответствии с уравнениями:
Na2CO3 → Na2O + CO2
СаСОз → СаО + СО2
В результате в состав стекла входят оксиды SiO2, Na2O и СаО. Они образуют сложные соединения — силикаты, которые являются натриевыми и кальциевыми солями кремниевой кислоты.
В стекло вместо Na2O с успехом можно вводить К2О, а СаО может быть заменен MgO, PbO, ZnO, BaO. Часть кремнезема можно заменить на оксид бора или оксид фосфора (введением соединений борной или фосфорной кислот). В каждом стекле содержится немного глинозема Аl2О3, попадающего из стенок стекловаренного сосуда. Иногда его добавляют специально. Каждый из перечисленных оксидов обеспечивает стеклу специфические свойства. Поэтому, варьируя этими оксидами и их количеством, получают стекла с заданными свойствами. Например, оксид борной кислоты В2О3 приводит к понижению коэффициента теплового расширения стекла, а значит, делает его более устойчивым к резким температурным изменениям. Свинец сильно увеличивает показатель преломления стекла. Оксиды щелочных металлов увеличивают растворимость стекла в воде, поэтому для химической посуды используют стекло с малым их содержанием.
Окраску стекла осуществляют введением в него оксидов некоторых металлов или образованием коллоидных частиц определенных элементов. Так, золото и медь при коллоидном распределении окрашивают стекло в красный цвет. Такие стекла называют золотым и медным рубином соответственно. Серебро в коллоидном состоянии окрашивает стекло в желтый цвет. Хорошим красителем является селен. В коллоидном состоянии он окрашивает стекло в розовый цвет, а в виде соединения CdS • 3CdSe — в красный. Такое стекло называют селеновым рубином. При окраске оксидами металлов цвет стекла зависит от его состава и от количества оксида-красителя. Например, оксид кобальта(II) в малых количествах дает голубое стекло, а в больших — фиолетово-синее с красноватым оттенком. Оксид меди (II) в натрий-кальциевом стекле дает голубой цвет, а в калиево-цинковом — зеленый. Оксид марганца (II) в натрий-кальциевом стекле дает красно-фиолетовую окраску, а в калиево-цинковом — сине-фиолетовую. Оксид свинца (II) усиливает цвет стекла и придает цвету яркие оттенки.
Существуют химические и физические способы обесцвечивания стекла. В химическом способе стремятся все содержащееся железо перевести в Fe3+. Для этого в шихту вводят окислители — нитраты щелочных металлов, шиоксид церия СеО2, а также оксид мышьяка (III) AS2O3 и оксид сурьмы(III) Sb2O3. Химически обесцвеченное стекло лишь слегка окрашено (за счет ионов Fe3+) в желтовато-зеленоватый цвет, но обладает хорошим светопропусканием. При физическом обесцвечивании в состав стекла вводят «красители», т. е. ионы, которые окрашивают его в дополнительные тона к окраске, создаваемой ионами железа, — это оксиды никеля, кобальта, редкоземельных элементов, а также селен. Диоксид марганца MnO2 обладает свойствами как химического, так и физического обесцвечивания. В результате двойного поглощения света стекло становится бесцветным, но его светопропускание понижается. Таким образом, следует различать светопрозрачные и обесцвеченные стекла, поскольку эти понятия различны.
В некоторых дворцах, парадных зданиях и культовых сооружениях в Европе в мелкие ячейки в оконных проемах вставляли пластинки слюды, которые ценились очень дорого. В домах простых людей для этой цели использовались бычий пузырь и промасленная бумага или ткань. В середине XVI в. даже во дворцах французских королей окна закрывались промасленным полотном или бумагой. Лишь в середине XVII в. при Людовике XIV в окнах его дворца появилось стекло в виде маленьких квадратиков, вставленных в свинцовый переплет. Листовое стекло большой площади долго не умели получать. Поэтому даже в XVIII в. застекленные окна имели мелкий переплет. Обратите внимание на реставрированные здания петровской эпохи, например на Меньшиковский дворец в Санкт-Петербурге. Однако вернемся к истокам производства оконного стекла.
В конце средневекового периода в Европе начали широко применять «лунный» способ изготовления листового стекла. В его основу также был положен метод выдувания. При этом способе вначале выдувался шар, затем он сплющивался, к его дну припаивалась ось, а около выдувательной трубки заготовка обрезалась. В результате получалось подобие вазы с припаянной ножкой-осью. Раскаленная «ваза» вращалась с большой скоростью вокруг оси и под действием центробежной силы превращалась в плоский диск. Толщина такого диска была 2—3 мм, а диаметр доходил до 1,5 м. Далее диск отделялся от оси и отжигался. Такое стекло было гладким и прозрачным. Характерная его особенность — наличие в центре диска утолщения, которое специалисты называют «пупком». Лунный способ производства сделал листовое стекло доступным для населения. Однако на смену ему уже в начале XVIII в. пришел другой более совершенный «халявный» способ, который использовался во всем мире почти в течение двух столетий. По существу, это было усовершенствование средневекового способа выдувания, в результате которого получался цилиндр. «Халявой» называли формируемую массу стекла на конце выдувной трубки. Она доходила до 15—20 кг и из нее в итоге получались листы стекла площадью до 2—2,5 м2.
Мелкие стеклянные изделия делают матовыми обработкой фтороводородной (плавиковой) кислотой. Последняя взаимодействует с диоксидом кремния, находящимся на поверхности, с образованием летучего тетрафторида кремния SiF4 в соответствии с уравнением
SiO2 + 4HF = SiF4 + 2H2O
Фотохромные стекла изменяют окраску под действием излучения. В настоящее время получили распространение очки со стеклами, которые при освещении темнеют, а в отсутствие интенсивного освещения вновь становятся бесцветными. Такие стекла применяют для защиты от солнца сильно остекленных зданий и для поддержания постоянной освещенности помещений, а также на транспорте. Фотохромные стекла содержат оксид бора В2О3, а светочувствительным компонентом является хлорид серебра AgCl в присутствии оксида меди(I) Cu2O. При освещении происходит процесс
![]()
Выделение атомарного серебра приводит к потемнению стекла. В темноте реакция протекает в обратном направлении. Оксид меди(I) играет роль своеобразного катализатора.
Хрусталь, хрустальное стекло — это силикатное стекло, содержащее различное количество оксида свинца. Часто на маркировке изделия указывается содержание свинца. Чем больше его количество, тем выше качество хрусталя. Хрусталь характеризуется высокой прозрачностью, хорошим блеском и большой плотностью. Изделия из хрусталя в руке чувствуются по массе.
Строго хрусталем называют свинцово-калиевое стекло. Хрустальное стекло, в котором часть КгО заменена на Na2O, а часть РbО заменена на CaO, MgO, BaO или ZnO, называют полухрусталем.
Считают, что хрусталь был открыт в Англии в XVII столетии.
Кварцевое стекло. Его получают плавлением чистого кварцевого песка или горного хрусталя, имеющих состав SiO2. Для изготовления кварцевого стекла требуется очень высокая температура (выше 1700 °С).
Расплавленный кварц обладает высокой вязкостью и из него трудно удаляются пузырьки воздуха. Поэтому кварцевое стекло часто легко узнается по заключенным в нем пузырькам. Важнейшим свойством кварцевого стекла является способность выдерживать любые температурные скачки. Например, кварцевые трубы диаметром 10—30 мм выдерживают многократное нагревание до 800—900 °С и охлаждение в воде. Брусья из кварцевого стекла, охлаждаемые с одной стороны, сохраняют на противоположной стороне температуру 1500 °С и потому используются в качестве огнеупоров. Тонкостенные изделия из кварцевого стекла выдерживают резкое охлаждение на воздухе от температуры выше 1300 °С и потому с успехом используются для высокоинтенсивных источников света. Кварцевое стекло из всех стекол наиболее прозрачно для ультрафиолетовых лучей. На этой прозрачности отрицательно сказываются примеси оксидов металлов и особенно железа. Поэтому для производства кварцевого стекла, идущего на изделия для работы с ультрафиолетовым излучением, предъявляются особо жесткие требования к чистоте сырья. В особо ответственных случаях кремнезем очищается переводом в тетрафторид кремния SiF4 (действием плавиковой кислоты) с последующим разложением водой на диоксид кремния SiO2 и фтороводород HF.
Кварцевое стекло прозрачно и в инфракрасной области.
Ситаллы — стеклокристаллические материалы, получаемые регулируемой кристаллизацией стекла. Стекло, как известно, — это твердый аморфный материал. Его самопроизвольная кристаллизация в прошлом приносила убытки на производстве. Обычно стекломасса довольно стабильна и не кристаллизуется. Однако при повторном нагревании изделия из стекла до определенной температуры стабильность стекломассы снижается и она переходит в тонкозернистый кристаллический материал. Технологи научились проводить процесс кристаллизации стекла, исключая что растрескивание.
Ситаллы обладают высокой механической прочностью и термостойкостью, водоустойчивы и газонепроницаемы, характеризуются низким коэффициентом расширения, высокой диэлектрической проницаемостью и низкими диэлектрическими потерями. Они применяются для изготовления трубопроводов, химических реакторов, деталей насосов, фильер для формования синтетических волокон, в качестве футеровки электролизных ванн и материала для инфракрасной оптики, в электротехнической и электронной промышленности.
Прочность, легкость и огнестойкость обусловили применение ситаллов в жилищном и промышленном строительстве. Из них изготавливают навесные самонесущие панели наружных стен зданий, перегородки, плиты и блоки для внутренней облицовки стен, мощения дорог и тротуаров, оконные коробки, ограждения балконов, лестничные марши, волнистую кровлю, санитарно-техническое оборудование. В быту с ситаллами чаще встречаются в виде белой непрозрачной жаростойкой кухонной посуды. Установлено, что ситаллы выдерживают около 600 резких тепловых смен. Изделия из ситаллов не царапаются и не прогорают. Их можно снять с плиты в раскаленном до красна состоянии и опустить в ледяную воду, извлечь из холодильника и поставить на открытое пламя, не опасаясь растрескивания или разрушения.
Ситаллы — один из видов стеклокристаллических материалов, которые ведут свою историю всего лишь с 50-х годов текущего столетия, когда был выдан на них первый патент.
Пеностекло — пористый материал, представляющий собой стеклянную массу, пронизанную многочисленными
пустотами. Оно обладает тепло- и звукоизоляционными свойствами, небольшой плотностью (примерно в 10 раз легче кирпича) и высокой прочностью, сравнимой с бетоном. Пеностекло не тонет в воде и потому используется для изготовления понтонных мостов и спасательных принадлежностей. Однако его главная область применения — строительство. Пеностекло является исключительно эффективным материалом для заполнения внутренних и наружных стен зданий. Оно легко поддается механической обработке: пилением, резанием, сверлением и обтачиванию на токарном станке.
Стеклянная вата и волокно. При нагревании стекло размягчается и легко вытягивается в тонкие и длинные нити. Тонкие стеклянные нити не имеют и признаков хрупкости. Их характерным свойством является чрезвычайно высокое удельное сопротивление разрыву. Нить диаметром 3—5 мкм имеет сопротивление на разрыв 200—400 кг/мм2, т. е. приближается по этой характеристике к мягкой стали. Из нитей изготавливают стекловату, стекловолокно и стеклоткани. Не трудно догадаться об областях использования этих материалов. Стекловата обладает прекрасными тепло- и звукоизоляционными свойствами. Ткани, изготовленные из стеклянного волокна, обладают чрезвычайно высокой химической стойкостью. Поэтому их применяют в химической промышленности в качестве фильтров кислот, щелочей и химически активных газов. Вследствие хорошей огнестойкости стеклоткани применяют для пошива одежды пожарных и электросварщиков, театральных занавесей, драпировок, ковров и т. п. Стеклоткани кроме огнестойкости и химической стойкости обладают также высокими электроизоляционными
Посуда из стекла. Качество посуды зависит от состава стекла, способа ее выработки и характера декоративной обработки. Самым дешевым стеклом является
кальциево-натриевое. Для посуды улучшенного качества используют кальциево-натриево-калиевое стекло, а для посуды высших сортов — кальциево-калиевое. Самые лучшие сорта посуды изготавливают из хрусталя.
Посудные изделия вырабатывают выдуванием или прессованием. Выдувание, в свою очередь, бывает машинным и ручным. Способ выработки, естественно, отражается на качестве посуды. Сложные по форме и художественные изделия изготавливают только ручным способом. Прессованные изделия легко отличаются от выдутых характерными мелкими неровностями на поверхности, в том числе и на внутренней. На выдутых изделиях они отсутствуют.
Мыла и моющие средства
Мыло было известно человеку до новой эры летоисчисления. Ученые не располагают информацией о начале приготовления мыла в арабских странах и Китае. Самое раннее письменное упоминание о мыле в европейских странах встречается у римского писателя и ученого Плиния Старшего (23—79 гг.). В трактате «Естественная история» (в 37 томах), который, по существу, был энциклопедией естественно-научных знаний античности, Плиний писал о способах приготовления мыла омылением жиров. Мало того, он писал о твердом и мягком мыле, получаемом с использованием соды и поташа соответственно. Раньше для стирки одежды использовали щелок, получающийся от обработки золы водой. Скорее всего это было до того, как стало известно, что зола от сжигания топлива растительного происхождения содержит поташ.
Несмотря на то что в конце эпохи средневековья в разных странах существовала довольно развитая мыловаренная промышленность, химическая сущность процессов, конечно, была не ясна. Лишь на рубеже XVIII и XIX вв. была выяснена химическая природа жиров и внесена ясность в реакцию их омыления. В 1779 г. шведский химик Шееле показал, что при взаимодействии оливкового масла с оксидом свинца и водой образуется сладкое и растворимое в воде вещество. Решающий шаг на пути изучения химической природы жиров был сделан французским химиком Шеврелем. Он открыл стеариновую, пальмитиновую и олеиновую кислоты, как продукты разложения жиров при их омылении водой и щелочами. Сладкое вещество, полученное Шееле, было Шеврелем названо глицерином. Сорок лет спустя Бертло установил природу глицерина и объяснил химическое строение жиров. Глицерин — трехатомный спирт. Жиры — сложные эфиры глицерина (глицериды) тяжелых одноосновных карбоновых кислот, преимущественно пальмитиновой СНз(СН2)14СООН, стеариновой СН3(СН2)16COOH и олеиновой СН3(СН2)7СН=СН(СН2)7СООН. Их формулу и реакцию гидролиза можно описать следующим образом:
CH2OOCR1 R1COONa CH2OH
| |
CHOOCR2 + 3NaOH→R2COONa + СНОН
| |
CH2OOCR3R3COONa CH2OH
жир соли глице-
кислот рин
В состав различных жиров входят в различных соотношениях пальмитиновая, стеариновая, олеиновая и другие кислоты. В растительных (жидких) жирах преобладают непредельные кислоты (содержащие этиленовые связи), а в животных (твердых) —- предельные кислоты, т. е. не содержащие двойных связей. Потребности в твердых животных жирах большие, чем в растительных. Поэтому жидкие растительные жиры переводят в твердые каталитической гидрогенизацией. В этом процессе остатки непредельных кислот в глицеридах превращаются (присоединением водорода) в остатки предельных кислот. Например,
![]()
Именно так получают кулинарные жиры, масло для обжаривания, салатное масло, а также жиры, идущие на производство маргарина. Гидрированные жиры называют саломаслами (сало из масла).
Если попытаться дать определение, то мытьем можно назвать очистку загрязненной поверхности жидкостью, содержащей моющее вещество или систему моющих веществ. В качестве жидкости в быту используют главным образом воду. Хорошая моющая система должна выполнять двойную функцию: удалять загрязнение с очищаемой поверхности и переводить его в водный раствор. Значит, моющее средство также должно обладать двойной функцией: способностью взаимодействовать с загрязняющим веществом и переводить его в воду или водный раствор. Следовательно, молекула моющего вещества должна иметь гидрофобную и гидрофильную части. Фобос по-гречески означает страх, боязнь. Значит, гидрофобность означает боящийся, избегающий воду. Филео — по-гречески — люблю, а гидрофильность — любящий, удерживающий воду. Гидрофобная часть молекулы моющего вещества обладает способностью взаимодействовать с поверхностью гидрофобного загрязняющего вещества. Гидрофильная часть моющего вещества взаимодействует с водой, проникает в воду и увлекает с собой частицу загрязняющего вещества, присоединенную к гидрофобному концу.
В производстве мыла давно используют канифоль, которую получают при переработке живицы хвойных деревьев. Канифоль состоит из смеси смоляных кислот, содержащих в цепи около 20 углеродных атомов. В рецептуру хозяйственного мыла обычно вводят 12—15 % канифоли от массы жирных кислот, а в рецептуру туалетных мыл — не более 10 %. Введение канифоли в больших количествах делает мыло мягким и липким.
Процесс производства мыла состоит из химической и механической стадий. На первой стадии (варка мыла) получают водный раствор солей натрия (реже калия) жирных кислот или их заменителей (нафтеновых, смоляных). На второй стадии проводят механическую обработку этих солей — охлаждение, сушку, смешивание с различными добавками, отделку и упаковку.
Варку мыла заканчивают обработкой мыльного раствора (мыльного клея) избытком щелочи (NaOH) или раствором NaCl. В результате этого на поверхность раствора всплывает концентрированный слой мыла, называемый ядром. Полученное таким образом мыло называют ядровым, а процесс его выделения из раствора — отсолкой или высаливанием. При высаливании происходит повышение концентрации мыла и его очистка от белковых, красящих и механических примесей — так получают хозяйственное мыло.
Особое место среди наполнителей занимает сапонин, получаемый выщелачиванием некоторых растений и прежде всего мыльного корня. Он хорошо растворяется в воде и его растворы сильно пенятся. Поэтому сапонин используют для улучшения пенообразования и применяют для дорогих сортов мыл.
Кроме использования мыла в качестве моющего средства оно широко применяется при отделке тканей, в производстве косметических средств, для изготовления полировочных составов и водоэмульсионных красок. Имеется и не столь безобидное его применение. Алюминиевое мыло (алюминиевые соли смеси жирных и нафтеновых кислот) применяют в США для получения некоторых видов напалма — самовоспламеняющегося состава, используемого в огнеметах и зажигательных авиабомбах. Само слово напалм происходит от начальных слогов нафтеновой и пальмитиновой кислот. Состав напалма довольно простой — это бензин, загущенный алюминиевым мылом.
В настоящее время химическая промышленность выпускает большое количество различных синтетических моющих средств (стиральных порошков). Наибольшее практическое значение имеют соединения, содержащие насыщенную углеводородную цепь из 10—15 атомов углерода, так или иначе связанную с сульфатной или сульфонатной группой, например
Производство синтетических моющих средств основано на дешевой сырьевой базе, а точнее на продуктах переработки нефти и газа. Они, как правило, не образуют малорастворимых в воде солей кальция и магния.
Следовательно, многие из синтетических моющих средств одинаково хорошо моют как в мягкой, так и в жесткой воде. Некоторые средства пригодны даже для стирки в морской воде. Синтетические моющие средства действуют не только в горячей воде, как это характерно для хозяйственного мыла, но и в воде при сравнительно низких температурах, что важно при стирке тканей из искусственных волокон. Наконец, концентрация синтетических моющих веществ даже в мягкой воде может быть гораздо ниже, чем мыла, полученного из жиров. Синтетические моющие средства обычно представляют довольно сложную композицию, поскольку в них входят различные добавки: оптические отбеливатели, химические отбеливатели, ферменты, пенообразователи, смягчители.
Химические средства гигиены и косметики
Слово гигиена происходит от греч. гигиенос, что означает целебный, приносящий здоровье, а косметика — от греч., означающее искусство украшать.
Одним из путей профилактики кариеса является очистка зубов и полоскание ротовой полости после приема пищи. Это приводит к предотвращению образования мягкого налета и зубного камня.
Трудно сказать, когда люди начали чистить зубы, но имеются сведения, что одним из древнейших препаратов для чистки зубов была табачная зола.
Важнейшим средством ухода за зубами являются зубные пасты. Они имеют меньшую истирающую способность по сравнению с порошками, более удобны в применении и характеризуются более высокой эффективностью. Зубные пасты — это многокомпонентные составы. Они подразделяются на гигиенические и лечебно-профилактические. Первые оказывают только очищающее и освежающее действие, а вторые, кроме того, служат для профилактики заболеваний и способствуют лечению зубов и полости рта.
Основные компоненты зубной пасты следующие: абразивные, связующие, загустители, пенообразующие. Абразивные вещества обеспечивают механическую очистку зуба от налетов и его полировку. В качестве абразивов чаще всего применяют химически осажденный мел СаСО3. Установлено, что компоненты зубной пасты способны влиять на минеральную составляющую зуба и, в частности, на эмаль. Поэтому в качестве абразивов стали применять фосфаты кальция: СаНРО4, Са3(РО4)2, Са2Р2О7, а также малорастворимый полимерный мета-фосфат натрия (NaРОз). Кроме того, в качестве абразивов в различных сортах паст применяют оксид и гидроксид алюминия, диоксид кремния, силикат циркония, а также некоторые органические полимерные вещества, например метилметакрилат натрия. На практике часто используют не одно абразивное вещество, а их смесь.
Из синтетических веществ широкое применение нашли производные клетчатки (хлопковой и древесной) — натрийкарбоксиметилцеллюлоза, оксиэтилированные этиловый и метиловый эфиры целлюлозы или просто этиловый и метиловый эфиры целлюлозы.
Борьбу с кариесом при помощи лечебно-профилактических зубных паст ведут по двум направлениям: 1) укрепление минеральной ткани зуба; 2) предупреждение образования зубного налета. Первое достигается введением в пасты соединений фтора: монофторфосфата натрия, формулу которого условно можно записать в виде двойной соли NaF∙NaPO3, а также фторида натрия NaF и фторида олова (II) SnF2. Существуют две точки зрения на влияние фторидных ионов на укрепление эмали зуба. 1. Ионы F![]() переводят гидроксидапатит эмали СаОН(РО4)з в менее растворимый в кислотах фто-рапатит Ca5F(PO4)з. 2. В результате обменной реакции в пасте образуется CaF2, который адсорбируется на гидроксидапатите и предохраняет его от воздействия кислот. Известно также, что фторидные соединения способствуют подавлению жизнедеятельности бактерий, вызывающих образование в полости рта органических кислот. В настоящее время в антикариесных пастах стали широко использовать ферменты, а иногда в них вводят антибиотики.
переводят гидроксидапатит эмали СаОН(РО4)з в менее растворимый в кислотах фто-рапатит Ca5F(PO4)з. 2. В результате обменной реакции в пасте образуется CaF2, который адсорбируется на гидроксидапатите и предохраняет его от воздействия кислот. Известно также, что фторидные соединения способствуют подавлению жизнедеятельности бактерий, вызывающих образование в полости рта органических кислот. В настоящее время в антикариесных пастах стали широко использовать ферменты, а иногда в них вводят антибиотики.
Дезодоранты и озоновый «щит» планеты.
Дезодоранты — это средства, устраняющие неприятный запах пота. На чем основано их действие? Пот выделяется особыми железами, расположенными в коже на глубине 1—3 мм. У здоровых людей на 98—99 % он состоит из воды. С потом из организма выводятся продукты метаболизма: мочевина, мочевая кислота, аммиак, некоторые аминокислоты, жирные кислоты, холестерин, в следовых количествах белки, стероидные гормоны и др. Из минеральных компонентов в состав пота входят ионы натрия, кальция, магния, меди, марганца, железа, а также хлоридные и иодидные анионы. Неприятный запах пота связан с бактериальным расщеплением его составляющих или с окислением их кислородом воздуха. Дезодоранты (косметические средства от пота) бывают двух типов. Одни тормозят разложение выводимых с потом продуктов метаболизма путем инактивации микроорганизмов или предотвращением окисления продуктов потовыделения. Действие второй группы дезодорантов основано на частичном подавлении процессов потовыделения. Такие средства называют антиперспиранами. Этими свойствами обладают соли алюминия, цинка, циркония, свинца, хрома, железа, висмута, а также формальдегид, таннины, этиловый спирт. На практике из солей в качестве антиперспиранов чаще всего используют соединения алюминия. Перечисленные вещества взаимодействуют с компонентами пота, образуя нерастворимые соединения, которые закрывают каналы потовых желез и тем самым уменьшают потовыделение. В оба типа дезодорантов вводят отдушки.
Концентрация озона в атмосфере зависит от содержания оксидов азота и фторхлорметанов. Оксиды азота постоянно присутствуют в низких концентрациях в результате фотохимического взаимодействия азота и кислорода. Оксид азота (II) разрушает озон, а оксид азота (IV) связывает атомарный кислород в соответствии с уравнениями
О3 + NO → NO2 + О2
NO2 + O → NO + О2
Оз + О → 2О2
Таким образом, оксиды азота играют роль катализаторов в разложении озона.
За 4,6 млрд. лет существования нашей планеты установилось равновесие, и жизнь на Земле возникла и развилась при определенном равновесном составе атмосферы. Однако интенсивное развитие сверхзвуковой авиации начинает оказывать влияние на создавшееся в атмосфере равновесие. Поскольку сверхзвуковые самолеты предназначены для полетов в стратосфере, верхний предел которой подходит к «озоновому» слою, то появляется опасность влияния сверхзвуковой техники на этот слой. При сгорании топлива в двигателях самолетов в довольно больших количествах образуются оксиды азота.
Другим источником опасности озоновому слою являются фторхлорметаны (главным образом CF2CI2 и CFCl3). Эти вещества широко используют в баллонах в аэрозольной упаковке, а также в качестве хладоагентов в промышленных и бытовых холодильниках.
Косметические средства.
В мире считается, что среди наиболее прибыльных отраслей промышленности на одном из первых мест стоит косметическая. Наблюдения показывают, что если нужно, то женщины могут отказать себе во многом, только не в том, что сделает их хотя бы чуточку красивее.
Искусство косметики уходит в далекое прошлое. Так, при раскопках найдены египетские мумии, ногти которых раскрашены. В усыпальницах египетских пирамид обнаружены натуральные краски и косметические инструменты, различные плитки для приготовления смеси красок и румян, сосуды для хранения мазей и масел. Найден письменный документ — папирус Эберса, в котором изложены косметические правила и рецепты. Его написание относят к пятому тысячелетию до новой эры.
Древние рукописи свидетельствуют, что уже тысячи лет назад женщины Востока подкрашивали веки в голубой цвет тончайшей пыльцой из толченой бирюзы. Бирюза — это природный минерал, имеющий состав СuА16(РО4)4(ОН)8∙4Н2О.
С незапамятных времен для подкрашивания бровей использовался мягкий природный минерал — сурьмяный блеск Sb2S3. В русском языке было выражение «сурьмить брови». Сурьмяный блеск поставлялся в различные страны арабами, которые называли его стиби. От этого названия и пошло латинское стибиум, означавшее в древности не химический элемент, а его сульфид Sb2S3. Природный сурьмяный блеск имеет цвет от серого до черного с синей или радужной побежалостью.
Достоверно известно, что в России косметические краски применялись в конце XVI и особенно широко в XVII в.
Промышленность выпускает перламутровые губные помады и кремы, а также шампуни с перламутровыми блесками. Перламутровый эффект в косметических средствах создается солями висмутила ВiOСl и BiO(NO3) или титанированной слюдой — перламутровым порошком, содержащим около 40 % ТiO2. Давно известны жемчужные или испанские белила. Их основным компонентом является BiO(NO3)2, образующийся при растворении нитрата висмута Bi(NO3)з в воде. В косметике эти белила используют для приготовления белого грима.
Для создания специальных косметических средств (гримов) применяют оксид цинка ZnO, получаемый прокаливанием основного карбоната (ZnOH)2CO3. В медицине его используют в присыпках (в качестве вяжущего, подсушивающего, дезинфицирующего средства) и для изготовления мазей.
Косметические декоративные пудры — многокомпонентные смеси. В них входят: тальк, каолин, ZnO, TiO2, MgCO3, крахмал, цинковые и магниевые соли стеариновой кислоты, а также органические и неорганические пигменты, в частности Fe2O3. Тальк придает пудре сыпучесть и скользящий эффект. Его недостатком является способность впитываться в кожу и придавать жирный блеск. Тем не менее, в состав пудр он входит в количестве до 50—80 %. Каолин обладает высокой укрывистостью и способностью впитывать избыток жировых выделений кожи. Его повышенная гигроскопичность способствует слеживаемости и неравномерному распределению пудры на коже, поэтому каолин вводят не более 25 %. Оксиды цинка и титана обладают хорошей укрывистостью. Кроме того, оксид цинка обладает антисептическими свойствами и потому одновременно выполняет роль дезинфицирующей добавки. Эти оксиды вводят в пудры до 15 %. В больших количествах они приводят к сухости кожи. Крахмал придает коже бархатистость, а благодаря стеаратам цинка и магния пудра хорошо удерживается на коже и делает ее гладкой.
Компактная пудра в отличие от рассыпной содержит связующие добавки: натрийкарбоксиметилцеллюлозу, высшие жирные кислоты, воски, многоатомные спирты и их эфиры, минеральные и растительные масла. Они позволяют получать при прессовании брикеты определенной формы, которые сохраняют прочность при длительном употреблении.
В быту в качестве дезинфицирующего и отбеливающего средства широко используют растворы (3, 6, 10 %-ные) пероксида водорода. Более концентрированный — 30%-ный раствор пероксида водорода — называют пергидролем, Пероксид водорода — неустойчивое (особенно на свету) химическое соединение. Оно разлагается на воду и кислород:
2Н2О2 = 2Н2О + О2
В момент образования кислород находится в атомарном состоянии и лишь затем переходит в молекулярный:
2О = О2
Атомарный кислород обладает особенно сильным окислительным свойством. Благодаря ему растворы пероксида водорода разрушают красящие вещества и отбеливают ткани из хлопчатобумажных и шерстяных тканей, шелк, перья, волосы. Способность пероксида водорода обесцвечивать волосы используют в косметике. Она основана на взаимодействии атомарного кислорода с красящим веществом волос меланином — смесью сложных органических веществ. При окислении меланин переходит в бесцветное соединение. Следует помнить, что пергидроль вызывает ожоги кожи и слизистых оболочек.
В настоящее время для окраски волос имеется большой ассортимент различных органических красителей.
![]()
![]() Иногда же для этой цели применяют соли серебра, меди, никеля, кобальта, железа. В таком случае крашение волос осуществляют при помощи двух растворов. Один из них содержит соли данных металлов: нитраты, цитраты, сульфаты или хлориды, а второй — восстановители: пирогаллол, таннин и др. При смешении этих растворов ионы металлов восстанавливаются до атомов, которые и осаждаются на поверхности волос.
Иногда же для этой цели применяют соли серебра, меди, никеля, кобальта, железа. В таком случае крашение волос осуществляют при помощи двух растворов. Один из них содержит соли данных металлов: нитраты, цитраты, сульфаты или хлориды, а второй — восстановители: пирогаллол, таннин и др. При смешении этих растворов ионы металлов восстанавливаются до атомов, которые и осаждаются на поверхности волос.
Наиболее распространенный лак для ногтей представляет раствор нитроцеллюлозы в органических растворителях. Нитроцеллюлозу получают нитрованием целлюлозы (хлопковой или древесной) смесью азотной и серной кислот. Она является сложным эфиром азотной кислоты и характеризуется общей формулой [С6Н7О2(ОН)3-X(ОNO2)X]N. В качестве растворителей используют амиловый эфир уксусной кислоты, ацетон, различные спирты, этиловый эфир, а также их смеси. В лак добавляют пластификаторы — касторовое масло или другие экстракты, которые препятствуют обезжириванию ногтей и предохраняют их ломкость.
Химия в земледелии
Земля как планета солнечной системы существует около 4,6 млрд. лет. Считают, что жизнь на ней зародилась 800—1000 тыс. лет назад. Ученые обнаружили следы деятельности первобытного человека, возраст которых оценивается 600—700 тыс. лет. Эра земледелия насчитывает всего лишь 17 тыс. лет.
За многомиллионные эпохи вода, воздух, а затем и живые организмы разрушали и измельчали каменные породы земной коры. Отмирая, живые организмы образовывали перегной или, как его называют ученые, гумус. Он смешивался с измельченной породой, склеивал и цементировал ее. Так зарождалась почва на нашей планете. Первая почва послужила основой развития последующих более крупных растений, которые, в свою очередь, способствовали новому ускоренному образованию гумуса. Еще с большим ускорением процесс почвообразования стал протекать с появлением животных, особенно населявших почвенный слой. Превращению органического вещества в гумус способствовали различного рода бактерии. Образование и распад органических веществ в почве считается главной причиной почвообразования.
Таким образом, почва состоит из минеральной и органической (гумуса) частей. Минеральная часть составляет от 90 до 99 % и более от всей массы почвы. В ее состав входят почти все элементы периодической системы Д. И. Менделеева
Почва как ионообменник из катионов «заряжена» главным образом ионами кальция Са2+, в меньшей мере — магния Mg2+ и еще в меньшей мере ионами аммония NH![]() , натрия Na+ и калия К+. Ионы кальция Са2+ и магния Mg2+ способствуют поддержанию прочной структуры почвы. Под структурностью почвы работники сельского хозяйства понимают ее способность распадаться на отдельные комочки. Ионы К+ или NH
, натрия Na+ и калия К+. Ионы кальция Са2+ и магния Mg2+ способствуют поддержанию прочной структуры почвы. Под структурностью почвы работники сельского хозяйства понимают ее способность распадаться на отдельные комочки. Ионы К+ или NH![]() и особенно Na+, напротив, способствуют разрушению структурных агрегатов почвы и усиливают вымывание гумуса и минеральных веществ. Во влажном состоянии такая почва становится липкой, а в сухом — превращается в глыбы, не поддающиеся обработке (солонец). Вытекающая из такой почвы вода имеет цвет чайного настоя, что указывает на потерю гумуса.
и особенно Na+, напротив, способствуют разрушению структурных агрегатов почвы и усиливают вымывание гумуса и минеральных веществ. Во влажном состоянии такая почва становится липкой, а в сухом — превращается в глыбы, не поддающиеся обработке (солонец). Вытекающая из такой почвы вода имеет цвет чайного настоя, что указывает на потерю гумуса.
Важное значение играет химическое связывание почвой анионов некоторых кислот. Нитратные NO![]() и хлоридные Сl
и хлоридные Сl![]() анионы не дают малорастворимых соединений с катионами, обычно содержащимися в почве.
анионы не дают малорастворимых соединений с катионами, обычно содержащимися в почве.
Напротив, анионы фосфорной, угольной, серной кислот образуют с ионами кальция малорастворимые соединения. Это и обусловливает химическую поглотительную способность почв.
Навоз.
В навозе в среднем содержится 0,5 % связанного в химические соединения азота, 0,25 % фосфора и 0,6 % калия. Содержание этих питательных элементов зависит от вида скота, характера скармливаемых кормов, от вида подстилки и других факторов. Кроме азота, фосфора и калия навоз содержит все элементы, включая и микроэлементы, необходимые для жизни растений. В качестве подстилки используют солому, опилки, но наилучшей считается торф. Подстилка позволяет лучше сохранять в навозе питательные вещества.
Минеральные удобрения.
В мире минеральные удобрения начали применять сравнительно недавно. Инициатором и активным поборником их использования в земледелии был немецкий химик Юстус Либих. В 1840 г. он выпустил в свет книгу «Химия в приложении к земледелию». В 1841г. по его почину в Англии была построена первая суперфосфатная установка. Калийные удобрения начали производить в 70-х годах прошлого века. Минеральный азот в то время поставлялся в почву с чилийской селитрой. Следует отметить, что в настоящее время считают рациональным вносить в почву фосфорные, калийные и азотные удобрения в отношении питательных веществ, примерно равном 1:1,5:3.
Азотсодержащие минеральные удобрения подразделяют на аммиачные, нитратные и амидные. К первой группе относится сам аммиак NНз (безводный и водные растворы) и его соли — прежде всего сульфат (NH4)2SO4 и хлорид аммония NH4CI. Ко второй группе селитры: натриевая NaNO3, калиевая KNO3 и кальциевая Ca(NO3)2. Промышленностью также выпускаются аммиачно-нитратные удобрения, например аммиачная селитра NH4NO3. К амидным удобрениям относятся цианамид кальция СаСN2 и мочевина (карбамид) NH2CONH2. Для уменьшения пыления цианамида кальция часто к нему добавляют до 3 % нефтяных масел. В результате такое удобрение имеет запах керосина. Цианамид кальция при гидролизе дает аммиак и карбонат кальция:
СаСN2 + 3H2O = СаСОз + 2NH3
Природа создала много кладовых фосфорного сырья, в том числе и в нашей стране. Эти кладовые состоят из апатитов и фосфоритов. В группе минералов под общим названием апатиты наиболее распространены фосфаты состава Са5Х(РО4)з, где X = F![]() , Cl
, Cl![]() , ОН
, ОН![]() . Соответствующие минералы называют фторапатитом, хлорапатитом, гидроксидапатитом. Наиболее распространен фторапатит. Апатиты входят в состав изверженных магматических пород. Осадочные породы, в которых содержится апатит с включениями частичек посторонних минералов (кварца, кальцита, глины и др.), называют фосфоритами.
. Соответствующие минералы называют фторапатитом, хлорапатитом, гидроксидапатитом. Наиболее распространен фторапатит. Апатиты входят в состав изверженных магматических пород. Осадочные породы, в которых содержится апатит с включениями частичек посторонних минералов (кварца, кальцита, глины и др.), называют фосфоритами.
В организме растений калий регулирует процесс дыхания, способствует усвоению азота и повышает накопление белков и Сахаров в растениях. Для зерновых культур калий увеличивает прочность соломы, а у льна и конопли повышает прочность волокна. Калий повышает стойкость озимых хлебов к морозам и к перезимовке и овощных культур к ранним осенним заморозкам. Недостаток калия у растений проявляется на листьях. Их края приобретают желтую и темно-коричневую окраску с красными крапинками.
Другие макроэлементы, входящие в питательные вещества.
Как уже было отмечено, почвы быстрее всего истощаются азотом, фосфором и калием. Кроме них растениям необходимы в довольно больших количествах и другие химические элементы: кальций, магний, сера, железо. Их содержание в почвах часто близко к потребностям растений и их вынос с товарной продукцией относительно невысок.
Микроудобрения.
Микроудобрениями называют питательные вещества, которые содержат химические элементы, потребляемые растениями в очень малых количествах. В настоящее время выявлена биологическая роль в жизни растительных и животных организмов бора, меди, марганца, молибдена и др. Удобрения, содержащие эти микроэлементы, получили соответствующие названия.
Свеча и электрическая лампочка
В настоящее время покупка свечи доступна каждому почти так же, как спички. Однако так было далеко не всегда. В начале прошлого века на Руси свечи ценились очень дорого и в домах простых людей обычно горела лучина или лампада с маслом. Керосиновые лампы появились позже. О щедрости людей судили по тому, какого размера свечу зажигал человек при посещении церкви.
В прошлом веке производство свечей было развитой отраслью промышленности. Существовали описания технологий производства и их химической сущности. В частности, такой труд в 1851г. был написан преподавателем Петербургского технологического института Н. Виттом.
Из его книги мы узнаем, что свечи были восковые, сальные, стеариновые, спермацетные и весьма дорогие парафиновые. О том, из каких материалов готовились свечи, будет рассказано ниже. Однако не сразу об этом. Нельзя не вспомнить, что в середине прошлого века великий английский ученый Майкл Фарадей выступил с лекцией на тему. «История свечи». Это был вдохновенный гимн творению человека и природы. Лекция была переведена на русский язык и часть ее опубликована. Автор рекомендует каждому, кто интересуется физикой и химией, прочитать это выдающееся творение.
Вероятно, первые свечи были восковые. Пчелиный воск — это дар природы и свеча из него могла быть изготовлена самым примитивным способом. Гораздо позже воск стали очищать. Технология опять же была весьма простой. Это достигалось плавлением воска и фильтрованием в расплавленном состоянии через ткань. Для отбелки воска, в зависимости от возможностей, использовали костяной уголь, диоксид серы или хлор.
Следует отметить, что с американских континентов в Европу завозился растительный воск. Он применялся для изготовления свеч взамен пчелиного, однако был гораздо дороже и потому не выдерживал конкуренции.
Нити для свечей проваривались в течении нескольких часов в щелоке, приготовленном из поташа и жженой извести. Затем следовало промывание водой и отбеливание хлорной известью.
Под стеарином вначале понимали два различных продукта, извлекаемых из говяжьего и бараньего сала. Один из них получали удалением из сала жидкостей прессованием. Твердый остаток и называли стеарином. Другой продукт получали химической обработкой сала вначале известью, а затем серной кислотой. По существу, это был гидролиз жиров (глицеридов) с последующим выделением смеси кислот: стеариновой, пальмитиновой и небольшого количества непредельных кислот.
Стеариновая кислота СН3(СН2)16СООН была открыта в сале в 1816г. французским химиком Шеврелем. Вместе с Гей-Люссаком в 1825г. он взял в Англии привилегию на приготовление стеариновых свеч.
Стеариновые свечи оказались дешевле, чем восковые. Однако русская церковь долго не соглашалась заменять восковые свечи на стеариновые. Одной из причин было то, что восковые свечи при сгорании издавали приятный запах.
Сальные свечи готовили из вытопленного сала, которое затем очищали механически (процеживанием через ткань) или химически (глиноземом или дубильными веществами) и обесцвечивали так же, как и воск. При горении сальные свечи сильно коптили.
Спермацет для спермацетных свечей извлекали из полостей, находящихся в голове китов. Он освобождался от сопутствующих жидких масел выжиманием холодным или горячим прессованием. Если была необходимость, то проводилась очистка посредством мыльного щелока. Свечи, изготовленные из спермацета, отличались белизной и полупрозрачностью. Однако они имели и недостаток. При горении со временем оплывали.
В текущем столетии, до истребления китов, дефицитный спермацет использовали главным образом как основу для кремов и различных мазей, а также в качестве высококачественного смазочного масла для прецизионных инструментов.
Парафиновые свечи вначале были довольно дорогими, так как парафин извлекали при перегонке дегтя растительных веществ. Затем в Англии его начали добывать из торфа. Однако и в том и другом случае он получался лишь в небольших количествах. Коренное изменение произошло с налаживанием крупномасштабной переработки нефти. Сейчас — это один из наиболее доступных нефтехимических продуктов. Парафин — смесь предельных углеводородов С18—С35. Смесь предельных углеводородов С36—С55 называют церезином. Современные свечи состоят из смеси парафина и церезина.
Лампочка состоит из стеклянного баллона, в который введены держатели спирали, и из самой спирали. Спираль изготовлена из вольфрама — одного из наиболее тугоплавких металлов. Его температура плавления равна 3410 °С. Кроме высокой тугоплавкости, вольфрам обладает еще одним очень важным свойством — высокой пластичностью. Из 1 кг. вольфрама можно вытянуть проволоку длиной 3,5 км, которой хватит на изготовление 23 тыс. 60-ватных лампочек. Держатель изготовлен из молибдена — элемента-аналога вольфрама. В периодической системе Д. И. Менделеева эти два элемента находятся в одной и той же подгруппе. Важнейшим свойством молибдена является малый коэффициент линейного расширения. При нагревании он увеличивается в размере так же, как и стекло. Поскольку при нагревании и охлаждении молибден и стекло изменяют размеры синхронно, последнее не трескается и потому не нарушается герметизация.
Известно, что интенсивность излучения тела возрастает пропорционально четвертой степени абсолютной температуры. Это следует из закона Стефана — Больцмана. Следовательно, повышение температуры вольфрамовой нити электрической лампочки всего на 100° с 24001 до 2500 °С приводит к увеличению светового потока] на 16 %. Кроме того, с увеличением температуры в общем потоке излучения увеличивается доля видимого света. Это явление отражается законом Вина, т.е. с увеличением температуры нити накаливания растет свете отдача, а значит, увеличивается экономичность лампочки. Повышению температуры мешает разогревание стеклянного баллона и испарение нити. Снизить разогревание баллона можно созданием в нем вакуума. Эти» путем уменьшается теплопроводность от нити до стекла. Однако в вакууме будет усиливаться испарение нити. Это будет приводить к ее утоньшению и, в конце концов, нить перегорит. Заполнение баллона инертным газом, например азотом, препятствует испарению нити и тем больше, чем тяжелее молекулы заполняющего газа. Оторвавшиеся от нити атомы вольфрама будут ударяться о молекулы газа, их путь до стенок баллона будет удлинен, а некоторые атомы могут вернуться к нити. Чем тяжелее молекулы заполняющего газа, тем больше они будут препятствовать испарению нити накаливания. Так, частичная замена азота на аргон позволяет увеличивать температуру вольфрамовой нити до 2600—2700 °С. Полностью заменить азот на аргон нельзя, так как последний обладает сравнительно высокой электрической проводимостью и появится опасность возникновения электрической дуги между молибденовыми держателями. Еще лучше предохраняют вольфрамовую нить от разрушения более тяжелые благородные газы — криптон и ксенон. Они позволяют поднять температуру нити до 2800 °С и снизить объем газового баллона. Заполнение ими ламп взамен аргона позволяет получить на 15 % больше светоотдачу, увеличить вдвое срок службы нити накаливания и на 50 % сократить объем баллона.
Для увеличения срока службы электрических ламп накаливания в баллон добавляют небольшое количество иода. Он выполняет роль собаки, охраняющей отару овец. В зоне с температурой приблизительно 1600 °С иод взаимодействует с оторвавшимися от нити атомами вольфрама, переводя их в соединение Wl2. При хаотическом движении рано или поздно молекула иодида вольфрама (II) попадает в область более высоких температур, где она продиссоциирует в соответствии с уравнением
WI2 → W + 2l
Таким образом, иод возвращает атомы вольфрама в зону, окружающую нить и, следовательно, препятствует ее испарению. В йодных лампах на стенках стеклянного баллона не бывает и следов темного налета металлического вольфрама. По этой причине светоотдача таких ламп со временем не снижается, а срок службы увеличивается.
Химические элементы в организме человека
Все живые организмы на Земле, в том числе и человек, находятся в тесном контакте с окружающей средой. Пищевые продукты и питьевая вода способствуют поступлению в организм практически всех химических элементов. Они ![]()
![]()
![]()
![]() повседневно вводятся в организм и выводятся из него. Анализы показали, что количество отдельных химических элементов и их соотношение в здоровом организме различных людей примерно одинаковы.
повседневно вводятся в организм и выводятся из него. Анализы показали, что количество отдельных химических элементов и их соотношение в здоровом организме различных людей примерно одинаковы.
Мнение о том, что в организме человека можно обнаружить практически все элементы периодической системы Д. И. Менделеева, становится привычным. Однако предположения ученых идут дальше — в живом организме не только присутствуют все химические элементы, но каждый из них выполняет какую-то биологическую функцию. Вполне возможно, что эта гипотеза не подтвердится. Однако по мере того как развиваются исследования в данном направлении, выявляется биологическая роль все большего числа химических элементов. Несомненно, время и труд ученых прольют свет и на этот вопрос.
Биоактивность отдельных химических элементов. Экспериментально установлено, что в организме человека металлы составляют около 3 % (по массе). Это очень много. Если принять массу человека за 70 кг., то на долю металлов приходится 2,1 кг. По отдельным металлам масса распределяется следующим образом: кальций (1700 г), калий (250г.), натрий (70г.), магнии (42г.), железо (5г.), цинк (3г.). Остальное приходится на микроэлементы. Если концентрация элемента в организме превышает 10![]() 2 %, то его считают макроэлементом. Микроэлементы находятся в организме в концентрациях 10
2 %, то его считают макроэлементом. Микроэлементы находятся в организме в концентрациях 10![]() 3—10
3—10![]() 5 %. Если концентрация элемента ниже 10
5 %. Если концентрация элемента ниже 10![]() 5 %, то его считают ультрамикроэлементом. Неорганические вещества в живом организме находятся в различных формах. Большинство ионов металлов образуют соединения с биологическими объектами. Уже сегодня установлено, что многие ферменты (биологические катализаторы) содержат ионы металлов. Например, марганец входит в состав 12 различных ферментов, железо — в 70, медь — в 30, а цинк — более чем в 100. Естественно, что недостаток этих элементов должен сказаться на содержании соответствующих ферментов, а значит, и на нормальном функционировании организма. Таким образом, соли металлов совершенно необходимы для нормального функционирования живых организмов. Это подтвердили и опыты по бессолевой диете, которая применялась для кормления подопытных животных. Для этой цели многократным промыванием водой из пищи удаляли соли. Оказалось, что питание такой пищей приводило к гибели животных
5 %, то его считают ультрамикроэлементом. Неорганические вещества в живом организме находятся в различных формах. Большинство ионов металлов образуют соединения с биологическими объектами. Уже сегодня установлено, что многие ферменты (биологические катализаторы) содержат ионы металлов. Например, марганец входит в состав 12 различных ферментов, железо — в 70, медь — в 30, а цинк — более чем в 100. Естественно, что недостаток этих элементов должен сказаться на содержании соответствующих ферментов, а значит, и на нормальном функционировании организма. Таким образом, соли металлов совершенно необходимы для нормального функционирования живых организмов. Это подтвердили и опыты по бессолевой диете, которая применялась для кормления подопытных животных. Для этой цели многократным промыванием водой из пищи удаляли соли. Оказалось, что питание такой пищей приводило к гибели животных
Шесть элементов, атомы которых входят в состав белков и нуклеиновых кислот: углерод, водород, азот, кислород, фосфор, сера. Далее следует выделить двенадцать элементов, роль и значение которых для жизнедеятельности организмов известны: хлор, иод, натрий, калий, магний, кальций, марганец, железо, кобальт, медь, цинк, молибден. В литературе имеются указания на проявление биологической активности ванадием, хромом, никелем и кадмием
Имеется большое число элементов, являющихся ядами для живого организма, например ртуть, таллий, свиней и др. Они оказывают неблагоприятное биологическое влияние, но без них организм может функционировать. Существует мнение, что причина действия этих ядов связана с блокированием определенных групп в молекулах протеинов или же с вытеснением из некоторых ферментов меди и цинка. Бывают элементы, которые в относительно больших количествах являются ядом, а в низких концентрациях оказывают полезное влияние на организм. Например, мышьяк является сильным ядом, нарушающим сердечно-сосудистую систему и поражающим печень и почки, но в небольших дозах он прописывается врачами для улучшения аппетита человека. Ученые считают, что микродозы мышьяка повышают устойчивость организма к действию вредных микробов. Широко известно сильное отравляющее вещество иприт S(СН2СН2С1)2. Однако в разбавленном в 20 000 тыс. раз вазелином под названием «Псориазина» его применяют против чешуйчатого лишая. Современная фармакотерапия пока еще не может обойтись без значительного числа лекарственных средств, в состав которых входят токсичные металлы. Как здесь не вспомнить поговорку, что в малых количествах лечит, а в больших — калечит.
Интересно, что хлорид натрия (поваренная соль) в десятикратном избытке в организме по сравнению с нормальным содержанием является ядом. Кислород, необходимый человеку для дыхания, в высокой концентрации и особенно под давлением оказывает ядовитое действие. Из этих примеров видно, что концентрация элемента в организме иногда играет весьма существенное, а порой и катастрофическое значение.
Железо входит в состав гемоглобина крови, а точнее в красные пигменты крови, обратимо связывающие молекулярный кислород. У взрослого человека в крови содержится около 2,6 г. железа. В процессе жизнедеятельности в организме происходит постоянный распад и синтез гемоглобина. Для восстановления железа, потерянного с распадом гемоглобина, человеку необходимо суточное поступление в организм около 25 мг. Недостаток железа в организме приводит к заболеванию — анемии. Однако избыток железа в организме тоже вреден. С ним связан сидероз глаз и легких — заболевание, вызываемое отложением соединений железа в тканях этих органов. Недостаток в организме меди вызывает деструкцию кровеносных сосудов. Кроме того, считают, что его дефицит служит причиной раковых заболеваний. В некоторых случаях поражение раком легких у людей пожилого возраста врачи связывают с возрастным снижением меди в организме. Однако избыток меди приводит к нарушению психики и параличу некоторых органов (болезнь Вильсона). Для человека вред причиняют лишь большие количества соединений меди. В малых дозах они используются в медицине как вяжущее и бактериостазное (задерживающее рост и размножение бактерий) средство. Так, например, сульфат меди (II) CuSO4 используют при лечении конъюнктивитов в виде глазных капель (0,25 %-ный раствор), а также для прижиганий при трахоме в виде глазных карандашей (сплав сульфата меди (II), нитрата калия, квасцов и камфоры). При ожогах кожи фосфором производят ее обильное смачивание 5 %-ным раствором сульфата меди (II).
Давно замечено бактерицидное (вызывающее гибель различных бактерий) свойство серебра и его солей. Например, в медицине раствор коллоидного серебра, (колларгол) применяют для промывания гнойных ран, мочевого пузыря при хронических циститах и уретритах, а также в виде глазных капель при гнойных конъюнктивитах и бленнорее. Нитрат серебра AgNO3 в виде карандашей применяют для прижигания бородавок, грануляций и т. п. В разбавленных растворах (0,1—0,25 %-ные) его используют как вяжущее и противомикробное средство для примочек, а также в качестве глазных капель. Ученые считают, что прижигающее действие нитрата серебра связано с его взаимодействием с белками тканей, что приводит к образованию белковых солей серебра — альбуминатов.
В настоящее время, бесспорно, установлено, что всем живым организмам присуще явление ионной асимметрии — неравномерное распределение ионов внутри и вне клетки. Например, внутри клеток мышечных волокон, сердца, печени, почек имеется повышенное содержание ионов калия по сравнению с внеклеточным. Концентрация ионов натрия, наоборот, выше вне клетки, чем внутри нее. Наличие градиента концентраций калия и натрия — экспериментально установленный факт. Исследователей волнует загадка о природе калий-натриевого насоса и его функционирования. На разрешение этого вопроса направлены усилия многих коллективов ученых, как в нашей стране, так и за рубежом. Интересно, что по мере старения организма градиент концентраций ионов калия и натрия на границе клетки падает. При наступлении смерти концентрация калия и натрия внутри и вне клетки сразу же выравнивается.
Биологическая функция ионов лития и рубидия в здоровом организме пока не ясна. Однако имеются сведения, что введением их в организм удается лечить одну из форм маникально-депрессивного психоза.
Биологам и медикам хорошо известно, что важнуюроль в организме человека играют гликозиды. Некоторые природные гликозиды (извлекаемые из растений) активно действуют на сердечную мышцу, усиливая сократительные функции и замедление ритма сердца. При попадании в организм большого количества сердечного гликозида может произойти полная остановка сердца. Ионы некоторых металлов влияют на действие гликозидов. Например, при введении в кровь ионов магния действие гликозидов на сердечную мышцу ослабляется Ионы кальция, наоборот, усиливают действие сердечных гликозидов
Некоторые соединения ртути также чрезвычайно ядовиты. Известно, что ионы ртути (II) способны прочно соединяться с белками. Ядовитое действие хлорида ртути (II) HgCl2 (сулемы) проявляется, прежде всего, в некрозе (омертвлении) почек и слизистой оболочки кишечника. В результате ртутного отравления почки теряют способность выделять из крови продукты жизнедеятельности организма.
Интересно, что хлорид ртути (I) Hg2Cl2 (древнее название каломель) безвреден для организма человека. Вероятно, это объясняется чрезвычайно низкой растворимостью соли, в результате чего ионы ртути не попадают в заметных количествах в организм.
Цианистый калий (Цианид калия) KCN — соль синильной кислоты HCN. Оба соединения являются быстродействующими и сильными ядами
При остром отравлении синильной кислотой и ее солями теряется сознание, наступает паралич дыхания и сердца. На начальной стадии отравления человек испытывает головокружение, ощущение давления во лбу, острую головную боль, учащенное дыхание, сердцебиение. Первая помощь при отравлении синильной кислотой и ее солями — свежий воздух, кислородное дыхание, тепло. Противоядиями являются нитрит натрия NaNO2 и органические нитросоединения: амилнитрит C5H11ONO и пропилнитрит C3H7ONO. Считают, что действие нитрита натрия сводится к превращению гемоглобина в мета-гемоглобин. Последний прочно связывает цианидные ионы в цианметагемоглобин. Этим путем дыхательные ферменты освобождаются от цианидных ионов, что и приводит к восстановлению дыхательной функции клеток и тканей.
В качестве противоядий на синильную кислоту широко используют серосодержащие соединения: коллоидную серу, тиосульфат натрия Na2S2O3, тетратионат натрия Na2S4O6, а также серосодержащие органические соединения, в частности, аминокислоты — глутатион, цистеин, цистин. Синильная кислота и ее соли при взаимодействии с серой превращаются в тиоцианаты в соответствии с уравнением
HCN + S → HNCS
Тиоцианаты же совершенно безвредны для человеческого организма.
С давних пор при опасности отравления цианидами рекомендовалось держать за щекой кусочек сахара. В 1915г. немецкие химики Рупп и Гольце показали, что глюкоза взаимодействует с синильной кислотой и некоторыми цианидами с образованием нетоксичного соединения циангидрина глюкозы:
ОН ОН ОН ОН ОН Н ОН OH OН ОН ОН Н
| | | | | | | | | | | |
СН2—СН—СН—СН—СН—С = О + HCN → СН2—СН—СН—СН—СН—С—ОН
|
CN
глюкоза циангидрин глюкозы
Свинец и его соединения являются довольно сильными ядами. В организме человека свинец накапливается в костях, печени и почках.
Весьма токсичны соединения химического элемента таллия, который относят к числу редких.
Следует указать, что все цветные и особенно тяжелые (расположенные в конце периодической системы) металлы в количествах выше допустимых ядовиты.
Углекислый газ в больших количествах содержится в организме человека и потому не может быть ядовитым. За 1 ч взрослый человек выдыхает примерно 20 л (около 40 г) этого газа. При физической работе количество выдыхаемого углекислого газа увеличивается до 35 л. Он образуется в результате сгорания в организме углеводов и жиров. Однако при большом содержании СО2в воздухе наступает удушье из-за недостатка кислорода. Максимальная продолжительность пребывания человека в помещении с концентрацией СО2 до 20 % (по объему) не должна превышать 2 ч. В Италии имеется получившая широкую известность пещера («Собачья пещера»), в которой человек стоя может находиться длительное время, а забежавшая туда собака задыхается и гибнет. Дело в том, что примерно до пояса человека пещера заполнена тяжелым (по сравнению с азотом и кислородом) углекислым газом. Поскольку голова человека находится в воздушном слое, то он не ощущает никаких неудобств. Собака же при ее росте оказывается в атмосфере углекислого газа и потому задыхается.
Врачи и биологи установили, что при окислении в организме углеводов до воды и углекислого газа на одну затраченную молекулу кислорода выделяется одна молекула СО2. Таким образом, отношение выделенного СО2 к поглощенному О2 (величина дыхательного коэффициента) равна единице. В случае окисления жиров дыхательный коэффициент равен примерно 0,7. Следовательно, определяя величину дыхательного коэффициента, можно судить, какие вещества преимущественно сгорают в организме. Экспериментально установлено, что при кратковременных, но интенсивных мышечных нагрузках энергия получается за счет окисления углеводов, а при длительных — преимущественно за счет сгорания жиров. Полагают, что переключение организма на окисление жиров связано с истощением резерва углеводов, что обычно наблюдается через 5—20 мин после начала интенсивной мышечной работы.
Антидоты.
Антидоты — вещества, устраняющие последствия воздействия ядов на биологические структуры и инакгавирующие яды посредством химической
Жёлтая кровяная соль K4[Fe(CN)6] образует малорастворимые соединения с ионами многих тяжелых металлов. Это свойство используют на практике для лечения отравлений солями тяжелых металлов.
Хорошим антидотом при отравлениях соединениями мышьяка, ртути, свинца, кадмия, никеля, хрома, кобальта и других металлов является унитиол:
СН2—СН—CH2SO3Na ∙ Н2О
| |
SH SH
Универсальным антидотом является молоко.
Использованная литература
1. Краткая химическая энциклопедия. – М.: Советская энциклопедия, 1961 – 1967. Т. I—V.
2. Советский энциклопедический словарь. – М:: Сов. энциклопедия, 1983.
3. Августиник А.И. Керамика. – Л.: Стройиздат, 1975.
4. Андреев И.Н. Коррозия металлов и их защита. – Казань: Татарское книжное изд-во, 1979.
5. Бетехтин А.Г. Минералогия. – М.: Гос. изд-во геологической литературы, 1950.
6. Бутт Ю.М., Дудеров Г.Н., Матвеев М.А. Общая технология силикатов. – М.: Госстройиздат, 1962.
7. Быстрое Г.П. Технология спичечного производства. – М.–Л.: Гослесбумиздат, 1961.
8. Витт Н. Руководство к свечному производству. – Санкт-Петербург: Типография департамента внешней торговли, 1851.
9. Войтович В.А., Мокеева Л.Н. Биологическая коррозия. – М.: Знание, 1980. № 10.
10. Войцеховская А.Л., Вольфензон И. И. Косметика сегодня. – М.: Химия, 1988.
11. Дудеров И.Г., Матвеева Г.М.,. Суханова В.Б. Общая технология силикатов. – М.: Стройиздат, 1987.
12. Козловский А.Л. Клеи и склеивание. – М.: Знание, 1976.
13. Козмал Ф. Производство бумаги в теории и на практике. – М.: Лесная промышленность, 1964.
14. Кукушкин Ю.Н. Соединения высшего порядка. – Л.: Химия, 1991.
15. Кульский Л.А., Даль В.В. Проблема чистой воды. – Киев: Наукова думка, 1974.
16. Лепешков И.Н., Розен Б.Я. Минеральные дары моря. – М.: Наука, 1972.
17. Лосев К.С. Вода, – Л.: Гидрометеоиздат, 1989.
18. Лукьянов П.М. Краткая история химической промышленности СССР. — М.: Изд-во АН СССР, 1959.
19. Лялько В.И. Вечно живая вода. – Киев: Наукова дума, 1972.
20. Петербургский А.В. Агрохимия и система удобрений. – М.: Колос, 1967.
21. Теддер Дж., Нехватал А., Джубб А. Промышленная органическая химия. — М.: Мир, 1977.
22. Улиг Г.Г., Реви Р.У. Коррозия и борьба с ней. – Л.: Химия, 1989.
23. Чалмерс Л. Химические средства в быту и промышленности – Л.: Химия, 1969.
24. Чащин А.М. Химия зеленого золота. — М.: Лесная промышленность, 1987.
25. Энгельгардт Г., Гранич К., Риттер К. Проклейка бумаги. – М.: Лесная промышленность, 1975.
Похожие работы
... (9, 10 класс). Таким образом, можно сделать вывод о том, что разработка элективного курса по данной теме является актуальной. ГЛАВА II. РАЗРАБОТКА ШКОЛЬНОГО ЭЛЕКТИВНОГО КУРСА «ПОЛИМЕРЫ ВОКРУГ НАС» II. 1. Программа курса профильной ориентации для учащихся 9 класса в рамках предпрофильной подготовки по курсу «Полимеры вокруг нас» Пояснительная записка Программа элективного курса «Полимеры ...
... углеводородное сырьё пойдёт на синтез разнообразных материалов. Топливом же будет служить ядерное горючее или какой-либо другой вид топлива.Это одно из решений сырьевой и энергетической проблем. 3.Продовольственная проблема и химия. Население нашей планеты растёт. По прогнозам ООН к 2000г. оно составит около 6,5 млрд. человек и будет, естественно, увеличиваться в последующие ...
... традиции: конваллятоксин - яд ландыша, тетродотоксин - яд рыбы фугу, сакситоксин - устричный токсин, ботулинический токсин - одно из самых ядовитых веществ, известных человеку. 2.2 Яды вокруг нас Насыщение окружающей человека природной среды вредными веществами становится все более осознаваемой опасностью для нормальной жизнедеятельности и здоровья. Это обстоятельство, этот фактор, наряду ...
... поведении в природе, в сознании фиксируется отрицательное отношение к флоре и фауне. Это ни в какой мере не учитывает особенности детей дошкольного и младшего школьного возраста: эмоциональной восприимчивости, подражательности, непосредственности поведения. Многие выпускники начальной школы были беспомощны, когда требовалось оказание помощи, проявление заботы, внимания к объекту. Даже если дети ...
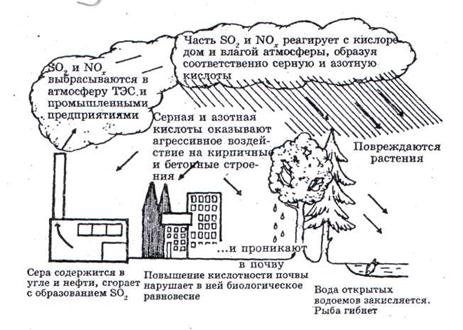

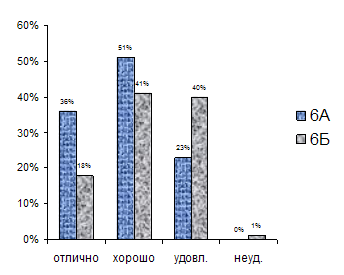
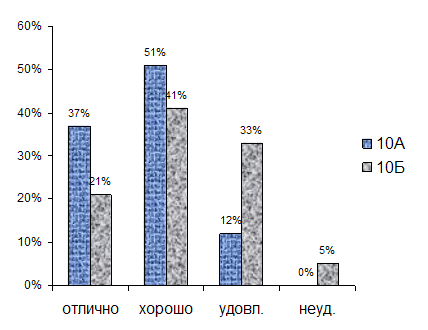
0 комментариев