Навигация
2. Окись азота – NO
3. Азотистый ангидрид – N2O3
4. Двуокись азота – NO2
5. Оксид азота – N2O5
Источники соединений азота:Естественные источники эмиссии соединений азота в атмосферу:
I. Почвенная эмиссия оксидов азота. В процессе деятельности живущих в почве денитрифицирующих бактерий из нитратов высвобождаются оксиды азота. Согласно данным на 1990 г. ежегодно во всем мире образуется этим путем около 8 млн. т. оксидов азота (в пересчете на азот).
II. Грозовые разряды. Во время электрических разрядов в атмосфере из-за очень высокой температуры и перехода в плазменное состояние молекулярные азот и кислород в воздухе соединяются в оксиды азота. Образовавшееся таким способом количество оксида азота составляет около 8 млн. т.
III. Горение биомассы. Данный вид источника может иметь как искусственное так и естественное происхождение. Наибольшее количество биомассы сгорает в результате процесса выжигания леса (с целью получения производственных площадей) и пожаров в саванне. При горении биомассы в воздух поступает 12 млн. т.оксидов азота (в пересчете на азот) в течении года.
IV. Прочие источники. Прочие источники естественных выбросов оксидов азота менее значительны и с трудом поддаются оценке. К ним относятся: окисление аммиака в атмосфере, разложение находящейся в стратосфере закиси азота, вследствие чего происходит попадание смеси образовавшихся оксидов NO и NO2 в тропосферу и, наконец, фотолитические и биологические процессы в океанах. Эти источники совместно вырабатывают в течении года от 2-ух до 12 млн.т.оксидов азота (в пересчете на азот).
Антропогенные источники эмиссии соединений азота в атмосферу:
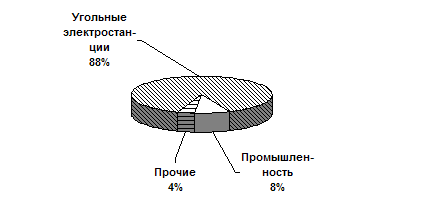
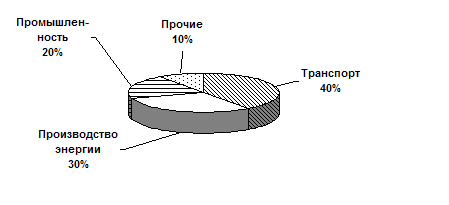
Среди антропогенных источников образования оксидов азота на первом месте стоит горение ископаемого топлива (уголь, нефть, газ и т.д.). Во время горения в результате возникновения высокой температуры находящиеся в воздухе азот и кислород соединяются. В данном случае количество образовавшегося оксида азота NO попорционально темрпературе горения. Кроме того, оксиды азота образуются в результате горения имеющихся в топливе азотосодержащих веществ. Сжигая ископаемое топливо, человечество ежегодно выбрасывает в воздушный бассеин Земли около12 млн.т. оксидов азота. Немного меньше оксидов азота, около 8 млн.т. в год поступает от сжигания горючего (бензина, дизельное топливо и т.д.) в двигателелях внутреннего сгорания.. Промышленностью во всем мире выбрасывается около 1 млн.т. азота ежегодно. Таким образом, по крайней мере 37% из почти 56 млн.т. ежегодных выбросов оксида азота образуется из антропогенных источников. Этот процент, однако, будет намного больше, если к нему прибавить продукты сжигания биомассы.
Атмосферный аммиак:Аммиак, имеющий в водном растворе щелочную реакцию, играет значительную роль в регулировании кислотных дождей, так как он может нейтрализовать атмосферные кислотные соединения:
NH3 + H2SO4 = NH4HSO4
NH3 + NH4HSO4 = (NH4)2SO4
NH3 + HNO3 = NH4NO3
Таким образом, нейтрализуются кислотные осадки и образуются сульфаты и нитрат аммония.
Важнейшим источником атмосферного аммиака является почва. Находящиеся в почве органические вещества разрушаются определенными бактериями, и одним из конечных продуктов этого процесса является аммиак. Ученым удалось установить, что активность бактерии, приводящая в конечном счете к образованию аммиака, зависит в первую очередь от температуры и влажности почвы. В высоких географических широтах (Северная Америка и Северная Европа), особенно в зимние месяцы, выделение аммиака почвой может быть незначительным. В то же время на этих территориях наблюдается наибольший уровень эмиссии двуокиси серы и оксидов азота, в результате чего находящиеся в атмосфере кислоты не подвергаются нейтрализации и, таким образом, возрастает опасность выпадения кислотного дождя. В процессе распада мочи домашних животных высвобождается большое количество аммиака. Этот источник аммиака настолько значителен, что в Европе он превышает возможности выделения аммиака почвой.
Химические превращения загрязняющих кислотных веществ в атмосфере:Попадающие в воздух загрязняющие вещества в значительной мере подвергаются физическим и химическим преобразованиям в атмосфере. Данные процессы протекают одновременно с распространением этих веществ.
Химические превращения соединений серы:
Как правило сера входит в состав выбросов не в полностью окисленной форме (степень окисления серы в ее двуокиси равна 4, т.е. к двум атомам кислорода присоединяется один атом серы). Если соединения серы находятся в воздухе в течение достаточно длительного времени, то под действием содержащихся в воздухе окислителей они превращаются в серную кислоту или сульфаты. В процессе окисления кислородом (О2) сернистого газа (SO2), сера повышает свою степень окисления и переходит в трехокись серы (SO3), которая в свою очередь являясь очень гигроскопичным веществом и взаимодействуя с атмосферной водой, очень быстро превращается в H2SO4. Именно по этой причине в обычных атмосферных условиях трехокись серы не содержится в воздухе в больших количествах. В результате реакции образуются молекулы серной кислоты, которые в воздухе или на поверхности аэрозольных частиц быстро конденсируются.
Кроме двуокиси серы в атмосфере находится также значительное количество других природных соединений серы, которые в конечном счете окисляются до серной кислоты (или сульфатов).
Химические превращения соединений азота:
Наиболее распространённым соединением азота, входящим в состав выбросов, является окись азота NO, которая при взаимодействии с кислородом воздуха образует двуокись азота. Последняя в результате реакции с радикалом гидроксила превращается в азотную кислоту NO2 + OH = HNO3. Полученная таким образом азотная кислота в отличае от серной может долгое время оставаться в газообразном состоянии, так как она плохо конденсируется. Это связанно с тем, что азотная кислота обладает большей летучестью, чем серная. Пары азотной кислоты могут быть поглощены капельками облаков или осадков или частицами аэрозоля.
Кислотная седиментация (кислотные дожди)
Заключительным этапом в круговороте загрязняющих веществ является седиментация, которая может происходить двумя путями:
Похожие работы
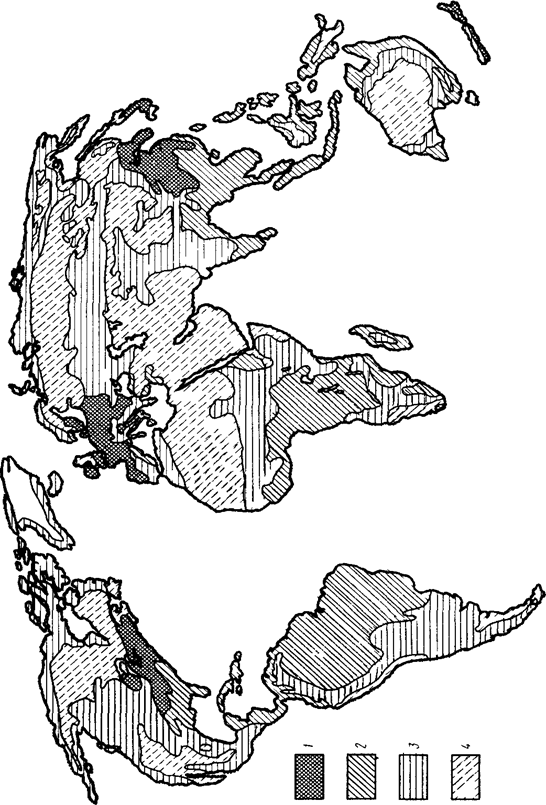
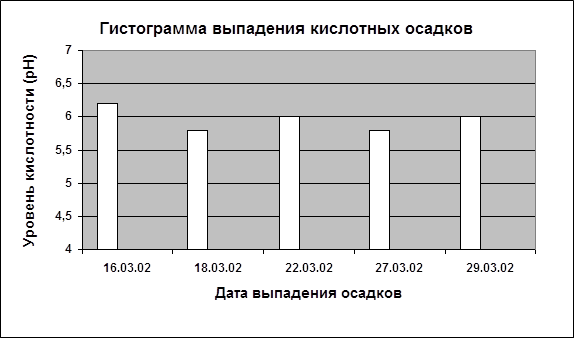
... -Петербург, Омск, Норильск, Красноярск, Иркутск и др.), насыщенных энергетическими установками и автотранспортом. Минимальные значения рН осадков в этих местах достигают 3,1-3,4 [5, с. 49]. Специфическая особенность кислотных дождей – их трансграничный характер, обусловленный переносом кислотообразующих выбросов воздушными течениями на большие расстояния – сотни и даже тысячи километров. Этому в ...
... образованием угольной кислоты (H2CO3). Чистый дождь, проходящий через незагрязненный воздух, представляет собой водный раствор с pH 5,6 (к моменту удара о землю). Как мы увидим дальше, основная причина выпадения кислотных дождей — это деятельность человека, однако есть и естественные причины, начиная с извержения вулканов и разряда молнии и кончая жизнедеятельностью бактерий. В общем, даже если бы ...
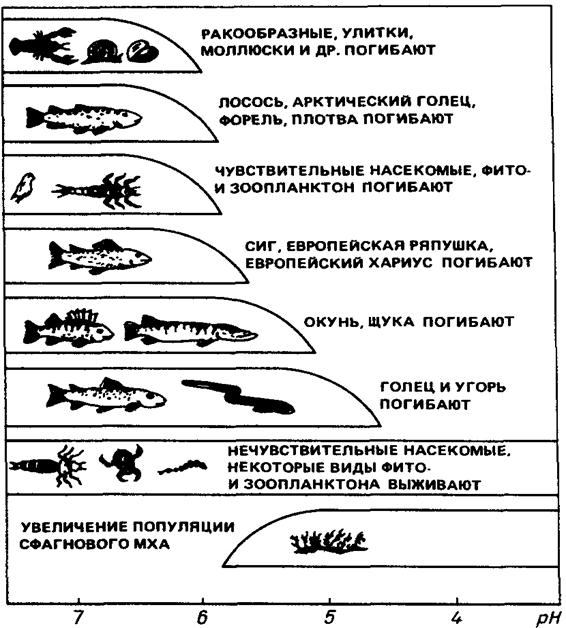
... поверхности направлении ощущается увеличение скорости ветра и горизонтальное движение воздуха вызывает турбулентность. Таким путем компоненты воздуха достигают Земли, и наиболее активные кислотные вещества легко взаимодействуют с поверхностью. Влияние кислотных осадков на биосферу. Кислотные осадки оказывают вредное воздействие не только на отдельные предмет или живые существа, но и на их ...
... на территории одного государства, могут оказывать воздействие на природу и граждан другого государства. Так правительства Норвегии и Швеции заявляют, что выпадение кислотных осадков на их территории частично обусловлено выбросами загрязнителей в Великобритании и Северной Европе. Промышленные и автомобильные выбросы в США неизменно вносят вклад в кислотные дожди над Канадой, а Канада в свою ...

0 комментариев