Навигация
Образующиеся вещества – сильные электролиты, хорошо растворимые в воде и полностью диссоциирующие на ионы
1. Образующиеся вещества – сильные электролиты, хорошо растворимые в воде и полностью диссоциирующие на ионы.
2. Одно (или несколько) из образующихся веществ – газ, осадок или слабый электролит (хорошо растворимый в воде).
Например, можно рассмотреть две реакции:
2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2, (1)
2Al + 2KOH + 6H2O = 2K[Al(OH)4] + 3H2. (2)
В ионной форме уравнения (1) и (2) запишутся следующим образом:
2Al + 2Na+ + 2OH- + 6 H2O = 2Na+ + 2[Al(OH)4]- + 3H2, (3)
2Al + 2K+ + 2OH- + 6 H2O = 2K+ + 2[Al(OH)4]- + 3H2, (4)
В данном случае алюминий не является электролитом, а молекула воды записывается в недиссоциированной форме потому, что является очень слабым электролитом. Неполярные молекулы водорода практически нерастворимы в воде и удаляются из сферы реакции. Одинаковые ионы в обеих частях уравнений (3), (4) можно сократить, и тогда эти уравнения преобразуются в одно сокращённое ионное уравнение взаимодействия алюминия с щелочами:
2Al + 2OH- + 6H2O = 2[Al(OH)4]- + 3H2. (5)
Очевидно, что при взаимодействии алюминия с любой щелочью реакция будет описываться уравнением (5). Следовательно, ионное уравнение, в отличие от молекулярного, относится не к одной какой-нибудь реакции между конкретными веществами, а к целой группе аналогичных реакций. В этом его большая практическая ценность и значение, например благодаря этому широко используются качественные реакции на различные ионы.
Так, при помощи ионов серебра Ag+ можно обнаружить присутствие в растворе ионов галогенов, а при помощи ионов галогенов можно обнаружить ионы серебра; при помощи ионов бария Ba2+ можно обнаружить ионы SO2- и наоборот.
С учётом вышеизложенного можно сформулировать правило, которым удобно руководствоваться при изучении процессов, протекающих в растворах электролитов.
Реакции между ионами в растворах электролитов идут практически до конца в сторону образования осадков, газов и слабых электролитов.
Следовательно, реакции идут с образованием веществ с меньшей концентрацией ионов в растворе в соответствии с законом действующих масс. Скорость прямой реакции пропорциональна произведению концентраций ионов реагирующих компонентов, а скорость обратной реакции пропорциональна произведению концентраций ионов продуктов. Но при образовании газов, осадков и слабых электролитов ионы связываются (уходят из раствора) и скорость обратной реакции уменьшается.
4. Представление о кислотах и основаниях
Определения кислот и оснований с точки зрения теории диссоциации были даны С. Аррениусом.
Кислотой называется соединение, образующее при диссоциации в водном растворе из положительных ионов только ионы водорода H+. В соответствии с этим определением к кислотам относятся, например, HCl, H2SO4, HNO3, H2S.
Основанием называется соединение, образующее при диссоциации в водном растворе из отрицательных ионов только гидроксид-ионы OH-. По современной номенклатуре основания принято называть гидроксидами элементов с указанием степени окисления: NaOH – гидроксид натрия, KOH – гидроксид калия, Ca(OH)2 – гидроксид кальция, Cr(OH)2 – гидроксид хрома (II), Cr(OH)3 – гидроксид хрома (III).
Гидроксиды металлов принято делить на две группы: растворимые в воде (образованные щелочными и щелочноземельными металлами) и нерастворимые в воде. Основное различие между ними заключается в том, что концентрация ионов OH- в растворах щелочей достаточно высока, для нерастворимых же оснований она определяется растворимостью вещества и обычно очень мала. Тем не менее небольшие равновесные концентрации иона OH- даже в растворах нерастворимых оснований определяют свойства этого класса соединений.
После Аррениуса было показано, что определение кислот и оснований в терминах теории электролитической диссоциации не охватывает всего многообразия кислотно-основных свойств веществ. Дальнейшее развитие химии потребовало уточнить и дополнить определения кислот и оснований.
Согласно протонной теории кислот и оснований, предложенной И. Бренстедом, кислотой называют вещество, отщепляющее при данной реакции протоны, а основанием – вещество, способное принимать протоны. Любая реакция отщепления протона выражается уравнением
кислота ® основание + H+.
На базе таких представлений понятными становятся основные свойства аммиака, который за счёт неподелённой пары электронов атома азота эффективно принимает протон при взаимодействии с кислотами, образуя за счёт донорно-акцепторной связи ион аммония:
HNO3 + NH3 « NH+ + NO-.
Возможно и ещё более общее определение кислот и оснований. Г. Льюис предположил, что кислотно-основные взаимодействия совсем необязательно происходят с переносом протона. В определении кислот и оснований по Льюису основная роль отводится участию электронных пар в химическом взаимодействии.
Катионы, анионы или нейтральные молекулы, способные принять одну или несколько пар электронов, называют кислотами Льюиса.
Так, например, фторид алюминия AlF3 – кислота, способная принимать электронную пару при взаимодействии с аммиаком:
AlF3 + :NH3 « [AlF3]:[NH3].
Катионы, анионы или нейтральные молекулы, способные отдавать электронные пары, называют основаниями Льюиса. В только что рассмотренном примере аммиак является основанием.
Определение Г. Льюиса охватывает все кислотно-основные процессы, рассмотренные ранее предложенными теориями.
Похожие работы
... HСlO3 Хлораты Хлористая НClO2 Хлориты Хлорноватистая HClO Гипохлориты Хромовая H2CrO4 Хроматы Циановодородная (синильная кислота) слота) HCN Цианиды Основные типы химических реакций Среди разнообразных химических реакций можно выделить два типа, существенно отличающихся друг от друга. К первому типу реакций относятся те, в ходе которых степень окисления ...
... , т. е. к увеличению скорости реакции. Количественно зависимость между скоростью реакции и молярными концентрациями реагирующих веществ описывается основным законом химической кинетики — законом действующих масс. Скорость химической реакции при постоянной температуре прямо пропорциональна произведению концентраций реагирующих веществ. Для мономолекулярной реакции скорость реакции ...
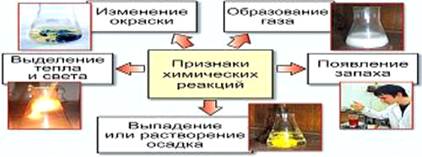
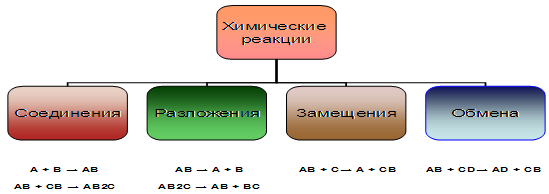
... – реакции, идущие без изменения степени окисления: S+4O4-2 + H2O → H2+ S+4O4-2 CH3NH2 + HCl → (CH3NH3)Cl Как видим, существует различные способы классификации химических реакций, из которых более подробно мы рассмотрим следующие. По признаку изменения числа исходных и конечных веществ. Здесь можно найти 4 типа химических реакций (рис.6): реакции соединения, реакции разложения, ...
... это целый класс реакций окисления органических веществ с участием катализатора, обладающего окислительно-восстановительными свойствами. Этот процесс протекает циклично т. е. состоит из многократных повторений. Колебательные химические реакции были открыты и научно обоснованы в 1951 г. советским учёным Борисом Петровичем Белоусовым. Б.П. Белоусов изучал окисление лимонной кислоты при её реакции с ...
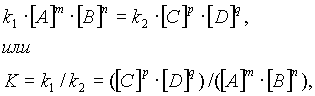
0 комментариев