Навигация
Тепловой эффект химической реакции и его практическое применение.
МИНИСТЕРСТВО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
Воронежский государственный технический университет
КУРСОВОЙ ПРОЕКТ
по дисциплине «Теоретические основы прогрессивной технологии»
Тема: «Тепловой эффект химической реакции и его практическое применение.»
|

Воронеж 2004
Содержание
| Введение …………………………………………………………………… | 3 |
| 1. Тепловой эффект химической реакции………………………………... | 4 |
| 1.1. Уравнения химических реакций……………………………... | 8 |
| 1.2. Основные законы термохимии………………………………. | 10 |
| 2. Применение теплового эффекта на практике…………………………. | 12 |
| 2.1.Жаропрочные покрытия………………………………………. | 1 |
| 2.2.Термохимический способ обработки алмаза………………... | 14 |
| 2.3.Техногенное сырьё для производства цемента……………… | 15 |
| 2.4. Биосенсоры……………………………………………………. | 16 |
| Заключение…………………………………………………………………. | 17 |
| Список литературы………………………………………………………… | 18 |
Введение
Тепловые эффекты химических реакций необходимы для многих технических расчетов. Они находят обширное применение во многих отраслях промышленности, а также в военных разработках.
Целью данной курсовой работы является изучение практического применения теплового эффекта. Мы рассмотрим некоторые варианты его использования, и выясним насколько важно использование тепловых эффектов химических реакций в условиях развития современных технологий.
1. Тепловой эффект химической реакции
В каждом веществе запасено определенное количество энергии. С этим свойством веществ мы сталкиваемся уже за завтраком, обедом или ужином, так как продукты питания позволяют нашему организму использовать энергию самых разнообразных химических соединений, содержащихся в пище. В организме эта энергия преобразуется в движение, работу, идет на поддержание постоянной (и довольно высокой!) температуры тела.
Одним из самых известных ученых, работающих в области термохимии, является Бертло. Бертло- профессор химии Высшей фармацевтической школы в Париже (1859г). Министр просвещения и иностранных дел.
Начиная с 1865 Бертло активно занимался термохимией, провел обширные калориметрические исследования, приведшие, в частности, к изобретению "калориметрической бомбы" (1881); ему принадлежат понятия "экзотермической" и "эндотермической" реакций. Бертло получены обширные данные о тепловых эффектах огромного числа реакций, о теплоте разложения и образования многих веществ.
Бертло исследовал действие взрывчатых веществ: температуру взрыва, скорости сгорания и распространения взрывной волны и др.
Энергия химических соединений сосредоточена главным образом в химических связях. Чтобы разрушить связь между двумя атомами, требуется затратить энергию. Когда химическая связь образуется, энергия выделяется.
Любая химическая реакция заключается в разрыве одних химических связей и образовании других.
Когда в результате химической реакции при образовании новых связей выделяется энергии больше, чем потребовалось для разрушения "старых" связей в исходных веществах, то избыток энергии высвобождается в виде тепла. Примером могут служить реакции горения. Например, природный газ (метан CH4) сгорает в кислороде воздуха с выделением большого количества теплоты (рис. 1а). Такие реакции являются экзотермическими.
· Реакции, протекающие с выделением теплоты, проявляют положительный тепловой эффект (Q>0, DH<0) и называются экзотермическими.
В других случаях на разрушение связей в исходных веществах требуется энергии больше, чем может выделиться при образовании новых связей. Такие реакции происходят только при подводе энергии извне и называются эндотермическими.
· Реакции, которые идут с поглощением теплоты из окружающей среды (Q<0, DH>0), т.е. с отрицательным тепловым эффектом, являются эндотермическими.
Примером является образование оксида углерода (II) CO и водорода H2 из угля и воды, которое происходит только при нагревании (рис. 1б).
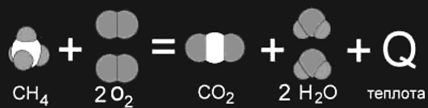
Рис. 1а
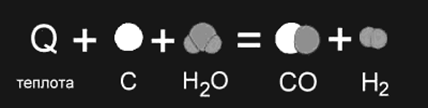
Рис. 1б
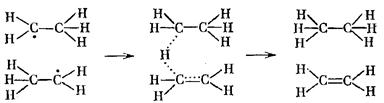
Рис. 1а,б. Изображение химических реакций при помощи моделей молекул: а) экзотермическая реакция, б) эндотермическая реакция. Модели наглядно показывают, как при неизменном числе атомов между ними разрушаются старые и возникают новые химические связи.
Таким образом, любая химическая реакция сопровождается выделением или поглощением энергии. Чаще всего энергия выделяется или поглощается в виде теплоты (реже - в виде световой или механической энергии). Эту теплоту можно измерить. Результат измерения выражают в килоджоулях (кДж) для одного моля реагента или (реже) для моля продукта реакции. Такая величина называется тепловым эффектом реакции.
Тепловой эффект - количество теплоты, выделившееся или поглощенное химической системой при протекании в ней химической реакции.Тепловой эффект обозначается символами Q или DH (Q = -DH). Его величина соответствует разности между энергиями исходного и конечного состояний реакции:
DH = Hкон.- Hисх. = Eкон.- Eисх.
Значки (г), (ж) обозначают газообразное и жидкое состояние веществ. Встречаются также обозначения (тв) или (к) - твердое, кристаллическое вещество, (водн) - растворенное в воде вещество и т.д.
Обозначение агрегатного состояния вещества имеет важное значение. Например, в реакции сгорания водорода первоначально образуется вода в виде пара (газообразное состояние), при конденсации которого может выделиться еще некоторое количество энергии. Следовательно, для образования воды в виде жидкости измеренный тепловой эффект реакции будет несколько больше, чем для образования только пара, поскольку при конденсации пара выделится еще порция теплоты.
Используется также частный случай теплового эффекта реакции - теплота сгорания. Из самого названия видно, что теплота сгорания служит для характеристики вещества, применяемого в качестве топлива. Теплоту сгорания относят к 1 молю вещества, являющегося топливом (восстановителем в реакции окисления), например:
| C2H2 | + | 2,5 O2 | = | 2 CO2 | + | H2O | + | 1300 кДж |
| ацетилен | теплота сгорания ацетилена |
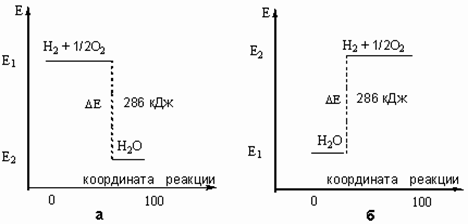
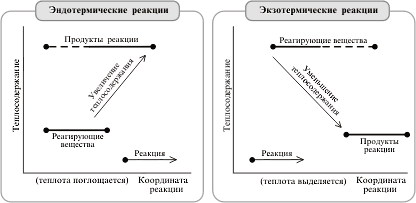
Запасенную в молекулах энергию (Е) можно отложить на энергетической шкале. В этом случае тепловой эффект реакции (D Е) можно показать графически (рис. 2).
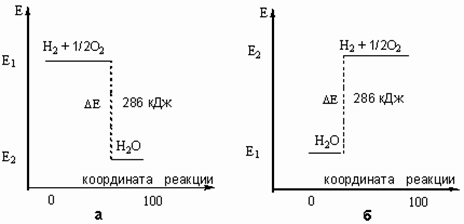
Рис. 2. Графическое изображение теплового эффекта (Q = D Е): а) экзотермической реакции горения водорода; б) эндотермической реакции разложения воды под действием электрического тока. Координату реакции (горизонтальную ось графика) можно рассматривать, например, как степень превращения веществ (100% - полное превращение исходных веществ).
Похожие работы
... в уравнениях реакций и не забывать о том, что складываемые, вычитаемые или сокращаемые моли вещества должны находиться в одинаковом агрегатном состоянии. 2. Применение теплового эффекта на практике Тепловые эффекты химических реакций нужны для многих технических расчетов. Например, рассмотрим мощную российскую ракету "Энергия", способную выводить на орбиту космические корабли и другие полезные ...
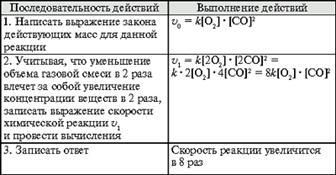
... , т. е. к увеличению скорости реакции. Количественно зависимость между скоростью реакции и молярными концентрациями реагирующих веществ описывается основным законом химической кинетики — законом действующих масс. Скорость химической реакции при постоянной температуре прямо пропорциональна произведению концентраций реагирующих веществ. Для мономолекулярной реакции скорость реакции ...
... условия сдвига равновесия вправо .... Глава 2. Прикладные аспекты преподавания темы «Закономерности течения химических реакций» Прикладные аспекты преподавания темы «Закономерности течения химических реакций» на мой взгляд удобнее всего рассматривать на уроках, которые следуют сразу за рассмотрением скорости реакции и химического равновесия, - это производство серной кислоты. 2.1 ...
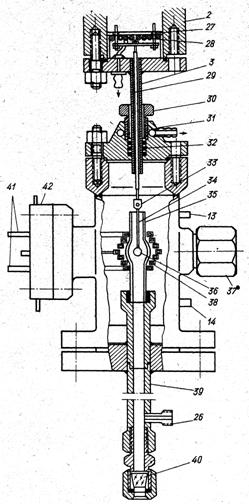
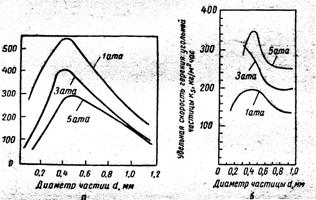
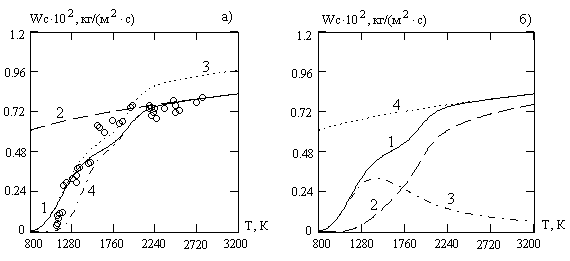
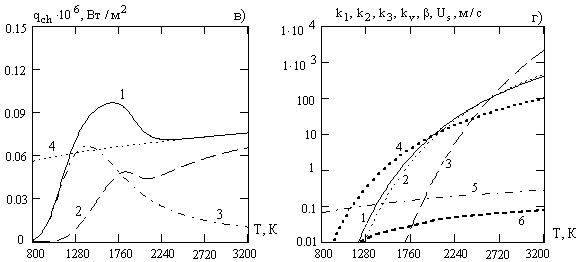
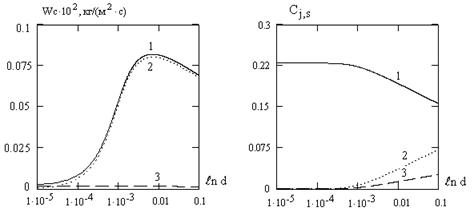
... датчика и осциллографа. Экспериментальные кривые зависимости времени τ горения частиц от давления p, соответствуют теоретической зависимости. Представляют интерес экспериментальные исследования процесса горения отдельной угольной частицы, движущейся в потоке газа. Такого рода опыты проводили Н. И. Сыромятников и 3.И.Леонтьева. После воспламенения частицы наблюдалось замедление скорости ее ...

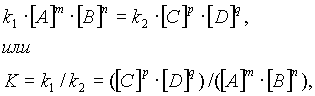



0 комментариев